Лекции биохимия 2. Резюме по модульной единице 4
 Скачать 2.84 Mb. Скачать 2.84 Mb.
|
S-МЕТИЛМЕТИОНИН (витамин U). По химическому строению пред-ставляет собой метилсульфоновое производное аминокислоты метионина: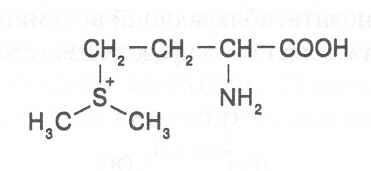 Чистые препараты витамина U получают в виде солянокислой соли S-метилметионинсульфонилхлорида. S-Метилметионин играет важную роль в активизации биохимических процессов в слизистой оболочке желудка и кишечника организма человека и оказывает положительное действие при лечении язвенных болезней желудка и двенадцатиперстной кишки. В биохимических процессах этот витамин может участвовать как активный донор метильных групп. При лечении язвенных заболеваний суточная доза витамина составляет не менее 250 мг. Витамин U синтезируется в растениях, особенно много его содержится в овощах, мг% в расчете на сухую массу: Томаты 20-45 Спаржа 100-150 Капуста белокочанная до 85 Сельдерей 15-25 АНТИВИТАМИНЫВ ходе изучения строения, свойств и биологической функции витаминов были найдены вещества, присутствие которых в организме вызывает авитаминоз по определенным витаминам, хотя данные витамины поступают в организм. Такие вещества были названы антивитаминами. Впервые механизм действия антивитаминов был выяснен в 1940 г. Д. Вудсом, который показал, что сульфаниламид (стрептоцид) является метаболическим конкурентом витамина парааминобензойной кислоты, участвующей в синтезе дигидроптероевой кислоты - предшественника другого витамина - фолиевой кислоты. По химическому строению сульфаниламид и парааминобензойная кислота представляют собой структурные аналоги: 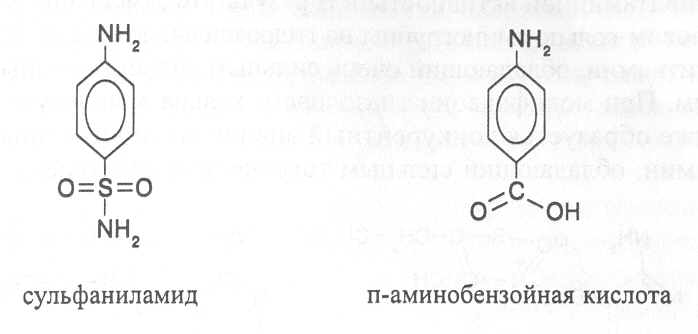 Сульфаниламид способен вместо п-аминобензойной кислоты вступать во взаимодействие с ферментом, катализирующим образование дигидроптероевой кислоты, при этом фермент становится неактивным, вследствие чего прекращается синтез дигидроптероевой кислоты и, как следствие, ингибируется также синтез фолиевой кислоты, что и может быть причиной авитаминоза. Однако, если в клетках организма повысить концентрацию п-аминобензойной кислоты, то действие сульфаниламида ослабляется. На основе сульфаниламида и его структурных аналогов были разработаны медицинские препараты, подавляющие рост микроорганизмов путем создания у них авитаминоза по фолиевой кислоте. В дальнейшем были изучены структурные аналоги других витаминов, обладающие антивитаминной активностью. Все они способны замещать в активном центре фермента биологически активную витаминную группировку на химически изменённую группировку структурного аналога, переводя фермент в неактивное состояние. Однако действие антивитаминов, представляющих структурные аналоги витаминов, является обратимым и они могут вытесняться из активного центра фермента повышенной концентрацией соответствующих витаминов. Довольно хорошо изучено биологическое действие химических аналогов тиамина. Замещение в пиримидиновом кольце тиамина метильной группы на этильную, пропильную и изопропильную приводит к существенному снижению витаминной активности структурных аналогов тиамина, а при введении в пиримидиновое кольцо бутилового радикала образуется соединение, обладающее антивитаминной активностью. В результате замещения в пиримидиновом кольце аминогруппы на гидроксильную группу образуется окситиамин, обладающий очень сильным антивитаминным действием. При модификации тиазолового кольца в молекуле тиамина также образуется конкурентный аналог этого витамина - пиритиамин, обладающий сильным токсическим действием. 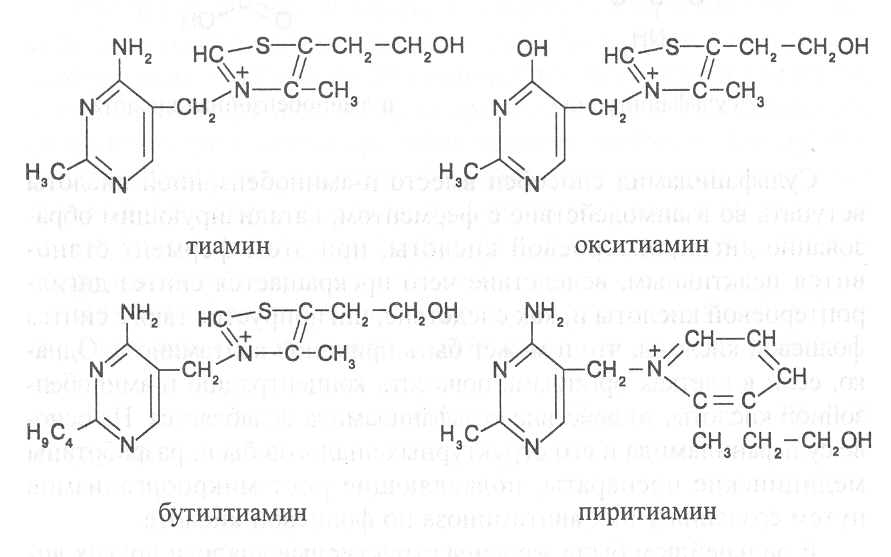 Известны также синтетические производные пиридоксина, которые ингибируют ферментные системы, имеющие в активном центре кофер-ментные формы этого витамина. Особенно сильным антивитаминным дей-ствием обладает 4-дезоксипиридоксин и токсопиримидин, представля-ющий собой оксипроизводное пиримидиновой группировки молекулы тиамина. В процессе изучения структурных аналогов выявлены антивита-минные формы для многих других витаминов: пантотеновой кислоты, никотиновой кислоты, рибофлавина, биотина, фолиевой кислоты, филло-хинона, токоферола, аскорбиновой кислоты. Как установлено в результате исследований, к антивитаминам отно-сятся химические вещества, способные образовывать с витаминами неак-тивные соединения, а также белковые молекулы, специфически связыва-ющие витамины. Так, например, изоникотилгидразид является антивита-мином пиридоксина, так как образует с пиридоксалем неактивное соеди-нение (по-видимому гидразон), которое не может превращаться в пири-доксальфосфат, вследствие чего в присутствии изоникотинилгидразида наблюдаются симптомы недостаточности витамина В6. В сыром яичном белке содержится антивитамин биотина – авидин, представляющий собой гликопротеид с молекулярной массой около 68000. Молекула авидина включает четыре полипептидные субъединицы, в каждой из которых имеется биотинсвязывающий участок, имеющий сильное химическое сродство к биотину. При скармливании опытным животным сырого яичного белка довольно быстро наблюдается сильно выраженный авитаминоз по биотину. Антивитаминное действие авидина очень часто используется исследователями в качестве теста для обнару-жения и изучения биотинсодержащих ферментов. 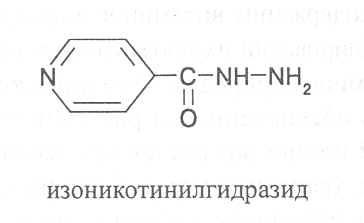 Вещества, обладающие антивитаминным действием, в значительных количествах содержатся в растительных продуктах. В проросших семенах гороха найдены антивитамины биотина и пантотеновой кислоты, в зерне кукурузы - антагонист никотиновой кислоты, в семенах льна – антивита-мин пиридоксина, в испорченном сладком клевере - антагонисты витамина К. Некоторые растительные белки подобно авидину способны специфи-чески связывать определенные витамины и таким образом действовать как антивитамины, в связи с чем не все растительные продукты могут упо-требляться в пищу в сыром виде. После проваривания растительной пищи белки, обладающие антивитаминным действием, теряют способность к связыванию витаминов, так как в процессе варки пищи они подвергаются тепловой денатурации. Вопросы для повторения.1. Какие вещества относят к витаминам и как они влияют на жизнедеятельность организмов? 2. Какие имеются сведения о классификации витаминов и потребности в витаминах разных организмов? 3. В чём состоят химические и биологические особен-ности важнейших витаминов (ретинола, кальциферола, токоферола, филлохинона, тиа-мина, рибофлавина, пиридоксина, пантотеновой, никотиновой, аскорбиновой и фоли-евой кислот, кобаламина, биотина, цитрина, миоинозита, S-метилметионина)? 4. Како-во содержание важнейших витаминов в зерне и бобовых культур, семенах масличных растений, клубнях картофеля, корнеплодах, кормовых травах, овощах, плодах и ягодах? 5. Как изменяется содержание витаминов в процессе роста и развития растений и при формировании их продуктивных органов? 6. Как влияют на накопление витаминов природно-климатические факторы, погодные условия и уровень обеспеченности растений элементами питания? 7. Какие возможны потери витаминов при нарушении технологических режимов сушки, хранения и переработки растительных продуктов? 8. В чём состоят особенности действия антивитаминов? 9. Какие имеются сведения о наличии антивитаминов в растительных продуктах? Резюме по модульной единице 5. К витаминам относятся вещества разного химического строения, которые строго необходимы для жизнедеятельности организмов в небольших количествах. Биологическая активность витаминов определяется тем, что они в качестве активных группировок входят в состав ферментов и предопределяют их каталитические свойства. При недостатке витаминов понижается активность соответствующих ферментов, вследствие чего замедляются или прекращаются биохимические реакции, катализируемые данными ферментами, и возникают заболевания, называемые авитаминозами. Растения и природные формы микроорганизмов синтезируют необходимые для их развития витамины. Однако человек и животные не способны к синтезу витаминов, поэтому должны получать их с пищей. Источниками многих витаминов для жвачных животных служат микроорганизмы их пищеварительной системы. Для человека основными источниками витаминов являются пищевые продукты растительного и животного происхождения, для сельскохозяйственных животных – растительные корма. Некоторые витамины содержатся в растительных и микробных продуктах в виде биохимических прешественников, называемых провитаминами (каротин – провитамин А, эргостерол – провитамин D). Витамины в качестве коферментов или непосредственно субстратов участвуют в окислительно-восстановительных процессах (токоферол, филлохинон, рибофлавин, никотиновая кислота, аскорбиновая кислота, цитрин), реакциях обмена азотистых веществ (пиридоксин, фолиевая кислота, кобаламин), липидов (биотин, пантотеновая кислота, миоинозит), процессах карбоксилирования (биотин) и декарбоксилирования (тиамин), обменных реакциях слизистых оболочек пищеварительной системы человека и животных (ретиналь, кальциферол, S-метилметионин). Некоторые химические вещества способны понижать биологическую активность витаминов, их называют антивитаминами. Известны антивитамины, являющиеся структурными аналогами витаминов, которые способны связываться с ферментами и переводить их в неактивное состояние. Другие антивитамины образуют с витаминами неактивные соединения. Известны также белковые антивитамины, которые представляют собой белки, образующие прочные комплексы с витаминами. Тестовые задания к лекции 2. Тесты № 29-66. Лекция 3. Основы биохимической энергетики. Аннотация. Излагаются закономерности биоэнергетических превращений в живых организмах. Рассматриваются возможности использования термодинамических функций (внутренняя энергия системы, энтальпия, энтропия, свободная энергия Гиббса) для характеристики энергетических превращений в ходе биохимических реакций. Изучаются термодинамические условия для осуществления сопряжённого синтеза веществ в живых организмах. Указывается роль макроэргических соединений в сопряжённом синтезе веществ и осуществлении связи между катаболическими и анаболическими реакциями. Рассматриваются основные группы макроэргических соединений и пути образования АТФ в организмах.Ключевые слова: биохимическая энергетика, биохимическая система, энтропия, энтальпия, теплота сгорания веществ, экзотермические и эндотермические реакции, самопроизвольные реакции, свободная энергия, экзергонические и эндергонические реакции, сопряжённые реакции синтеза веществ, макроэргические соединения, фототрофные и хемотрофные организмы, катаболические и анаболические реакции.Рассматриваемые вопросы.
Модульная единица 6. Биохимическая энергетика. Цели и задачи изучения модульной единицы. Изучить закономерности биоэнергетических превращений в организмах. Научить студентов использовать сведения по биохимической энергетике для прогнозирования интенсивности и направленности биохимических процессов в растительных организмах и обоснования изменений химического состава растительной продукции. 6.1. Принципы функционирования биоэнергетических систем. В клетках живого организма одновременно происходят многие тысячи биохимических реакций, которые сопровождаются выделением или поглощением энергии, а также превращением одних форм энергии в другие. Так, например, в листьях растений в ходе фотосинтеза осуществляется поглощение электромагнитной энергии солнечного света и превращения её в электрическую энергию заряженных частиц, которая затем в хлоропластах трансформируется в энергию трансмембранного электрохимического потенциала, инициирующего синтез молекул АТФ. А с участием АТФ проходит синтез жизненно важных органических веществ. И таким образом энергия солнечного света переходит в энергию химических связей органических веществ, синтезируемых в растительном организме. Как узнаем далее, часть поглощённой листьями световой энергии превращается в тепло и энергию излучения в виде флуоресценции и фосфоресценции. У всех живых организмов в процессе биохимических реакций дыхания происходит превращение химической энергии углеводов, жиров, азотистых веществ в тепловую энергию, а также энергию мембранных потенциалов внутриклеточных структур и химическую энергию АТФ, восстановленных динуклеотидов, которые затем становятся источниками энергии для синтеза новых органических веществ, необходимых для поддержания жизненных функций организма. Совокупность всех биоэнергетических превращений в организме, обеспечивающих его нормальную жизнедеятельность в изменяющихся условиях окружающей среды, изучает раздел биохимии, называемый биохимической энергетикой. В связи с тем, что основу жизненных явлений, происходящих в организме, составляют химические и физические процессы, для изучения биоэнергетических превращений применяются законы химической термодинамики. И поэтому для оценки энергетических параметров биохимических реакций используются термодинамические функции – внутренняя энергия системы (U), энтальпия (Н), энтропия (S), свободная энергия Гиббса (G) и др. При этом в ходе биохимических превращений определяются не абсолютные их значения, а изменения термодинамических функций - DU, DH, DS, DG. Очень часто такие изменения термодинамических функций оценивают при стандартных условиях и тогда их обозначают специальным символом - DU˚, DH˚, DS˚, DG˚. За стандартные условия в биохимической энергетике принимаются: давление 101,3 кПа, температура 25˚С (298,16 К), концентрация веществ 1 моль/л, рН физиологической среды 7,0. Кроме того, следует учитывать, что биохимические реакции, катализируемые ферментами, протекают очень быстро и они осуществляются при атмосферном давлении и температуре, которые изменяются очень медленно. Поэтому можно считать, что биоэнергетические превращения в ходе биохимических реакций происходят при постоянной температуре и постоянном давлении. В результате определения изменений термодинамических функций можно выяснить, происходит ли в ходе биохимического процесса выделение или поглощение энергии, установить возможность трансформации различных видов энергии и решить вопрос о количестве выделяемой или поглощаемой энергии. На основе полученных таким образом данных можно оценить вероятность самопроизвольного осуществления биохимических реакций, а также выявить возможные источники энергии для осуществления биосинтетических процессов. Живые организмы, их клетки и многие компоненты внутриклеточных структур представляют собой открытые термодинамические системы, которые обмениваются и веществом, и энергией с окружающей средой. При этом такой обмен является необходимым условием поддержания их жизнедеятельности. Если обмен организма веществом и энергией с окружающей средой прекращается, то организм погибает. Так, например, растения не могут произрастать без света, кислорода, углекислого газа, поступления воды и питательных веществ. Человек и животные не могут жить без пищи, воды и кислорода. Простейшая биохимическая система включает реагирующие вещества, продукты реакции, а также фермент, катализирующий данную биохимическую реакцию. Реагирующие вещества поступают в биохимическую систему из окружающей физиологической среды, а продукты реакции выходят из системы в окружающую среду. В зависимости от характера биохимического превращения в ходе реакции может происходить выделение в том или ином виде энергии в окружающую среду или, наоборот, поглощение энергии из окружающей среды, в результате чего будет происходить изменение внутренней энергии биохимической системы. В том случае, когда система выделяет определённое количество энергии в окружающую среду, общий запас её внутренней энергии уменьшается, а при поглощении энергии из окружающей среды – увеличивается. Изменение внутренней энергии системы происходит в соответствии с первым законом термодинамики – законом сохранения энергии, который для открытых систем имеет следующую формулировку: при любом процессе сумма внутренней энергии системы и энергии окружающей среды остаётся величиной постоянной. Исходя из этого, изменение внутренней энергии системы равно алгебраической сумме всех энергий, уходящих из системы в окружающую среду и входящих в неё из окружающей среды. Общий запас внутренней энергии биохимической системы зависит от её состава, массы, потенциальной и кинетической энергии молекул, атомов и частиц, входящих в состав системы, внутримолекулярной, внутриядерной и гравитационной энергии, термодинамических параметров (температуры, давления, объёма), а также обмена веществами и энергией с окружающей средой. Вместе с тем внутренняя энергия системы является функцией её состояния. В процессе биохимических превращений система переходит из одного термодинамического состояния в другое, при этом изменение внутренней энергии системы не зависит от пути перехода, а определяется разностью между конечным (U2) и начальным состоянием (U1) и поэтому можно записать DU = U2 – U1. И каким бы путём не осуществлялся переход системы от состояния U1 к состоянию U2, через ряд промежуточных стадий или в результате прямого превращения, согласно первому закону термодинамики величина DU не изменяется. Это важное положение используется в биохимической энергетике для оценки энергетических изменений в ходе биологического окисления веществ, которое осуществляется в клетках организмов постепенно, проходя множество промежуточных стадий. Однако суммарный энергетический эффект окисления в этих процессах равен количеству энергии, которое выделяется при сгорании органических веществ. Поэтому, сопоставляя теплоту сгорания исходных веществ и образующихся при биологическом окислении кислородом продуктов, можно с достаточно высокой точностью определять энергетические изменения в ходе указанных биохимических реакций. 6. Теплота сгорания некоторых биохимических продуктов (кДж×моль-1)
С помощью термодинамических расчётов и в специальных экспериментах доказано, если в процессе горения вещества система не совершает никакой работы, то по количеству выделившегося тепла можно судить об изменении внутренней энергии системы, так как в таком процессе DU = Q. В связи с этим для многих органических соединений, являющихся продуктами биохимических реакций, определена теплота сгорания ( табл. 6), которая представляет собой термохимический показатель, выражающий, количество тепла при полном сгорании 1 моля вещества с образованием высших оксидов. |
