Соединения свинца
 Скачать 2.4 Mb. Скачать 2.4 Mb.
|
|
ВЭЖХ -анализ Условия хроматографирования: хроматограф жидкостный хроматографическая колонка (6282 мм), заполненная обращено-фазным сорбентом Сепарон подвижная фаза - элюент - смесь 0,05М водного раствора двузамещенного фосфата аммония и метанола (60:40) скорость потока элюирования - 100 мкл/мин детектирование - при длине волны 240 нм. Подготовка пробы: кровь/моча + стандарт + вода + ацетатный буфер перемешивание центрифугирование упаривание органики анализ Приготовление стандартных образцов. Для приготовления эталонных растворов используется чистые субстанции барбитала, фенофарфитала, циклобарбитала, барбамила и этаминала натрия. Эти растворы служат для идентификации указанных веществ, определения их хроматографических параметров, а также для приготовления контрольных растворов при проведении количественных анализов. Градуировка хроматографа проводится по фенобарбиталу, барбамилу и этаминалу натрия. Качественный анализ. Идентификация проводится следующим образом: сопоставляют время удерживания и коэффициент емкости определяемого компонента и образца сравнения - фенобарбитала; сравнивают УФ-спектры предполагаемого компонента и образца сравнения; оценивают совпадение значений времени удерживания определяемого компонента и образца сравнения при добавлении контрольного раствора в раствор экстракта из биопробы (причем концентрация образца сравнения должна быть близка к концентрации определяемого компонента); сопоставляют УФ-спектры определяемого компонента и образца сравнения при двух длинах волн, и оценивается их спектральное отношение. Концентрация определяемого вещества (Ci) в растворе экстракта из биопробы определяется по формуле 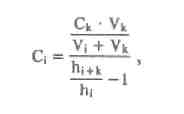 где гдеCk - концентрация "добавки" в растворе подвижной фазы; Vk - объем добавленного контрольного раствора; Vi- объем раствора экстракта с определяемым веществом; hi - высота сигнала определяемого вещества в растворе экстракта из биопробы; hi+k - высота сиrnала определяемого вещества после добавки в раствор экстракта контрольного раствора. Метод внешнего стандарта В соответствии с методом внешнего стандарта и с учетом линейности зависимости выходного сигнала от массы вещества последовательно, с анализом раствора экстракта биопробы, проводят анализ контрольного раствора идентифицированного вещества. концентрация контрольного раствора (Ck) должна быть близка к концентрации определяемого вещества в растворе экстракта. Анализы контрольного раствора и экстракта биопробы должны проводитьсяв одном масштабе регистрации. Концентрация определяемого вещества в растворе экстракта (Ci) рассчитывается по формуле Ci = Ck*hi/Hk, где Ck - концентрация контрольного раствора; hi- высота сигнала определяемого наркотического вещества в растворе экстракта биопробы; hk - высота пика вещества контрольного раствора. Метод внутреннего стандарта В соответствии с методом внутреннего стандарта в биообьект до операции пробоподготовки добавляется известное количество вещества, принятого за стандарт. В анализе барбитуратов в количестве внутренних стандартов рекомендуется использовать одно изследующих веществ: апробарбитал, метилфенобарбитал, фенилubдантоин и другне вещества, которые в данных условиях xpoмaтoграфического разделения должны полностью отделяться от других компонентов образца, должны элюироваться близко к пику анализируемого соединения, не реагировать с другими компонентами, т.е. удовлетворять требованиям, предъявляемым к внутреннему стандарту. Можно использовать одновременно два и более внутренних стандарта. Концентрация определяемогo вещесгва (CI) рассчитывается по формуле Ci = Cbc * Hi /Hbc *1/Fi/bc, где Свс - концентрация внутреннего стандарта; hi - высота пика (или площадь) определяемого вещества; hвс - высота пика (или площадь) стандарта; Fi/вc - относительный калибровочный фактор. Относительный калибровочный фактор компонента Fi/вc вычисляется по формуле Fi/bc = Hi * Cbc/Ci * Hbc, где hl- высота пика (или площадь) компонента известной концентрации (калибровочный раствор); CI - концентрация калибровочного раствора определяемого компонента; hвс - высота пика (или площадь) внутреннего стандарта; Сbc - концентрация внутреннего стандарта УФ-спектрофотометрия. Спектрофотометрическое определение основано на способности фенобарбитала к лактим-лактамной (амидоимидольной) таутомерии. При pH=2,0 барбитурат находится в растворе в лактамной форме, не обладающей специфической абсорбцией в пределах 200-300 нм. При pH=10,0 образуется монолактимная форма, в гетероциклическом ядре возникает двойная связь, наблюдается поглощение при 240 нм. При pH=13 и выше в растворе присутствует дилактимная форма с двумя двойными связями в кольце. Абсорбция наблюдается при 255-260 нм. Для определения рекомендованы методы прямого и дифференциального спектрофотометрирования. Прямая СФМ: проводится при pH=10 и 240 нм. Дифференциальные методы: при pH=2,0-10,0 и 239 нм - если исследуются внутренние органы трупа; при pH=10,0-13,0 и 260 нм - если исследуется кровь и моча. Дифференциальные методы дают более надежные результаты, т.к. исключают влияние посторонних веществ, экстрагируемых хлороформом из кислого раствора вместе с фенобарбиталом. УФ-спектральные характеристики фенобарбитала: при pH = 9,2 наблюдается поглощение при 239 нм (εа = 452); при pH = 13,0 поглощение при 254 нм (εа = 342). Для расчета содержания барбитурата пользуются калибровочным графиком или значениями показателя удельного поглощения. В сочетании с хроматографией метод УФ-спектрофотометрии является достаточно специфичным, быстрым и чувствительным. Определяются микрограммовые количества фенобарбитала. Фенобарбитал Депрессант центральной нервной системы. Кристаллическое вещество с температурой плавления 245°. Вещество кислого характера, pKa=7,3. Плохо растворимо в воде, хорошо растворимо в этаноле и в водных растворах щелочей. УФ-спектр имеет два максимума поглощения при щелочных значениях pH (при pH=9,2 λнм=239; при pH=13,0 λнм=254). ИК-спектр имеет следующие характеристические частоты: 1684, 1712, 1770, 1310. Соединение быстро всасывается после орального введения, экскретируется в неизменном виде до 30%. Препарат пролонгированного действия (10-18 часов), период полувыведения 3 дня. Фенобарбитал используется как снотворное и противосудорожное средство. Фенобарбитал дает длительный сон, мало изменяется в организме и выводится в значительной степени почками в неизменном состоянии. В относительно больших дозах фенобарбитал способен вызывать смертельное отравление. (0,6 – 1 г.). ВРД 0,2, ВСД 0,5. В организме человека фенобарбитал подвергается, в основном, в печени ряду превращений: Окислению одного из радикалов Окислению до кислот и кетонов Десульфированию Демитилированию Гидролизу Метод Валова 100 г измельченного биологического материала + 180 мл воды и 20 мл 10 %-го раствора гидроксида натрия 30 мин при частом перемешивании центрифугируют 30 мин надосадочная жидкость + 120 мл 10 %-го раствора вольфрамата натрия и 1 н. раствор серной кислоты (до рН=2) нагревают на кипящей водяной бане 20 мин центрифугирование центрифугат процеживают через ватный тампон собирают в делительную воронку + диэтиловый эфирэфирный слой + 50 мл 10%-го гидроксида натрия водный слой отделяют + 25 %-ным раствор серной кислоты до рН=2 + диэтиловый эфир эфирная вытяжка Подтверждающие исследования Цветные реакции: • с аммиачным раствором нитрата или ацетата кобальта. При наличии барбитуратов появляется розово-фиолетовое окрашивание. • мурексидная проба. Через некоторое время по краям сухого остатка появляется розовое и красное окрашивание, которое становится интенсивней при смачивании остатка 25% раствором гидрата окиси аммония. Микрокристаллоскопические реакции: перекристаллизация: на предметное стекло помещают сухой остаток. Через 24 часа наблюдают форму осадка – сферолиты, в виде «ежиков». с железоиодидным комплексом. Раствор хлорида окисного железа + концентрированная соляная кислота + калия иодид. Через 10 минут наблюдают образование сростков кристаллов. Бензонал 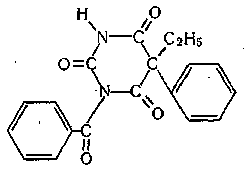 Кристаллическое вещество с температурой плавления 137°. Вещество кислого характера, pKa=7,3. Бензонал трудно растворяется в воде и этиловом спирте, легче — в диэтиловом эфире, хлороформе и диметилформамиде. Экстрагируется органическими растворителями из кислых водных растворов. Бензонал в основном применяется для лечения судорожных форм эпилепсии. Иногда он применяется для лечения больных, страдающих припадками, не сопровождающимися судорогами. ВРД 0,3, ВСД 0,6. Метаболитами бензонала являются бензойная кислота и фенобарбитал, который, в свою очередь, подвергается метаболизму. Бензонал и его метаболиты в основном выделяются с мочой. Выделение бензонала из биологического материала. 100 г измельченного биологического материала + 10 мл р-ра соляной кислоты + 50 г сульфата аммония перемешивают + 200 мл смеси равных объемов этилового спирта и хлороформа настаивают 2 ч при перемешиваниивытяжку сливают и фильтруют через плотный бумажный фильтр промывают смесью этилового спирта и хлороформа (1 : 1) водную фазу, насыщенную сульфатом аммония, отделяют и не исследуют. Слой органических растворителей выпаривают досуха + 200 мл горячей воды перемешивают и фильтруют + три порции хлороформахлороформные вытяжки + фосфатный раствор (рН = 7,4) хлороформный слой фильтруют через бумажный фильтр хлороформную вытяжку используют для идентификации и количественного определения бензонала. Поскольку бензонал частично разлагается в организме на фенобарбитал и бензойную кислоту, наличие последней определяют в водной фазе. С этой целью водную фазу подкисляют раствором соляной кислоты (1 : 1) до рН = 2 и взбалтывают с 10 мл хлороформа. От водной фазы отделяют хлороформную вытяжку, которую исследуют на наличие бензойной кислоты. Подтверждающие исследования Бензонал с изопропиламином и солями кобальта дает фиолетовую окраску С солями кобальта и щелочами бензонал дает сине-фиолетовую окраску Бензонал можно обнаружить по форме кристаллов, которые образуются после прибавления к нему метилового спирта и концентрированной соляной кислоты. Через несколько минут в поле зрения под микроскопом появляются ромбической формы кристаллы или сростки из них. Обнаружение методом хроматографии. НФ: силикагель ПФ: хлороформ:н-бутанол:25% раствор аммиака Д: 0,02 %-м хлороформным раствором дифенилкарбазида, затем раствором сульфата ртути. Пятна бензонала на пластинке имеют Rf =* 0,40...0,45. 10. При наличии барбамила пятна на хроматограмме приобретают сине-фиолетовую или красно-фиолетовую окраску. Гексенал 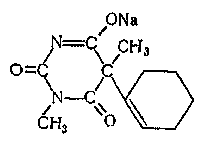 Хорошо растворяется в воде, этиловом спирте и хлороформе, слабо — в диэтиловом эфире. Гексенал экстрагируется органическими растворителями из кислых водных растворов. Гексенал проявляет снотворное действие, а в больших дозах он имеет наркотические свойства. Его применяют для наркоза в сочетании с оксидом азота (I), фторотаиом и с некоторыми другими веществами. Гексенал и сам может применяться для кратковременного наркоза (продолжительностью 15—20 мин). Гексенал относится к барбитуратам короткого периода действия. В организме он подвергается метаболизму несколькими путями: Гидроксилирование циклогексильной группы окисление с образованием 3'-кетогексабарбитала N-деметилирование. N-деметилирования при атоме азота в третьем положении норгексабарбитал. Определенное количество гексенала, поступившего в организм, метаболизируется путем разрыва цикла барбитуровой кислоты. Подтверждающие исследования От прибавления солей кобальта и изопропиламина к гексеналу появляется фиолетовая окраска. Гексенал с солями кобальта и щелочью дает розовую или красную окраску. От прибавления концентрированной серной кислоты к гексеналу образуется осадок, состоящий из сростков игольчатых кристаллов. Гексенал с подкисленным спиртовым раствором иодида калия образует кристаллический осадок. 5. Обнаружение гексенала по УФ-спектрам. Гексенал в ходе химико-токсикологического анализа выделяется из биологического материала в виде гексобарбитала, который можно обнаружить по спектрам поглощения В ИК-области спектра гексенал (диск с бромидом калия) имеет основные пики при 1712, 1660, 1390, 1358 см-1, Тиопентал-натрий 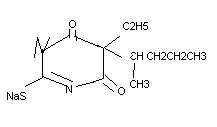 Легко растворим в воде, практически нерастворим в бензоле и эфире. Средство для внутривенного наркоза. Анализ см. «Общая информация» ПРОИЗВОДНЫЕ 1,4-БЕНЗОДИАЗЕПИНА Общие свойства веществ. Распределение производных 1,4-бенздиазепина по органам происходит в три стадии: 1-ая характеризуется падением концентрации в крови и накоплением в паренхиматозных органах; на 2-ой стадии идет накопление соединений во всех органах. Предел накопления соединений в тканях определяется кажущимся объемом распределения (Vр); 3-я стадия, самая продолжительная по времени – характеризуется накоплением соединений в органах выделения (печени, почках), с одновременным уменьшением в остальных тканях органов. Наибольшее содержание 1,4-бенздиазепинов в ЖКТ, тканях печени, почек. Ультрафиолетовые спектры В электронных спектрах производных 1,4-бенздиазепина имеется 3 полосы поглощения с λmax в областях: 200-215 нм 220-240 нм 290-330 нм Две первые полосы соответствуют возбуждению ароматических хромофоров. Третью длинноволновую полосу относят к азометиновой связи, сопряженной с бензогруппой. По характеру поглощения в УФ-области 1,4-бенздиазепины относятся к соединениям, абсорбция которых изменяется от величины значений рН: в кислой среде – за счет протонирования атома азота 1 (у хлордиазепоксида) и 4 (1,2-дигидропроизводных 1,4-бенздиазепина – нитразепам, оксазепам, диазепам); в щелочной среде в молекуле 1,2-дигидропроизводных 1,4-бенздиазепина наблюдается изменение хромофорной системы (увеличение сопряжения за счет лактим-лактамной таутомерии азометиновой связи в положения 1,2 - нитразепам, оксазепам). Кислотный гидролиз хлордиазепоксида (I), протекающий в мягких условиях, приводит к образованию 4-окси-1,2-дигидро-3Н-1,4-бенздиазепин-2-онов (II). В более жестких условиях эти соединения гидролизуются до 2-аминобензофенонов (III), альфа-аминокислот (IV) и аминов (V). Метаболизм Окисление 1.1. N-деметилирование В молекуле диазепама у атома азота в 1 положении В метиламинной группе хлордиазепоксида Пробоподготовка. Изолирование из тканей и органов трупа. Анализ производных 1.4-бензодиазепина по нативным соединениям. Возможно использование любых общих методов пробоподготовки. М-д изолирования нейтральным ацетоном Биоматериал + н-ацетон ацетоновое извлечение + 0,5н HCL + н-гексан очищенная ацетоно-водная вытяжка ацетоно-водная фаза + NaOH + эфир эфирное извлечение ТСХ, элюирование исследование не бензодиазепины. М-д Васильевой Биоматериал + вода, подкисленная органической кислотой водная вытяжка водная фаза + NH4OH + хлороформ органическая фаза выпаривание исследование на бензодиазепины М-д Стаса-Отто Биоматериал + 96% этанол + органическая кислота спиртовой экстракт упаривание + 100% спирт отделение осадка очищенный экстракт упаривание остаток + горячая вода фильтрование водная фаза + NaOH + хлороформ органическая фаза исследование на бензодиазепины ТСХ-скрининг Общая система НФ: силуфол ПФ: хлороформ:этилацетат Д: Р-в Драгендорфа Р-р FeCl3 + HCl + HNO3 Частная система НФ: силуфол ПФ: хлороформ:этилацетат:метанол Д: Р-в Драгендорфа Р-р FeCl3 + HCl + HNO3 Обнаружение: а) реактив Драгендорфа в разбавленной уксусной кислоте образует оранжевые и желто-оранжевые комплексные соли; б) реактив FPN (хлорид железа (III) в смеси хлорной и азотной кислот) окисляет бензодиазепины с образованием окрашенных продуктов желтого цвета; в) реактив Марки образует окрашенные продукты желтого цвета; г) подкисленный йодплатинат образует темноокрашенные пятна. Количественное определение |
