Соединения свинца
 Скачать 2.4 Mb. Скачать 2.4 Mb.
|
|
Количественное онределение: Определяют аргентометрическим способом (индикатор — железо-аммонийные квасцы) по количеству хлори-иона, образовавшегося при нагревании ГХЦГ на кипящей водяной бане в течении 2 часов с 0.3 н раствором едкого натра. Колориметрическое и спектрофотометрическое определение основано на отщеплении 6 атомов хлора,дальнейшем переведении полученного бензола в мета-динитробензола,который в сильно щелочной среде дает с метилэтилкетоном красно-фиолетовое окрашивание. Г 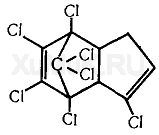 ептахлор Гептахлор (везикол 104, гептазол, гептанал и др.) — 1, 4, 5, 6, 7, 8, 8-гептахлор-эндометиленбицикло [4.3.0] нонадиен-1,5 — принадлежит к ядохимикатам группы полихлорциклодиена. Он представляет собой белое кристаллическое вещество (т. пл. 95—96 °С) со слабым камфарным запахом. Практически нерастворим в воде, растворяется в этиловом спирте, лучше — в керосине, ароматических углеводородах, галогенпроизводных углеводородов и в некоторых других органических растворителях. Технический препарат представляет собой воскообразную массу (т. пл. 46—74°С), в которой содержится 65—72 % гептахлора. В качестве примесей в техническом препарате могут быть хлориндан, нонахлор, октахлор и др. Гептахлор выпускается в виде 25 %-го концентрата эмульсии, которую применяют в качестве инсектицида для обработки семян некоторых сельскохозяйственных культур. Гептахлор высокотоксичен. Обладает выраженным кожно-резорбтивным действием, имеет кумулятивные свойства. При попадании в организм через пищевой канал в крови он окисляется до эпоксигептахлора, который более токсичен, чем сам гептахлор. Гептахлор и эпоксигептахлор накапливаются в тканях организма. В почве эти вещества сохраняются в течение нескольких лет. Наличие остаточных количеств гептахлора в пищевых продуктах не допускается. Изолирование: Выделение гептахлора из биологического материала. 25 г измельченного биологического материала вносят в колбу, прибавляют воду до получения кашицеобразной массы. К этой кашицеобразной массе прибавляют 40 мл н -гексана, взбалтывают, затем смесь оставляют на 30 мин при периодическом взбалтывании содержимого колбы. После этого с биологического материала сливают слой органического растворителя, а биологический материал еще раз настаивают с н -гексаиом, как указано выше. Гексановые вытяжки соединяют и переносят в делительную воронку, в которую прибавляют 10 мл насыщенного раствора сульфата натрия в 20 %-м растворе серной кислоты, и взбалтывают. Затем отделяют слой н-гексана, который еще несколько раз взбалтывают с насыщенным раствором сульфата натрия в 20 %-м растворе серной кислоты (до получения бесцветной водной фазы). Очищенные таким образом н -гексановые вытяжки взбалтывают с сухим безводным сульфатом натрия, затем их сливают с сульфата натрия. Полученные гексановые вытяжки выпаривают досуха. Сухие остатки используют для обнаружения гептахлора. Выделение гептахлора из мочи. В делительную воронку вносят 20 мл мочи и 20 мл диэтилового эфира. Смесь взбалтывают 15 мин. Эфирную вытяжку отделяют, мочу еще 2 раза взбалтывают с диэтиловым эфиром (порции по 20 мл). Эфирные вытяжки соединяют, прибавляют к ним 10 г безводного сульфата натрия и взбалтывают, затем сливают эфирную вытяжку, которую выпаривают досуха. Сухие остатки используют для обнаружения гептахлора. Выделение гептахлора из крови. В пробирку с притертой пробкой вносят 2 мл крови, 10 мл диэтилового эфира и смесь взбалтывают 15 мин. После разделения фаз сливают эфирную вытяжку, а кровь еще 2 раза взбалтывают с диэтиловым эфиром (порции по 10 мл). Эфирные вытяжки соединяют, прибавляют к ним 5 г безводного сульфата натрия и взбалтывают. Эфирную вытяжку сливают с сульфата натрия и выпаривают досуха. В сухих остатках определяют наличие гептахлора Качественное определение: 1.Реакция с диэтиламином. В пробирку вносят 1—2 мл раствора исследуемого вещества в дихлорэтане. Затем по стенке пробирки приливают 5—7 капель реактива, состоящего из одного объема диэтиламина и двух объемов 0,1 н. раствора гидроксида калия в метиловом спирте. Смесь взбалтывают. При наличии гептахлора в пробе жидкость приобретает зеленую окраску, которая быстро исчезает. 2.Реакция с диэтаноламином. В пробирку вносят 1—2 мл раствора исследуемого вещества в дихлорэтане и прибавляют несколько капель реактива (смесь 1 части диэтаноламина и двух частей раствора гидроксида калия в метиловом спирте). Появление фиолетовой окраски указывает на наличие гептахлора в пробе. Реакция с диэтаноламином специфична для обнаружения гептахлора. 3.Реакция с анилином и пиридином. В пробирку вносят 2—3 мл раствора исследуемого вещества в бензоле, прибавляют 5 капель анилина и 2 капли 0,1 н. раствора гидроксида калия в метиловом спирте. Пробирку помещают на 15 с на кипящую водяную баню, затем вносят в нее 1 мл пиридина и снова пробирку помещают на 10 с на кипящую водяную баню. Содержимое пробирки перемешивают. При наличии гептахлора в пробе через 1—3 мин раствор приобретает темно-зеленую окраску. 4.Обнаружение гептахлора методом хроматографии. На линию старта на хроматографической пластинке наносят несколько капель исследуемой жидкости. Через 2 см правее на линию старта наносят каплю раствора «свидетеля». Пятна подсушивают на воздухе, затем пластинку вносят в камеру для хроматографирования, на дно которой налит слой н -гексана. Пластинку оставляют в камере для хроматографирования до тех пор, пока жидкость не поднимется на 10 см выше линии старта. Затем пластинку вынимают из камеры, подсушивают на воздухе, опрыскивают водно-ацетоновым раствором аммиаката серебра. После этого пластинку в течение 10—15 мин облучают УФ-светом. Источник облучения должен находиться на расстоянии 20 см от пластинки. При наличии гептахлора в исследуемой пробе пятна на пластинке приобретают серовато-черную окраску. Этилмеркулхлорид Изолирование: Выделение этилмеркурхлорида из внутренних органов трупов и объектов растительного происхождения. В колбу вместимостью 250 мл вносят 25 г тщательно измельченного биологического материала (печень, почки) или такое же количество объектов растительного происхождения (зерно, крупа, мука и др.), прибавляют 50 мл 3 н. раствора соляной кислоты. Смесь оставляют на 30—60 мин при периодическом взбалтывании содержимого колбы. Затем содержимое колбы подвергают центрифугированию. Надосадочную жидкость сливают, а твердые частицы исследуемого объекта еще раз настаивают с 3 н. раствором соляной кислоты, как указано выше, а затем содержимое колбы центрифугируют. Кислые надосадочные жидкости соединяют и 2 раза взбалтывают с хлороформом (по 10 мл) в течение 5 мин. Хлороформные вытяжки соединяют и подвергают исследованию на наличие этилмеркурхлорида методом хроматографии. Выделение этилмеркурхлорида из мочи. В делительную воронку вносят 50 мл мочи и 5 мл концентрированной соляной кислоты. Смесь оставляют на 30 мин при периодическом взбалтывании. Затем прибавляют 10 мл хлороформа и взбалтывают 5 мин, а потом отделяют хлороформную вытяжку. Водную фазу еще 2 раза взбалтывают с хлороформом по 10 мл. Хлороформные вытяжки соединяют и определяют в них наличие этилмеркурхлорида методом хроматографии. Выделение этилмеркурхлорида из крови. В колбу вместимостью 100 мл вносят 2 мл крови и 5 мл 0,1 н. раствора гидроксида натрия. Колбу нагревают на кипящей водяной бане в течение 5—10 мин до получения однородной жидкости. После охлаждения в колбу вносят 20 мл концентрированной соляной кислоты и смесь оставляют на 10—15 мин при частом перемешивании. Далее смесь подвергают центрифугированию. Центрифугат переносят в делительную воронку и дважды взбалтывают с хлороформом (по 10 мл) в течение 5 мин. Соединенные хлороформные вытяжки используют для обнаружения этилмеркурхлорида при помощи метода хроматографии. Качественное определение: 1.Проба с медной проволокой основана на способности металлической меди вытеснять ртуть из этилмеркурхлорида. При погружении хорошо очищенной медной проволоки или медной пластинки в раствор, содержащий этилмеркурхлорид, последний разлагается. Выделившаяся при этом ртуть откладывается на металлической меди в виде серого налета. Для обнаружения в сером налете ртути ее переводят в иодид, а затем — в тетра-иодмеркуриат меди (I) или производят возгонку. Медную проволоку, на которой отложилась ртуть в виде серого налета, нагревают с несколькими кристалликами иода. При этом образуется желтоватого или красного цвета иодид ртути (II). От прибавления к иодиду ртути раствора иода в иодиде калия образуется тетраиодмеркуриат калия K 2 [HgI 4 ]. Находящийся в растворе избыток иодида калия с сульфатом меди (II) образует белый осадок иодида меди (I). Этот осадок с тетраиодмеркуриатом калия дает тетраиодмеркуриат меди (I) Cu 2 HgI 4, имеющий красную или оранжево-красную окраску. Появление этой окраски указывает на наличие ртути (этилмеркурхлорида) в исследуемом объекте 2.Обнаружение этилмеркурхлорида методом хроматографии. Этот метод основан на переведении этилмеркурхлорида в дитизонат и на последующем обнаружении дитизоната этилмеркурхлорида методом хроматографии в тонком слое сорбента. По данным некоторых авторов, при взаимодействии дитизона с этилмеркурхлоридом образуется дитизонат ртути, а не дитизонат этилмеркурхлорида. Для обнаружения этилмеркурхлорида в соответствующих объектах (внутренние органы трупов, моча, кровь) методом хроматографии в тонком слое сорбента используются хлороформные вытяжки из этих объектов, получение которых описано выше. 5—10 мл хлороформной вытяжки из соответствующего объекта, содержащего этилмеркурхлорид, вносят в делительную воронку, прибавляют 20 мл ацетатного буферного раствора (рН = 4,5), 10 мл воды и 1 мл раствора дитизона в хлороформе. Содержимое делительной воронки хорошо взбалтывают в течение 1 мин. После этого отделяют хлороформный слой. Взбалтывание водной фазы с новыми порциями хлороформного раствора дитизона (по 1 мл) проводят до тех пор, пока последняя порция раствора дитизона не перестанет изменять зеленую окраску на желтую. Хлороформные вытяжки соединяют, выпаривают в струе холодного воздуха. Сухой остаток растворяют в 0,5 мл хлороформа и определяют наличие этилмеркурхлорида методом хроматографии. На хроматографическую пластинку наносят 2—3 капли хлороформного раствора сухого остатка и каплю раствора «свидетеля» (хлороформного раствора дитизоната этилмеркурхлорида). Пятна нанесенных на пластинку растворов подсушивают на воздухе, а затем пластинку вносят в камеру для хроматографирования, насыщенную парами системы растворителей: н -гептана и хлороформа (2:5). При наличии дитизоната этилмеркурхлорида на пластинке обнаруживаются желтые пятна. Севин ( 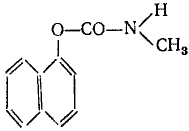 1-нафтил-N-метилкарбоминат) Севин — белое кристаллическое вещество.Температура плавления 142 градуса.Плохо растворим в воде,лучше растворяется в органических растворятелях.При комнатной температуре устойчив по отношению к воде, свету, кислороду воздуха. Подвергается гидролизу. Изолирование: проводится повторной экстракцией бензолом. Бензол затем удаляется, остаток растворяется в 10 — 15 мл этанола. Качественное определение: 1.Реакция перекристаллизации. Из спиртового или хлороформного раствора севин кристаллизуется в виде характерных кристалов и сростков(кресты и дендриды). 2.С 1% раствором пикриновой кислоты севин образует желтые сростки кристаллов в виде снопов и пучков. 3.С 2% раствором хлорной ртути севин образует бецветные кристаллы, в виде вытянутых шестиугольников и призм. Реакции окрашивания. Реакции основаны на предварительном гидролизе севина до L-нафтола и последущим его обнаружении. 1.Реакция с купробромидом натрия, добавляют раствор NaOH, выдерживают при температуре 55-60 в течении 10 минут, прибавляют раствор HCL, и свежеприготовленного реактива(CUCL2+NaBr). При нагревании смеси до 60 появляется красно-фиолетовое окрашивание, переходящее при энергичном встряхивании с хлороформом, в хлороформный слой. 2.Реакция с 4-аминоантипирином. Появляется оранжево-красное окрашивание, переходящее в хлороформый слой. 3.Реакция с 0,05 % раствором NaNo2 в разбавленной серной кислоте — желтое окрашивание переходящее в оранжевоепри добавлении NaOH. 4.Реакция с 1% свежеприготовленным раствором FeCl — розовое окрашивание. Количественное определение: севина основано на реакции взаимодействия продукта его щеочного гидролиз L-нафтола с купробромидом натрия. Фотоэлектроколориметрия. Натрия фторид, кальция фторид. Фтор присутствует в переменных количествах в почве и ествественных водных запасов. Известны острые и хронические отравления , вызванные приемом пищи, содержащей фториды.Симптомы и признаки острого отравления фторидами включают: тошноту, рвоту, диарею, боль в животе и парастезию. Объектами исследования на фториды являются главным образом кровь, моча, пищевые продукты и при смертельном исходе — внутренние органы. Изолирование: тщательно измельченые внутренние органы трупа, содержимое желудка, пищевые продукты и другие объекты в количестве 25 г подщелачивают избытком гидроксида кальция, смачивают раствором нитрата аммония или концентрированной азотной кислотой, высушивают и прокаливаютпри температуре не выше 500 градусов до полного сжигания. Полученную золу смешивают с раствором хлорида кальция, кипетят, охлаждают. Отфильтрованный осадок промывают дистиллированной водой до нейтральной реакции, сжигают остаток вместе с фильтром и золу исследуют на наличие фторидов. Качественное определение: 1.Часть остатка в платиновом тигле смачивают несколькими каплями воды и обливают небольшим количеством концентрированной серной кислоты, тигель быстро закрывают часовым стеклом, нижняя поверхность которого покрыта воском или парафином. Часть слоя воска или парафина предварительно удаляют. Тигель оставляют на сутки, защитный слой воска или парафина удаляют и наблюдают травление стекла. 2.Часть золы смешивают с SiO2 (песком), помещают в пробирку и приливают концентрированную серную кислоту. В отверстии пробирки держат стеклянную палочку с каплей воды. В случае наличия фтористого водорода капля мутнеет вследствии выделения кремнеевой кислоты. 3.Небольшое количество золы вносят в короткое колено реактивной трубки,заполненной 2% раствором K2Cr2O7 в концентрированной серной кислоте, перемешивают и наблюдают за появлением несмачиваемости стенок трубки в коротком колене — реакция основана на способности HF разрушать стекло и делать его гидрофобным (несмачиваемым). 4.Капельная реакция: при нанесении водного раствора , содержащего F-, на фильтровальную бумагу, пропитанную цирконализариновым лаком, красная окраска бумаги исчезает(красное окрашивание-желтое). Кремнефтористые соли(фторосиликаты) Na2SiF6. При выпаривании свободная кремнефтористая кислота разлагается на части: H2SiF4 ->2HF+SiF4 Сухие кремнефтористые соли разлагаются при нагревании на фтористуюсоль и фтористый кремний:Na2SiF6->2NaF+SiF4. Качественное определение: 1.К раствору кремнефторида добавляют раствор хлорида бария. Кристаллический осадок отфильтровывают и высушивают на воздухе. 2.Добавление к раствору соли раствора едкого натра вызывает выпадениее осадка кремнеевой кислоты:NaHF2->NaF+HF; 4NaF+SiO2+H2O=SiF4+4NaOH. 3SiF4+3H2O=2H2SiF6+H2SiO3(следы в растворе); H2SiF6+2NaOH=Na2SiF6+H2O. Хлор Свободный хлор имеет широкое применение в технике. Вступая в реакцию с составными частями организма , хлор образует соли хлористоводородной кислоты, являющиеся номальной составной часть организма. Вода действует на хлор очень медленно, но в присутствии легкоокисляющихся веществ происходит быстрый гидролиз хлора,обуславливающий процесс окисления. В связи с этим обнаружение свободного хлора во внутренних органах трупа невозможно. Наблюдающийся иногда в течении двух дней запах хлора от трупа обуславливается продуктами гидролиза хлора, следами хлорноватисной кислоты. Для обнаружения хлорноватистой кислоты, исследуемый бъект измельчают, помещают в колбу, отверстие колбы закрывают пробкой с двумя трубками, из которых одна доходит до дна трубки и соединена с двумя промывными склянками аппарата Киппа для получения угольного ангидрида. В первую склянку наливают воду , а во вторую раствор нитрата серебра.Другая трубка,оканчивающаяся под пробкой, соединена с двумя склянками Дрекселя, содержащими подкисленный раствор йодида калия,смешанный с крахмальным клейстером. Слабо нагревая колбу с объектом на водяной бане,медленно пропускают ток угольного ангидрида. Отсутствие посинения указывает на отсутствие хлорноватистой кислоты, а также хлора, брома и йода. При появлении посинения ток угольного ангидрида пропускают снова в воду,содержащую сернистую кислоту: NaHSO3+H2SO4=NaHSO4+SO2+H2O. По кончании пропускания жидкость слабо нагревают до удаления избытка сернистой кислоты и в растворе обнаруживают ион хлора при помощи нитрата серебра, сравнивая цвет осадка с цветом осадка хлорида серебра. Количественное определение: титрование ратвором нитрата серебра. Хлорамин п редставляет собой амид пара-сульфоновой кислоты с толуолом или бензолом, в котором один или два атома водорода амидогруппы замещены активным хлором. Хлорамины — кристаллические вещества, растворимые в воде и в этиловом спирте. Качественное определение: 1.При добавлении к раствору хлорамина йодида калия выделяется йод. 2.Ратвор предварительно испытывают реакцией с нитратом серебра на отсутствие иона хлора , затем прибавляют раствор карботана натрия, насыщенного сернистым ангидридом,подкисляют азотной кислотой и добавляют нитрат серебра — оьразуется белый, творожистый осадок, нерастворимый в азотной кислоте. |
