Соединения свинца
 Скачать 2.4 Mb. Скачать 2.4 Mb.
|
|
Для ГЖХ обнаружения производных 1,4-бензодиазепина и их метаболитов используется общая система: стеклянная колонка 2 м х 4мм с 2,5% SE-30 на хромосорбе Q. Газ-носитель – аргон/метан Температура колонки от 150 до 300 С Температура инжектора – 230 Температура детектора - 300 Подготовка пробы: кровь/моча + вода + р-р NaHCO3 центрифугирование центрифугат ТФЭ + вода промывают картридж хлороформом остаток растворяют в метаноле. ГХ/МС анализ Газовый хроматограф/ масс-спектрометр Стандарты: смесь бензодиазепинов Экстракция: пробирка + биожидкость + стандарт встряхивают + NaCl + NH4Cl + н-бутилхлорид экстракция центрифугирование органический слой + ацетонитрил + гексан выпаривание + этиловый эфир + KOH центрифугирование анализ ВЭЖХ -анализ Условия хроматографирования: хроматограф жидкостный ПФ: ацетонитрил:ацетатный буфер скорость потока элюирования - 100 мкл/мин детектирование - при длине волны 240 нм. Подготовка пробы: моча + ацетат Na + b-глюкуронидаза настаивание 2 часа + ацетатный буфер. Приготовление стандартных образцов. Для приготовления эталонных растворов используется чистые субстанции. Эти растворы служат для идентификации указанных веществ, определения их хроматографических параметров, а также для приготовления контрольных растворов при проведении количественных анализов. Качественный анализ. Идентификация проводится следующим образом: сопоставляют время удерживания и коэффициент емкости определяемого компонента и образца сравнения; сравнивают УФ-спектры предполагаемого компонента и образца сравнения; оценивают совпадение значений времени удерживания определяемого компонента и образца сравнения при добавлении контрольного раствора в раствор экстракта из биопробы (причем концентрация образца сравнения должна быть близка к концентрации определяемого компонента); сопоставляют УФ-спектры определяемого компонента и образца сравнения при двух длинах волн, и оценивается их спектральное отношение. Концентрация определяемого вещества (Ci) в растворе экстракта из биопробы определяется по формуле 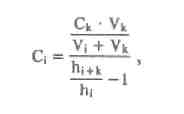 где гдеCk - концентрация "добавки" в растворе подвижной фазы; Vk - объем добавленного контрольного раствора; Vi- объем раствора экстракта с определяемым веществом; hi - высота сигнала определяемого вещества в растворе экстракта из биопробы; hi+k - высота сиrnала определяемого вещества после добавки в раствор экстракта контрольного раствора. Метод внешнего стандарта В соответствии с методом внешнего стандарта и с учетом линейности зависимости выходного сигнала от массы вещества последовательно, с анализом раствора экстракта биопробы, проводят анализ контрольного раствора идентифицированного вещества. концентрация контрольного раствора (Ck) должна быть близка к концентрации определяемого вещества в растворе экстракта. Анализы контрольного раствора и экстракта биопробы должны проводитьсяв одном масштабе регистрации. Концентрация определяемого вещества в растворе экстракта (Ci) рассчитывается по формуле Ci = Ck*hi/Hk, где Ck - концентрация контрольного раствора; hi- высота сигнала определяемого наркотического вещества в растворе экстракта биопробы; hk - высота пика вещества контрольного раствора. Метод внутреннего стандарта В соответствии с методом внутреннего стандарта в биообьект до операции пробоподготовки добавляется известное количество вещества, принятого за стандарт. Это вещество должно полностью отделяться от других компонентов образца, элюироваться близко к пику анализируемого соединения, не реагировать с другими компонентами, т.е. удовлетворять требованиям, предъявляемым к внутреннему стандарту. Можно использовать одновременно два и более внутренних стандарта. Концентрация определяемогo вещесгва (CI) рассчитывается по формуле Ci = Cbc * Hi /Hbc *1/Fi/bc, где Свс - концентрация внутреннего стандарта; hi - высота пика (или площадь) определяемого вещества; hвс - высота пика (или площадь) стандарта; Fi/вc - относительный калибровочный фактор. Относительный калибровочный фактор компонента Fi/вc вычисляется по формуле Fi/bc = Hi * Cbc/Ci * Hbc, где hl- высота пика (или площадь) компонента известной концентрации (калибровочный раствор); CI - концентрация калибровочного раствора определяемого компонента; hвс - высота пика (или площадь) внутреннего стандарта; Сbc - концентрация внутреннего стандарта 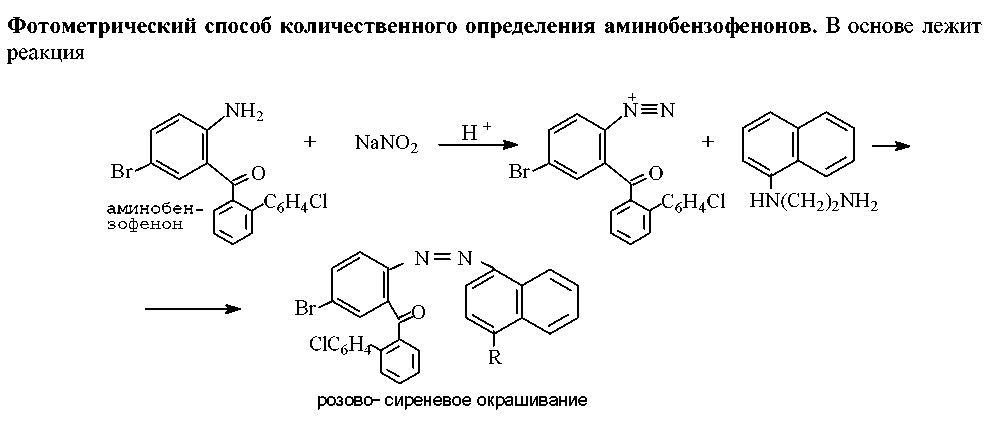 Изучив отечественные и зарубежные литературные источники, описывающие различные инструментальные методы анализа группы производных бензодиазепина, а также опираясь на результаты наших исследований мы пришли к выводу, что оптимальной комбинацией в анализе производных бензодиазепина является применение в качестве: предварительного метода анализа – метод ПФИА с использованием пороговой концентрации 100 нг/мл, подтверждающего метода анализа – метод газовой хроматографиии с масс селективным детектором или газовой хроматографии с электронно-захватным детектором, метода количественного определения – высоко-эффективная жидкостная хроматография с диодно-матричным детектором. Хлордиазепоксид (элениум, хлозепид) Практически нерастворим в воде, растворим в воде соли 1,4-бенздиазепинов. В органических растворителях растворимость зависит от структуры. Наиболее высокая растворимость наблюдается в апротонных растворителях (диметилформамиде, диметилсульфоксиде). Слабое основание. pKa = 2.93 Выводятся производные 1,4-бенздиазепина, в основном, почками в виде основных соединений и метаболитов. Наличие в органах активных метаболитов производных 1,4-бенздиазепина снижает скорость элиминации. Время полувыведения (Т ½) 8-28 часов. Хлордиазепоксид относится к транквилизаторам. Он оказывает успокаивающее действие на центральную нервную систему, обладает противосудорожной активностью, потенцирует действие снотворных веществ и анальгетиков, проявляет умеренный снотворный эффект. Хлордиазепоксид (7-хлор-2-метиламино-5-фенил-ЗН-1,4-бензодиазепин-4-оксид) быстро всасывается из желудочно-кишечного тракта. Метаболитами хлордиазепоксида является N-деметилхлордиазепоксид и лактам (7-хлор-1,3-дигидро-5-фенил-2Н-1,4-бензодиазепин-2-он-4-оксид). Часть неизмененного хлордиазепоксида и его метаболитов выделяется с мочой, а часть — образует конъюгаты, которые тоже выделяются с мочой. Пробоподготовка. 25 г измельченного биологического материала + вода + HCl до рН = 1 3 раза по одному часу вытяжки центрифугируют центрифугат подщелачивают до рН = 10 + хлороформ 3 раза взбалтывают хлороформные вытяжки соединяют обнаружение и количественное определение хлордиазепоксида. 5 - 10 мл плазмы крови или мочи + аммиак дважды взбалтывают с хлороформом хлороформные вытяжки + вода взбалтывают хлороформный слой + 5 мл р-ра соляной кислоты взбалтывают 5 мин солянокислые вытяжки отделяют нагревают на водяной бане затем нагревают при 125 °С на парафиновой бане 30 мин (при этом образуется 2-амино-5-хлорбензофенон) + 0,5 мл 10 %-го р-ра нитрита натрия + 0,5 мл 0,5 %-го раствора сульфамината аммония + 0,5 мл 0,1 %-го раствора N-1-нафтилэтилендиамина дигидрохлорида вишнево-красная окраска. Цветные реакции. Реакция с нингидрином, хлордиазепоксид дает коричневую окраску. Реакция с реактивом Марки, хлордиазепоксид дает желтую окраску. Реакция с реактивом Фреде, хлордиазепоксид дает оранжевую окраску. Реакция Витали — Морена, хлордиазепоксид дает желтую окраску. ТСХ-обнаружение Обнаружение хлордиазепоксида методом хроматографии в тонком слое сорбента. НФ: силикагель КСК или пластинки «силуфол» ПФ: этилацетат : 25 %-го р-р аммиака : метиловый спирт хлороформ : ацетон Д: р-в Драгендорфа Использование спектров. Обнаружение хлордиазепоксида по УФ- и ИК-спектрам. Хлордиазепоксид в 0,1 н. растворе гидроксида натрия имеет максимумы поглощения при 243 и 260 нм; в 0,1 н. растворе серной кислоты хлордиазепоксид имеет максимумы поглощения при 245 и 306 нм. Хлордиазепоксид в 0,1 н. растворе соляной кислоты имеет максимумы поглощения при 246 и 308 нм. Диазепам (седуксен) 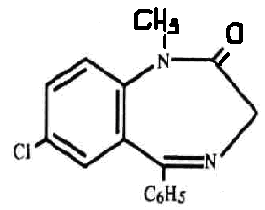 Диазепам (седуксен, эридан,реланиум и др.) представляет собой белый или белый с желтоватым оттенком кристаллический порошок, не растворяется в воде, трудно растворяется в этиловом спирте, растворяется в хлороформе. Т1/2 = 20-55 часов. По действию на организм диазепам относится к транквилизаторам. Он способствует нормализации сна, применяется для лечения невротических состояний, уменьшает чувство страха и т. д. Диазепам быстро всасывается в пищевом канале. Метаболизм: образуются продукты N-деметилирования оксазепам глюкуронид гидроксилирование диазепама глюкуронид Выделение из крови и мочи. 10 мл мочи/5 мл крови + равный объем фосфатного буферного раствора (рН = 7,0) 2 раза по 5 мин взбалтывают с диэтиловым эфиром эфирные вытяжки + NaOH дважды взбалтывают + вода эфирная вытяжка + HCl встряхивание 10 мин отделение солянокислой вытяжки ФЭК Параллельно измеряют оптическую плотность диазепама, обработанного указанным выше способом. Наличие максимумов поглощения при 242 и 287 нм указывает на наличие диазепама в крови или моче. Качественные реакции. Реакция с нингидрином. Р-р диазепама в этиловом спирте + 10 мг нингидрина водяная баня + 5 мл этилового спирта синяя окраска + 1 %-го раствора сульфата меди красная. ТСХ-обнаружение. НФ: силикагель КСК/силуфол ПФ: этилацетат : р-р аммиака : метиловый спирт хлороформ : ацетон Д: реактив Драгендорфа. Спектральный анализ. Диазепам в 2 н. растворе соляной кислоты имеет максимумы поглощения при 242 и 287 нм, в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 241, 284 и 359 нм; в ИК-области спектра диазепам имеет основные пики при 1681, 1484 и 1313 см -1. Оксазепам 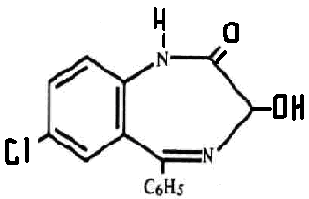 Т1/2 = 5-15 часов. Он представляет собой кристаллический порошок, почти не растворимый в воде, растворимый в этиловом спирте и хлороформе. По фармакологическим свойствам оксазепам близкий к хлордиазепоксиду и диазепаму. Он менее токсичен, чем диазепам, обладает слабым противосудорожным действием и миорелаксантным эффектом. Метаболизм. Оксазепам явдяется одним из метаболитов диазепама. После приема оксазепама максимальный уровень его в плазме достигается через 4 ч, а через 48 ч он исчезает из плазмы. Оксазепам находится в плазме в виде глюкуронида. В виде глюкуронида он выделяется с мочой, а с калом он выделяется в неизмененном виде. Выделение из биологического материала 25 г исследуемого объекта + 3 мл насыщенного р-ра гидрофосфата натрия uомогенизирование гомогенат + 100 мл диэтилового эфира взбалтывают эфирные вытяжки соединяют фильтруют через бумажный фильтр профильтрованные эфирные вытяжки обнаружение и количественное определение оксазепама. Выделение из крови и мочи. 10 мл крови/мочи + 100 мл диэтилового эфира взбалтывают 10 мин, 2 раза отделяют эфирную вытяжку фильтруют через бумажный фильтр профильтрованные эфирные вытяжки обнаружение и количественное определение оксазепама. Качественные реакции. Цветная реакция 25—50 мл объединенной эфирной вытяжки выпаривают досуха сухой остаток растворяют в 5 мл 6 н. раствора соляной кислоты и фильтруют 1 мл фильтрата кипятят 5—10 мин помещают в холодильник на 15 мин + 1 мл смеси (0,3 г бромида калия, 0,3 г нитрита натрия в 6 мл воды) взбалтывают и помещают в холодильник на 30 мин + 0,5 мл 10%-го раствора мочевины + 1 мл 1 %-го спиртового раствора α-нафтола и 1 мл 40 %-го водного раствора гидроксида натрия красная окраска ТСХ-обнаружение. НФ: силуфол ПФ: хлороформ : пропиловый спирт : ацетон Д: тиосульфат натрия. При налички оксазепама на пластинке появляются оранжевые или желтоватые пятна. Обнаружение по УФ- и ИК-спектрам. Растворы оксазепама в этиловом спирте имеют максимумы полос поглощения при 230 и 315 нм. В ИК-области спектра оксазепам (диск с бромидом калия) имеет основные пики при 1687, 1706, 693 и 830 см -1. Нитразепам 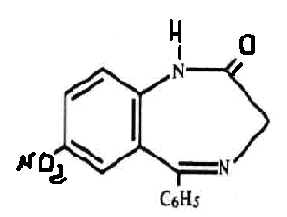 T1|2 = 18-38 часов. Нитразепам — светло-желтый или светло-желтый с зеленым оттенком кристаллический порошок. Практически нерастворим в этиловом спирте и хлороформе. Нитразепам оказывает транквилизирующее, мышечно-расслабляющее, снотворное действие и т. д. Он усиливает снотворное действие других снотворных средств и анальгетиков. Применяется при нарушении сна, неврозах, психопатиях. Метаболизм. Метаболитами нитразепама являются 7-амино-метаболит, 7-ацетиламино-метаболит. В течение 48 ч из организма выделяется около 23 % принятой дозы нитразепама. В неизмененном виде с мочой выделяется около 5 % этого препарата. Свыше 8 % нитразепама выделяется с мочой в виде 7-амино- метаболита и около 10%—в виде 7-ацетиламино-метаболита. Часть неизмененного нитразепама может быть обнаружена в кале. Выделение из биологического материала. Биологический материал трижды настаивают с насыщенным раствором щавелевой кислоты (рН=1) Через 1 ч после каждого настаивания вытяжки отделяют от биологического материала центрифугированием кислый центрифугат трижды взбалтывают со смесью хлороформа и этилацетата кислый центрифугат подщелачивают до рН = 10 трижды взбалтывают с новыми порциями смеси хлороформа и этилацетата исследование на наличие нитразепама. Предварительные пробы на наличие в моче. 5 мл мочи + аммиак до рН=10 + 250 г дитионита натрия (Na2S2O4) взбалтывают 10 мин нагревают при 50 °С в течение часа и охлаждают жидкость 10 мин взбалтывают с 10 мл смеси (метиленхлорида и этилацетата) от водной фазы отделяют слой смеси органических растворителей взбалтывают с 10 мл 5 %-го раствора буры фаза органических растворителей + 5 мл 0,2 н. раствора соляной кислоты взбалтывают органические растворители. 4 мл кислой водной фазы охлаждают в ледяной воде + 0,2 мл 0,4 н. раствора нитрита натрия + 0,2 мл 2%-го раствора сульфамината аммония перемешивают + 0,2 мл 0,4 %-го раствора N-1-нафтилэтилендиамина дигидрохлорида вишнево-красная окраска. Выделение метаболитов нитразепама из мочи. 5 мл мочи + аммиак до рН=10 взбалтывают 10 мин нагревают при 50 °С в течение часа и охлаждают жидкость 10 мин взбалтывают с 10 мл смеси (метиленхлорида и этилацетата) от водной фазы отделяют слой смеси органических растворителей взбалтывают с 10 мл 5 %-го раствора буры фаза органических растворителей + 5 мл 0,2 н. раствора соляной кислоты взбалтывают органические растворители. 4 мл кислой водной фазы охлаждают в ледяной воде + 0,2 мл 0,4 н. раствора нитрита натрия + 0,2 мл 2%-го раствора сульфамината аммония перемешивают + 0,2 мл 0,4 %-го раствора N-1-нафтилэтилендиамина дигидрохлорида вишнево-красная окраска. Обнаружение нитразепама и его метаболитов методом хроматографии. ПФ: силикагель/силуфол НФ: этилацетат : метилен : аммиак Д: р-в Драгендорфа Обнаружение по УФ- и ИК-спектрам. Раствор нитразепама в этиловом спирте имеет максимумы поглощения при 218 и 260 нм, в 0,1 и. растворе серной кислоты имеет максимум поглощения при 277 нм и изгиб около 340 нм; нитразепам в ИК-области спектра (диск с бромидом калия) имеет основные пики при 1692, 1615, 1352 и 702 см -1. |
