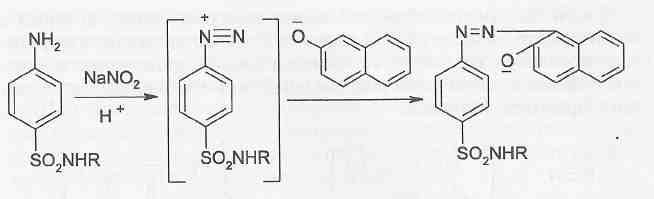
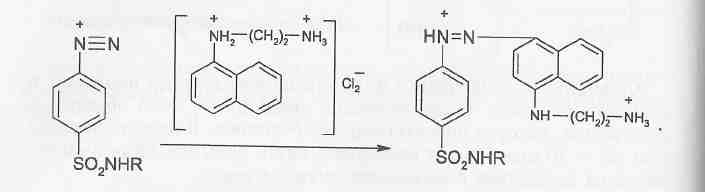
Соединения свинца
 Скачать 2.4 Mb. Скачать 2.4 Mb.
|
10 преобладает свободный амин, соль диазония инактивируется вследствие образования диазотат-иона.Выделение из биологического материала (по Б. М. Саломатину). 100 г измельченного биологического материала + этиловый спирт, подкисленным 10% р-м щавелевой кислоты до рН = 2...3. кислые спиртовые вытяжки на водяной бане (при 40 °С) упаривают до густоты сиропа + 96° этиловым спиртом фильтруют выпаривают досуха + 100 мл воды (темп. 40—60 °С) жидкость охлаждают и фильтруют + 5 % р-р щавелевой кислоты до рН = 2...3 + диэтиловый эфир (по 50 мл 2 раза) + 50%-м р-м гидроксида натрия до рН = 13 + 4 порции диэтилового объединенные эфирные вытяжки + 0,5 н р-р серной кислоты водные вытяжки соединяют и нагревают 3 мин на водяной бане (темп. 50—60 °С) кислые водные вытяжки используют для обнаружения. Обнаружение тизерцина Реакции с реактивами Марки и Фреде. Тизерцин с реактивами Марки и Фреде дает синевато-красную окраску. Реакция с реактивом Манделина. К 1 мл исследуемого раствора прибавляют 0,1 мл реактива Манделина. Жидкость взбалтывают и охлаждают в ледяной воде. К жидкости прибавляют 5 мл концентрированной серной кислоты. При наличии тизерцина раствор приобретает красно-фиолетовую окраску. Обнаружение тизерцина методом хроматографии. НФ: силуфол ПФ: аммиак : этиловый спирт / этилацетат : ацетон Д: 50 % раствор серной кислоты в этиловом спирте. Обнаружение тизерцина по УФ- и ИК-спектрам. Раствор тизерцина в этиловом спирте имеет максимумы поглощения при 255 и 310 нм; тизерцин в 0,1 н. растворе соляной кислоты имеет максимумы поглощения при 251 и 302 нм. В ИК-области спектра основание тизерцина (диск с бромидом калия) имеет основные пики при 1587, 1460, 1269 и 1446 см -1. Тиоридазин 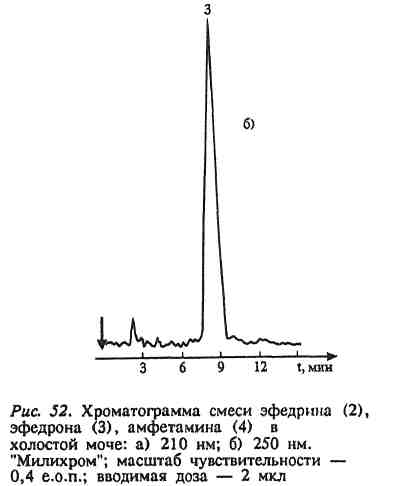 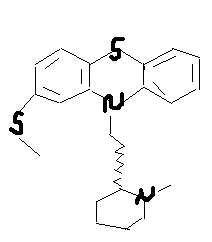 ПРОИЗВОДНЫЕ ПИРАЗОЛОНА 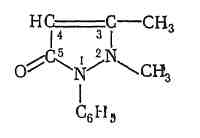 Антипирин. Антипирин.Хорошо растворим в воде, спирте, хлороформе, хуже в эфире. Отравления антипирином наблюдаются в связи с широким его применением в качестве лекарства При повышенной чувствительности могут возникать смертельные отравления при приеме лечебных доз препарата. Этот препарат обладает болеутоляющим, жаропонижающим и противовоспалительным действием. Он уменьшает проницаемость капилляров и препятствует развитию воспалительных процессов. Антипирин при местном применении оказывает кровоостанавливающее действие. В организме при любом пути введения быстро всасывается, и следы их обнаруживаются в моче уже через 10—20 минут после введения. Выделяется антипирин медленно и главным образом с мочой. В неизмененном виде выделяется —5%. Основной метаболит антипирина 4-гидрооксиантипирин: 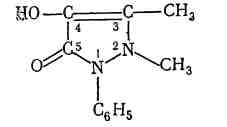 Он быстро на 95% связывается с глюкуроновой кислотой и в плазме крови не обнаруживается. Максимальный уровень его в плазме достигается через 1—2 ч после поступления в организм. Антипирин относительно медленно метаболизируется в органах и тканях. Около 5% дозы антипирина выделяется из организма в несвязанном виде, больше 50 % этого препарата подвергается метаболизму. Около 30—40 % введенной дозы антипирина связывается с глюкуроновой кислотой и выделяется в виде глюкуронида. Анальгин Растворим в воде, спирте, практически нерастворим в эфире, хлороформе, ацетоне. Хорошо и быстро всасывается в желудочно-кишечном тракте. В стенке кишечника гидролизуется с образованием активного метаболита — неизмененный метамизол в крови отсутствует (только после внутривенного введения незначительная его концентрация обнаруживается в плазме). Связь активного метаболита с белками — 50-60 %. Метаболизируется в печени, выводится почками. В терапевтических дозах проникает в материнское молоко. Изолирование М–д Васильевой. Биоматериал + вода + органическая кислота водная вытяжка + NH4OH + хлороформ органическая фаза выпаривание анализ М-д Стаса-Отто Биоматериал + 96% этанол + органическая кислота спиртовой экстракт упаривание + 100% этанол осаждение белков отделение осадка очищенный экстракт упаривание сухой остаток + горячая вода фильтрование + NH4OH + хлороформ органическая фаза анализ М-д Крамаренко Биоматериал + вода + серная кислота водная вытяжка + электролит осаждение белка отделение осадка очищенная водная вытяжка + эфир (доп. очистка) + NaOH до рН = 8-9 + хлороформ органическая фаза анализ ТСХ-скрининг НФ: силикагель ПФ: хлороформ : ацетон Д: 10% р-р FeCl3 сине-фиолетовое Обнаружение антипирина 1. Хлорид окисного железа дает с остатком из щелочного хлороформного извлечения кроваво-красное окрашивание, обусловленное образованием комплекса: 2. Раствор антипирина, подкисленный разведенной серной кислотой, при добавлении нескольких капель раствора нитрита натрия принимает зеленое окрашивание, а при больших количествах выпадает зеленый осадок нитрозоантипирина: 3. Реакция образования азокрасителя. Если к антипирину прибавить раствор нитрита натрия и уксусную кислоту, то образуется нитрозоантипирин (см. предыдущую реакцию), который при взаимодействии с α-нафтиламином образует пиразолоновый азокраситель, имеющий красную окраску. 4. Реакция с хлоридом железа (III). От прибавления к антипирину раствора хлорида железа (III) образуется ферропирин, растворы которого имеют красную окраску. Обнаружение антипирина по УФ- и ИК-спектрам. Антипирин в 0,1 н. растворе серной кислоты имеет максимум поглощения при 230 нм и изгибы при 259 и 265 нм; в ИК-области спектра антипирин (диск с бромидом калия) имеет основные пики при 1660, 770 и 1486 см -1. Количественное определение антипирина. Метод – йодометрия. + ацетат натрия для связывания HI. Извлекают хлороформом. Обнаружение анальгина 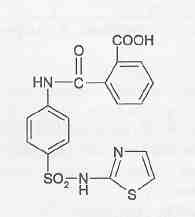 Реакции окисления + серебра нитрат белый осадок черный осадок металлического серебра + KIO3 малиновое окрашивание бурый осадок гидролитическое расщепление 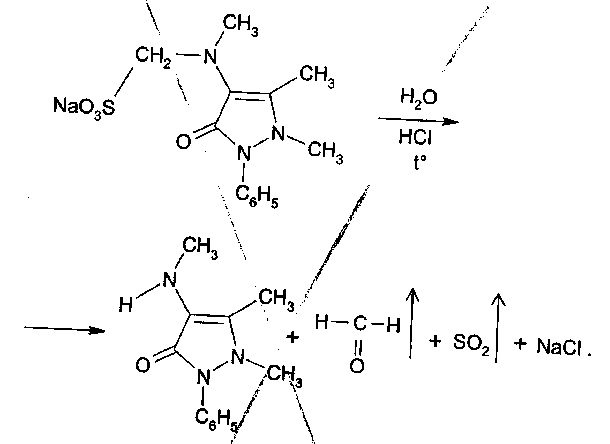 Количественное определение анальгина Основано на способности анальгина к окислению. Метод – йодометрия. Hcl – для разложения анальгина. Титрант – I2 до желтого окрашивания. 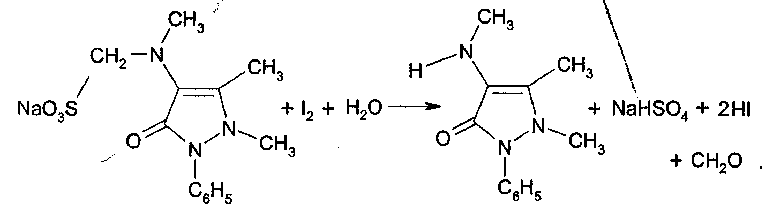 ПРОИЗВОДНЫЕ БЕНЗОЛСУЛЬФАНИЛАМИДОВ Сульфацил-Na 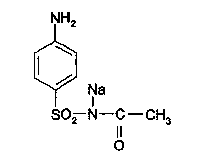 п-Аминобензолсульфонилацетамиднатрий. п-Аминобензолсульфонилацетамиднатрий.Белый кристаллический порошок, легко растворим в воде, практически нерастворим в спирте. Антибактериальное средство Сульфадиметоксин 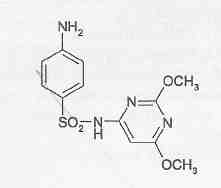 4-(п-Аминобензолсульфамидо-)-2,6-диметоксипиримидин. Белый или белый с кремоватым оттенком кристаллический порошок. Практически нерастворим в воде, мало растворим в спирте, легко - в разбавленных растворах кислот и щелочей. Лекарственные формы: порошок, таблетки. Антибактериальное средство длительного действия Фталазол 2-(п-Фталиламинобензолсульфамидо)-тиазол. Белый или белый со слегка желтоватым оттенком порошок. Практически нерастворим в воде, очень мало растворим в спирте. Растворим в растворах щелочей, легко растворим в водном растворе едкого натрия. Лекарственные формы: порошок, таблетки. Антибактериальное средство. Метод кислотно-основного титрования в диметилформамиде рекомендуется для оценки качества фталазола, который титруется как двухосновная кислота: 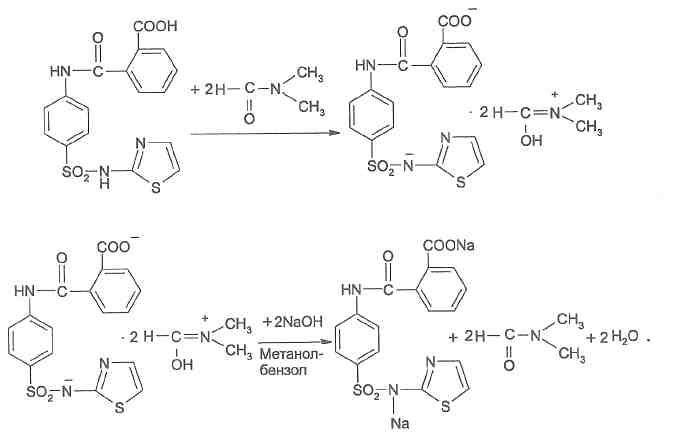 Все бензолсульфониламиды имеют характерные спектры поглощения в ИК-области. ИК-спектроскопия с использованием стандартных образцов или спектров сравнения применяется для идентификации лекарственной веществ. Это амфолиты с преобладанием кислотных свойств. За счет кислотных свойств бензолсульфониламиды и их производные взаимодействуют с солями тяжелых металлов: меди, серебра, железа, кобальта. В результате реакции образуются комплексные соединения, как правило, нерастворимые в воде, с характерной окраской. Взаимодействие с меди (П) сульфатом имеет дифференцирующее значение и применяется для подтверждения подлинности лекарственных веществ данной группы. Реакция проводится в умеренно-щелочной среде, при этом бензолсульфониламиды нейтрализуют 0,1 н. раствором щелочи по тимоловому синему. С солями серебра образуют соединения в виде белого осадка. Реакция протекает количественно.  Сочетание с первичными аминами наиболее легко протекает в слабокислой среде. В сильнокислой среде (рН |