01 Болезни органов дыхания. Сокращения и условные обозначения
 Скачать 2.33 Mb. Скачать 2.33 Mb.
|
|
Эмпиема плевры. Если к плевральному экссудату присоединяется гноеродная микрофлора, то развивается гнойный плеврит - эмпиема плевры. К ее возникновению приводят разнообразные причины. Они же часто определяют особенности клинической картины и характер течения (острое или хроническое) эмпиемы. Эмпиему плевры относят к хирургическим заболеваниям, но в большинстве случаев ее диагностирует врач-терапевт. На первом этапе диагностического поиска обнаруживают нарастание существующих жалоб: возобновляется (возникает) боль в груди, ухудшается общее состояние и самочувствие, вновь до высоких цифр повышается температура тела, что нередко сопровождается ознобом и потоотделением, нарастает одышка. В анамнезе есть указания на предшествующую пневмонию, обострение бронхоэктатической болезни, прогрессирование туберкулезного процесса, субплеврально расположенный абсцесс легких или инфицирование плевральной полости во время и (или) после операционной травмы. На втором этапе диагностического поиска обнаруживают объективные симптомы гнойно-резорбтивного истощения или гнойно-резорбтивной лихорадки. Часто она имеет гектический характер. Характерны бледность кожного покрова с землистым оттенком и похудание. При массивном выпоте (распространенная или тотальная эмпиема) может возникать болезненность межреберьев, присоединяются признаки дыхательной недостаточности. Хроническое течение эмпиемы может осложниться образованием наружных, бронхоплевральных и плевромедиастинальных свищей и развитием амилоидоза внутренних органов (отеки, гепатолиенальный синдром и др.). При ограниченной эмпиеме изменения внутренних органов выражены в меньшей степени. На третьем этапе диагностического поиска, как и при экссудативном плеврите, наибольшую информацию предоставляет плевральная пункция и рентгенологическое исследование органов грудной клетки. При плевральной пункции получают мутную жидкость или типичный гной, посев которого на питательные среды позволяет поставить этиологический диагноз и определить чувствительность возбудителя к антибактериальным средствам. Рентгенологически обнаруживают эмпиему без деструкции или с деструкцией легочной ткани. Помимо рентгенографии легких, информацию, необходимую для уточнения характера поражения, дает КТ. В ряде случаев, особенно при эмпиеме неясной этиологии, необходимо проводить торакоскопию. О тяжести течения процесса можно судить по изменению анализов крови и мочи: нарастают гипохромная анемия и лейкоцитоз со сдвигом лейкоцитарной формулы влево. В моче присутствует белок, возможно обнаружение цилиндров. Диагностика Критерии установления диагноза: • определение характерных симптомов заболевания (боль в боку, сопровождающаяся шумом трения плевры, выпот в плевральной полости); • уточнение характера выпота; • определение основного заболевания, приведшего к развитию плеврита. Формулировка развернутого клинического диагноза должна учитывать: • этиологию плеврита (если есть точные сведения); • клинико-морфологическую форму (сухой, экссудативный, эмпиема плевры); • при осумкованных плевритах - локализацию (диафрагмальный, междолевой, медиастинальный и др.); • характер течения (острый, хронический, рецидивирующий). В формулировке диагноза допускают два варианта: • диагноз начинают с плеврита; • диагноз начинают с основного заболевания, а плеврит указывают в качестве осложнения. Лечение Лечебные мероприятия, проводимые больным плевритом, должны предусматривать : • воздействие на основное заболевание (этиологическое лечение). • патогенетическое лечение (с учетом характера выпота и клинико-морфологической формы плеврита); • устранение наиболее выраженного синдрома, определяющего тяжесть состояния; • повышение общей реактивности организма. В подавляющем большинстве случаев плеврит бывает симптомом какого-либо самостоятельного заболевания, поэтому назначают этиологическое лечение. При плевритах туберкулезной этиологии следует длительно (4-6 мес) проводить антибактериальную терапию. В первые 2 мес назначают противотуберкулезное лечение четырьмя препаратами: изониазидом (внутрь по 10 мг/кг) + пиразинамидом (внутрь по 20-25 мг/кг) + рифампицином (внутрь 10 мг/кг) + стрептомицином (внутримышечно по 16 мг/кг) или этамбутолом (внутрь по 20-25 мг/кг). Все препараты вводят 1 раз в сутки. Этамбутол назначают при высокой устойчивости туберкулезной палочки в регионе, где проживает больной, к стрептомицину и изониазиду. Продолжают лечение с помощью назначения двух схем: ежедневное применение изониазида в комбинации с рифампицином или их прием через день в течение 4 мес. Начинать лечение с применения противотуберкулезных препаратов можно также при плеврите неясной этиологии. При пневмонии антибиотики следует назначать с учетом чувствительности микрофлоры бронхиального содержимого к антибиотикам (см. раздел «Пневмония»). Если диагностированы системные заболевания соединительной ткани и аллергические состояния, то проводят иммуносупрессивную терапию, чаще всего - с помощью глюкокортикоидов. Патогенетическое лечение включает применение противовоспалительных и десенсибилизирующих препаратов, из которых наиболее эффективна ацетилсалициловая кислота (по 2-3 г/сут), фенилбутазон (по 0,15 г 3 раза в сутки), кальция хлорид (10% раствор по одной столовой ложке 4-5 раз в день). В ряде случаев при экссудативных плевритах, отличающихся торпидным течением с недостаточно быстрым рассасыванием выпота, с этой же целью назначают небольшие дозы преднизолона (10-20 мг/сут). При сухих плевритах и упорном сухом кашле назначают этилморфин, кодеин и другие противокашлевые препараты. Устранение наиболее выраженного синдрома, определяющего тяжесть состояния, заключается в эвакуации экссудата с помощью плевральной пункции, так как основные клинические симптомы обусловлены накоплением жидкости в плевральной полости. Эвакуация экссудата преследует две цели: предупреждение развития эмпиемы и устранение функциональных расстройств, связанных со сдавлением жизненно важных органов. Плевральную жидкость следует удалять в раннем периоде при больших выпотах, вызывающих одышку и смещение сердца, или если перкуторные границы тупости спереди доходят до II ребра. В целях предупреждения коллапса одномоментно рекомендуют эвакуировать не более 1,5 л жидкости. Разгрузочные пункции следует выполнять редко, так как при этом теряется много белка. Чтобы уменьшить накопление выпота, ограничивают питье, назначают мочегонные препараты и глюкокортикоиды. В остальных случаях плевральную пункцию с удалением экссудата лучше проводить в фазе стабилизации или даже резорбции, так как ранняя эвакуация выпота ведет к нарастанию отрицательного давления в плевральной полости, что способствует накоплению в ней экссудата. Небольшой по объему серозный экссудат, связанный с туберкулезом или другим инфекционным заболеванием, удалять необязательно, но при длительном отсутствии положительной динамики лучше прибегнуть к пункции и ввести внутриплеврально гидрокортизон (50-125 мг). При экссудативных плевритах, обусловленных неспецифическим инфекционным процессом, целесообразно удалять даже небольшой по объему выпот с введением в плевральную полость антибактериальных средств для профилактики эмпиемы. В комплексе лечебных мероприятий при острой эмпиеме плевры удаление гнойного экссудата и повторное введение в плевральную полость антибиотиков наиболее эффективно проводить в сочетании с общей антибактериальной терапией. Лечение хронической эмпиемы плевры может быть только оперативным. Для повышения общей реактивности организма проводят гигиенические мероприятия и используют физические методы воздействия. Больным сухим плевритом можно проводить лечение в домашних условиях. Необходимы покой, частое проветривание помещения, а при повышении температуры тела - постельный режим. Сохранили свое значение такие давние методы лечения, как согревающий компресс с тугим бинтованием нижних отделов грудной клетки, банки, смазывание кожи йодной настойкой и т.д. После исчезновения боли, нормализации температуры тела и СОЭ для предотвращения образования шварт больному рекомендуют выполнение дыхательной гимнастики. При экссудативных плевритах имеет значение диетотерапия: богатое витаминами (особенно аскорбиновой кислотой) и белками питание, ограничение приема воды и соли. Занятия ЛФК с включением дыхательных упражнений для предупреждения образования массивных плевральных спаек необходимо проводить уже в период рассасывания экссудата. После стихания острых явлений с этой же целью и для восстановления функции легких назначают ручной и вибрационный массаж. После курса медикаментозного лечения больных можно направлять на санаторно-курортное лечение в местные лесные санатории и курорты южного берега Крыма. Лица, перенесшие экссудативный плеврит туберкулезной этиологии, должны находиться под наблюдением в противотуберкулезном диспансере не менее двух лет. При эмпиеме плевры очень важны средства, повышающие специфическую и неспецифическую резистентность организма (у-глобулин, гипериммунная плазма). Для коррекции нарушений белкового и водно-солевого обмена выполняют внутривенные инфузии белковых препаратов, растворов электролитов, декстрозы и т.д. Прогноз Сухие и экссудативные плевриты (негнойные) никогда не определяют прогноз основного заболевания. Их исход зависит от эффективности лечения основного заболевания. Прогноз при гнойных плевритах и особенно при эмпиеме плевры всегда серьезный. Профилактика Основное направление профилактики плевритов - полноценное лечение заболеваний, при которых развивается плеврит. ЛЕГОЧНОЕ СЕРДЦЕ Легочное сердце (ЛС) - клинический синдром, обусловленный гипертрофией и (или) дилатацией правого желудочка, которые возникли в результате гипертензии малого круга кровообращения. Последняя, в свою очередь, развивается вследствие заболевания бронхов и легких, деформации грудной клетки или поражения легочных сосудов. В последнее время (2003) комитет экспертов ВОЗ придерживается следующего определения: «Cor pulpmonale (легочное сердце) - легочная АГ, служащая следствием заболеваний, нарушающих функцию и (или) структуру легких; легочная АГ приводит к развитию гипертрофии и дилатации правого желудочка и со временем может вызвать развитие правожелудочковой сердечной недостаточности». С этим определением отождествляют понятие «легочная гипертензия» (ЛГ) и ЛС. Классификация Б.Е. Вотчал (1964) предлагает классифицировать легочное сердце по четырем основным признакам (табл. 1-9): • характеру течения; • состоянию компенсации; • преимущественному патогенезу; • особенностям клинической картины. Таблица 1-9. Классификация легочного сердца (Вотчал Б.Е., 1964) 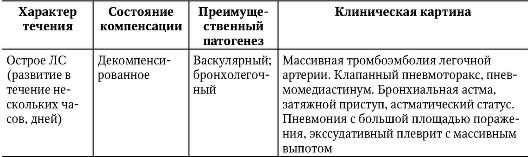 Окончание табл. 1-9 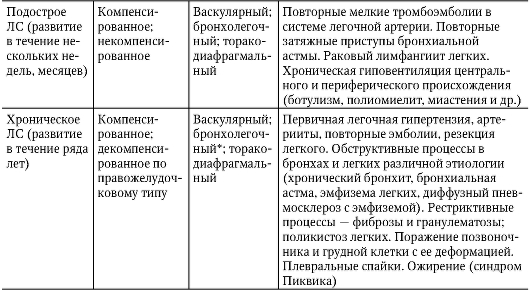 * При этом варианте можно использовать существующие классификации легочно-сердечной недостаточности. Примечания • Диагноз легочного сердца ставят после диагноза основного заболевания. При формулировке диагноза используют только первые две графы классификации. Графы 3 и 4 способствуют углубленному пониманию патофизиологической сущности процесса и выбору лечебной тактики. • Степень недостаточности кровообращения оценивают по общепринятой классификации. В зависимости от темпа развития легочной гипертензии различают острое, подострое и хроническое ЛС. При остром развитии ЛГ возникает в течение нескольких часов или дней, при подостром - нескольких недель или месяцев, при хроническом - в течение нескольких лет. Острое ЛС чаще всего (около 90% случаев) регистрируют при легочных эмболиях или внезапном повышении внутригрудного давления, подострое - при раковых лимфангиитах и торакодиафрагмальных поражениях. Хроническое ЛС в 80% случаев возникает при поражении бронхолегочной системы, причем у 90% таких пациентов заболевание связано с хроническими заболеваниями легких, сопровождающимися нарушением бронхиальной проходимости. Васкулярная и торакодиафрагмальная форма ЛС развивается в 20% случаев. Этиология Этиология хронического легочного сердца. Все заболевания, вызывающие хроническое ЛС, по классификации экспертов ВОЗ (1960) делят на три группы: • первично влияющие на прохождение воздуха в легких и альвеолах; • первично влияющие на движение грудной клетки; • первично поражающие легочные сосуды. К первой группе относят болезни, первично поражающие бронхолегочную систему (ХОБЛ, хронические бронхиты и пневмонии, эмфизема легких, фиброзы и гранулематозы легких, туберкулез, профессиональные заболевания легких и др.). Вторую группу составляют заболевания, ведущие к нарушению вентиляции вследствие патологических изменений подвижности грудной клетки (кифосколиоз, патология ребер и диафрагмы, болезнь Бехтерева, ожирение и др.). В роли этиологического фактора заболеваний третьей группы выступает первичное поражение легочных сосудов (повторные тромбоэмболии легочной артерии, васкулиты, первичная легочная гипертензия, атеросклероз легочной артерии и др.). Несмотря на то что к настоящему времени в мировой литературе известно около ста заболеваний, приводящих к развитию хронического ЛС, самыми частыми причинами остаются хронические респираторные заболевания (в первую очередь - ХОБЛ). Перечень основных хронических респираторных заболеваний приведен в табл. 1-10. Таблица 1-10. Хронические респираторные заболевания, приводящие к развитию лё- 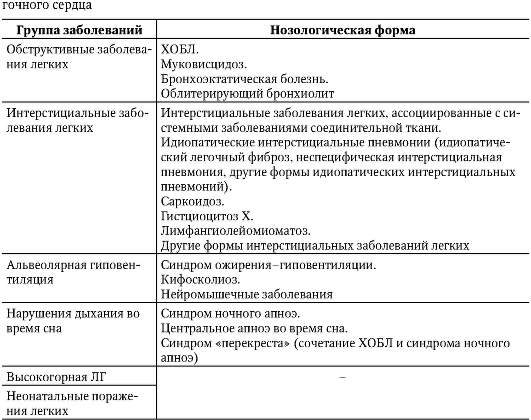 Патогенез Основной механизм формирования ЛС - повышение давления в системе легочной артерии - ЛГ. Критерий существования ЛГ при хронических респираторных заболеваниях - повышение среднего давления в легочной артерии в покое выше 20 мм рт.ст. (в норме этот показатель составляет 9-16 мм рт.ст.). Среди механизмов, приводящих к возникновению легочной гипертензии, различают анатомические и функциональные (рис. 1-7). К анатомическим механизмам относят: • закрытие просвета сосудов системы легочной артерии в результате облитерации или эмболизации; • сдавление легочной артерии извне; • значительное уменьшение русла малого круга кровообращения в результате пульмонэктомии. К функциональным механизмам относят: • сужение легочных артериол (вазоконстрикция) при низких значениях РаО2 (альвеолярная гипоксия) и высоких величинах РаСО2 в альвеолярном воздухе; • повышение давления в бронхиолах и альвеолах; 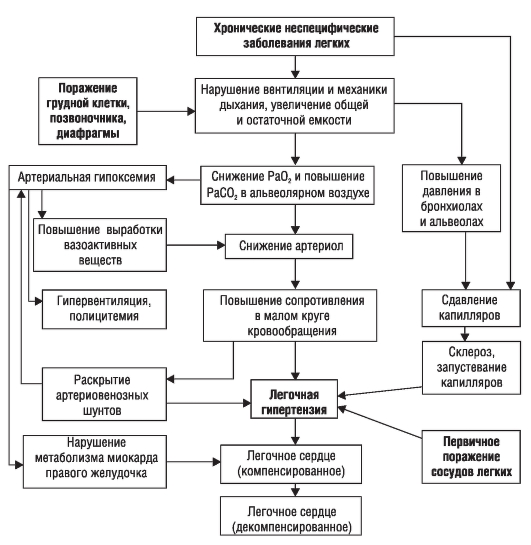 Рис. 1-7. Патогенез хронического легочного сердца • увеличение содержания в крови веществ и метаболитов прессорного действия; • увеличение минутного объема сердца; • повышение вязкости крови. Решающее значение в формировании ЛГ принадлежит функциональным механизмам. Ведущая роль среди них принадлежит вазоконстрикции легочных сосудов (артериол). Наиболее существенная причина, вызывающая сужение легочных сосудов, - альвеолярная гипоксия. Она особенно выражена при нарушениях бронхиальной проходимости. Кроме того, альвеолярная гипоксия возникает при гиповентиляции торакодиафрагмального происхождения. Альвеолярная гипоксия вызывает легочную вазоконстрикцию посредством прямых и непрямых механизмов. Прямой эффект гипоксии связан с развитием деполяризации гладкомышечных клеток сосудов и их сокращением, а также изменением функции калиевых каналов клеточных мембран. К непрямым механизмам относят воздействие на стенку сосудов таких эндогенных медиаторов, как лейкотриены, гистамин, серотонин, ангиотензин II и катехоламины. Все вышеперечисленные медиаторы относят к вазоконстрикторам; их продукция значительно усиливается в условиях гипоксии. Освобождение указанных медиаторов сопровождается отеком эндотелия капилляров, скоплением тромбоцитов (микротромбозы) и вазоконстрикцией. Рефлекс Эйлера-Лильестранда (спазм легочных артериол при уменьшении РаО2 в альвеолах) распространяется на сосуды, имеющие мышечный слой, в том числе и артериолы. Сужение последних также приводит к росту давления в легочной артерии. Другие нарушения газообмена, такие, как гиперкапния и ацидоз, также приводят к развитию ЛГ, в том числе за счет увеличения сердечного выброса. Альвеолярная гипоксия, вызывая артериальную гипоксемию, способствует повышению давления в легочной артерии, что приводит: • к увеличению минутного объема сердца через раздражение хеморецепторов аортально-каротидной зоны; • развитию полицитемии и увеличению вязкости крови; • повышению содержания молочной кислоты, других метаболитов и биогенных аминов (серотонин и др.), способствующих росту давления в легочной артерии; • резкой активизации ренин-ангиотензин-альдостероновой системы (РААС); • повреждению сосудистого эндотелия и увеличению выработки вазоконстриктора - эндотелина. Помимо этого артериальная гипоксемия приводит к уменьшению выработки сосудорасширяющих субстанций (простациклина, эндотелиального гиперполяризующего фактора, эндотелиального расслабляющего фактора), продуцируемых клетками сосудистого эндотелия легких в норме. Давление в легочной артерии повышается при сдавлении капилляров, обусловленном: • эмфиземой и повышением давления в альвеолах и бронхиолах (при непродуктивном надсадном кашле, интенсивной и физической нагрузке); • нарушением биомеханики дыхания и повышением внутригрудного давления в фазе затянувшегося выдоха (при бронхообструктивном синдроме). Сформировавшаяся ЛГ приводит к развитию гипертрофии правых отделов сердца (сначала - правого желудочка, затем - правого предсердия). В дальнейшем существующая артериальная гипоксемия вызывает возникновение дистрофических изменений в миокарде правых отделов сердца, что способствует более быстрому развитию сердечной недостаточности. Его также ускоряют токсическое влияние на миокард инфекционных процессов в легких, недостаточное снабжение миокарда кислородом, существующая ИБС, АГ и другие сопутствующие заболевания. На основании обнаружения признаков стойкой ЛГ и гипертрофии правого желудочка при отсутствии признаков сердечной недостаточности ставят диагноз компенсированного ЛС. При регистрации признаков правожелудочковой недостаточности диагностируют декомпенсированное ЛС. Клиническая картина Клиническая картина хронического легочного сердца включает симптомы: • основного заболевания, приведшего к развитию хронического ЛС; • дыхательной (легочной) недостаточности; • сердечной (правожелудочковой) недостаточности. Развитию хронического ЛС (как и возникновению гипертензии малого круга) обязательно предшествует легочная (дыхательная) недостаточность. Ее относят к категории так называемой вентиляционной дыхательной недостаточности, которая развивается вследствие нарушения функции дыхательной помпы и дыхательного центра. Дыхательная недостаточность - состояние организма, при котором невозможно поддержание нормального газового состава крови, либо это происходит в результате более интенсивной работы аппарата внешнего дыхания и повышенной нагрузки на сердце, что приводит к снижению функциональных возможностей организма. Выделяют три степени дыхательной недостаточности. При дыхательной недостаточности I степени одышка и тахикардия возникают лишь при повышенной физической нагрузке; цианоза нет. Показатели функции внешнего дыхания (минутный объем дыхания (МОД), ЖЕЛ) в покое соответствуют должным величинам, но при выполнении нагрузки изменяются; максимальная вентиляция легких (МВЛ) снижается. Газовый состав крови не изменен (недостатка кислорода в организме нет), функция кровообращения и кислотно-основное состояние (КОС) в норме. При дыхательной недостаточности II степени одышка и тахикардия возникают уже при незначительном физическом напряжении. Показатели легочных объемов (МОД, ЖЕЛ) отклонены от нормы, МВЛ значительно снижена. Выражен цианоз. В альвеолярном воздухе снижается РаО2 и увеличивается РаСО2. Содержание газов в крови благодаря перенапряжению вентиляции не изменено или незначительно изменено. Определяют дыхательный алкалоз. Возможно возникновение первых признаков нарушения кровообращения. При дыхательной недостаточности III степени одышка и тахикардия возникают в покое; резко выражен цианоз. Значительно снижена ЖЕЛ, а МВЛ не выполнима. Отмечают недостаточность кислорода в организме (гипоксемия) и избыток углекислоты (гиперкапния). При исследовании КОС обнаруживают дыхательный ацидоз. Выражены признаки сердечной недостаточности. Существует и иная классификация дыхательной недостаточности, степени тяжести в соответствии с которой определяют по газометрическим показателям (табл. 1-11). Таблица 1-11. Классификация дыхательной недостаточности по степеням тяжести 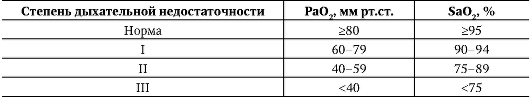 Несмотря на то что эта классификация универсальна и может иметь большое практическое значение (лечение дыхательной недостаточности II степени предполагает обязательное назначение кислородотерапии, а III стадии - респираторной поддержки), ее нельзя широко использовать в амбулаторной практике в связи с невозможностью определения PaO2 в артериальной крови. Понятия «дыхательная недостаточность» и «легочная недостаточность» близки друг к другу, но первый термин шире, чем второй, так как в него входит не только недостаточность внешнего дыхания, но и недостаточность транспорта газов от легких к тканям и от тканей к легким, а также недостаточность тканевого дыхания, развивающаяся при декомпенсированном ЛС. ЛС развивается на фоне дыхательной недостаточности II степени и чаще III степени. Симптомы последней сходны с таковыми сердечной недостаточности, поэтому перед врачом стоит трудная задача их дифференциальной диагностики и определения перехода компенсированного ЛС в декомпенсированное. Компенсированное легочное сердце. На первом этапе диагностического поиска обнаружить какие-нибудь специфические жалобы невозможно, так как их нет. Жалобы больных в этот период определяются основным заболеванием, а также той или иной степенью дыхательной недостаточности. На втором этапе диагностического поиска можно обнаружить прямой клинический признак гипертрофии правого желудочка - усиленную пульсацию, определяемую в прекардиальной области (в четвертом межреберье слева от грудины). При выраженной эмфиземе, когда сердце оттеснено от передней грудной стенки эмфизематозно расширенными легкими, обнаружить указанный признак удается редко. В то же время при эмфиземе легких эпигастральная пульсация, обусловленная усиленной работой правого желудочка, может возникать и при отсутствии его гипертрофии, в результате низкого стояния диафрагмы и опущения верхушки сердца. Аускультативных данных, специфичных для компенсированного ЛС, нет. Предположение о существовании ЛГ становится более вероятным при обнаружении акцента или расщепления II тона над легочной артерией. При высокой степени ЛГ можно выслушать диастолический шум Грэхема Стилла. Признаком компенсированного ЛС также считают громкий I тон над трехстворчатым клапаном по сравнению с I тоном над верхушкой сердца. Значение этих аускультативных признаков относительно, так как они могут отсутствовать у больных с выраженной эмфиземой легких. Решающим для диагностики компенсированного ЛС считают третий этап диагностического поиска, позволяющий обнаружить гипертрофию правых отделов сердца. Значение различных инструментальных методов диагностики неодинаково. Показатели функции внешнего дыхания отражают тип нарушения дыхания (обструктивный, рестриктивный, смешанный) и степень дыхательной недостаточности, но их нельзя использовать для дифференциальной диагностики компенсированного ЛС и дыхательной недостаточности. Рентгенологические методы позволяют обнаружить ранний признак ЛС - выбухание конуса легочной артерии (лучше определять в первом косом положении) и ее расширение. В этом случае можно отметить умеренное увеличение правого желудочка. ЭКГ - наиболее информативный метод диагностики ЛС. Существуют убедительные прямые ЭКГ-признаки гипертрофии правого желудочка и правого предсердия, коррелирующие со степенью легочной гипертензии: • R в V1 >=7 мм; • R/S в V1 >=1; • RV1+SV1 >=10,5 мм; • время внутреннего отклонения в отведении V1>= 0,03-0,05 с; • комплекс QR в отведении V1 (при отсутствии ИМ); • неполная блокада правой ножки пучка Гиса при R в V1 >10 мм; • полная блокада правой ножки пучка Гиса при R в V1 >15 мм; • инверсия зубца Т в отведении V1-V2. При обнаружении двух прямых признаков и более на ЭКГ диагноз ЛС считают достоверным. Большое значение имеет обнаружение признаков гипертрофии правого предсердия: (P-pulmonale) во II, III, aVF и правых грудных отведениях. Фонокардиография (ФКГ) может помочь в графическом обнаружении высокой амплитуды легочного компонента II тона и диастолического шума Грехема Стилла - признака ЛГ высокой степени. В настоящее время этот метод редко используют в диагностике ЛС. Не используют также такие бескровные методы исследования гемодинамики, по результатам которых можно было бы судить о величине давления в легочной артерии, как реопульмонография, кинетокардиография и др. Один из наиболее информативных неинвазивных методов оценки давления в легочной артерии - ЭхоКГ. Кроме этого она позволяет оценить размеры камер и толщину стенок сердца, сократительную и насосную функцию миокарда, динамику и форму внутрисердечных потоков. Использование М-режима, двухмерной ЭхоКГ и особенно импульсной допплерокардиографии, несмотря на легочную гиперинфляцию, затрудняющую диагностику, открывает возможность определения максимального систолического давления в легочной артерии, выраженности гипертрофии правого желудочка и др. Относительно новый метод диагностики ЛГ - МРТ. С ее помощью можно достаточно точно оценить толщину стенки, объем полости и фракцию выброса правого желудочка, но этот метод довольно дорог и доступен лишь в специализированных центрах. Радионуклидную вентрикулографию также относят к новым, неинвазивным, хорошо воспроизводимым методам оценки фракции выброса правого желудочка. Вместе с тем само значение этого показателя в диагностике ЛГ признают далеко не все, так как он не может служить истинным маркером дисфункции правого желудочка. Самый достоверный способ диагностики ЛГ - измерение давления в правом желудочке и легочной артерии с помощью катетера. В покое у здоровых людей верхний предел нормального систолического давления в легочной артерии равен 25 мм рт.ст. Тем не менее этот метод нельзя рекомендовать в качестве основного, так как его использование возможно лишь в специализированном стационаре. Нормальные показатели систолического давления в легочной артерии в покое не исключают диагноза ЛС. Известно, что уже при минимальных физических нагрузках, а также при обострении бронхолегочной инфекции и усилении бронхиальной обструкции оно начинает повышаться (более 25 мм рт.ст.) неадекватно нагрузке. При компенсированном ЛС венозное давление и скорость кровотока остаются в пределах нормы. Обсуждают значение повышения концентрации мозгового натрийуретического пептида как биологического маркера ЛГ. Считают, что при ЛС, развивающемся на фоне хронических респираторных заболеваний органов дыхания, содержание мозгового натрийуретического пептида в крови выше 33 пг/мл имеет важное диагностическое и прогностическое значение. Декомпенсированное легочное сердце. Диагностику декомпенсированного ЛС при несомненных признаках правожелудочковой недостаточности считают не сложной. Начальные стадии сердечной недостаточности при ЛС диагностировать затруднительно, так как ранний симптом сердечной недостаточности - одышка - не может служить подспорьем в этом случае. Это связано с тем, что она возникает у больных хроническими респираторными заболеваниями в качестве признака дыхательной недостаточности задолго до развития сердечной недостаточности. Вместе с тем анализ динамики жалоб и основных клинических симптомов позволяет обнаружить начальные признаки декомпенсации ЛС. На первом этапе диагностического поиска обнаруживают изменение характера одышки: она становится более постоянной, меньше зависит от погоды. Увеличивается частота дыханий, а при бронхиальной обструкции удлиняется выдох, и число дыханий может резко уменьшаться. После кашля интенсивность и длительность одышки возрастают, она не уменьшается после приема бронходилататоров. Одновременно нарастает дыхательная недостаточность, достигая III степени (одышка в покое). Прогрессирует утомляемость и снижается трудоспособность, возникают сонливость и головная боль (результат гипоксии и гиперкапнии). Больные могут жаловаться на боли в области сердца неопределенного характера. Их происхождение достаточно сложно и связано с сочетанием ряда факторов, в том числе метаболическими нарушениями в миокарде, его гемодинамической перегрузкой при ЛГ и недостаточным развитием коллатералей в гипертрофированном миокарде. Иногда боли в сердце могут сочетаться с выраженным удушьем, возбуждением и резким общим цианозом, что характерно для гипертонических кризов в системе легочной артерии. Внезапный подъем давления в легочной артерии объясняют раздражением барорецепторов правого предсердия и повышенным давлением крови в правом желудочке. Жалобы больных на отеки, тяжесть в правом подреберье и увеличение размеров живота при соответствующем (чаще всего - хроническом) легочном анамнезе позволяют заподозрить декомпенсированное ЛС. На втором этапе диагностического поиска можно обнаружить симптом постоянно набухших шейных вен, так как после присоединения к дыхательной еще и сердечной недостаточности шейные вены набухают не только на выдохе, но и на вдохе. На фоне диффузного цианоза (признак легочной недостаточности) развивается акроцианоз, пальцы и кисти рук становятся холодными на ощупь. Отмечают пастозность голеней и отеки нижних конечностей. Регистрируют постоянную тахикардию, причем в покое этот симптом более выражен, чем при нагрузке. Определяют выраженную эпигастральную пульсацию, обусловленную сокращениями гипертрофированного правого желудочка. При его дилатации может развиться относительная недостаточность трехстворчатого клапана, что обусловливает возникновение систолического шума у мечевидного отростка грудины. По мере развития сердечной недостаточности тоны сердца становятся глухими. Возможно повышение АД вследствие гипоксии. Следует помнить об увеличении печени как раннем признаке недостаточности кровообращения. Она может выступать из-под края реберной дуги у больных с эмфиземой и без признаков сердечной недостаточности. При развитии сердечной недостаточности на начальных стадиях обнаруживают увеличение преимущественно левой доли печени. Ее пальпация чувствительна или болезненна. По мере нарастания симптомов декомпенсации обнаруживают положительный симптом Плеша. Асцит и гидроторакс наблюдают редко и, как правило, при сочетании ЛС с ИБС или гипертонической болезнью (ГБ) стадии. Третий этап диагностического поиска имеет меньшую значимость в диагностике декомпенсированного ЛС. Рентгенологические данные позволяют обнаружить более выраженное увеличение правых отделов сердца и патологические изменения легочной артерии: • усиление сосудистого рисунка корней легких при относительно светлых периферических отделах; • расширение правой нисходящей ветви легочной артерии - важнейший рентгенологический признак ЛГ; • усиление пульсации в центре легких и ее ослабление в периферических отделах. На ЭКГ - прогрессирование симптомов гипертрофии правых желудочка и предсердия, часто - блокада правой ножки предсердно-желудочкового пучка (пучка Гиса) и нарушения ритма (экстрасистолы). При исследовании гемодинамики обнаруживают нарастание давления в легочной артерии (выше 45 мм рт.ст.), замедление скорости кровотока и повышение венозного давления. Последнее у больных ЛС свидетельствует о присоединении сердечной недостаточности (этот симптом не считают ранним). В крови можно обнаружить эритроцитоз (реакция на гипоксию), повышение гематокрита и увеличение вязкости крови, в связи с чем СОЭ у таких больных может оставаться нормальной даже при активности воспалительного процесса в легких. Диагностика При установлении диагноза компенсированного ЛС решающая роль принадлежит обнаружению гипертрофии правых отделов сердца (желудочка и предсердия) и ЛГ. В диагностике декомпенсированного ЛС основное значение помимо этого имеет обнаружение симптомов правожелудочковой сердечной недостаточности. Формулировка развернутого клинического диагноза учитывает: • основное заболевание, приведшее к формированию ЛС; • дыхательную недостаточность (степень выраженности); • ЛС (стадия) - компенсированное, декомпенсированное (указывают степень выраженности правожелудочковой недостаточности, т.е. ее стадию). Лечение Комплекс лечебных мероприятий включает воздействие: • на заболевание, послужившее причиной развития ЛС (так как наиболее частая причина - хронические респираторные заболевания, то в период обострения воспалительного процесса в бронхолегочной системе особая роль принадлежит проведению антибактериальной терапии; • на звенья патогенеза ЛС (восстановление нарушенной вентиляции и дренажной функции бронхов, улучшение бронхиальной проходимости, снижение легочной гипертензии, устранение правожелудочковой недостаточности). Улучшению бронхиальной проходимости способствуют уменьшение воспаления и отека слизистой оболочки бронхов (антибиотики, ингаляционные глюкокортикоиды) и ликвидация бронхоспазма (симпатомиметические средства, аминофиллин, особенно его препараты пролонгированного действия, холинолитические средства и блокаторы медленных кальциевых каналов). Бронхиальному дренажу способствуют средства, разжижающие мокроту, отхаркивающие препараты, а также постуральный дренаж и специальный комплекс ЛФК. Восстановление бронхиальной вентиляции и улучшение бронхиальной проходимости приводят к улучшению альвеолярной вентиляции и нормализации кислородтранспортной системы крови. Основную роль в улучшении вентиляции играет газовая терапия. • В связи с тем что альвеолярной гипоксии принадлежит главная роль в развитии ЛГ, коррекцию гипоксии с помощью кислорода считают наиболее обоснованным методом лечения. Оксигенотерапию проводят под контролем газов крови и показателей кислотно-основного состояния (в том числе длительную ночную терапию с содержанием кислорода во вдыхаемом воздухе около 30%). При необходимости используют гелиево-кислородную смесь. • Лечение вдыханием СО2 при резком снижении его содержания в крови, что возникает при выраженной гипервентиляции. Лучший метод борьбы с гиперкапнией и респираторным ацидозом - неинвазивная респираторная поддержка. • Обсуждают применение ингаляционного оксида азота (NO) в качестве мощного вазодилатирующего средства. По показаниям больному назначают дыхание с положительным давлением в конце выдоха (вспомогательная искусственная вентиляция легких или регулятор искусственного дыхания - небулятор Люкевича). Применяют специальный комплекс дыхательной гимнастики, направленный на улучшение легочной вентиляции. Не оправдало себя применение нового дыхательного аналептика - арманора8. Нормализации кислородтранспортной системы крови можно достичь: • увеличением поступления кислорода в кровь (гипербарическая оксигенация); • повышением кислородной функции эритроцитов с помощью экстракорпоральных методов (гемосорбция, эритроцитоферез и др.); • усилением отщепления кислорода в тканях (нитраты). Для снижения давления в легочной артерии пытаются применять различные группы лекарственных средств: теофиллины, салуретики, блокаторы альдостерона, а-адреноблокаторы, ингибиторы ангиотензинпревращающего фермента (АПФ) и особенно антагонисты рецепторов ангиотензина II. Применение вазодилататоров - блокаторов медленных кальциевых каналов, нитратов, гидралазина, празозина, - несмотря на их способность улучшать показатели легочной гемодинамики при краткосрочном применении, при длительном использовании (3 мес и более) положительного эффекта не оказывает. Наряду с этим применение вазодилататоров резко ограничено развитием серьезных побочных эффектов. Данные об эффективности ингибиторов АПФ неубедительны. В качестве перспективных препаратов для снижения давления в легочной артерии рассматривают антагонисты рецепторов ангитотензина II. В течение последних лет создано несколько новых перспективных препаратов, эффективность которых уже доказана в лечении больных первичной ЛГ. К числу таких лекарственных средств относят простациклин и его аналоги (в том числе илопрост для ингаляций), антагонисты рецепторов эндотелина (бозентан) и ингибиторы фосфодиэстеразы V типа (силденафил). Вспомогательную роль в снижении давления в легочной артерии могут играть препараты, замещающие релаксирующий фактор эндотелиального происхождения (молсидомин) и воздействие на микроциркуляторное русло, осуществляемое с помощью ксантинола нитотината, действующего на сосудистую стенку, а также гепарина натрия, дипиридамола и декстрана (ср. мол. масса 30 000-40 000), оказывающих благотворное действие на внутрисосудистое звено гемостаза. Возможно проведение кровопусканий (при эритроцитозе и других признаках плеторического синдрома). Показанием к кровопусканию (флеботомии) служит повышение гематокрита выше 65-70%. Его цель - снижение гематокрита до уровня менее 50%. Воздействие на правожелудочковую недостаточность проводят согласно принципам лечения сердечной недостаточности: мочегонные, антагонисты альдостерона, периферические вазодилататоры (эффективны пролонгированные нитраты). Вопрос о применении сердечных гликозидов решают индивидуально. Их эффективность у больных с ЛС отмечают только при его сочетании с патологическими изменениями левого желудочка и при развитии мерцательной аритмии. Диуретики следует назначать с осторожностью, начиная с небольших доз, так как чрезмерное сокращение объема внутрисосудистой жидкости может привести к уменьшению объема наполнения правого желудочка и снижению сердечного выброса, а также к повышению вязкости крови. Прогноз Неблагоприятным прогноз становится при возникновении признаков декомпенсации сердца и зависит от стадии сердечной недостаточности. Он более благоприятен при положительном эффекте от внутривенного введения аминофиллина и во многом определяется этиологией ЛС. Профилактика С целью предупреждения развития ЛС следует проводить активное лечение основных болезней (хронических респираторных заболеваний, васкулитов, ожирения и др.), вести активную профилактику тромбоэмболии легочной артерии (полноценное лечение тромбофлебитов вен нижних конечностей) и др. Глава 2. БОЛЕЗНИ ОРГАНОВ КРОВООБРАЩЕНИЯ Глава 3. БОЛЕЗНИ ОРГАНОВ ПИЩЕВАРЕНИЯ Глава 4. БОЛЕЗНИ ПОЧЕК Глава 5. БОЛЕЗНИ СИСТЕМЫ КРОВИ Глава 6. СИСТЕМНЫЕ ВАСКУЛИТЫ Глава 7. ДИФФУЗНЫЕ ЗАБОЛЕВАНИЯ СОЕДИНИТЕЛЬНОЙ ТКАНИ Глава 8. БОЛЕЗНИ СУСТАВОВ ЗАКЛЮЧЕНИЕ ЛИТЕРАТУРА |
