Справочный материал. Глава 23 – Сердечно-сосудистая система. Справочный материал по Физиологии. Глава 23 Сердечнососудистая система
 Скачать 0.85 Mb. Скачать 0.85 Mb.
|
|
Кровоснабжение сердца Стенку сердца снабжают кровью правая и левая венечные (коронарные) артерии. Обе венечные артерии отходят от основания аорты (вблизи места прикрепления створок аортального клапана). Задняя стенка левого желудочка, некоторые отделы перегородки и большая часть правого желудочка кровоснабжаются правой венечной артерией. Остальные отделы сердца получают кровь из левой венечной артерии (рис. 23–2). 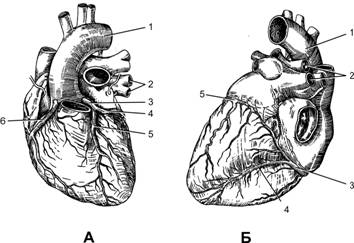 Рис. 23–2. Венечные артерии сердца [10]. А — по передней стенке сердца: 1 — аорта, 2 — лёгочные вены, 3 — левая венечная артерия, 4 — огибающая ветвь левой венечной артерии, 5 — передняя межжелудочковая ветвь левой венечной артерии, 6 — правая венечная артерия; Б — по задней стенке сердца: 1 — аорта, 2 — лёгочные вены, 3 — правая венечная артерия, 4 — задняя межжелудочковая ветвь правой венечной артерии, 5 — огибающая ветвь левой венечной артерии. При сокращении левого желудочка миокард пережимает венечные артерии, и поступление крови к миокарду практически прекращается — 75% крови по венечным артериям притекает к миокарду во время расслабления сердца (диастолы) и низкого сопротивления сосудистой стенки. Для адекватного коронарного кровотока диастолическое давление крови не должно опускаться ниже 60 мм рт.ст. При физической нагрузке коронарный кровоток усиливается, что связано с увеличением работы сердца по снабжению мышц кислородом и питательными веществами. Венечные вены, собирая кровь от большей части миокарда, впадают в венечный синус в правом предсердии. От некоторых областей, расположенных преимущественно в «правом сердце», кровь поступает непосредственно в сердечные камеры. Ишемическая болезнь сердца (ИБС) развивается вследствие локального сужения просвета крупной или среднего калибра венечной артерии из-за наличия атеросклеротической бляшки. В этом случае коронарный кровоток усиливаться не может, что необходимо в первую очередь при физической нагрузке, поэтому при ИБС физическая активность приводит к возникновению болей в сердце. Кровоснабжение плода Обогащённая кислородом кровь (см. рис. 20–7) с относительно низкой концентрацией СО2 из плаценты по пупочной вене поступает в печень, а из печени — в нижнюю полую вену. Часть крови из пупочной вены через венозный проток, минуя печень, сразу попадает в систему нижней полой вены. В нижней полой вене происходит перемешивание крови. Кровь с высоким содержанием СО2 поступает в правое предсердие из верхней полой вены, которая собирает кровь из верхней части тела. Через овальное отверстие (отверстие в межпредсердной перегородке) часть крови поступает из правого предсердия в левое. При сокращении предсердий клапан закрывает овальное отверстие, и кровь из левого предсердия поступает в левый желудочек и далее в аорту, т.е. в большой круг кровообращения. Из правого желудочка кровь направляется в лёгочную артерию, которая артериальным (боталловым) протоком связана с аортой. Следовательно, через артериальный проток и овальное отверстие сообщаются малый и большой круги кровообращения. На ранних этапах внутриутробной жизни потребность в крови в несформированных лёгких, куда перекачивает кровь правый желудочек, ещё не велика. Поэтому степень развития правого желудочка определяется уровнем развития лёгких. По мере развития лёгких и увеличения их объёма всё больше крови направляется к ним и всё меньше проходит через артериальный проток. Закрытие артериального протока происходит вскоре после рождения (в норме — до 8 нед жизни), когда лёгкие начинают получать всю кровь из правых отделов сердца. После рождения перестают функционировать и редуцируются, превращаясь в соединительнотканные тяжи, и другие сосуды (сосуды пуповины и венозный проток). Овальное отверстие закрывается также после рождения. Иннервация сердца Работу сердца контролируют сердечные центры продолговатого мозга и моста через парасимпатические и симпатические волокна (рис. 23–3). Холинергические и адренергические (преимущественно безмиелиновые) волокна образуют в стенке сердца несколько нервных сплетений, содержащих внутрисердечные ганглии. Скопления ганглиев в основном сосредоточены в стенке правого предсердия и в области устьев полых вен. 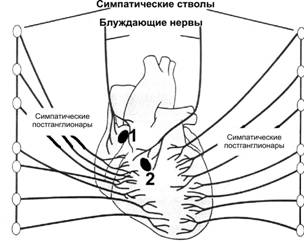 Рис. 23–3. Иннервация сердца. 1 — синусно-предсердный узел, 2 — предсердно-желудочковый узел (АВ-узел). Парасимпатическая иннервация. Преганглионарные парасимпатические волокна для сердца проходят в составе блуждающего нерва с обеих сторон. Волокна правого блуждающего нерва иннервируют правое предсердие и образуют густое сплетение в области синусно-предсердного узла. Волокна левого блуждающего нерва подходят преимущественно к АВ-узлу. Именно поэтому правый блуждающий нерв оказывает влияние главным образом на ЧСС, а левый — на АВ-проведение. Желудочки имеют менее выраженную парасимпатическую иннервацию. Внутрисердечные нейроны почти все холинергические (парасимпатические). На них, а также на МИФ клетках (малых интенсивно флюоресцирующих клетках — разновидности нейронов, находящихся практически во всех вегетативных ганглиях), заканчиваются терминали холинергических аксонов блуждающего нерва. Эффекты парасимпатической иннервации: сила сокращений предсердий уменьшается — отрицательный инотропный эффект, ЧСС снижается — отрицательный хронотропный эффект, предсердно-желудочковая задержка проведения увеличивается — отрицательный дромотропный эффект. Симпатическая иннервация. Преганглионарные симпатические волокна для сердца идут от боковых рогов верхних грудных сегментов спинного мозга. Постганглионарные адренергические волокна образованы аксонами нейронов ганглиев симпатической нервной цепочки (звёздчатый и отчасти верхний шейный симпатические узлы). Они подходят к органу в составе нескольких сердечных нервов и равномерно распределяются по всем отделам сердца. Терминальные ветви пронизывают миокард, сопровождают венечные сосуды и подходят к элементам проводящей системы. Миокард предсердий имеет более высокую плотность адренергических волокон. Каждый пятый кардиомиоцит желудочков снабжается адренергической терминалью, заканчивающейся на расстоянии 50 мкм от плазмолеммы кардиомиоцита. Эффекты симпатической иннервации: сила сокращений предсердий и желудочков увеличивается — положительный инотропный эффект, ЧСС возрастает — положительный хронотропный эффект, интервал между сокращениями предсердий и желудочков (т.е. задержка проведения в АВ-соединении) укорачивается — положительный дромотропный эффект. В целом стимуляция симпатических нервов увеличивает скорость спонтанной деполяризации мембран водителей ритма (т.е. ЧСС), облегчает проведение ПД в волокнах Пуркинье и увеличивает частоту и силу сокращения рабочих кардиомиоцитов; стимуляция парасимпатических нервов, наоборот, уменьшает частоту генерации импульсов пейсмейкерами, снижает скорость проведения ПД в волокнах Пуркинье и уменьшает силу сокращения и ЧСС. Между симпатической и парасимпатической иннервацией существуют реципрокные тормозные отношения. Ацетилхолин действует пресинаптически, уменьшая выделение норадреналина из симпатических нервов. Нейропептид Y, выделяющийся из норадренергических окончаний, тормозит выделение ацетилхолина. Афферентная иннервация. Чувствительные нейроны ганглиев блуждающих нервов и спинномозговых узлов (C8–Th6) образуют свободные и инкапсулированные нервные окончания в стенке сердца. Афферентные волокна проходят в составе блуждающих и симпатических нервов. Свойства миокарда Основные свойства сердечной мышцы — возбудимость, автоматизм, проводимость, сократимость. Возбудимость Возбудимость — свойство отвечать на раздражение электрическим возбуждением в виде изменений мембранного потенциала (МП) с последующей генерацией ПД. Электрогенез в виде МП и ПД определяется разностью концентраций ионов по обе стороны мембраны, а также активностью ионных каналов и ионных насосов. Через пору ионных каналы ионы проходят по электрохимическому градиенту, тогда как ионные насосы обеспечивают движение ионов против электрохимического градиента. В кардиомиоцитах наиболее распространённые каналы — для ионов Na+, K+, Ca2+ и Cl–. Типы ионных каналов кардиомиоцитов суммированы в табл. 23–1. Таблица 23–1. Ионные каналы кардиомиоцитов
МП покоя кардиомиоцита составляет –90 мВ. Стимуляция порождает распространяющийся ПД, вызывающий сокращение (рис. 23–4). Деполяризация развивается быстро, как в скелетной мышце и нерве, но, в отличие от последних, МП возвращается к исходному уровню не сразу, а постепенно. 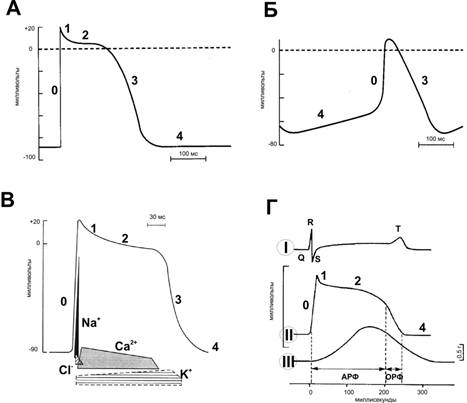 Рис. 23–4. Потенциалы действия. А — Желудочек. Б — Синусно-предсердный узел. В — Ионная проводимость. I — ПД, регистрируемый с поверхностных электродов; II — внутриклеточная регистрация ПД; III — Механический ответ. Г — Сокращение миокарда. АРФ — абсолютная рефрактерная фаза; ОРФ — относительная рефрактерная фаза. 0 — деполяризация; 1 — начальная быстрая реполяризация; 2 — фаза плато; 3 — конечная быстрая реполяризация; 4 — исходный уровень. Деполяризация длится около 2 мс, фаза плато и реполяризация продолжаются 200 мс и более. Как и в других возбудимых тканях, изменение внеклеточного содержания K+ влияет на МП; изменения внеклеточной концентрации Na+ воздействуют на величину ПД. Быстрая начальная деполяризация (фаза 0) возникает вследствие открытия потенциалозависимых быстрых Na+ каналов, ионы Na+ быстро устремляются внутрь клетки и меняют заряд внутренней поверхности мембраны с отрицательного на положительный. Начальная быстрая реполяризация (фаза 1) — результат закрытия Na+ каналов, входа в клетку ионов Cl– и выхода из неё ионов K+. Последующая продолжительная фаза плато (фаза 2 — МП некоторое время сохраняется приблизительно на одном уровне) — результат медленного открытия потенциалозависимых Ca2+ каналов: ионы Ca2+ поступают внутрь клетки, равно как ионы и Na+, при этом ток ионов K+ из клетки сохраняется. Конечная быстрая реполяризация (фаза 3) возникает в результате закрытия Ca2+ каналов на фоне продолжающегося выхода K+ из клетки через K+ каналы. В фазу покоя (фаза 4) происходит восстановление МП за счёт обмена ионов Na+ на ионы K+ посредством функционирования специализированной трансмембранной системы — Na+-К+ насоса. Указанные процессы касаются именно рабочего кардиомиоцита; в клетках водителя ритма фаза 4 несколько отличается. Быстрый Na+ канал имеет наружные и внутренние ворота. Наружные ворота открываются в начале деполяризации, когда МП равен –70 или –80 мВ; при достижении критического значения МП внутренние ворота закрываются и предотвращают дальнейший вход ионов Na+ до тех пор, пока ПД не прекратится (инактивация Na+ канала). Медленный Ca2+ канал активируется небольшой деполяризацией (МП в пределах от –30 до –40 мВ). Сокращение начинается сразу после начала деполяризации и продолжается в течение всего ПД. Роль Ca2+ в сопряжении возбуждения с сокращением подобна его роли в скелетной мышце (см. главу 6 Ы Отсылка. Ы). Однако в миокарде триггером, активирующим T-систему и вызывающим выделение Ca2+ из саркоплазматической сети, выступает не сама деполяризация, а внеклеточный Ca2+, поступающий внутрь клетки во время ПД. На протяжении фаз 0–2 и примерно до середины фазы 3 (до достижения МП во время реполяризации уровня –50 мВ) мышца сердца не может быть возбуждена снова. Она находится в состоянии абсолютного рефрактерного периода, т.е. состоянии полной невозбудимости. После абсолютного рефрактерного периода возникает состояние относительной рефрактерности, в котором миокард остаётся до фазы 4, т.е. до возвращения МП к исходному уровню. В период относительной рефрактерности сердечная мышца может быть возбуждена, но только в ответ на очень сильный стимул. Сердечная мышца не может, как скелетная мышца, находиться в тетаническом сокращении. Тетанизация (стимуляция высокой частотой) сердечной мышцы в течение сколько-нибудь продолжительного времени приведёт к летальному исходу. Мускулатура желудочков должна быть рефрактерной; говоря иными словами, быть в «периоде неуязвимости» до конца ПД, поскольку стимуляция миокарда в этот период может вызывать фибрилляцию желудочков, которая при достаточной длительности фатальна для больного. Автоматизм и проводимость Автоматизм — способность пейсмейкерных клеток инициировать возбуждение спонтанно, без участия нейрогуморального контроля. Возбуждение, приводящее к сокращению сердца, возникает в специализированной проводящей системе сердца и распространяется посредством неё ко всем частям миокарда. Проводящая система сердца. Структуры, входящие в состав проводящей системы сердца, — синусно-предсердный узел, межузловые предсердные пути, АВ-соединение (нижняя часть проводящей системы предсердий, прилегающая к АВ-узлу, собственно АВ-узел, верхняя часть пучка Хиса), пучок Хиса и его ветви, система волокон Пуркинье (рис. 23–5). 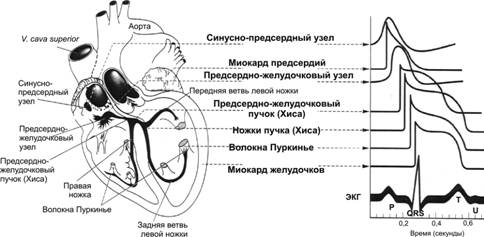 Рис. 23–5. Слева — проводящая система сердца. Справа — типичные ПД [синусового (синусно-предсердного) и АВ-узлов (предсердно-желудочкового), других частей проводящей системы и миокарда предсердий и желудочков] в корреляции с ЭКГ. Водители ритма. Все отделы проводящей системы способны генерировать ПД с определённой частотой, определяющей в конечном итоге ЧСС, — т.е. быть водителем ритма. Однако синусно-предсердный узел генерирует ПД быстрее других отделов проводящей системы, и деполяризация от него распространяется в другие участки проводящей системы прежде, чем они начнут спонтанно возбуждаться. Таким образом, синусно-предсердный узел — ведущий водитель ритма, или водитель ритма первого порядка. Частота его спонтанных разрядов определяет частоту биений сердца (в среднем 60–90 в минуту). Функциональная анатомия проводящей системы сердца Топография. Синусно-предсердный узел располагается в месте впадения верхней полой вены в правое предсердие. Предсердно–желудочковый узел (АВ-узел) находится в правой задней части межпредсердной перегородки, непосредственно позади трёхстворчатого клапана. Связь между синусно-предсердным и АВ-узлами осуществляется двумя путями: диффузно миоцитами предсердия и по специальным внутрисердечным проводящим пучкам. АВ-узел служит только проводящим путём между предсердиями и желудочками. Он продолжается в пучок Хиса, подразделяющийся на левую и правую ножки и мелкие пучки. Левая ножка пучка Хиса, в свою очередь, делится на переднюю и заднюю ветви. Ножки и пучки проходят под эндокардом, где контактируют с системой волокон Пуркинье; последние распространяются ко всем частям миокарда желудочков. Асимметрия вегетативной иннервации. Синусно-предсердный узел происходит из эмбриональных структур правой стороны тела, а АВ-узел — из структур левой стороны тела. Это объясняет факт, почему правый блуждающий нерв преимущественно распределён в синусно-предсердном узле, а левый блуждающий нерв — в АВ-узле. Соответственно, симпатическая иннервация правой стороны распределена преимущественно в синусно-предсердном узле, симпатическая иннервация левой стороны — в АВ-узле. Потенциалы действия. В правой части рис. 23–5 представлены типичные трансмембранные потенциалы для синусно-предсердного и АВ-узлов, а также других отделов проводящей системы: ствола Хиса, ножек пучка Хиса, волокон Пуркинье, предсердной и желудочковой мышц и их корреляция с электрической активностью, зарегистрированной внеклеточно — электрокардиограммой. Пейсмейкерные потенциалы МП пейсмейкерных клеток после каждого ПД возвращается к пороговому уровню возбуждения. Этот потенциал, называемый препотенциалом (пейсмейкерным потенциалом) — триггер для следующего потенциала (рис. 23–6А). На пике каждого ПД после деполяризации возникает калиевый ток, приводящий к запуску процессов реполяризации. Когда калиевый ток и выход ионов K+ уменьшаются, мембрана начинает деполяризоваться, формируя первую часть препотенциала. Открываются Ca2+ каналы двух типов: временно открывающиеся Ca2+в каналы и длительно действующие Ca2+д каналы. Кальциевый ток, идущий по Ca2+в каналам, образует препотенциал, кальциевый ток в Ca2+д каналах создаёт ПД. 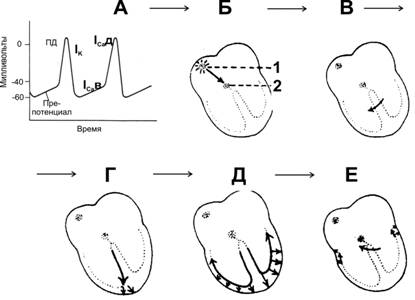 |
