Справочный материал. Глава 23 – Сердечно-сосудистая система. Справочный материал по Физиологии. Глава 23 Сердечнососудистая система
 Скачать 0.85 Mb. Скачать 0.85 Mb.
|
|
Рис. 23–6. РАСПРОСТРАНЕНИЕ ВОЗБУЖДЕНИЯ ПО СЕРДЦУ. А. Потенциалы пейсмейкерной клетки. IK, ICaд, ICaв — ионные токи, соответствующие каждой части пейсмейкерного потенциала. Б–Е. Распространение электрической активности в сердце. 1 — синусно-предсердный узел. 2 — предсердно-желудочковый (АВ) узел. ПД в синусно-предсердном и АВ-узлах создаются главным образом ионами Ca2+ и некоторым количеством ионов Na+. У этих потенциалов отсутствует фаза быстрой деполяризации перед фазой плато, которая имеется в других частях проводящей системы и в волокнах предсердия и желудочков. Стимуляция парасимпатического нерва, иннервирующего ткани синусно-предсердного узла, гиперполяризует мембрану клеток и тем самым уменьшает скорость возникновения препотенциала действия. Ацетилхолин, выделяемый нервными окончаниями, открывает специальные ацетилхолин–зависимые K+ каналы в пейсмейкерных клетках, повышая проницаемость мембраны для ионов K+ (что увеличивает положительный заряд наружной стороны клеточной мембраны и ещё больше усиливает отрицательный заряд внутренней стороны клеточной мембраны) Кроме того, ацетилхолин активирует мускариновые M2-рецепторы, что приводит к понижению уровня цАМФ в клетках и замедлению открытия медленных Ca2+ каналов в период диастолы. В результате замедляется скорость спонтанной диастолической деполяризации. Необходимо учитывать, что сильная стимуляция блуждающего нерва (например, при массаже каротидного синуса) может на некоторое время полностью останавливать процессы генерации импульсов в синусно-предсердном узле. Стимуляция симпатических нервов ускоряет деполяризацию и увеличивает частоту генерирования ПД. Норадреналин, взаимодействуя в том числе с 1 адренорецепторами, повышает внутриклеточное содержание цАМФ, открывает Ca2+д каналы, увеличивает ток ионов Ca2+ в клетку и ускоряет спонтанную диастолическую деполяризацию (фазу 0 ПД). Частота разрядов синусно-предсердного и АВ-узлов подвержена влиянию температуры и различных биологически активных веществ (например, повышение температуры увеличивает частоту разрядов). Распространение возбуждения по сердечной мышце Деполяризация, возникающая в синусно-предсердном узле, распространяется радиально по предсердиям и затем сходится (конвергирует) в АВ-соединении (рис. 23–6). Деполяризация предсердий полностью завершается в течение 0,1 с. Так как проведение в АВ-узле происходит медленнее по сравнению с проведением в миокарде предсердий и желудочков (табл. 23–2), возникает предсердно-желудочковая (АВ-) задержка длительностью 0,1 с, после которой возбуждение распространяется на миокард желудочков. Продолжительность предсердно-желудочковой задержки сокращается при стимуляции симпатических нервов сердца, тогда как под влиянием раздражения блуждающего нерва её длительность увеличивается. Таблица 23–2. Скорость проведения возбуждения (м/с) в тканях сердца
От основания межжелудочковой перегородки волна деполяризации с большой скоростью распространяется по системе волокон Пуркинье ко всем частям желудочка в течение 0,08–0,1 с. Деполяризация миокарда желудочка начинается с левой стороны межжелудочковой перегородки и распространяется прежде всего вправо сквозь среднюю часть перегородки. Затем волна деполяризации проходит по перегородке вниз к верхушке сердца. Вдоль стенки желудочка она возвращается к АВ-узлу, переходя с субэндокардиальной поверхности миокарда на субэпикардиальную. Пучок Хиса. Кардиомиоциты этого пучка проводят возбуждение от АВ-соединения к волокнам Пуркинье. Проводящие кардиомиоциты пучка Хиса входят также в состав синусно-предсердного и предсердно-желудочкового узлов. Волокна Пуркинье. Проводящие кардиомиоциты волокон Пуркинье — самые крупные клетки миокарда. Кардиомиоциты волокон Пуркинье не имеют Т-трубочек и не образуют вставочных дисков. Они связаны с помощью десмосом и щелевых контактов. Последние занимают значительную площадь контактирующих клеток, что обеспечивает наиболее высокую скорость проведения возбуждения по миокарду желудочков. Нарушения автоматизма и проводимости Патология синусно-предсердного узла Синусовая брадикардия может быть физиологической (например, у тренированных спортсменов) и патологической. При снижении ЧСС до 35 в минуту может произойти потеря сознания, что опасно возникновением различных осложнений (вплоть до летального исхода). Синдром слабости синусно-предсердного узла — нарушение образования импульсов в синусно-предсердном узле, что приводит к брадикардии и длительным паузам в его работе. Клинически синдром проявляется брадикардией и обмороками. Остановка синусно-предсердного узла — прекращение генерации импульсов. Пауза, превышающая 10–20 с, ведёт к потере сознания — развивается гипоксия головного мозга, что сопровождается судорожным синдромом (синдромом Морганьи–Адамса–Стокса). Патология АВ-узла. Блокаду АВ-узла обозначают термином «АВ-блокада». При ней в разной степени затрудняется проведение возбуждения к пучку Хиса и сократительному миокарду. При крайне выраженной АВ-блокаде (полном прекращении АВ-проведения) предсердия и желудочки сокращаются каждые в своём ритме: для предсердий водителем ритма выступает синусно-предсердный узел, а для желудочков — АВ-соединение. Полная АВ-блокада ввиду редкого ритма сокращения желудочков также может приводить к обморокам, во время которых возможен летальный исход. Причины АВ-блокад — инфаркт миокарда, миокардит; иногда причину поражения проводящей системы установить не удаётся (идиопатическая АВ-блокада). Кроме того, блокада может наступить вследствие применения препаратов, оказывающих отрицательный дромотропный эффект на проводящую систему (сердечные гликозиды, блокаторы медленных кальциевых каналов и -адреноблокаторы). Блокады ножек пучка Хиса характеризуются полным прекращением проведения возбуждения по левой (одновременно по её передней и задней ветвям) или правой ножке предсердно-желудочкового пучка. Возможно нарушения проведения изолированно по передней или задней ветви левой ножки пучка Хиса. Дополнительные проводящие пути (рис. 23–6–1) — аномальные проводящие пути, по которым возбуждение способно распространяться «в обход» нормальной проводящей системы от предсердий к желудочкам. Эти дополнительные проводящие пути не обладают свойством задерживать проведение возбуждения (как это происходит в АВ-соединении), что не только нарушает внутрисердечную гемодинамику (желудочки сокращаются до того, как успеют заполниться кровью из предсердий, для чего и необходима АВ-задержка), но вследствие аномального маршрута распространения возбуждения может привести к серьёзным аритмиям, зачастую представляющим опасность для жизни больного. Так, функционирование дополнительного пути проведения, называемого пучком Кента, обусловливает развитие синдрома Вольффа–Паркинсона–Уайта. 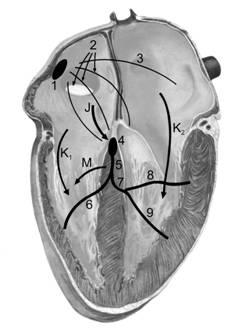 Рис. 23–6–1. Дополнительные проводящие пути сердца [17]. 1 — синусно-предсердный узел, 2 — межузловые проводящие пути, 3 — пучок Бахмана, 4 — АВ-соединение, 5 — пучок Хиса, 6 — правая ножка пучка Хиса, 7 — левая ножка пучка Хиса, 8 — передняя ветвь левой ножки пучка Хиса, 9 — задняя ветвь левой ножки пучка Хиса; К1 и К2 — пучки Кента, J — пучок Джеймса, М — пучок Махейма Бахмана пучок начинается от синусно предсердного узла, часть волокон расположена между предсердиями (межпредсердный пучок к ушку левого предсердия), часть волокон направляется к предсердно желудочковому узлу (передний межузловой тракт). Венкебаха пучок начинается от синусно предсердного узла, его волокна направляются в левое предсердие и к предсердно желудочковому узлу (средний межузловой тракт). Джеймса пучок соединяет одно из предсердий с АВ-соединением или проходит внутри этого соединения, по этому пучку возбуждение может преждевременно распространиться на желудочки. Пучок Джеймса важен для понимания патогенеза синдрома Лауна–Генона–Ливайна. Более быстрое распространение импульса при этом синдроме через дополнительный проводящий путь приводит к укорочению интервала PR (PQ), однако расширения комплекса QRS нет, поскольку возбуждение распространяется от АВ-соединения обычным путём. Кента пучок — дополнительное предсердно-желудочковое соединение — аномальный пучок между левым предсердием и одним из желудочков. Этот пучок играет важную роль в патогенезе синдрома Вольффа–Паркинсона–Уайта. Более быстрое распространение импульса через этот дополнительный проводящий путь приводит к: 1) укорочению интервала PR (PQ); 2) более раннему возбуждению части желудочков — возникает волна , обусловливающая расширение комплекса QRS. Махейма пучок (атриофасцикулярный тракт). Патогенез синдрома Махейма объясняется наличием дополнительного проводящего пути, связывающего пучок Хиса с желудочками. При проведении возбуждения через пучок Махейма импульс распространяется через предсердия к желудочкам обычным путём, а в желудочках часть их миокарда возбуждается преждевременно в связи с наличием дополнительного проводящего пути. Интервал PR (PQ) при этом нормальный, а комплекс QRS уширен из-за волны . Гетеротопические очаги возбуждения — участки миокарда, генерирующие возбуждение и подавляющие активность (временно на одно сокращение или постоянно) нормального водителя ритма (синусно-предсердного узла). В итоге сокращение всего сердца инициируется именно этим активным участком миокарда, выступающим гетеротопическим водителем ритма. Экстрасистола — преждевременное (внеочередное) сокращение сердца, инициированное возбуждением, исходящим из миокарда предсердий, AВ-соединения или желудочков. Экстрасистола прерывает доминирующий (обычно синусовый) ритм. Во время экстрасистолы пациенты обычно ощущают перебои в работе сердца. Пароксизмальная тахикардия — внезапно начинающиеся и внезапно прекращающиеся приступы тахикардии — возникает в результате активности гетеротопических очагов автоматизма или (чаще) патологической циркуляции волны возбуждения по миокарду (соответственно пароксизмальная тахикардия может быть предсердной, АВ-узловой и желудочковой). Желудочковая пароксизмальная тахикардия возникает при наличии гетеротопического очага автоматизма в желудочках сердца и/или при патологической циркуляции волны возбуждения по миокарду. Сократимость Свойство сократимости миокарда обеспечивает контрактильный аппарат кардиомиоцитов, связанных в функциональный синцитий при помощи ионопроницаемых щелевых контактов. Это обстоятельство синхронизирует распространение возбуждения от клетки к клетке и сокращение кардиомиоцитов. Увеличение силы сокращения миокарда желудочков — положительный инотропный эффект катехоламинов — опосредовано 1 адренорецепторами (через эти рецепторы действует также симпатическая иннервация) и цАМФ. Сердечные гликозиды также усиливают сокращения сердечной мышцы, оказывая ингибирующее влияние на Na+,K+ АТФазу в клеточных мембранах кардиомиоцитов. Сердечная недостаточность Сердечная недостаточность — нарушение способности сердца обеспечивать кровоснабжение органов и тканей в соответствии с их метаболическими потребностями. Наиболее распространённая причина сердечной недостаточности — нарушение сократительной способности миокарда, вследствие чего насосная функция сердца становится недостаточной. Другие причины — увеличение постнагрузки (т.е. сердцу приходится перекачивать кровь из сердца в аорту и лёгочные артерии с большими усилиями из-за затруднения кровотока «после сердца»), изменения преднагрузки (т.е. на нагрузка на сердце возрастает и ему приходится больше работать из-за увеличения, например, притока крови к сердцу и увеличения в нём давления в диастолу — нагрузка увеличивается «перед сердцем»). Сердечная недостаточность — «конечная точка» любого заболевания сердца. Практически любой кардиологический больной имеет сердечную недостаточность различной степени выраженности. Сердечная недостаточность на ранних этапах обычно затрагивает только один круг кровообращения — большой или малый. При поражении левых отделов сердца возникающая левожелудочковая сердечная недостаточность будет характеризоваться застоем по малому кругу кровообращения. Застой приводит к повышению давления в сосудах лёгких — лёгочной гипертензии. Первое и наиболее распространённое клиническое проявление — одышка при физической нагрузке. Самые тяжёлые и опасные проявления левожелудочковой сердечной недостаточности — отёк лёгких (вследствие избытка крови «до левых отделов сердца») и кардиогенный шок (вследствие катастрофического недостатка перекачивания крови в большой круг кровообращения). При поражении правых отделов сердца возникает правожелудочковая сердечная недостаточность. Она характеризуется застоем крови в большом круге кровообращения (в венозном русле, обладающем значительными возможностями депонирования крови) и клинически характеризуется отёками, увеличением печени, набуханием вен шеи. При максимально выраженной сердечной недостаточности (особенно в её терминальную стадию) застойные явления возникают в обоих кругах кровообращения. Снижение сократительной способности может быть обусловлено следующими причинами. Инфаркт миокарда — некроз участка сердечной мышцы, соответственно с потерей его способности к сокращению. В острую стадию инфаркта миокарда снижение сократительной способности выражено в максимальной степени (исчезает сократимость некротизированной ткани и существенно снижается сократимость близрасположенных участков миокарда), что при вовлечении более 50% миокарда левого желудочка приводит к острой сердечной недостаточности — кардиогенному шоку и отёку лёгких. В рубцовую стадию инфаркта миокарда замещение поражённой части стенки желудочков соединительной тканью также обусловливает снижение сократительных свойств миокарда. При нефункционировании значительной части миокарда развивается сердечная недостаточность, теперь уже имеющая хронический характер. Врождённые и приобретённые пороки сердца приводят: 1) к перегрузке полостей сердца давлением или объёмом; 2) к гипертрофии миокарда различных камер сердца. В этих условиях сократимость миокарда снижается, что в сочетании с увеличением пред- и постнагрузки результируется развитием сердечной недостаточности. Артериальная гипертензия. Многие больные с гипертонической болезнью или симптоматическими артериальными гипертензиями страдают сердечной недостаточностью. Причины — увеличение постнагрузки (сердцу приходится перекачивать кровь против повышенного системного давления) и относительная коронарная недостаточность вследствие развития гипертрофии миокарда. Кроме того, важен диастолический компонент сердечной недостаточности — во время диастолы нарушены процессы расслабления миокарда (миокард не расслабляется в той же степени, как у здорового человека), что нарушает возможности полноценного выброса крови из сердца в систолу. Снижение сократительной способности миокарда характерно для стойкой тяжёлой артериальной гипертензии, быстро приводящей к развитию сердечной недостаточности. Токсические кардиомиопатии (алкоголь, кобальт, катехоламины, доксорубицин), врождённые, инфекционные, при поражениях сердца на фоне системных заболеваний соединительной ткани и др. также нарушают сократимость и расслабление миокарда Электрокардиография Сокращения миокарда сопровождаются (и обусловлены) высокой электрической активностью кардиомиоцитов, что формирует изменяющееся электрическое поле. Колебания суммарного потенциала электрического поля сердца, представляющего алгебраическую сумму всех ПД (см. рис. 23–5), могут быть зарегистрированы с поверхности тела. Регистрацию этих колебаний потенциала электрического поля сердца на протяжении сердечного цикла осуществляют при записи электрокардиограммы (ЭКГ) — последовательности положительных и отрицательных зубцов (периоды электрической активности миокарда), часть из которых соединяет так называемая изоэлектрическая линия (период электрического покоя миокарда). Электрокардиограмма Нормальная электрокардиограмма (рис. 23–10Б) состоит из основной линии (изолиния) и отклонений от неё, называемых зубцами и обозначаемых латинскими буквами Р, Q, R, S, Т, U. Отрезки ЭКГ между соседними зубцами — сегменты. Расстояния между различными зубцами — интервалы. 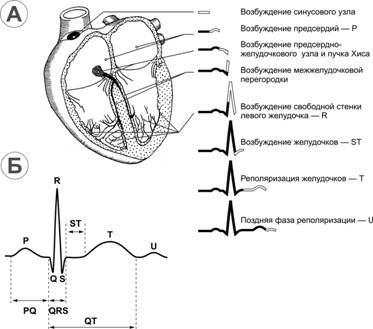 |
