экзамен биология. Сущность жизни. Основные уровни организации и свойства живого. Жизнь
 Скачать 0.92 Mb. Скачать 0.92 Mb.
|
|
Брахидактилия (короткопалость). Этот признак редкий и встречается, как правило, только у одного родителя. При наличии признака у родителя в среднем половина сыновей и дочерей имеют этот признак. Брахидактилию можно обнаружить уже при рождении ребёнка по изменению фаланг пальцев рук и ног. Отклонения от нормы в данном случае не угрожают жизни человека, не делают его неполноценным членом общества.
Остеогенез (нарушение соединительной ткани) так же имеет аутосомно-доминантный тип наследования. При этом дефект одного гена приводит к множественным нарушениям: склонность к переломам костей, обусловленная недостатком в них кальция, склонность к вывихам, связанная с гиперподвижностью суставов.
Синдром Марфана. У больных резко выражен астенический тип сложения (высокий рост, истончение подкожной клетчатки, мышечная слабость), удлинение пальцев кистей и стоп, долихоцефалия — изменение формы головы, когда продольный размер значительно превышает поперечный, так называемое птичье лицо — узкое, с близкорасположенными глазами, тонким носом и выступающей вперед верхней челюстью (прогнатия); деформация ушных раковин, высокое небо. Иногда наблюдается расщепление твердого неба (волчья пасть). Конечности, пальцы кистей и стоп удлинены, грудная клетка воронкообразной или килевидной формы, ребра тонкие и длинные, межреберные промежутки широкие, позвоночник искривлен. Аутосомно-рецессивное наследование признаков. Характерные особенности:
Примеры:
Наследование групп крови систем АВ0 и резус-фактора у человека. Причины возникновения, клинические проявления и профилактика резус-конфликта. Группа крови системы АВ0 контролируется одним аутосомным геном, т.е. геном, расположенным в одной из аутосомных хромосом. Локус этого гена обозначается латинской буквой I (от слова «изогемагглютиноген»), а его три аллеля IА, IВ и I0 обозначаются для краткости, как А, В и 0. Аллели А и В — кодоминантны по отношению друг к другу, и оба доминантны по отношению к аллелю 0. При сочетании различных аллелей могут образоваться 4 группы крови, различающихся между собой иммунологическими свойствами как эритроцитов, так и сыворотки (табл.V.1). Эритроциты содержат антигены (агглютиногены), а в сыворотке находится вещество агглютинин, называемое антителом. 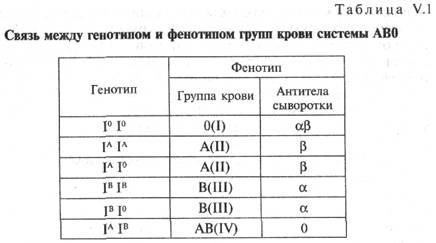 Определение групповой принадлежности человека по системе АВО осуществляется при проведении реакции агглютинации (рис. V.З).  Знать групповую принадлежность крови человека — необходимое условие безопасного проведения переливания крови. Термин «универсальный донор» обозначает лицо с 0(I) группой крови, так как его эритроциты не могут быть агглютинированы сывороткой ни одного реципиента. «Универсальный реципиент» — индивид с АВ (IV) группой крови, сыворотка которого не может агглютинировать эритроциты какого-либо донора. Антиген Rh — один из эритроцитарных антигенов системы резус, располагается на поверхности эритроцитов. В системе резус различают 5 основных антигенов. Основным (наиболее иммуногенным) является антиген Rh (D), который обычно подразумевают под названием резус-фактор. Эритроциты примерно 85% людей несут этот белок, поэтому их относят к резус-положительным (позитивным). У 15% людей его нет, они резус-отрицательны (негативны). Наличие резус-фактора не зависит от групповой принадлежности по системе АВ0, не изменяется в течение жизни, не зависит от внешних причин. Он появляется на ранних стадиях внутриутробного развития, у новорожденного уже обнаруживается в существенном количестве. Определение резус-принадлежности крови применяется в общей клинической практике при переливании крови и ее компонентов, а также в гинекологии и акушерстве при планировании и ведении беременности. Несовместимость крови по резус-фактору (резус-конфликт) при переливании крови наблюдается, если эритроциты донора несут Rh-агглютиноген, а реципиент является резус-отрицательным. В этом случае у резус-отрицательного реципиента начинают вырабатываться антитела, направленные против резус-антигена, приводящие к разрушению эритроцитов. Переливать эритроциты, плазму и особенно цельную кровь от донора к реципиенту нужно строго соблюдая совместимость не только по группе крови, но и по резус-фактору. Присутствие и титр уже имеющихся в крови антител к резус-фактору и других аллоиммунных антител можно определить, указав тест «анти-Rh (титр)». Определение группы крови, резус-фактора, а также наличия аллоиммунных антиэритроцитарных антител должно проводиться при планировании или во время беременности для выявления вероятности иммунологического конфликта матери и ребёнка, который может приводить к гемолитической болезни новорождённых. Возникновение резус-конфликта и развитие гемолитической болезни новорождённых возможно в том случае, если беременная резус-отрицательна, а плод — резус-положителен. В случае, если у матери Rh +, а плод — резус-отрицателен, опасности гемолитической болезни для плода нет. Гемолитическая болезнь плода и новорожденных — гемолитическая желтуха новорожденных, обусловленная иммунологическим конфликтом между матерью и плодом из-за несовместимости по эритроцитарным антигенам. Болезнь может быть обусловлена несовместимостью плода и матери по D-резус- или АВО-антигенам, реже имеет место несовместимость по другим резус- (С, Е, с, d, e) или М-, N-, Kell-, Duffy-, Kidd-антигенам. Любой из указанных антигенов, проникая в кровь резус-отрицательной матери, вызывает образование в её организме специфических антител. Последние через плаценту поступают в кровь плода, где разрушают соответствующие антигенсодержащие эритроциты. Предрасполагают к развитию гемолитической болезни новорождённых нарушение проницаемости плаценты, повторные беременности и переливания крови женщине без учёта резус-фактора и др. При раннем проявлении заболевания иммунологический конфликт может быть причиной преждевременных родов или повторных выкидышей. Профилактика развития резус-конфликта и гемолитической болезни новорождённых.
Наследование резус-фактора крови. В основе закономерностей наследования лежат следующие понятия. Ген, кодирующий резус-фактор D (Rh), является доминантным, аллельный ему ген d - рецессивным (резус-положительные люди могут иметь генотип DD или Dd, резус-отрицательные - только генотип dd). Человек получает от каждого из родителей по 1 гену - D или d, и у него возможны, таким образом, 3 варианта генотипа - DD, Dd или dd. В первых двух случаях (DD и Dd) анализ крови на резус-фактор даст положительный результат. Только при генотипе dd человек будет иметь резус-отрицательную кровь. Варианты сочетания генов, определяющих наличие резус-фактора, у родителей и ребёнка:
Влияние факторов среды на формирование и степень выраженности признаков. Понятие о факторах среды 1 и 2 порядка. Роль факторов среды и наследственности в развитии заболеваний с наследственной предрасположенностью. Среда 1 порядка - это непосредственное окружение, в котором осуществляют свои функции отдельные гены и генотип в целом. Оно образовано всей совокупностью факторов внутренней среды организма: клеточное содержимое (исключая ДНК), характер прямых межклеточных взаимодействий, биологически активные вещества (гормоны). Особенно большое влияние на функцию генотипа факторы этой среды оказывают в период активных формообразовательных процессов, прежде всего в эмбриогенезе. Среда 1 порядка адекватно отвечает изменениям в среде 2 порядка. Основную роль здесь играет эндокринная система. Так, гормоны непосредственно влияют на экспрессивность генов, и если по каким-либо причинам гормон поступает в кровь в ненормальном количестве, то и признак будет выражен по-другому. Влияние среды 2 порядка. Один из классических примеров у животных – опыты Ильина с изменением окраски у горностаевых кроликов. У этой породы мех белый, но отдельные части тела - лапы, уши, кончики морды, хвост - черные. Если на спине кролика, которая покрыта белой шерстью, выбрить небольшой участок и поместить животное в условия пониженной температуры, то на оголенном месте вырастает черная шерсть. Этот факт наглядно свидетельствует о роли одного из физических факторов внешней среды – температуры - в формировании такого признака, как окраска шерсти кролика. Общие закономерности мутагенеза. Мутагенные факторы среды. Классификации мутаций в зависимости от типа клеток, их биологические последствия. Мутагенез - процесс возникновения мутаций. Мутагены - факторы среды, вызывающие мутации. Мутации- количественные или качественные изменения генома. Организм, во всех клетках которого обнаруживается мутация, называется мутантом. Это происходит в том случае, если организм развивается из мутантной клетки (гаметы, зиготы, споры). В ряде случаев мутация обнаруживается не во всех соматических клетках организма; такой организм называют генетической мозаикой. Это происходит, если мутации появляются в ходе онтогенеза – индивидуального развития. Трудности определения понятия «мутация» лучше всего иллюстрирует классификация ее типов. Существует несколько принципов такой классификации: I. По характеру изменения генома:
II. По проявлению в гетерозиготе:
III. По уклонению от нормы или так называемого дикого типа:
IV. В зависимости от причин, вызывающих мутации:
Только эти четыре способа классификации изменений генетического материала носят достаточно строгий характер и имеют универсальное значение. Каждый из подходов в этих способах классификации отражает некоторую существенную сторону возникновения либо проявления мутаций у любых организмов: эукариот, прокариот и их вирусов. Существуют и более частные подходы к классификации мутаций: V. По локализации в клетке:
VI. По отношению к возможности наследования:
Очевидно, два последних способа классификации мутаций применимы только к эукариотам, а рассмотрение мутаций с точки зрения их возникновения в соматических или половых клетках имеет отношение только к многоклеточным эукариотам. Наконец, очень часто мутации классифицируют по их фенотипическому проявлению, т. е. в зависимости от изменяющегося признака. Тогда рассматривают мутации
В основе мутагенеза лежат изменения в молекулах нуклеиновых кислот, хранящих и передающих наследственную информацию. Эти изменения выражаются в виде генных мутаций или хромосомных перестроек. Кроме того, возможны нарушения митотического аппарата клеточного деления, что ведет к геномным мутациям типа полиплоидии или анеуплоидии. Повреждения нуклеиновых кислот (ДНК, РНК) заключаются либо в нарушениях углеводно-фосфатного остова молекулы (ее разрыв, вставка или выпадение нуклеотидов), либо в химических изменениях азотистых оснований, непосредственно представляющих генные мутации или приводящих к их появлению в ходе последующей репликации поврежденной молекулы. Могут возникать как вследствие ошибочной рекомбинации и репарации, так и при действии на геном повреждающих факторов(мутагенов). Мутагенез - внесение изменений в нуклеотидную нить ДНК (мутаций). Различают естественный (спонтанный-без каких-либо причин или под действием каких-либо факторов) и искусственный (индуцированный-результат направленных действий) мутагенез. Генеративная мутация половых клеток:
Эффект мутаций в клетках эмбриона и плода:
Различают мутагены:
Актуальна проблема оценки мутагенной мутагенной канцерогенной и тератогенной активности высокочастотных и магнитных полей.Накопление дозы облучения приводит применение в медицине Х-лучевой диагностики и терапии.
Классификация и механизмы возникновения хромосомных и геномных мутаций. Фенотипические проявления геномных мутаций у человека. Геномные мутации- мутации, обусловленные изменением числа хромосом. К ним относятся полиплоидия и гетреплоидия (анэуплоидия). Полиплоидия-увеличение числа хромосом кратное гаплоидному набору. Появляется в результате нарушения хода митоза и мейоза. Полиплоидные организмы часто встречаются среди растений. Полиплоидия позволяет сохраняться и побеждать в борьбе за существование. Типы полиплоидов:
У человека в норме некоторые соматические клетки полиплоидны: клетки печени, они сохраняют способность делиться, в клетках мегакариоцитов полиплоидия представляет собой нормальное состояние. У человека описаны геномные мутации по типу полиплоидии, которые редко наблюдаются у живорожденных, а в основном обнаруживается у абортированных эмбрионов и у мертворежденных. Если в некоторых клетках человека насчитывается по 69 хромосом – это триплоидия, по 92 – тетраплоидия. Триплоидия одна из наиболее часто встречающихся спонтанных аномалий набора хромосом в эмбриогенезе человека. Около 20% нарушений хромосом у зародышей приходится на триплоидию. Синдром триплоидии (69, XXY) был впервые обнаружен у человека в 60-х годах. К настоящему времени опубликовано около 60 случаев триплоидии у детей. Продолжительность жизни около 7 дней. При тетраплоидии погибают в течение первых 2 месяцев эмбриогенеза. Гетероплоидия или анеуплоидия - изменение числа хромосом в кариотипе не кратному гаплоидному набору. Возникают моносомики и полисомики. |
