Тема 1. Процесс термитной сварки. Тема Процесс термитной сварки
 Скачать 0.55 Mb. Скачать 0.55 Mb.
|
Физико-химические и металлургические основы термитной сварки.Термитная сварка — это процесс формирования соединения металлических деталей жидким металлом регламентируемого химического состава, который образуется в результате термитной (алюмино- термической) реакции. Суть термитной реакции заключается в том, что алюминий способен восстанавливать оксиды металлов с выделением большого количества тепловой энергии. Это приводит к изменению потенциального состояния системы и рекристаллизации компонентов, принимающих участие в данном процессе: где Q — теплота реакции, Дж; U — U2 — изменение энергетического состояния материалов, Дж; А — работа по рекристаллизации компонентов, Дж. Большая часть тепловой энергии, образующейся при термитной реакции, продолжительное время поддерживает металл в жидком состоянии с существенным перегревом выше ликвидуса, что и позволяет применять его для различных технологических целей. Термитная реакция существенно отличается от свободного горения веществ тем, что она протекает за счет кислорода, связанного в оксиды металлов. Поэтому данная реакция протекает в ограниченных объемах и в вакууме. Термитный процесс с железоалюминиевым составом протекает в соответствии со следующей зависимостью: где М, — металл, стоящий левее в ряду напряжений химических элементов; М2 — металл, стоящий правее в ряду напряжений, в данном случае Fe; М20 — оксиды железа (FeO и Fe2Os); М[0 — оксид алюминия (А1203); Q — теплота реакции, Дж. Основным высококалорийным горючим, применяющимся в термитных смесях, является алюминий. После кислорода и кремния алюминий является самым распространенным элементом земной коры и составляет около 8% массы Земли (железо 4,7%). Алюминий в тонко измельченном состоянии при нагревании на воздухе быстро окисляется, выделяя большое количество тепла, и образует оксид алюминия А1203 — прочное химическое соединение с температурой плавления 2050 °С и температурой кипения 2980 °С. Теплота образования оксида алюминия 1588 кДж/моль. Удельный вес алюминия 2,7 г/см3 при 20 °С; в расплавленное состоянии, при температуре 1000 °С — 2,35 г/см3. Температура плавления технически чистого алюминия (99,5%) — 659,8 °С; температура кипения —2400 °С. Для окисления алюминия на 1,12 г металла требуется 1 г кислорода. При этом алюминий, сгорая, выделяет 2998 кДж тепла и развивает температуру до 3000 °С. Термитная смесь для сварки состоит из алюминиевого металлического порошка, железной окалины и различных присадок, вводимых в нее для легирования получаемой термитной стали. Для старта реакции при термитной сварке необходимо выполнить ряд обязательных условий. 1. Необходимо рассчитать состав термитной шихты так, чтобы на старте реакции выделилось необходимое количество тепла для перевода в перегретое жидкое состояние продуктов реакции. 2. Необходимо обеспечить состояние компонентов, составляющих термитную шихту, в виде мелких фракций при их однородном перемешивании. 3. Для старта термитной реакции в объеме термитной смеси необходимо обеспечить нагрев выше 1350 °С. Это обеспечивает ускоренное распространение фронта реакции на весь объем термитной смеси. Термитная реакция очень активно протекает в течение 30 с от старта, а затем ее активность спадает. За указанный промежуток времени образуется жидкий перегретый металл в количестве 0,5 от исходной массы шихты, и шлак. Некоторое количество выделившейся тепловой энергии тратится на нагрев тигля, лучеиспускание и прочие потери. Оставшегося тепла хватает для расплавления шихты и перегрева жидкого металла и шлака до температуры 2550—2700°С. Из-за существенной разницы в плотности жидкого металла и шлака последний поднимается вверх на поверхность, а жидкий металл, наоборот, перемещается на самое дно тигля. Указанный процесс обеспечивает получение рафинированного металла. Наличие дефектов, равномерность химического состава и наличие примесей в термитном металле регламентируется свойствами компонентов, формирующих термитную смесь. Для получения металла (стали) нужного химического состава в шихту вводят в измельченном состоянии легирующие материалы: ферромарганец, ферромолибден, ферротитан, феррованадий, углерод и т. д, Участие легирующих элементов в термитной реакции весьма разностороннее: это легирование термитной стали, ее глубокое раскисление и рафинирование. Наблюдается частичная утрата легирующих элементов в термитной смеси на испарение и переход в шлак. Ценные ферросплавы (ферротитан, феррованадий и др.) повышают прочность термитной стали, так как в ходе реакции, находясь в жидком состоянии, они образуют карбидную фазу титана и ванадия. Наличие в стали перечисленных карбидов увеличивает ее мелкозернистость, повышает твердость и т.п. Длительность термитной реакции от момента зажигания термита до ее окончания и полного отделения металла от шлака находится в прямой зависимости от количества сжигаемого термита и колеблется от 15 до 40—50 с. Условия, требуемые для осуществления термитной реакции. Для осуществления реакции горения термита требуется соблюдение определенных обязательных условий, к которым относятся следующие. 1. Химическая чистота основных компонентов, составляющих термитную смесь. 2. Определенный гранулометрический состав компонентов шихты. 3. Строго регламентируемое соотношение основных составляющих термитной смеси. 4. Быстрый нагрев термита до температуры воспламенения. В железоалюминиевом термите в качестве восстановителя используется порошок технически чистого алюминия, а в качестве окислителя — размолотая железная окалина. Для достижения требуемой активности и теплового эффекта термитной реакции требуется химическая чистота как окислителя, так и восстановителя. Влияние химической чистоты восстановителя на качество сварных соединений показано в табл. 1.1. Таблица 1.1 Влияние химической чистоты порошка технически чистого алюминия на качество сварных швов
Окислитель в виде железной окалины должен включать минимальное количество вредных примесей: кремний, сера и фосфор. Баланс окалины по кислороду составляет 24,5—26% 02.Такого количества кислорода явно мало для осуществления термитной реакции с большим экзотермическим эффектом. Для увеличения общего количества кислорода, содержащегося в связанном состоянии в окалине, ее нагревают до высоких температур в окислительной среде. Большое влияние на ход реакции оказывает измельчение составляющих термитной шихты. Более крупные компоненты используются в реакциях с большими порциями шихты. Для небольших порций термита применяют более измельченные порошки. Эффективное протекание термитной реакции с большим экзотермическим эффектом зависит также от правильного соотношения между основными компонентами шихты. В случае применяется окалина, состоящая только из оксида железа Бе2Оз(кислородный баланс 30,06%), то по формуле (1.3) требуемое соотношение содержания основных компонентов определится: Если окалина состоит из закиси железа FeO (содержание кислорода 22,27%), то соотношение будет: В зависимости от показателя кислородного баланса окалины, который находится в диапазоне 22,27—30,06%, содержание алюминия, как это следует из формул (1.3) и (1.4), варьируется в пределах 20—25,24%. Отклонение от указанных пределов в ту или иную сторону нарушает нормальные соотношения восстановителя и окислителя в термите, что приводит к снижению его калорийности, повышает в термитном металле содержание А1 или насыщает металл кислородом, что отрицательно влияет на качество термитной сварки. Для активного старта реакции окисления алюминия необходимо термитную шихту нагреть до точки воспламенения. Для железоалюминиевой термитной смеси при оптимальных условиях температура воспламенения составляет 1340—1360 °С. Температура воспламенения является той критической точкой, с которой начинается активная фаза протекания термитной реакции. Следует отметить, что медленно термитные процессы, протекающие с малой скоростью, проявляются даже при комнатной температуре. Медленно протекающие термитные процессы безопасны, хотя они снижают экзотермический эффект горения термитной шихты. Указанное явление ограничивает длительность хранения термитной шихты. Термохимические реакции. Компоненты термитной шихты имеют различные примеси: окалина Mn, Si, S, Р, С, Ni, Сг, Си и др.; алюминиевый порошок — Si, Си, Mg, Zn, Pb и др. Наряду с основной термохимической реакцией между алюминием и окислами железа происходит ряд дополнительных химических реакций:  Оксиды железа во время реакции диссоциируют с образованием чистого железа: В соответствии с рядом напряжений все элементы, стоящие левее, во время реакции способны из окислов вытеснять элементы, расположенные правее. Следовательно, из ряда напряжений (табл. 1.2) алюминий имеет возможность вытеснять из окислов Mn, Si, Cr, Ni и т.д. При взаимодействии как основных компонентов термитной шихты, так и их примесей, наблюдается выделение значительного количества тепловой энергии, т.е. все реакции носят экзотермический характер. Таблица 1.2 Ряд напряжений элементов
Все термитные реакции, протекающие при горении термита, подчинены принципу постоянства сумм тепловых эффектов (закон Гесса). Этот закон гласит, что какими бы путями из исходных веществ ни получались определенные химические продукты, суммы тепловых эффектов всех отдельных реакций вдоль каждой ветви (пути) одинаковы. Так, тепловой эффект соединений: 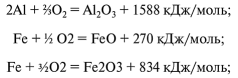 или тепловой эффект реакций выразится: 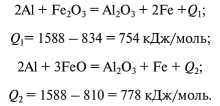 Энергия не теряется и не генерируется вновь, а только трансформируется из одного состояния в другое (закон сохранения энергии). Поэтому алюминий при окислении и образовании оксида А1203 выделяет 1588 кДж/моль тепловой энергии. В то же время для восстановления железа из его оксида Fe203 затрачивается 834 кДж/моль. Получаемая разница в 716 кДж/моль затрачивается на выполнение сварки стыка. Восстановление железа из оксида сопровождается сокращением кислородного баланса в окалине. Оксид железа Fe203 постепенно переходит в закись железа FeO, которая в свою очередь, теряя кислород, формирует чистое железо. 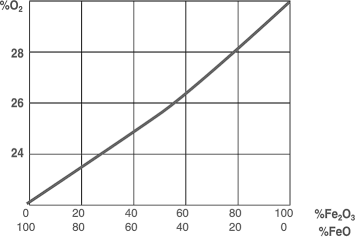 Рис. 1.1. Зависимость между кислородным балансом окалины и содержанием закисного и окисного железа Содержание кислорода в окалине связано с количеством закисного и окисного железа определенной зависимостью (рис. 1.1). Тепловой баланс термитных реакций. В процессе термохимических реакций между алюминием и оксидами железа выделяется теплота, которая для реакций с оксидом и закисью железа имеет значения:  При сгорании 1 кг термита выделится 3540 кДж тепла. Температура нагрева, развиваемая во время реакции, будет: где Т — температура реакции, °С; Q — теплотворная способность термита, кДж/кг; m — масса термита, кг; CpFe и Срд|20з — теплоемкости, кДж/кг • град; а, Ь — процентное содержание Fe и А1203 в термитном расплаве. Для реакции по уравнению (1.5) температура составит 2670 “С, в то время как для реакции по уравнению (1.6) при теплотворной способности 2545 кДж/кг температура реакции составит 2260 °С. Если в железной окалине колебание кислородного баланса находится в пределах: то отклонение в теплотворной способности термита будет: и по температуре реакции Изменение кислородного баланса окалины на 1 % вызывает соответствующие изменения в теплотворности термита на 96 кДж/кг. Для минимального уровня кислородного баланса (23,59% 02) колебания по теплотворной эффективности термитной смеси может составлять 18 — 20%. Для определения абсолютных значений теплотворной способности железоалюминиевого термита используется адиабатический калориметр. В частности, в таком калориметре было проведено тестирование термитной смеси, содержащей 98,18% порошка технически чистого алюминия, у которого кислородный баланс окалины был на уровне 25,05% 02. Тепловой эффект от сгорания термита резко изменяется при варьировании соотношения между содержаниями основных компонентов, составляющих термитную шихту (рис. 1.2). 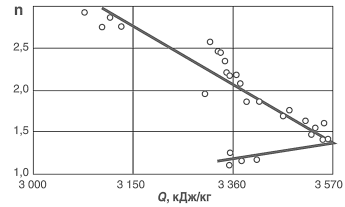 Рис. 1.2. Калорийность термита для различных значений соотношения основных компонентов шихты 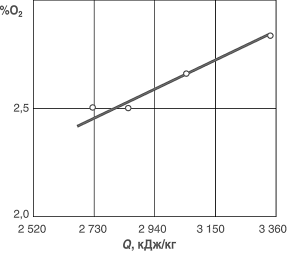 Рис. 1.3. Изменение теплотворной способности термита в зависимости от кислородного баланса шихты Увеличение кислородного баланса железной окалины способствует увеличению количества тепла, выделяющегося при сгорании термита, которое достигает максимума в 3570 кДж/кг при максимальных значениях содержания кислорода в окалине (рис. 1.3). Обработка результатов калориметрических измерений суммарного экзотермического эффекта реакции горения термитной шихты, уточняет предварительные расчеты, которые будут приведены ниже в данном подразделе. С введением в термитную шихту металлической обсечки теплотворная способность термита несколько снижается, так как часть ее расходуется на расплавление обсечки. Стальная обсечка увеличивает выход термитного металла из расплава, однако чрезмерное ее содержание в шихте может охладить термитный металл. Результаты калориметрических измерений процесса горения термита с качественными показателями (z = 1,030; А1 = 96,32%; 02 = 26,58%) выявили значения экзотермического эффекта термитной реакции, которые приведены на рис. 1.4. Если принять содержание обсечки в шихте в размере 10%, что установлено практикой термитных сварок в различных странах для средних сечений рельсов, то для этих значений теплотворная способность термита снизится на 8%. Для термитов, имеющих высокий кислородный баланс окалины, снижение теплотворной способности за 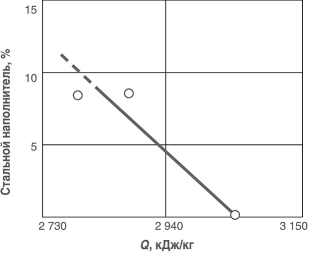 Рис. 1.4. Изменение теплоты реакции термита с введением в шихту металлического наполнителя (стальная обсечка) счет введения указанного выше количества обсечки несущественно. Для термитов с содержанием 24% 02 суммарное снижение теплотворной способности достигает 25—30%, что неприемлемо для сварки. В то же время для термитных смесей с уровнем кислородного баланса 24—25% 02 общее снижение теплотворной способности может составлять 27—32%, что недопустимо для осуществления процесса сварки. Обязательным условием постоянства теплотворной способности термита является стабильность состава железной окалины по кислороду. Если разброс по кислородному балансу окалины допускался в диапазоне 2,61—4,54% (колебания по теплотворной способности AQ = 252—630 кДж/кг или 13,5—15,1% потерь тепла), то колебание кислородного баланса для окалины допускается по закисному железу в диапазоне 13,5—14%. Это обеспечивает высокую стабильность термита по его теплотворной способности. Продукты термитных реакций. Продуктами термитных реакций алюминия с оксидами железа являются шлаковая составляющая в виде оксида алюминия А1203 и металлическое железо в виде расплава. Шлак или термито-корунд применяется в стекольной промышленности при производстве огнеупоров. Термито-корунд имеет огнеупорность более 2000 °С, температуру начала деформации под нагрузкой 0,2 МПа — 1800 °С, предел прочности при сжатии 100 МПа. Наряду с высокими показателями огнеупорности, термито-корунд обладает абразивными свойствами, которые позволяют использовать его в инструментальной промышленности. Введение в термитную шихту цирконового концентрата или других элементов IV, V и VI групп периодической системы элементов Д.И. Менделеева повышает огнеупорные свойства термито-корунда, а использование элементов этой группы как окислов в термитном процессе ведет к получению материалов с высокой огнеупорностью. В случае производства огнеупоров или абразивов термитным способом продуктом реакции является шлак, а отходом — металл. В то же время при термитной сварке и термитном литье продуктом уже становится металла, а отходом — шлак. В термитном процессе оксиды железа восстанавливаются до железа с ферритной структурой и физико-механическими свойствами: предел прочности не превышает 330—350 МПа, твердость 120 единиц по Бринеллю. Введение в термитное железо легирующих элементов приводит к резкому повышению его механических свойств и формированию термитной стали любого заданного химического состава. Получение термитного металла заданного химического состава. Для сварки рельсовой стали составляют термитную шихту с введением легирующих компонентов: углерода, марганца и редко кремния. Практикой установлено, что термитной сталью в среднем усваивается: углерода — 70%, марганца — 60%, кремния — 50%. Рассчитывая химический состав термитной стали, следует принять во внимание наличие углерода в количестве 0,08—0,25%, марганца до 0,47% и кремния до 0,35% как в металлическом наполнителе, так и в окалине. По химическому составу от рельсовой стали термитная отличается тем, что она содержит 0,08—0,18% алюминия, который практически не изменяет механические свойства стали, но способствует модифицированию ее структуры.  Рис. 1.5. Схема термитной спички Разработанные способы расчета термитной шихты позволяют получить термитную сталь по содержанию алюминия в металле — с точностью до 0,1% и до 0,15% — по ряду других элементов от расчетного значения. Помимо углеродистых сталей, термитным способом можно получить высоко- и низкомарганцовистые стали, стали аустенитного класса, обладающие антикоррозионными и жароупорными свойствами. Воспламеняющие средства, применяемые при осуществлении термитных реакций. Для зажигания термитных смесей применяют легковоспламеняемые составы, которые при горении развивают температуру, превышающую 1500—1600 °С. Для этого используется переходной состав, загорающийся при 150—200°С, который вызывает загорание второго состава с температурным барьером в 400—600°С. Этот состав при своем горении перекрывает, температурный барьер начала термитной реакции. На упомянутом выше принципе основывается конструкция термитных спичек, показанных на рис. 1.5. Наряду с термитными спичками можно пользоваться переходными составами, приведенными в табл. 1.3. Таблица 1.3 Составы для воспламенения термитных смесей
В ряде случаев для поджига термитной шихты применяется электрическая дуга. Термитный состав также можно зажечь электрической дугой. При зажигании брикетированного термита хорошие результаты дает электрозапал из двух-трех витков мягкой стальной проволоки диаметром 0,8—1,0 мм. Спираль электрозапала при подключении к низковольтному источнику электрического тока сначала разогревает термитную шихту, а затем, перегорая, вызывает реакцию термитных компонентов. Этим способом воспламенения термита удобно пользоваться при зажигании больших порций шихты. |
