Учебное пособие для подготовки к Единому Государственному Экзамену. Под редакцией профессора, доктора педагогических наук, директора моу Лицей 13 С. А. Старченко. Троицк 2016. 124
 Скачать 1.57 Mb. Скачать 1.57 Mb.
|
|
В задаче 7.7 необходимо использовать то обстоятельство, что работа газа в циклическом процессе численно равна площади цикла на графике зависимости давления от объема, причем со знаком «плюс», если цикл проходится по часовой стрелке, и «минус» - если против. Поэтому во втором цикле работа газа положительна, в третьем отрицательна. Первый цикл состоит из двух циклов, один из которых проходится по, второй - против часовой стрелки, причем, как следует из графика 1, площади этих циклов равны. Поэтому работа газа за цикл в процессе 1 равна нулю (ответ - 2). 2). Задача 8.7. Поскольку в результате совершения циклического процесса газ возвращается в первоначальное состояние, то изменение внутренней энергии газа равно нулю (ответ - 2). 3). Задача 9.7. Применяя первый закон термодинамики ко всему циклическому процессу и учитывая, что изменение внутренней энергии газа равно нулю (см. предыдущую задачу), заключаем, что A = Q. (ответ - 3). 4).Задача 10.7. Поскольку работа газа численно равна площади цикла на диаграмме «давление-объем», то работа газа в процессе равна A = pV/2. (ответ - 1). 5). Задача 1.7. Аналогично в этой задаче газ за цикл совершает работу А = 2pV. (ответ - 1). 6). Задача 2.7. Работа газа в любом процессе равна сумме работ на отдельных участках процесса. Поскольку процесс 2-3 изохорический, то работа газа в этом процессе равна нулю. Поэтому А = А1-2 + А3-1. (ответ - 3). 7). Задача 3.7. По определению КПД показывает, какую часть количества теплоты, полученного у нагревателя, двигатель превращает в работу. (ответ - 4). 8). Задача 4.7. Работа двигателя за цикл равна разности количеств теплоты, полученного от нагревателя Q1 и отданного холодильнику Q2: А = Q1 - Q2. Поэтому КПД цикла есть  . .(ответ - 3). 9). Задача 5.7. По формуле (15.3) находим КПД цикла Карно  . .(ответ - 2). 10). Задача 6.7. Пусть температура нагревателя первоначального цикла Карно равна T1, температура холодильника Т2. Тогда по формуле (15.3) для КПД первоначального цикла имеем  Отсюда находим T2/T1 = 0,5 . Поэтому для КПД нового цикла Карно получаем  . .(ответ - 2). 11). В задаче 8.8 формулы (2),(3) и(4) представляют собой разные варианты записи определения КПД теплового двигателя (см. формулы (15.1) и (15.2)). Поэтому не определяет КПД двигателя только формула 1. (ответ - 1). 12). Задача 9.8. Мощностью двигателя называется работа, совершенная двигателем в единицу времени. Поскольку работа двигателя равна разности полученного от нагревателя и отданного холодильнику количеств теплоты, имеем для мощности двигателя N  = 700 Вт. = 700 Вт.(ответ - 3). 13). Задача 10.8. По формуле (15.2) имеем для КПД двигателя  . .(ответ - 2). 14). Задача 1.8. Для нахождения КПД теплового двигателя удобно использовать последнюю из формул (15.2). Имеем  где А - работа газа, Qx - количество теплоты, отданное холодильнику. (ответ - 3). 15). Задача 2.8. Пусть газ совершает за цикл работу А. Поскольку количество теплоты, полученное от нагревателя равно A + Qx (Qx - количество теплоты, отданное холодильнику), и работа А составляет 20 % от этой величины, то для работы справедливо соотношение А = 0,2(А + 100). Отсюда находим А = 25 Дж. (ответ - 1). 16). Задача 3.8. Поскольку работа теплового двигателя равна 100 Дж при КПД двигателя 25 %, то двигатель получает от нагревателя количество теплоты 400 Дж. Поэтому он отдает холодильнику 300 Дж теплоты в течение цикла. (ответ- 4). 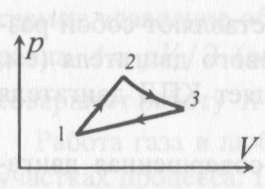 17). В задаче 4.8 газ получает или отдает теплоту только в процессах 1-2 и 3-1 (процесс 2-3 по условию адиабатический). Поэтому данное в условии задачи количество теплоты Q1-2 является количеством теплоты, полученным от нагревателя в течение цикла, Q3-1, - количеством теплоты, отданном холодильнику. Поэтому работа газа равна 17). В задаче 4.8 газ получает или отдает теплоту только в процессах 1-2 и 3-1 (процесс 2-3 по условию адиабатический). Поэтому данное в условии задачи количество теплоты Q1-2 является количеством теплоты, полученным от нагревателя в течение цикла, Q3-1, - количеством теплоты, отданном холодильнику. Поэтому работа газа равна А = Q1-2- Q3-1. (ответ - 1). 18). Задача 5.8. Цикл состоит из двух изотерм 2-3 и 4-1 и двух изохор 1-2 и 3-4.  Работа газа в изохорических процессах равна нулю. Сравним работы газа в изотермических процессах. Для этого удобно построить график зависимости давления от объема в рассматриваемом процессе, поскольку работа газа есть площадь под этим графиком. Работа газа в изохорических процессах равна нулю. Сравним работы газа в изотермических процессах. Для этого удобно построить график зависимости давления от объема в рассматриваемом процессе, поскольку работа газа есть площадь под этим графиком. График зависимости давления от объема для заданного в условии процесса приведен на рисунке. Поскольку изотерме 2-3 соответствует большая температура, чем изотерме 4-1, то она будет расположена выше на графике p- V. Объем газа в процессе 2-3 увеличивается, в процессе 4-1 уменьшается. Таким образом, график процесса на графике p-V проходится по часовой стрелке, и, следовательно, работа газа за цикл положительна. (ответ - 1).  19). Задача 6.8. Для сравнения работ газа на различных участках процесса построим график зависимости давления от объема. Этот график представлен на рисунке. 19). Задача 6.8. Для сравнения работ газа на различных участках процесса построим график зависимости давления от объема. Этот график представлен на рисунке. Из рисунка следует, что работы газа в процессах 1-2 и 3-4 одинаковы по модулю (этим работам отвечают площади прямоугольников, «залитых» на рисунке светлой и темной «заливкой»). Работе газа на участке 4-1 отвечает площадь под графиком 4-1, которая меньше площади под графиком 1-2. Работе газа на участке 2-3 отвечает площадь под кривой 2-3 на рисунке, которая заведомо больше площади «залитых» прямоугольников. Поэтому в процессе 2-3 газ и совершает наибольшую по абсолютной величине (среди рассматриваемых процессов) работу. (ответ - 2.). 20). Задача 7.8. Согласно определению коэффициент полезного действия представляет отношение работы газа за цикл А к количеству теплоты Q, полученному от нагревателя 𝛈 = А/Q. Как следует из данного в условии задачи графика, и в процессе 1-2-4-1 и в процессе 1-2-3-1 газ получает теплоту только на участке 1-2. Поэтому количество теплоты, полученное газом от нагревателя в процессах 1-2-4-1 и 1-2-3-1 одинаково. А вот работа газа в процессе 1-2-4-1 вдвое меньше (так площадь треугольника 1-2-4 как вдвое меньше площади треугольника 1-2-4-1). Поэтому коэффициент полезного действия процесса 1-2-4-1 - 𝛈1вдвое меньше коэффициента полезного действия процесса 1-2-3-1 - 𝛈.  (ответ - 1). 5. Задания на проверку элементов знаний и умений по теме: свойства газов, жидкостей и твердых тел. Фазовые переходы. Влажность (Задачи: 9.9; 10.9; 1.9; 2.9; 3.9; 4.9; 5.9; 6.9; 7.9; 8.9; 10.10; 1.10; 2.10; 3.10; 4.10; 5.10; 6.10; 7.10; 8.10; 9.10.) Задачи и вопросы, в которых рассматриваются свойства газов, жидкостей и твердых тел, а также переходы между ними (фазовые переходы), входят в программу школьного курса физики и часто включаются в ЕГЭ. Начнем со свойств трех агрегатных состояний вещества. Плотности жидкостей и твердых тел близки друг к другу, но сильно отличаются от плотности газа. Отсюда следует, что расстояния между молекулами в жидкости и твердом теле не сильно отличаются друг от друга, но гораздо меньше расстояния между молекулами в газе. Различие же молекулярного строения жидкостей и твердых тел заключается в том, что большинство твердых тел имеют кристаллическую структуру: их молекулы располагаются в определенном порядке, повторяя определенную структурную единицу, которая называется элементарной ячейкой. Различают моно- и поликристаллы. Монокристаллом называется такое кристаллическое тело, порядок в расположении молекул которого имеет место вдоль всего тела. Очень часто монокристаллическое тело обладает правильной геометрической формой. Поликристалл представляет собой совокупность связанных друг с другом, хаотически ориентированных по отношению друг к другу маленьких монокристаллов. Из-за того, что разные направления в элементарной ячейке кристалла неэквивалентны, ряд его физических свойств, таких как прочность, электро - или теплопроводность неодинаковы в различных направлениях. Это свойство кристалла называется анизотропией. Конечно, это касается только монокристалла. Поликристаллы из-за различных ориентаций монокристаллических частей являются изотропными. Также изотропными являются жидкости, молекулы которых расположены беспорядочно. Существуют, однако, такие тела, которые являются твердыми, но в расположении молекул, которых нет кристаллического порядка. Такие тела называются аморфными. Аморфными являются биополимеры, стекло и ряд других веществ. Отсутствие порядка в расположении молекул проявляется в отсутствие у аморфных тел строго определенной температуры плавления (см. ниже). Как показывает опыт, при изменении температуры и внешнего давления возможны переходы вещества из одного агрегатного состояния в другое. Переход кристаллического твердого тела в жидкое называется плавлением, обратный процесс - кристаллизацией. Переход жидкости в пар называется испарением (или кипением, если этот процесс сопровождается образованием пузырьков пара в жидкости), обратный процесс - конденсацией. Плавление и кристаллизация твердых (кристаллических) тел происходит при строго определенной для каждого вещества (при фиксированном давлении) температуре. При плавлении необходимо сообщить твердому телу энергию, которая расходуется не на нагревание тела, а на разрыв кристаллических связей между его молекулами. При кристаллизации эта дополнительная энергия выделяется. Плавление аморфных тел происходит по-другому: при увеличении температуры они плавятся постепенно (т.е. становятся более мягкими и пластичными), и невозможно указать такую температуру, ниже которой тело твердое, выше - жидкое. При испарении жидкостей молекулы вылетают с их поверхности и переходят в газовую фазу. При этом из жидкости могут вылететь только самые быстрые молекулы, поэтому температура жидкости в процессе испарения понижается. Испарение может происходить при любой температуре (за исключением абсолютного нуля), однако с ростом температуры интенсивность испарения возрастает. Благодаря хаотическому тепловому движению наряду с процессом испарения идет и обратный процесс - конденсация пара, - в результате которого молекулы пара могут вернуться в жидкость. Поскольку скорость процесса конденсации зависит от плотности пара над поверхностью жидкости, при определенной концентрации пара скорости процессов испарения и конденсации совпадают. В этом состоянии не происходит изменения количества жидкости и пара, и устанавливается динамическое равновесие между жидкостью и паром. Пар, находящийся в динамическом равновесии со своей жидкостью называется насыщенным. Насыщенный пар - это пар максимально возможной плотности (при фиксированной температуре). Действительно, если плотность пара станет больше плотности насыщенного пара, то скорость процесса конденсации станет больше скорости испарения - излишек пара сконденсируется, а оставшийся пар станет насыщенным. Пар, имеющий плотность, меньшую плотности насыщенного пара при данной температуре, называется ненасыщенным. Поскольку скорость процесса испарения зависит от температуры жидкости, динамическое равновесие между жидкостью и ее паром при большей температуре установится при больших концентрациях пара. Это значит, что концентрация насыщенного пара возрастает с температурой, и, следовательно, его давление растет с ростом температуры быстрее, чем по линейному закону. Характеристикой воздуха, в котором находятся водяные пары, является его относительная влажность φ, которая показывает какую долю парциальное давление данного пара р (или его концентрация) составляет от давления (или концентрации) насыщенного пара при данной температуре рнас:  (16.1) (16.1)Если, например, парциальное давление водяного пара в воздухе при некоторой температуре равно 103 Па, а давление насыщенного пара при этой температуре равно 2·103 Па, то относительная влажность этого воздуха составляет 50 %. Очевидно, изменяя температуру и объем воздуха можно менять его относительную влажность. Поскольку концентрация насыщенного пара зависит от температуры, при нагревании воздуха, в котором находится неизменное количество водяных паров, будет убывать его относительная влажность, при охлаждении - возрастать. Если в последнем процессе относительная влажность достигает 100 %, излишек пара конденсируется и при дальнейшем охлаждении относительная влажность не изменяется. Процесс конденсации излишка пара при охлаждении можно наблюдать прохладными ночами летом, когда выпадает роса и образуется туман (маленькие капельки воды). Т Температура, при которой пар становится насыщенным и образуется конденсат, называется точкой росы этого пара. Также можно изменять относительную влажность воздуха, уменьшая или увеличивая его объем при неизменной температуре. В первом процессе растет концентрация пара (и, следовательно, его относительная влажность), во втором убывает. Конечно, в этих рассуждениях предполагается, что масса водяного пара не изменяется (т.е. не происходит дополнительного испарения воды или конденсации пара). Процесс испарения жидкости с образованием пузырьков внутри нее называется кипением. Причина кипения заключается в следующем. Благодаря хаотическому тепловому движению в жидкости всегда образуются микроскопические пузырьки пара. Поскольку они очень малы, пар в них мгновенно становится насыщенным. Дальнейшая «судьба» этих пузырьков зависит от соотношения давлений: внутреннего, которое равно давлению насыщенного пара при данной температуре, и внешнего, которое равно давлению атмосферного воздуха (в пренебрежении гидростатическим давлением жидкости). Если внутреннее давление меньше внутреннего, пузырек пара пропадет, а пар из него перейдет в жидкость, если наоборот - пузырек будет расширяться, при этом за счет интенсивного испарения жидкости с поверхности пузырька, пар в нем будет оставаться насыщенным. Затем такие пузырьки всплывают, и пар из них уходит из жидкости. Таким образом, кипение жидкости происходит при такой температуре, при которой давление насыщенного пара этой жидкости равно атмосферному давлению. 1). |
