для самостоятельного решения
1.
|
Ион
|
Млн –1
|
%0
|
ммоль/л
|
|
Na+
|
5,8
|
0,0058
|
0,25
|
|
Mg2+
|
3,4
|
0,0034
|
0,14
|
|
Са2+
|
20
|
0,020
|
0,50
|
|
К+
|
2,1
|
0,0021
|
0,054
|
|
Сl–
|
5,7
|
0,0057
|
0,16
|
|
SO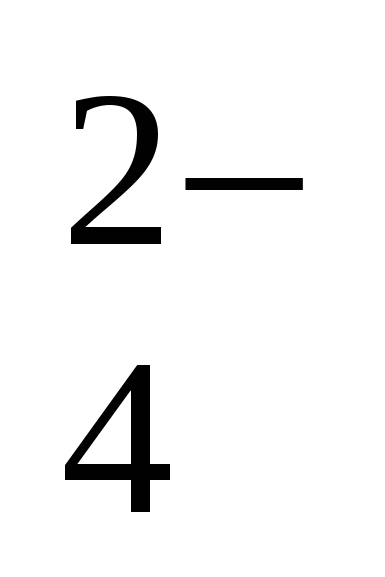
|
12
|
0,012
|
0,12
|
|
HCO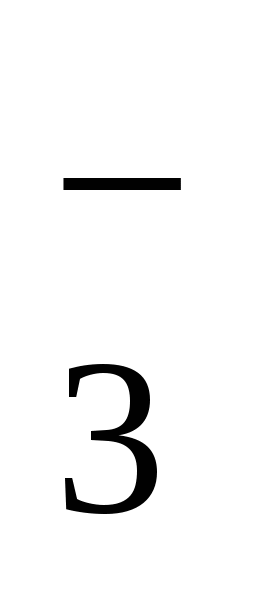
|
35
|
0,035
|
0,57
|
2. СО2(1000)М(0,1/0,97)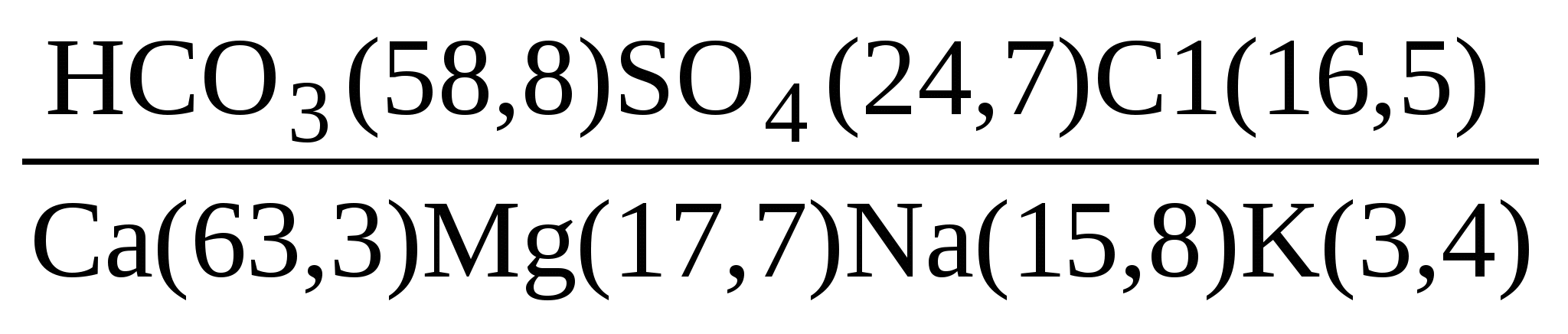 ; 3. 28,3 г; 4. М = 34,3 г/л; класс вод с повышенной соленостью; 5. Гидрокарбонатные воды кальциевой группы третьего типа; 6. 1,28 . 10–4 моль; 7. Вторая вода более агрессивна; 8. = 0,22 < 1, следовательно, будет идти процесс растворения гипса; 9. Ангидрит более устойчив; 10. СF = 19,3 мг/л, что в 26 раз превышает ПДК; 11. Общая жесткость равна 7,8 . 10–2 моль/м3, что соответствует 0,22 немецких градусов жесткости, 0,39 французских градусов жесткости и 3,90 американских градусов жесткости; жесткость карбонатная равна 0,020 моль/м3, вода относится к группе очень мягких вод; 12. рН 6,9; рН = 1,3; 13. рН 4,9; аСO2 = +16%; aSО2 = +93%; aNH3 = –9%; 14. рН 5,7: SO ; 3. 28,3 г; 4. М = 34,3 г/л; класс вод с повышенной соленостью; 5. Гидрокарбонатные воды кальциевой группы третьего типа; 6. 1,28 . 10–4 моль; 7. Вторая вода более агрессивна; 8. = 0,22 < 1, следовательно, будет идти процесс растворения гипса; 9. Ангидрит более устойчив; 10. СF = 19,3 мг/л, что в 26 раз превышает ПДК; 11. Общая жесткость равна 7,8 . 10–2 моль/м3, что соответствует 0,22 немецких градусов жесткости, 0,39 французских градусов жесткости и 3,90 американских градусов жесткости; жесткость карбонатная равна 0,020 моль/м3, вода относится к группе очень мягких вод; 12. рН 6,9; рН = 1,3; 13. рН 4,9; аСO2 = +16%; aSО2 = +93%; aNH3 = –9%; 14. рН 5,7: SO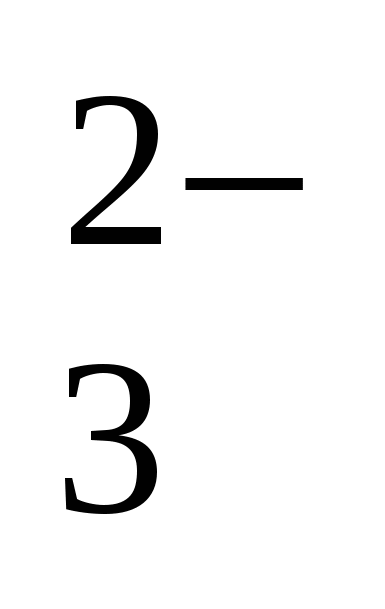 , HSO , HSO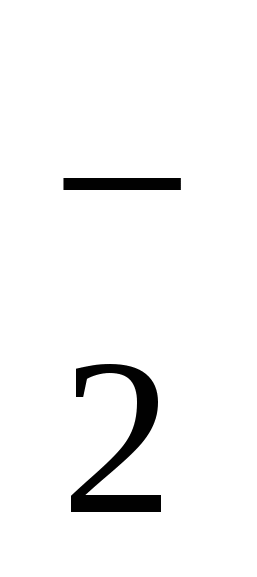 ; рН 4,5: HSO ; рН 4,5: HSO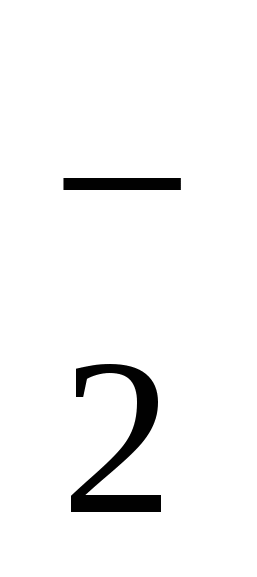 ; 15. При рН 7: [СО2(р-р)] = 3,37 . 10–4 моль/л; [HCO ; 15. При рН 7: [СО2(р-р)] = 3,37 . 10–4 моль/л; [HCO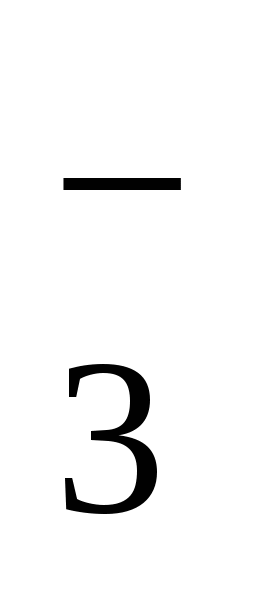 ] = 1,5 . 10–3 моль/л; РСО2 = 1,11 Па; при рН 10,5: [НСО ] = 1,5 . 10–3 моль/л; РСО2 = 1,11 Па; при рН 10,5: [НСО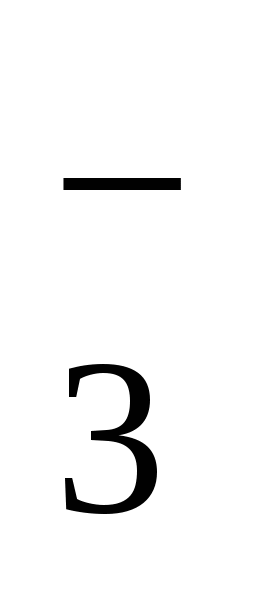 ] = 2,21 . 10–4 моль/л; [СО ] = 2,21 . 10–4 моль/л; [СО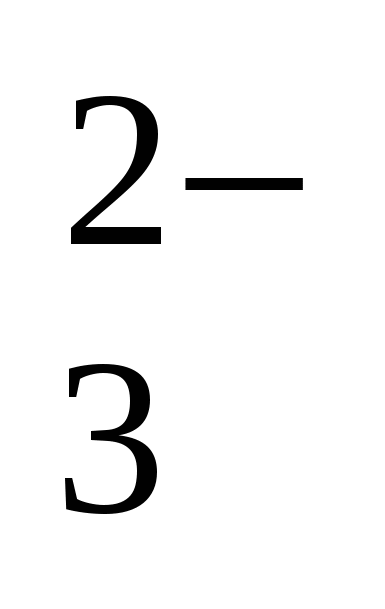 ] = 4,80 . 10–4 моль/л; 16. m = 34,2 мг/л; 17. рН 10,9; 18. Щ = 2,84 . 10–3 моль/л; Ж = 9,24 . 10–3 моль/м3; вид – солоноватые, класс – сульфатные, 2-й THn; ] = 4,80 . 10–4 моль/л; 16. m = 34,2 мг/л; 17. рН 10,9; 18. Щ = 2,84 . 10–3 моль/л; Ж = 9,24 . 10–3 моль/м3; вид – солоноватые, класс – сульфатные, 2-й THn;
(l/30)[SO4(62,6)HCO3(18,8)Cl(18,6)]/[Na(39,5)Ca(30,4)Mg(30,l)]; 19. рН = 11,4; 20. Щ = 5,48 . 10–3 моль/л; Ж = 5,48 . 10–3 моль/м3; 21. рН = 9,3; 22. h = 0,18 м за 1000 лет; 23. См. штриховые линии на рис. 13; 24. 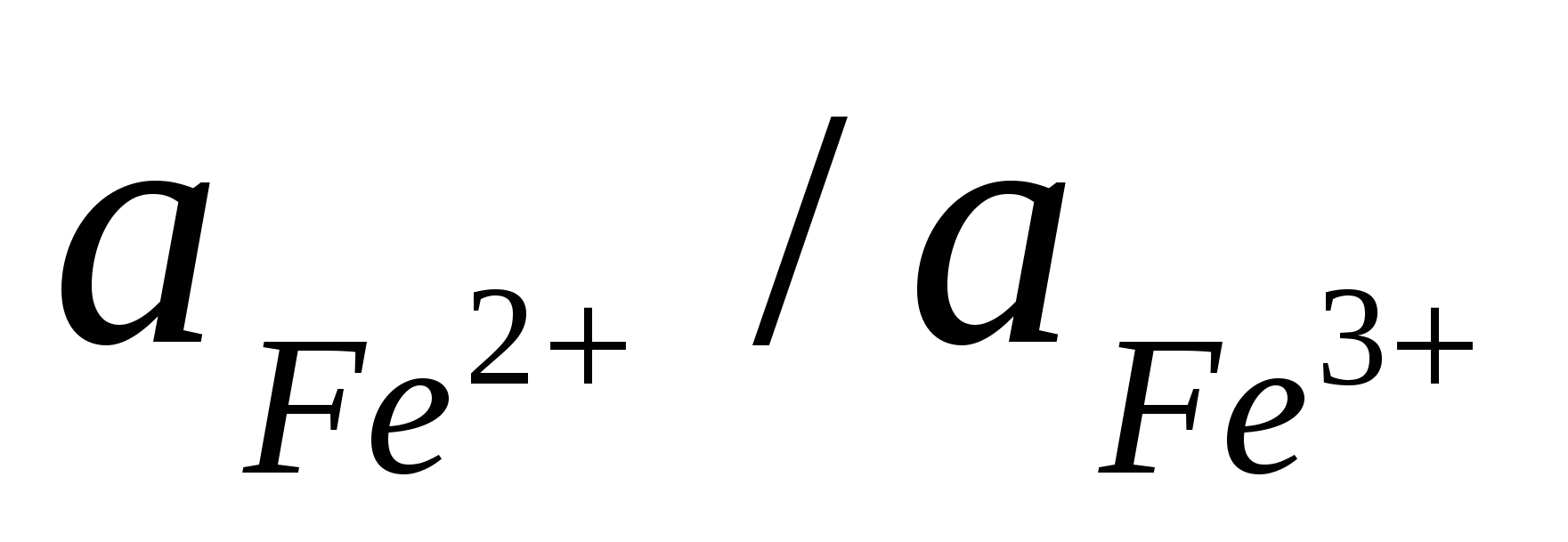 = 0,49; 25. = 0,49; 25. 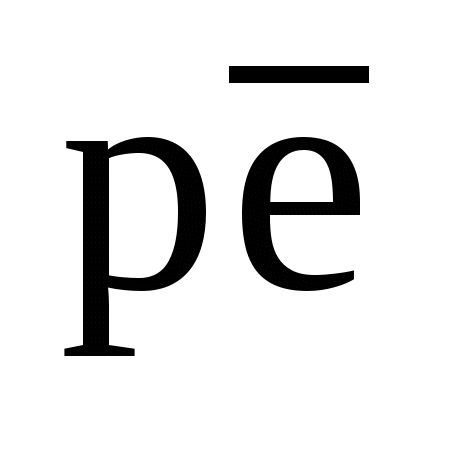 = 13,3; = 13,3; 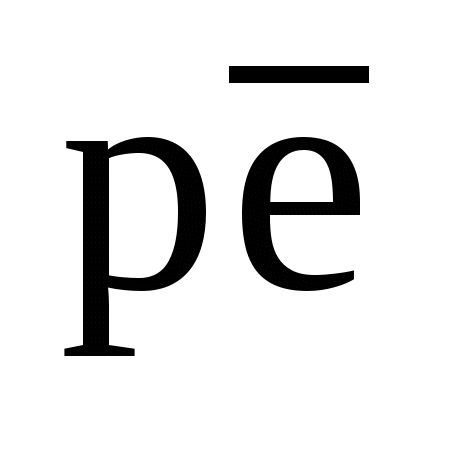 = 2,5; 26. РО2= 10–67 атм; 27. 1340 мг/л; 28. V= 59,6 м3; 29. m = 0,22 кг; V = 145 л. = 2,5; 26. РО2= 10–67 атм; 27. 1340 мг/л; 28. V= 59,6 м3; 29. m = 0,22 кг; V = 145 л.
|
 Скачать 31.55 Mb.
Скачать 31.55 Mb.