Коллок2. Вариант 1 Основные положения спектроскопии. Спектр электромагнитного излучения
 Скачать 2.57 Mb. Скачать 2.57 Mb.
|
|
Вариант 1 1.Основные положения спектроскопии. Спектр электромагнитного излучения. Совокупность всех частот (длин волн) электромагнитного излучения называют электромагнитным спектром. В зависимости от длины волны в электромагнитном спектре выделяют следующие участки .Гамма, рентгеновское, ультрафиолетовое, спектроскопия, инфракрасное,микроволновое, радиоволны. Энергия фотонов, длина волны, частота, волновое число; связь между ними; термины, символы, единицы измерения. Свет – это проток частиц (фотонов, квантов): может рассеиваться, отражаться, количество частиц можно посчитать. Энергия электромагнитного излучения (фотона) Е зависит от частоты излучения и определяется соотношением 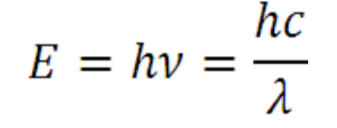 где h – постоянная Планка, равная Дж с 34 6,62 10 .  Волновые характеристики излучения: длина волны , частота колебаний ν, волновое число . Длина волны показывает наименьшее расстояние между точками, колеблющимися в одинаковых фазах. Это линейная величина, в единицах СИ измеряется в метрах (м) и его долях. Частота 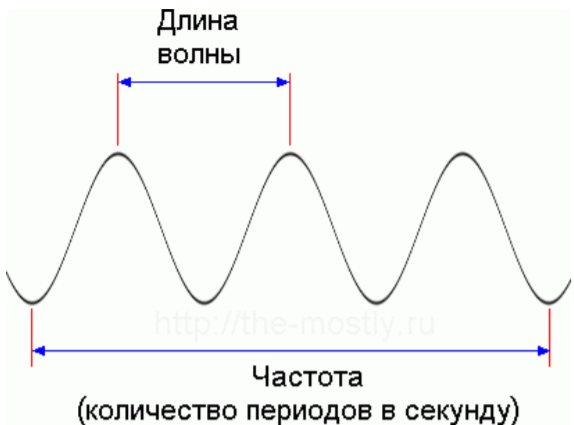 Волновое число Длина волны и частота колебаний связаны между собой соотношением: 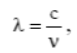 Величина, обратная длине волны, называется волновым числом ν = 1/λ. Составляющие внутренней энергии частиц и соответствующие им диапазоны электромагнитного излучения. Имеется целый ряд типов электромагнитного излучения, начиная с радиоволн и заканчивая гамма-лучами. Электромагнитные лучи всех типов распространяются в вакууме со скоростью света и отличаются друг от друга только длинами волн. 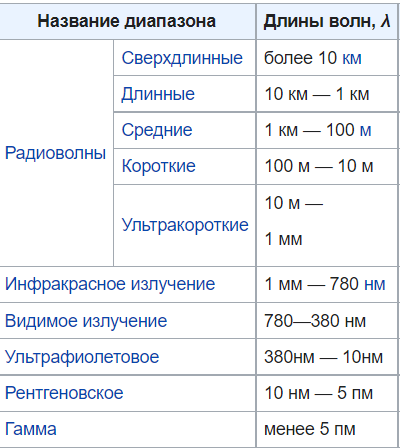 Основные спектроскопические аналитические методы и их возможности. Спектроскопические методы подразделяют на атомные и молекулярные в зависимости от того, какие частицы формируют аналитический сигнал. Методы, основанные на излучении низких энергий (сопоставимых с энергиями химических связей или меньше их), являются методами молекулярного анализа. Методы же, использующие излучение высоких энергий, относятся к атомным (элементным). Атомно-эмиссионная спектроскопия. Принцип метода. Во всех вариантах метода пробу вносят в источник возбуждения, в котором создается высокая температура. При этом последовательно происходят процессы испарения пробы, атомизации первоначальных продуктов испарения, возбуждения образовавшихся атомов, испускания света возбужденными атомами и регистрация излучения. Для качественного анализа полученный спектр сопоставляют гидрометаллургической переработки руд, различные концентраты и т. Д Молекулярный абсорбционный анализ можно классифицировать в соответствии с участком электромагнитного спектра, используемого для облучения анализируемого вещества. В этом случае название метода соответствует названию области спектра.1. Ультрафиолетовая спектроскопия (УФ-спектроскопия). Для облучения используется ультрафиолетовое излучение, λ = 180–400 нм. 2. Спектроскопия видимой области. Используется видимая часть спектра с набором длин волн: 400–760 нм. 3. Инфракрасная спектроскопия (ИК-спектроскопия). Для облучения анализируемого вещества используется инфракрасная область спектра. 2.Хроматография. Явление, лежащие в основе разных видов хроматографии. По признаку природы явлений, лежащих в основе разделения, хроматографию подразделяют на четыре основных вида: адсорбционная, распределительная, осадочная и эксклюзионная. В основе адсорбционной хроматографии лежит адсорбция разделя-емых веществ на твердой поверхности выбранного адсорбента. В основе распределительной хроматографии лежит различная растворимость разделяемых веществ в жидкости. Разделение протекает на границе двух фаз, несмешивающихся между собой, – неподвижной (жид-кости) и подвижной (жидкости или газа), поэтому процесс разделения определяется различием коэффициентов распределения разделяемых веществ между обеими фазами. В основе осадочной хроматографии лежит образование нераство-римых соединений в результате химических реакций разделяемых веществ с реактивом-осадителем. Эксклюзионная хроматография представляет собой жидкостную хроматографию, основанную на различной способности молекул разного размера проникать в поры неионогенного геля, который служит неподвижной фазой. Классификация методов по агрегатному состоянию фаз, по механизму разделения, по технике выполнения. По агрегатному состоянию подвижной и неподвижной фаз: 1.газовая (подв.) a. газо-жидкостная(подв. + жидк.) происходит растворение веществ в жидкой фазе. b. газо-твердофазная или газо-адсорбционная (подв. + тв.) газы удерживаются поверхностью 2.жидкостная(подв.) a. жидкостно-жидкостная или распределительная(подв. + жидк.) жидкости не смешиваются. b. жидкостно-твердофазная или жидкостно-адсорбционная (подв. + тв.) вещества удерживаются поверхностью По механизму разделения веществ: 1. Адсорбционная разлиные способности в сорбции 2. Распределительная разделение веществ происходит на различии растворимостей веществ 3. Ионнообменная разделение веществ происходит в результате различий в способности к ионному обмену 4. Активная на поверхности сорбента присутствуют селективные сорбенты 5. Гель-проникающая или Эксклюзионная основана на различной сорбции веществ разного размера внутрь пор сорбента По технике выполнения: 1. Колоночная в колонке находится неподвижная фаза 2. Плоскостная или Планарная тонкий слой сорбента закрепляется на плоскости инертного вещества. после чего край вещества погружают в емкость с жидкой фазой. за счет капиллярных свойства жидкость поднимается по сорбенту.. различные вещества имеют разную скорость. (могут окрашивать в разные цвета) используется для качественного анализа Уравнение Ван Деемтера. Уравнение Ван-Деемтера[1] используется в хроматографии и описывает зависимость между высотой, эквивалентной теоретической тарелке, и средней линейной скоростью подвижной фазы.  Хроматограмма и ее “параметры” 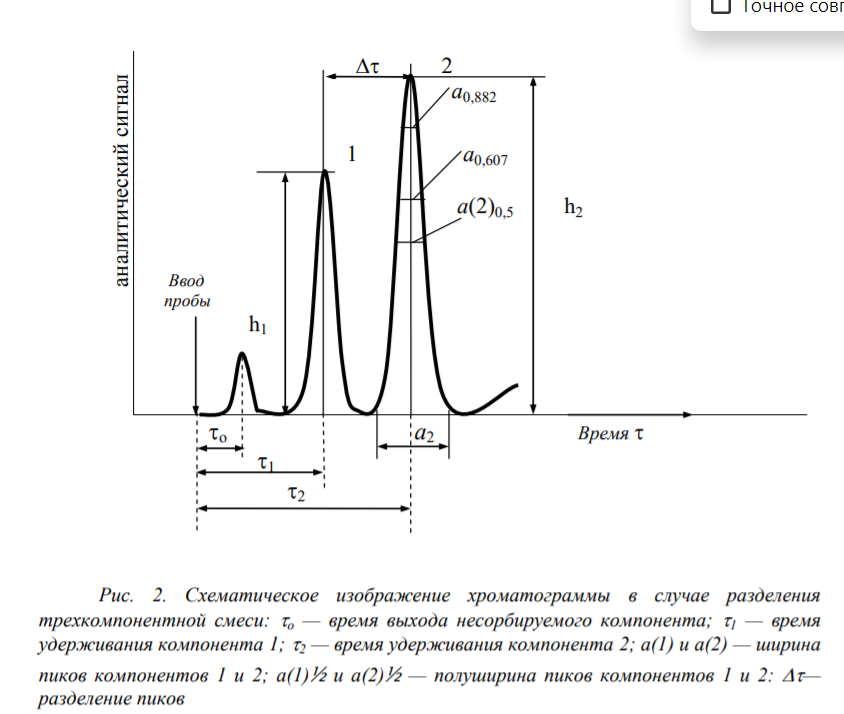 Области применения метода.  Вариант 2. 1.Люминесцентный анализ: Явление, лежащие в основе люминесценции. Люминесценция - излучение, представляющее собой избыток над тепловым излучением тела и продолжающееся в течение времени, значительно превышающего период световых колебаний (1015 с). Классификация и виды люминесценции. типы люминесценции: • фотолюминесценция - возникает при возбуждении атомов светом (ультрафиолетовые лучи и коротковолновая часть видимого света); • рентгенолюминесценция - возникает при возбуждении атомов рентгеновским и γ-излучением (экраны рентгеновских аппаратов, индикаторы радиации); • катодолюминесценция - возникает при возбуждении атомов электронами (кинескопы, экраны осциллографов, мониторов); • радиолюминесценция - возникает при возбуждении атомов продуктами радиоактивного распада; • электролюминесценция - возникает при возбуждении атомов под действием электрического поля (возбуждение молекул газа электрическим разрядом - газоразрядные лампы); • хемилюминесценция - возникает при возбуждении молекул в процессе химических реакций; • биолюминесценция - возникает в биологических объектах в результате определенных биохимических реакций; • сонолюминесценция - возникает под действием ультразвука. По длительности остаточного свечения различают флуоресценцию и фосфоресценцию: • флуоресценция - кратковременное остаточное свечение, длительность которого составляет 10-9-10-8с; • фосфоресценция - продолжительное остаточное свечение, длительность которого составляет 10-4 -104 с. Закон Вавилова. Закон Вавилова заключается в том, что квантовый выход флуоресценции не зависит от длины волны возбуждения люминесценции. Квантовым выходом люминесценции называют отношение числа квантов, высвеченных в виде люминесценции, к числу Закон Стокса-Ломмеля. Закон Стокса—Ломмеля обуславливает взаимное расположение спектров люминесценции и поглощения и формулируется следующим образом: спектр люминесценции в целом и его максимум сдвинут по сравнению со спектром поглощения и его максимумом в длинноволновую область. это означает, что средняя энергия квантов люминесценции меньше средней энергии поглощенных квантов. Правило зеркальной симметрии Лёвшина. Правило Левшина, называемое также законом зеркальной симметрии, утверждает, что спектры флуоресценции по форме зеркально симметричны длинноволновой полосе спектра поглощения, если они построены в шкале частот (энергий). 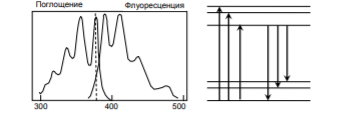 Слева: спектры; справа – электронные уровни и переходы. Тушение люминесценции. Уменьшение выхода люминесценции под влиянием этих факторов называют тушением люминесценции. Концентрационное тушение. Указанный эффект начинает проявляться с некоторой пороговой» концентрации С0, при этом имеет место экспоненциальная зависимость выхода люминесценции от концентрации: j = j0 e-u(C - Co) , где j0 — выход люминесценции при бесконечном разбавлении; u — константа. Температурное тушение. Повышение температуры вызывает уменьшение выхода флуоресценции и фосфоресценции. Это связано с тем, что безызлучательная дезактивация электронно-возбужденных состояний осуществляется преимущественно при соударениях излучающих молекул, а частота таких соударений в растворах прямо пропорциональна температуре. Охлаждение наоборот. Тушение посторонними веществами. Выход люминесценции может уменьшаться в присутствии посторонних веществ, называемых тушителями. (тяжелые анионы и катионы (I−, Br−, Cs+, Cu2+ и др.); парамагнитные ионы и молекулы (Mn2+, O2 и др.); молекулы растворителя.) Статическое тушение обусловлено образованием нелюминесцирующего продукта взаимодействия люминофора с тушителем. Динамическое тушение происходит, когда взаимодействие люминофора и тушителя имеет физический характер, а тушение люминесценции осуществляется за счет передачи энергии от электронно-возбужденных молекул люминофора к частицам тушителя. Чувствительность и селективность метода. Люминесцентные методы анализа отличаются большой чувствительностью: для большинства определяемых соединений пределы обнаружения не превышают 10-3 мкг/мл. В комбинации с чувствительностью и селективностью биохимических реакций он позволяет определять исключительно низкие концентрации вещества. Например, при определении озона удается обеспечить абсолютную селективность. Примеры практического применения. -В фармакологии подобный анализ используют для идентификации лекарств и препаратов, обладающих ярко выраженными люминесцентными свойствами. – применение люминесцентных добавок для выявления неоднородностей и дефектов в металлургии; – получение декоративных красящих составов; – изготовление элементов фотолюминесцентных эвакуационных систем. 2.Газовая Хроматография: Явление, лежащее в основе газовой хроматографии. Газовая хроматография (ГХ) — процесс разделения компонентов смеси, основанный на различии в равновесном распределении компонентов между двумя фазами —подвижной и неподвижной Виды газовой хроматографии. 1.газо-твердофазная - адсорбционная хроматография. Разделение в газо-адсорбционной хроматографии достигается за счет различной адсорбции на НФ. 2.газо-жидкостная- распределительная хроматография. НФ – высокомолекулярная жидкость, нанесенная на твердый носитель. Разделение достигается за счет различной растворимости компонентов образца в ПФ и НФ. Устройство хроматографа. 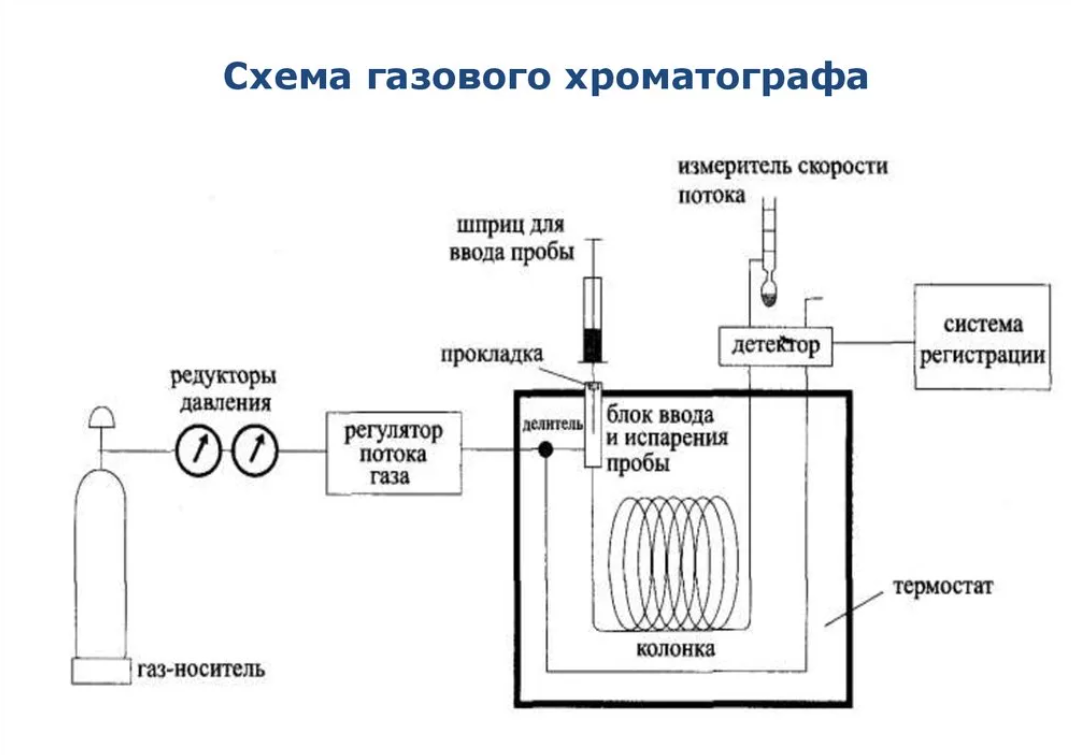 Газовый хроматограф представляет собой устройство для анализа сложных газовых веществ путем их дифференцирования на монокомпоненты. Далее компоненты смеси подвергаются анализу на предмет качественных и количественных характеристик. При этом исследования можно проводить с применением любых физических и химических способов. Основные виды используемых колонок. Насадочным. оборудования, при котором оно равномерно заполнено твердой фазой — силикагелем, оксидом алюминия, целлюлозой. Капиллярным. Неподвижная фаза не занимает весь объем трубки, а нанесена на ее внутренние стенки тонким слоем. Носитель с растворенным веществом проходит по колонке с большой скоростью, разделяясь на поверхности адсорбента. Подобный способ хроматографии позволяет увеличить скорость и точность анализа, поэтому является предпочтительным для разделения большинства сложных веществ. Капиллярные колонки делят на: – открытые (незаполненные); – открытые с пористым слоем ; – открытые с твердым носителем . Основные типы детекторов. Из существующих типов детекторов, используемых в газовой хроматографии, наиболее распространенные – это пламенно-ионизационный детектор (ПИД) и детектор по теплопроводности (ДТП),называемый термокондуктометрическим. Примеры практического применения. При производственном анализе для переработки нефти, газа, пластмассы. В фармацевтической отрасли, при производстве пищевых продуктов, парфюмов, пр. Для экологического мониторинга, чтобы выявить пестициды, диоксины, гербициды, бифенилы, полиароматические углеводы. При использовании недр, добыче газа, нефти. Для проведения судебно-медицинской экспертизы на предмет выявления наркотиков, сильнодействующих, взрывчатых веществ. Для проведения лабораторных, научных исследований. Вариант 3. 1.Основные положения спектроскопии: Основные и возбужденные состояния молекул (на примере двухатомной молекулы). 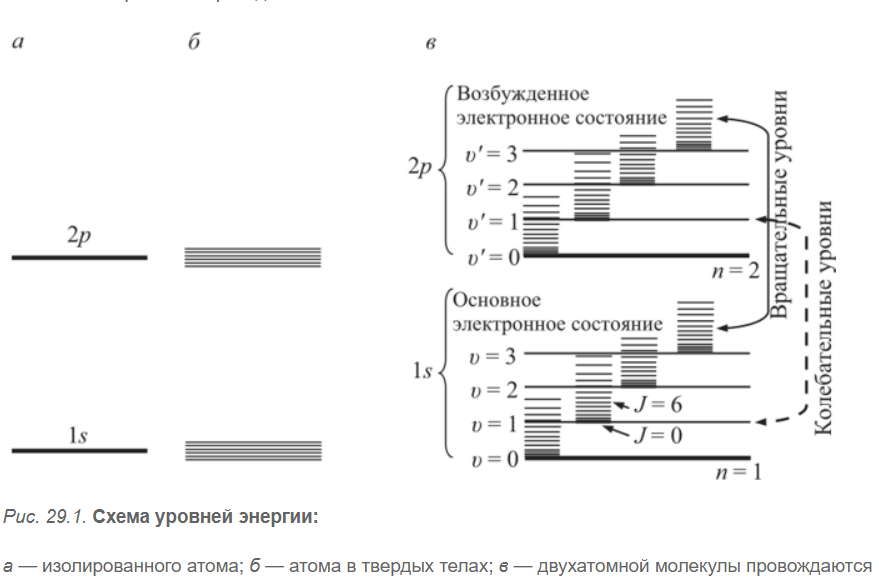 изменением колебательной энергии молекулы, а при колебательных переходах изменяется и вращательная энергия. изменением колебательной энергии молекулы, а при колебательных переходах изменяется и вращательная энергия.Схемы электронных уровней молекулы. 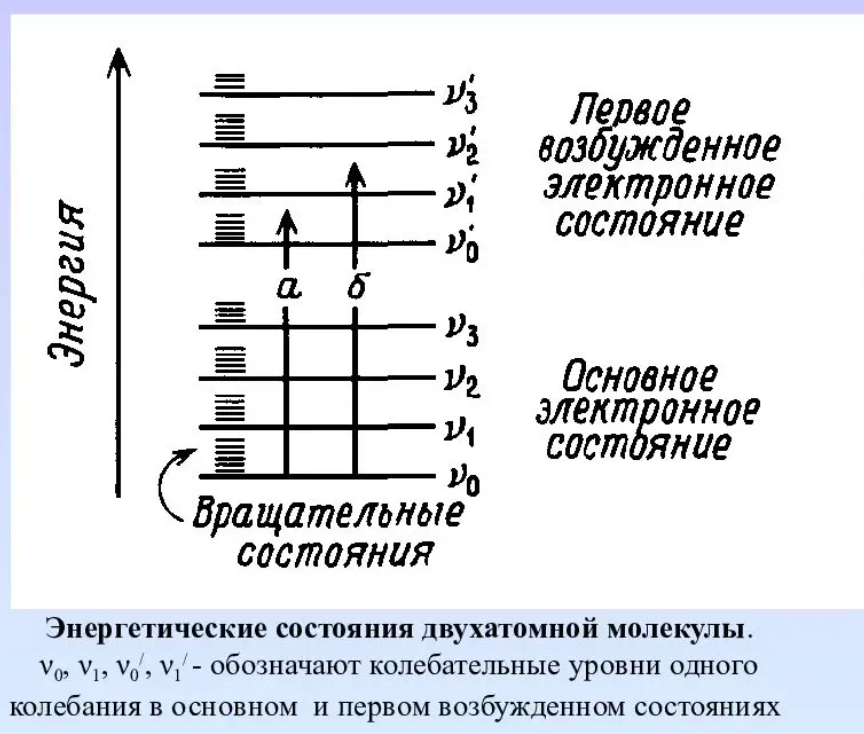 Принцип Франка-Кондона. Франка - Кондона принцип является правилом в спектроскопии и химии квантовой , что объясняет интенсивность колебательных переходов . Вибронные переходы - это одновременные изменения электронных и колебательных уровней энергии молекулы из-за поглощения или испускания фотона соответствующей энергии. Принцип гласит, что во время электронного перехода изменение с одного уровня колебательной энергии на другой будет более вероятно, если две колебательные волновые функции перекрываются более значительно. |
