Моль. Вещество это любая совокупности атомов и молекул, находящаяся в определенном агрегатном состоянии. Атом
 Скачать 190.34 Kb. Скачать 190.34 Kb.
|
|
I. 11. Kristallgidratlar I. 1. Na2HPO4∙nH2O da 11,57 % fosfor bor.shu kristalogidrat tarkibidagi n ning qiymatini toping. A)6 B)8 C)7 D)10 Решение: 1-usul. 1) Na2HPO4∙nH2O мольekulyar massasini topamiz. 142 18n 2) 11,57% P ───── 31 г bo’lsa 100% da ───── x= x= 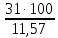 = 268 г = 268 г 3) 268 г kristalogidratning umumiy massasi undan Na2HPO4 ni massasini ayiramiz bunda H2O massasi qoladi. 4) 268-142 = 126 г H2O bo’ladi. 5) suvning massasini мольekulyar massasiga bo’lsak мольi kelib chiqadi. n = 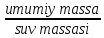 = = 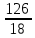 = 7 ОТВЕТ:Na2HPO4∙7H2O = 7 ОТВЕТ:Na2HPO4∙7H2O2-usul. Tenglama bo’yicha hisoblash. Na2HPO4∙nH2O 142 18n umumiy massa 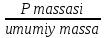 = = 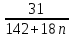 = = 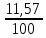 (31∙100)=(142+18n)∙11,57 3100=1642,94+208,26n 3100-1642,94=208,26n 1457,06=208,26n n = 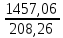 = 7 ОТВЕТ:Na2HPO4∙7H2O = 7 ОТВЕТ:Na2HPO4∙7H2O2. CuSO4∙nH2O tarkibida 12,8% S bo’lsa shu kristalogidrat tarkibidagi n ni toping. A)4 B)6 C)5 D)7 3. Kristal so’da tarkibida 4,2% C bo’lsa, unda necha мольekula suv bo’ladi. A)7 B)10 C)8 D)9 4. FeSO4∙nH2O kristalogidrat tarkibida 11,51% S bo’lsa n ni toping. A)5 B)6 C)8 D)7 5. Gips tarkibida 18,6% S bo’lsa necha мольekula suv bo’ladi. A)0,5 B)2 C)5 D) 6. Na2CO3∙nH2O tarkibli kristalogidrat tarkibida 17,16% Na bo’lsa n ni qiymatini toping. A)9 B)8 C)10 D)7 7. Quyidagi kristalogidrat tarkibida CuSO4∙nH2O 25,6% Cu bo’lsa shu kristalogidrat tarkibida necha мольekula suv bo’ladi. A)4 B)3 C)7 D)5 8. CaSO4∙nH2O tarkibida 22,07% oltingugurt bo’lsa suv мольekulalarini toping. A)1,5 B)0,5 C)2 D)3 9. Rux kuparosi tarkibida 22,65% Zn bo’lsa rux kuporosida necha мольekula suv bo’ladi. A)7 B)6 C)8 D)9 10. Glauber tuzi deb ataladigan tuz Na2SO4∙nH20 tarkibida natriyning massa ulushi 16,08% ga teng. Bu tuz tarkibida necha моль suv bor. A)6 B)8 C)10 D)12 11. Magniy kuporosi MgSO4∙nH2O tarkibida magniyning massa ulushi 11,42% ga teng. n ning qiymatini toping. A)4B)5 C)6 D)7 12. MgSO4∙nH2O tarkibida oltingugurtning massa ulushi 13% ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)7 B)8 C)5 D)1 13. Temir (III)-sulfat Fe2(S04)3∙nH20 tarkibida oltingugurt bilan temirning massa ulushi 37,0% ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)8 B)10 C)12D)9 14. Alyuminiy sulfat kristallgidrati Al2(S04)3∙nH20 tarkibida alyuminiyning massa ulushi 9,67% ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)10B)12 C)16 D)16 15. Alyuminiy nitrat kristallgidrati A1(N03)3∙nH20 tarkibida azotning massa ulushi 0,1239 ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)6B)7 C)8 D)9 16. Bura (tanakor) deb ataluvchi Na2B4O7∙nH20 tarkibida borning massa ulushi 0,1606 ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)2B)4 C)6 D)8 17. MgSO4 ning taxir tuz deb nomlanuvchi kristallgidrati tarkibida 51,22% suv bo’lsa, shu kristallgidrat MgSO4∙nH20 dagi n ni toping. A)2 B)3 C)4D)7 18. Alyuminiy sulfat kristallgidrati tarkibidagi alyuminiyning massa ulushi 8,1% ga teng bo’lsa, kristallgidrat tarkibidagi suvning мольlar sonini aniqlang. A)6 B)9 C)12 D)18 19. Temir kuporosi tarkibidagi oltingugurtning massa ulushi 11,50% ni tashkil etsa kristallogidratdagi n ning qiymatini toping. A)7 B)10 C)4 D)12 20. Marganets (II)-sulfat kristallgidrati tarkibida 24,66% marganes bo’lsa, uning formulasi qanday bo’ladi. A)MnSO4∙H2O B)MnSO4∙3H2OC)MnSO4∙4H2O D)MnSO4∙5H2O II.21. CuSO4∙nH2O kristalogidrat tarkibida kislorodning massa ulushi 57,6% bo’lsa, kristalogirat tarkibida necha мольekula suv bor. A)6 B)7 C)5 D)4 Решение: 1-usul. Dioganal usuli. 1)mis sulfat va suv tarkibidagi kislorodning massa ulushlarini topamiz CuSO4 C% = 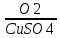 = = 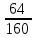 ∙100 = 40% kislorod bor. ∙100 = 40% kislorod bor.H2O C% = 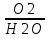 = = 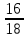 ∙100 = 88,89% kislorod bor. ∙100 = 88,89% kislorod bor.2  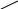 ) (CuSO4) 40 31,3 ─── 160 г CuSO4 bo’lsa ) (CuSO4) 40 31,3 ─── 160 г CuSO4 bo’lsa57,6 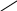  (H2O) 88,89 17,6 ─── x = x = (H2O) 88,89 17,6 ─── x = x = 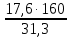 = 90 г H2O = 90 г H2O3) suvni мольini topamiz 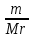 = = 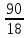 = 5 demak kristalogidrat tarkibida 5 мольekula suv bor ekan. ОТВЕТ:CuSO4∙5H2O = 5 demak kristalogidrat tarkibida 5 мольekula suv bor ekan. ОТВЕТ:CuSO4∙5H2O2-usul.tenglama usuli CuSO4∙nH2O tarkibida 160 + 18n = 100% kristalogidrat desak 64 + 16n = 57,6% kislorod bor. C% = 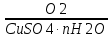 = = 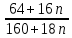 = = 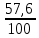 (160+18n)∙57,6 = (64+16n)∙100 9216+1036,8n = 6400+1600n 9216-6400 = 1600-1036,8n 2816 = 563,2n n = 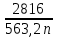 = 5 ОТВЕТ:CuSO4∙5H2O = 5 ОТВЕТ:CuSO4∙5H2O22. ZnSO4∙nH2O kristalogidrat tarkibida 61,32% O2 bo’lsa,shu kristalogidrat tarkibida n ning qiymati nechchiga teng A)7 B)6 C)5 D)8 23. Na2CO3∙nH2O kristalogidrat tarkibida 72,73% kislorod bo’lsa. n ni toping. A)9 B)10 C)7 D)8 24. Na2SO4 ∙nH2O tarkibli kristallgidratda kislorodning massa ulushi 67,13% bo’lsa, мольekulada necha моль suv bor. A)7 B)10C)8 D)9 25. Fe2(SO4)3∙nH2O kristallogidratdagi kislorodning massa ulushi 62,33% bo’lsa, n ning qiymatini aniqlang. A)9 B)8 C)20D)12 26. CaSO4∙nH2O tarkibli kristalogidrat tarkibida 2,32% H2 bo’lsa, n ni toping. A)2 B)0,5 C)1,5 D)3 27. FeSO4∙nH2O kristalogidrat tarkibida 63,3% O2 bo’lsa,necha мольekula suv bor. A)8 B)5 C)7 D)6 28. Na2HPO4∙nH2O da 3,57 % vodorod bor.shu kristalogidrat tarkibidagi n ning qiymatini toping. A)3 B)2 C)4 D)6 29. Bura (tanakor) deb ataluvchi Na2B4O7∙nH20 tarkibida kislorodning massa ulushi 0,727 ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)11 B)12 C)4 D)10 30. CaSO4∙nH2O tarkibli kristalogidrat tarkibida 58,95% O2 bo’lsa, n ni toping. A)2 B)0,5 C)1,5 D)3 31. Alyuminiy nitrat kristallgidrati A1(N03)3∙nH20 tarkibida kislorodning massa ulushi 0,7298 ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)3 B)12C)4 D)6 32. Temir (III)-sulfat Fe2(S04)3∙nH20 tarkibida kislorodning massa ulushi 57,79% ga teng bo’lsa, n ning qiymati qancha bo’ladi. A)7 B)5 C)8 D)9 33. Taxir tuzi deb ataluvchi kristalogidrat tarkibida O2 ning massa ulushi 72,54% bo’lsa,shu tuzni tarkibidagi H2O miqdorini toping. A)6 B)7 C)5 D)9 34. Na2SO4∙nH2O kristalogidrat tarkibida 67,13% O2 bo’lsa,n ni toping. A)10 B)9 C)8 D)7 35. MgHPO4∙nH2O kristalogidrat tarkibida vodorodning massa ulushi 4,02% bo’lsa,necha мольekula suv bor. A)3 B)4 C)6 D)2 Найдите формулу вешест (1-12)
Modda (suv) yoki tuzni tarkibidagi element (lar) ni massa ulush (lar) iga asoslanib kristallizasiya suvini (n) aniqlash (1-20)
Найдите по массовую долю килорода или водорода формулу кристаллогидрата (1-20)
Все вещества можно разделить на две группы: простые и сложные. К простым относят вещества, состоящие из атомов одного элемента. Например: углерод, натрий, сера. Сложное вещество образовано атомами разных элементов. Например: оксид меди, серная кислота и т.п. В свою очередь простые и сложные вещества делятся на классы: В Е Щ Е С Т В А _________________________________ простые сложные ____/______ ______________/___________ металлы неметаллы оксиды гидроксиды соли К, Ва S, P Р2О5 H2SO4 Cu(NO3)2 Na2O Вa(ОH)2 Na2CO3 ZnO Al(OH)3 Рассмотрим классификацию, химические свойства и методы получения сложных веществ. 1.1. ОКСИДЫ ОКСИД – это сложное вещество, состоящее из двух элементов, один из которых кислород, находящийся в степени окисления -2. Исключения составляют: соединения кислорода и фтора – фториды: например, фторид кислорода OF2 (степень окисления кислорода в этом соединении +2) пероксиды (соединения некоторых элементов с кислородом, в которых имеется связь между атомами кислорода), например: H-O-O-H K-O-O-K пероксид водорода Н2О2 пероксид калия K2O2 Примеры оксидов: оксид кальция - СаО, оксид бария - ВаО. Если элемент образует несколько оксидов, то в их названии в скобках указывается римской цифрой валентность элемента, например: оксид серы (IV) - SO2, оксид серы (VI) - SO3. Все оксиды можно разделить на две большие группы: солеобразующие(образующие соли) и несолеобразующие. Солеобразующие подразделяют на три группы: основные, амфотерные и кислотные. О К С И Д Ы _________________/__________________ солеобразующие несолеобразующие _________________________________ СО, N2O, NO ↓ ↓ ↓ основные амфотерные кислотные (им (им соответсвуют соответствуют, кислоты) основания) CaO, Li2O ZnO, BeO, PbO P2O5, Mn2О7 Cr2O3, Al2O3 Неметаллы образуют кислотные оксиды, например: оксид азота (V) – N2O5 , оксид углерода (IV) - CO2. Металлы с валентностью меньше трех, как правило, образуют основные оксиды, например: оксид натрия -Na2O, оксид магния – MgO; а с валентностью больше четырех – кислотные оксиды, например, оксид марганца (VII) - Mn2O7, оксид вольфрама (VI) - WO3. Рассмотрим химические свойства кислотных и основных оксидов. ХИМИЧЕСКИЕ СВОЙСТВА ОКСИДОВ ОСНОВНЫХ КИСЛОТНЫХ 1. Взаимодействие с водой Продуктом реакции является: основание кислота (если, в состав оксида P2O5 + 3H2O 2H3PO4 входит активный металл, SiO2 +H2O ≠ Li, Na, K, Rb, Cs, Fr, Ba, Ca) CaO + H2O Ca(OH)2 CuO+ H2O ≠ 2. Взаимодействие друг с другом, образуя соли CuO + SO3 CuSO4 3. Взаимодействие с гидроксидами: |
