Значение биохимии в подготовке врача. Биологическая химия
 Скачать 8.33 Mb. Скачать 8.33 Mb.
|
|
| Печень | Мышцы | Жировая ткань |
| | Активация | |
| 1 . Фосфодиэстераза | 1 . Фосфодиэстераза | 1 . ЛП-липаза |
| 2. Фосфофруктокиназа | 2. Фосфофруктокиназа | 2. Фосфофруктокиназа |
| 3. Пируваткиназа | 3. Пируваткиназа | 3. Пируваткиназа |
| 4. Пируватдегидрогеназный комплекс | 4. Пируватдегидрогеназный комплекс | 4. Ацетил-КоА-карбоксилаза |
| 5. Фосфатаза гликогенсинтазы и гликогенфосфорилазы | 5. Фосфатаза гликогенсинтазы | |
| б.Ацетил-КоА-карбоксилаза | | |
| | Индукция | |
| 1 . Глюкокиназа | | 1 . Глицеральдегидфосфат- дегидрогеназа |
| 2. Цитратлиаза | | 2. Пальмитатсинтаза |
| 3. Пальмитатсинтаза | | |
| 4. Пируваткиназа | | |
| 5. Ацетил-КоА-карбоксилаза | | |
| 6. Глюкозо-6-фосфатдегидрогеназа | | |
| | Репрессия | |
| Фосфоенолпируваткарбоксикиназа | | |
в результате чего происходит активация синтеза гликогена и тормозится его распад.
Эффекты инсулина, обусловленные фосфорилированием и дефосфорилированием ферментов, проявляются очень быстро, в течение нескольких секунд и минут. Параллельно с активацией ферментов гликолиза инсулин тормозит глюконеогенез, репрессируя синтез ключевого фермента глюконеогенеза - фосфоенолпируваткарбок-сикиназы (ФЕП карбоксикиназы).
Влияние инсулина на метаболизм жиров. Инсулин в жировой ткани тормозит мобилизацию жиров. Он активирует фосфатазу, которая дефосфорилирует и тем самым инактивирует гормончувствительную ТАГ-липазу. Таким образом, под влиянием инсулина снижается концентрация жирных кислот, циркулирующих в крови. Инсулин стимулирует потребление нейтральных аминокислот в мышцах и синтез белков в печени, мышцах и сердце.
3. Механизм действия инсулина
Действие инсулина начинается с его связывания со специфическим гликопротеиновым рецептором на поверхности клетки-мишени. Рецепторы инсулина обнаружены почти во всех типах клеток, но больше всего их в гепатоцитах и клетках жировой ткани. Так как концентрация инсулина в крови составляет 10-10 М, количество рецепторов, связанных с инсулином, зависит от их количества на мембране клетки. Клетки с разным содержанием рецепторов реагируют по разному на одну и ту же концентрацию гормона.
Снижение чувствительности клеток к гормону (десенситизация) опосредуется 2 механизмами. Первый включает утрату рецепторов путём их интернализации. Комплекс инсулин-рецептор захватывается внутрь клетки эндоцитозом. В результате интернализации часть рецепторов подвергается разрушению в лизосомах, а часть возвращается в плазматическую мембрану. Второй механизм десенситизации - ковалентная модификация рецептора в результате фосфорилирования. Рецептор инсулина относят к типу рецепторов, обладающих тирозинкиназной активностью. Стимулированное инсулином аутофосфорилирование β-субъединицы IR по остаткам тирозина приводит к фосфорилированию других внутриклеточных белков - субстратов инсулинового рецептора (IRS). Известно несколько таких субстратов: IRS-1, IRS-2, а также некоторые белки семейства STAT.
Главную роль в формировании ответной реакции клетки на инсулиновый сигнал играет IRS-1. IRS-1 - фосфопротеин, состоящий из более чем 1200 аминокислотных остатков. Часть остатков серина, тирозина и треонина фосфорилирована. При стимуляции инсулином степень фосфорилирования IRS-1 увеличивается и придаёт ему способность соединяться с другими цитозольными белками. Это приводит к активации нескольких сигнальных путей, представляющих каскад реакций активации специфических протеинкиназ. В результате активации протеинкиназ происходит фосфорилирование ферментов и факторов транскрипции, что составляет основу многочисленных эффектов инсулина.
Эффекты инсулина могут проявляться в течение секунд и минут (транспорт веществ, фосфорилирование и дефосфорилирование белков, активация и ингибирование ферментов, синтез РНК) или через несколько часов (синтез ДНК, белков, рост клеток).
Основную роль в поддержании энергетического гомеостаза играют гормоны инсулин и глюкагон. а также другие контринсулярные гормоны - адреналин, кортизол, йодтиронины и соматотропин. Инсулин и глюкагон играют главную роль в регуляции метаболизма при смене абсорбтивного и постабсорбтивного периодов и при голодании.
А. Абсорбтивный период
Абсорбтивный период характеризуется временным повышением концентрации глюкозы, аминокислот и жиров в плазме крови. Клетки поджелудочной железы отвечают на это повышение усилением секреции инсулина и снижением секреции глюкагона. Увеличение отношения инсулин/глюкагон вызывает ускорение использования метаболитов для запасания энергоносителей: происходит синтез гликогена, жиров и белков. Режим запасания включается после приёма пищи и сменяется режимом мобилизации запасов после завершения пищеварения. Тип метаболитов, которые потребляются, депонируются и экспортируются, зависит от типа ткани. Главные органы, связанные с изменениями потока метаболитов при смене режимов мобилизации и запасания энергоносителей, - печень, жировая ткань и мышцы (рис. 11-28).
1. Изменения метаболизма в печени
в абсорбтивном периоде
После приёма пищи печень становится главным потребителем глюкозы, поступающей из пищеварительного тракта. Почти 60 из каждых 100 г глюкозы, транспортируемой портальной системой, задерживается в печени. Увеличение потребления печенью глюкозы - не результат ускорения её транспорта в клетки (транспорт глюкозы в клетки печени не стимулируется инсулином), а следствие ускорения метаболических путей, в которых глюкоза превращается в депонируемые формы энергоносителей: гликоген и жиры.
При повышении концентрации глюкозы в гепатоцитах происходит активация глюкокиназы, превращающей глюкозу в глюкозо-6-фосфат. Глюкокиназа имеет высокое значение Кm для глюкозы, что обеспечивает высокую скорость фосфорилирования при высоких концентрациях глюкозы. Кроме того, глюкокиназа не ингибируется глюкозо-6-фосфатом (см. раздел 7). Инсулин индуцирует синтез мРНК глюкокиназы. Повышение концентрации глюкозо-6-фосфата в гепатоцитах обусловливает ускорение синтеза гликогена. Этому способствуют одновременная инактивация гликогенфосфорилазы и активация гликогенсинтазы. Под влиянием инсулина в гепатоцитах ускоряется гликолиз в результате повышения активности и количества ключевых ферментов: глюкокиназы, фосфофруктокиназы и пируваткиназы. В то же время происходит торможение глюконеогенеза в результате инактивации фруктозо-1,6-бисфосфатазы и снижения количества фосфоенолпируваткарбоксикиназы - ключевых ферментов глюконеогенеза. Повышение концентрации глюкозо-6-фосфата в гепатоцитах в абсорбтивном периоде, сочетается с активным использованием NADPH для синтеза жирных кислот, что способствует стимуляции пентозофосфатного пути.
Ускорение синтеза жирных кислот обеспечивается доступностью субстратов (ацетил-КоА и NADPH), образующихся при метаболизме глюкозы, а также активацией и индукцией ключевых ферментов синтеза жирных кислот (см. раздел 8 и табл. 11-7).
В абсорбтивном периоде в печени ускоряется синтез белков. Однако количество аминокислот, поступающих в печень из пищеварительного тракта, превышает возможности их использования для синтеза белков и других азотсодержащих соединений. Излишек аминокислот либо поступает в кровь и транспортируется в другие ткани, либо дезаминируется с последующим включением безазотистых остатков в общий путь катаболизма (см. раздел 9).
2. Изменения метаболизма в адипоцитах
Основная функция жировой ткани - запасание энергоносителей в форме триацилгли-церолов. Под влиянием инсулина ускоряется транспорт глюкозы в адипоциты. Повышение
588
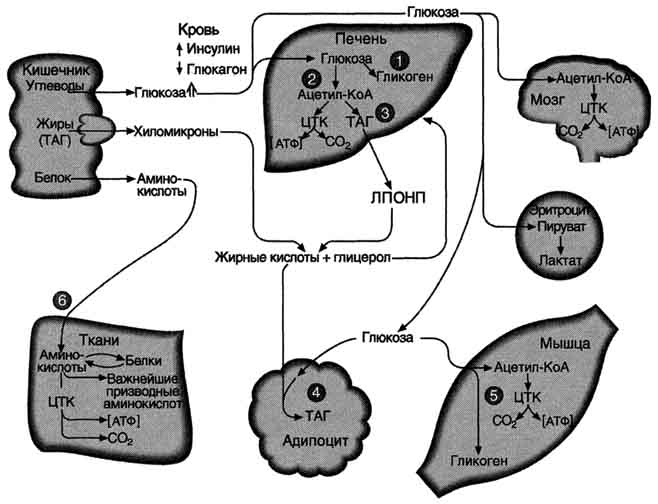
Рис. 11-28. Пути использования основных энергоносителей в абсорбтивном периоде. 1 - биосинтез гликогена в печени; 2 - гликолиз; 3 - биосинтез ТАГ в печени; 4 - биосинтез ТАГ в жировой ткани; 5 - биосинтез гликогена в мышцах; 6 - биосинтез белков в разных тканях, в том числе в печени.
внутриклеточной концентрации глюкозы и активация ключевых ферментов гликолиза обеспечивают образование ацетил-КоА и глицерол-3-фосфата, необходимых для синтеза ТАГ. Стимуляция пентозофосфатного пути обеспечивает образование NADPH, необходимого для синтеза жирных кислот. Однако биосинтез жирных кислот de novo в жировой ткани человека протекает с высокой скоростью только после предшествующего голодания. При нормальном ритме питания для синтеза ТАГ используются в основном жирные кислоты, поступающие из ХМ и ЛПОНП под действием ЛП-липазы (см. раздел 8). Вместе с тем при увеличении отношения инсулин/глюкагон гормончувствительная ТАГ-липаза находится в дефосфорилированной неактивной форме, и процесс липолиза тормозится.
3. Изменение метаболизма в мышцах
в абсорбтивном периоде
В абсорбтивном периоде под влиянием инсулина ускоряется транспорт глюкозы в клетки мышечной ткани. Глюкоза фосфорилируется и окисляется для обеспечения клетки энергией, а также используется для синтеза гликогена. Жирные кислоты, поступающие из ХМ и ЛПОНП, в этот период играют незначительную роль в энергетическом обмене мышц. Поток аминокислот в мышцы и биосинтез белков также увеличиваются под влиянием инсулина, особенно после приёма белковой пищи.
589
Б. Постабсорбтивный период
Постабсорбтивным состоянием называют период после завершения пищеварения до следующего приёма пищи. Если пища не принимается в течение суток и более, то это состояние определяют как голодание. Типичным постабсорбтивным периодом считают состояние после 12-часового ночного перерыва в приёме пищи. В начале постабсорбтивного периода концентрация глюкозы в крови снижается, вследствие чего снижается секреция инсулина и повышается концентрация глюкагона. При снижении индекса инсулин/глюкагон ускоряются процессы мобилизации депонированных энергоносителей (рис. 11-29).
В постабсорбтивном периоде изменения метаболизма направлены, главным образом, на поддержание концентрации в крови глюкозы, которая служит основным энергетическим субстратом для мозга и единственным источником энергии для эритроцитов. Основные изменения метаболизма в этот период происходят в печени и жировой ткани.
1. Изменения метаболизма в печени
В печени прежде всего ускоряется мобилизация гликогена (см. раздел 7). Однако запасы гликогена в печени истощаются в течение 18-24 ч голодания. Главным источником глюкозы по мере исчерпания запасов гликогена становится глюконеогенез, который начинает ускоряться через

Рис. 11-29. Изменения метаболизма основных энергоносителей при смене абсорбтивного состояния на постабсорбтивное. КТ - кетоновые тела; ЖК - жирные кислоты.
590
4-6 ч после последнего приёма пищи. Субстратами для синтеза глюкозы служат глицерол, аминокислоты и лактат. При высокой концентрации глюкагона скорость синтеза жирных кислот снижается вследствие фосфорилирования и инактивации ацетил-КоА-карбоксилазы, а скорость р-окисления возрастает. Вместе с тем увеличивается снабжение печени жирными кислотами, которые транспортируются из жировых депо. Ацетил-КоА, образующийся при окислении жирных кислот, используется в печени для синтеза кетоновых тел.
2. Изменения метаболизма в жировой ткани
В жировой ткани при повышении концентрации глюкагона снижается скорость синтеза ТАГ и стимулируется липолиз. Стимуляция липолиза - результат активации гормончувствительной ТАГ-липазы адипоцитов под влиянием глюкагона. Жирные кислоты становятся важными источниками энергии в печени, мышцах и жировой ткани.
Таким образом, в постабсорбтивнрм периоде концентрация глюкозы в крови поддерживается на уровне 80-100 мг/дл, а уровень жирных кислот и кетоновых тел возрастает.
Сахарный диабет - заболевание, возникающее вследствие абсолютного или относительного дефицита инсулина.
А. Основные клинические формы сахарного диабета
Согласно данным Всемирной организации здравоохранения, сахарный диабет классифицируют с учётом различия генетических факторов и клинического течения на две основные формы: диабет I типа - инсулинзависимый (ИЗСД), и диабет II типа - инсулиннезависимый (ИНСД).
1. Инсулинзависимый сахарный диабет
Инсулинзависимый сахарный диабет - заболевание, вызываемое разрушением р-клеток островков Лангерханса поджелудочной железы.
Деструкция β-клеток - результат аутоиммунных реакций. В аутоиммунной реакции принимают участие лимфоциты и макрофаги (моноциты). Эти клетки продуцируют цитокины, которые либо непосредственно повреждают β-клетки, либо опосредуют клеточные реакции против β-клеток.
Провоцировать возникновение диабета I типа может вирусная инфекция, вызывающая деструкцию b-клеток. К таким вирусам, называемым β-цитотропными, относят вирусы оспы, краснухи, кори, цитомегаловирус, эпидемического паротита, Коксаки, аденовирус. Некоторые р-цитотропные вирусы вызывают лизис β-клеток.
Известны некоторые токсические вещества, например, такие как производные нитрозомочевины и другие нитро- или аминосодержащие соединения, избирательно поражающие β-клетки и индуцирующие аутоиммунную реакцию. Кроме того, ИЗСД может быть результатом частичного генетически обусловленного дефекта системы иммунологического надзора и сочетаться с другими аутоиммунными заболеваниями. На долю ИЗСД приходится примерно 25-30% всех случаев сахарного диабета. Как правило, разрушение β-клеток происходит медленно, и начало заболевания не сопровождается нарушениями метаболизма. Когда погибает 80-95% клеток, возникает абсолютный дефицит инсулина, и развиваются тяжёлые метаболические нарушения. ИЗСД поражает в большинстве случаев детей, подростков и молодых людей, но может проявиться в любом возрасте (начиная с годовалого).
2. Инсулинонезависимый сахарный диабет
Инсулинонезависимый сахарный диабет - общее название нескольких заболеваний, развивающихся в результате относительного дефицита инсулина, возникающего вследствие нарушения секреции инсулина, нарушения превращения проинсулина в инсулин, повышения скорости катаболизма инсулина, а также повреждения механизмов передачи инсулинового сигнала в клетки-мишени (например, дефекта рецептора инсулина, повреждения внутриклеточных посредников инсулинового сигнала и др.). ИНСД поражает людей, как правило, старше 40 лет. Сахарный диабет II типа характеризуется высокой частотой семейных форм. Риск ИНСД у ближайших родственников больного достигает 50%, тогда как при ИЗСД он не превышает 10%. Заболевание поражает преимущественно жителей развитых стран, особенно горожан.
Возможными причинами ИНСД могут быть: образование антител к рецепторам инсулина; генетический дефект пострецепторного аппарата инсулинзависимых тканей; нарушения регуляции секреции инсулина. К факторам, определяющим развитие и клиническое течение болезни, относят ожирение, неправильный режим питания, малоподвижный образ жизни, стресс.
Мутации генов, контролирующих секрецию инсулина, энергетический обмен в β-клетках и обмен глюкозы в клетках-мишенях инсулина, приводят к возникновению нескольких форм ИНСД с аутосомно-доминантным наследованием.
Основным провоцирующим фактором инсулинонезависимого диабета служит ожирение.
592
Этот тип диабета часто сочетается с гиперинсулинемией, что способствует ожирению. Таким образом, ожирение, с одной стороны, важнейший фактор риска, а с другой - одно из ранних проявлений сахарного диабета.
