Значение биохимии в подготовке врача. Биологическая химия
 Скачать 8.33 Mb. Скачать 8.33 Mb.
|
|
А. Антидиуретический гормон Антидиуретический гормон (АДГ), или вазопрессин - пептид с молекулярной массой около 1100 Д, содержащий 9 аминокислот, соединённых одним дисульфидным мостиком. 1. Синтез и секреция антидиуретического гормона АДГ синтезируется в нейронах гипоталамуса в виде предшественника препрогормона, который поступает в аппарат Гольджи и превращается в прогормон. В составе нейросекреторных гранул прогормон переносится в нервные окончания задней доли гипофиза (нейрогипофиз). Во время транспорта гранул происходит процессинг прогормона, в результате чего он расщепляется на зрелый гормон и транспортный белок - нейрофизин. Гранулы, содержащие зрелый антидиуретический гормон и нейрофизин, хранятся в терминальных расширениях аксонов в задней доле гипофиза, из которых секретируются в кровоток при соответствующей стимуляции. Стимулом, вызывающим секрецию АДГ, служит повышение концентрации ионов натрия и увеличение осмотического давления внеклеточной жидкости. При недостаточном потреблении воды, сильном потоотделении или после приёма большого количества соли осморецепторы гипоталамуса, чувствительные к колебаниям осмолярности, регистрируют повышение осмотического давления крови. Возникают нервные импульсы, которые передаются в заднюю долю гипофиза и вызывают высвобождение АДГ. Секреция АДГ происходит также в ответ на сигналы от барорецепторов предсердий. Изменение осмолярности всего на 1% приводит к заметным изменениям секреции АДГ. 2. Механизм действия Для АДГ существуют 2 типа рецепторов: V1 и V2. Рецепторы V2, опосредующие главный физиологический эффект гормона, обнаружены на базолатеральной мембране клеток собирательных трубочек и дистальных канальцев - наиболее важных клеток-мишеней для АДГ, которые относительно непроницаемы для молекул воды. В отсутствие АДГ моча не концентрируется и может выделяться в количествах, превышающих 20 л в сутки (норма 1,0-1,5 л в сутки). Связывание АДГ с V2(рис. 11-32) стимулирует аденилатциклазную систему и активацию протеинкиназы А. В свою очередь, протеинкиназа А фосфорилирует белки, стимулирующие экспрессию гена мембранного белка - аквапорина-2. Аквапорин-2 перемещается к апикальной мембране собирательных канальцев и встраивается в неё, образуя водные каналы. Это обеспечивает избирательную проницаемость мембраны клеток для воды, которые свободно диффундируют в клетки почечных канальцев и затем поступают в интерстициальное пространство. Поскольку в результате происходит реабсорбция воды из почечных канальцев и экскреция малого объёма высококонцентрированной мочи (антидиурез), гормон называют антидиуретическим гормоном. Рецепторы типа V1 локализованы в мембранах ГМК сосудов. Взаимодействие АДГ с рецептором V1 приводит к активации фосфолипазы С, которая гидролизует фосфатидилинозитол-4,5-бисфосфат с образованием инозитолтрифосфата и диацилглицерола. Инозитолтрифосфат вызывает высвобождение Са2+ из ЭР. Результатом действия гормона через рецепторы V1 является сокращение гладкомышечного слоя сосудов. Сосудосуживающий эффект АДГ проявляется при высоких концентрациях гормона. Поскольку сродство АДГ к рецептору V2 выше, чем к рецептору V1, при физиологической концентрации гормона в основном проявляется его антидиуретическое действие. 3. Несахарный диабет Дефицит АДГ, вызванный дисфункцией задней доли гипофиза, а также нарушениями в системе передачи гормонального сигнала, приводит к развитию несахарного диабета. При этом происходит нерегулируемая экскреция воды, а наиболее опасным последствием является дегидратация организма. Под названием "несахарный диабет" объединяют заболевания с разной этиологией. Так, 598 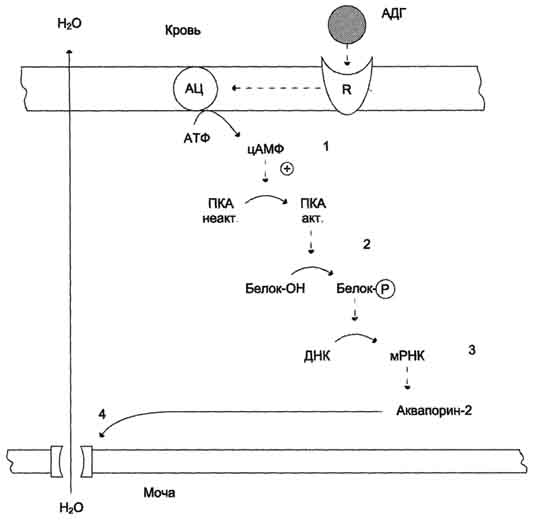 Рис. 11-32. Биологическое действие АДГ в клетках почечных канальцев. 1 - АДГ связывается с мембранным рецептором V2, вызывая активацию аденилатциклазы (АЦ) и образование цАМФ; 2 - цАМФ активирует протеинкиназу, фосфорилирующую белки; 3 - фосфорилированные белки индуцируют транскрипцию гена белка аквапорина; 4 - аквапорин встраивается в мембрану клетки почечного канальца. основными причинами центрального несахарного диабета могут быть генетические дефекты синтеза препро-АДГ в гипоталамусе, дефекты процессинга и транспорта проАДГ (наследственная форма), а также повреждения гипоталамуса или нейрогипофиза (например, в результате черепно-мозговой травмы, опухоли, ишемии). Нефрогенный несахарный диабет возникает вследствие мутации гена рецептора АДГ типа V2 (наследственная форма), следствием которого является неспособность почек реагировать на гормон. Основное проявление несахарного диабета - гипотоническая полиурия, т.е. выделение большого количества мочи низкой плотности. Снижение секреции АДГ приводит также к усиленному потреблению воды. Диагностические критерии несахарного диабета: выраженная полиурия (до 20 л в сутки, плотность мочи <1,010, в норме - 1,020). Б. Альдостерон Альдостерон - наиболее активный минера-локортикостероид, синтезирующийся в коре надпочечников из холестерола. Синтез и секреция альдостерона клетками клубочковой зоны непосредственно стимулируются низкой концентрацией Na+ и высокой концентрацией К+ в плазме крови. На секрецию альдостерона влияют также простагландины, 599 АКТГ. Однако наиболее важное влияние на секрецию альдостерона оказывает ренинангиотензиновая система. Альдостерон не имеет специфических транспортных белков, но за счёт слабых взаимодействий может образовывать комплексы с альбумином. Гормон очень быстро захватывается печенью, где превращается в тетрагидроальдостерон-3-глюкуронид и экскретируется с мочой. 1. Механизм действия альдостерона В клетках-мишенях гормон взаимодействует с рецепторами, которые могут быть локализованы как в ядре, так и в цитозоле клетки. Образовавшийся комплекс гормон-рецептор взаимодействует с определённым участком ДНК и изменяет скорость транскрипции специфических генов. Результат действия альдостерона - индукция синтеза: а) белков-транспортёров Na+ из просвета канальца в эпителиальную клетку почечного канальца; б) Nа+,К+,-АТФ-азы, обеспечивающей удаление ионов натрия из клетки почечного канальца в межклеточное пространство и переносящей ионы калия из межклеточного пространства в клетку почечного канальца; в) белков-транспортёров ионов калия из клеток почечного канальца в первичную мочу; г) митохондриальных ферментов ЦТК, в частности цитратсинтазы, стимулирующих образование молекул АТФ, необходимых для активного транспорта ионов (рис. 11-33). Суммарным биологическим эффектом индуцируемых альдостероном белков является увеличение реабсорбции ионов натрия в канальцах нефронов, что вызывает задержку NaCl в организме, и возрастание экскреции калия. 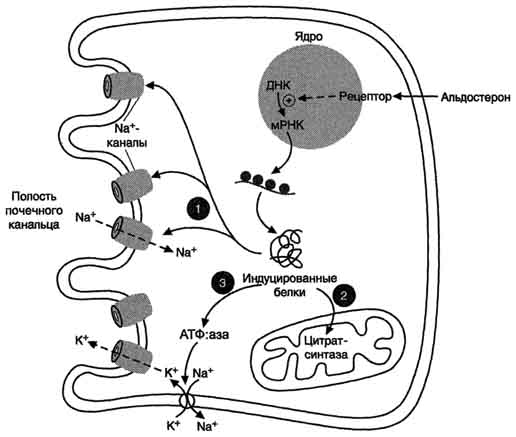 Рис. 11-33. Механизм действия альдостерона. Альдостерон, взаимодействуя с внутриклеточными рецепторами и стимулируя синтез белков: 1 - увеличивает реабсорбцию Na+ из мочи; 2 - индуцирует синтез ферментов ЦТК, активность которых обеспечивает продукцию АТФ; 3 - активирует Nа+,К+,-АТФ-азу, которая поддерживает низкую внутриклеточную концентрацию ионов натрия и высокую концентрацию ионов калия. 600 2. Роль системы ренин-ангиотензин- альдостерон в регуляции водно-солевого обмена Главным механизмом регуляции синтеза и секреции альдостерона служит система ренинангиотензин. Ренин - протеолитический фермент, продуцируемый юкстагломерулярными клетками, расположенными вдоль конечной части афферентных (приносящих) артериол, входящих в почечные клубочки (рис. 11-34). Юкстагломерулярные клетки особенно чувствительны к снижению перфузионного давления в почках. Уменьшение АД (кровотечение, потеря жидкости, снижение концентрации NaCl) сопровождается падением перфузионного давления в приносящих артериолах клубочка и соответствующей стимуляцией высвобождения ренина. Субстратом для ренина служит ангиотензиноген. Ангиотензиноген - α2-глобулин, содержащий более чем 400 аминокислотных остатков. Образование ангиотензиногена происходит в печени и стимулируется глюкокортикоидами и эстрогенами. Ренин гидролизует пептидную связь в молекуле ангиотензиногена и отщепляет N-концевой декапептид (ангиотензин I), не имеющий биологической активности. Под действием карбоксидипептидилпептидазы, или антиотензин-превращающего фермента (АПФ), выявленного в эндотелиальных клетках, лёгких и плазме крови, с С-конца ангиотензина I удаляются 2 аминокислоты и образуется октапептид - ангиотензин II. Ангиотензин II, связываясь со специфическими рецепторами, локализованными на поверхности клеток клубочковой зоны коры надпочечников 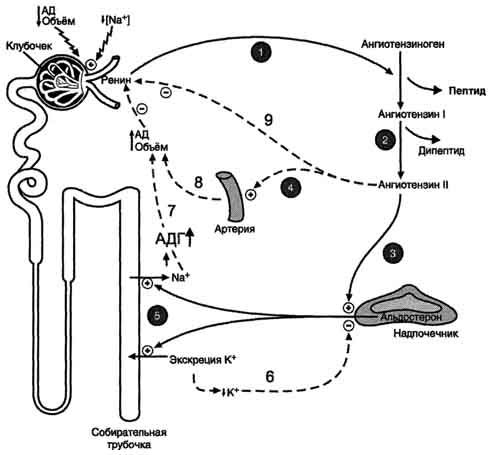 Рис. 11-34. Система ренинангиотензинальдостерон. Ренин, протеолитический фермент, катализирует превращение ангиотензиногена (гликопротеина) в ангиотензин I (декапептид). 1 - ренин, протеолитический фермент, катализирует превращение ангиотензиногена (глйкопротеина) в ангиотензин I; 2 - ангиотензин I превращается в ангиотензин II под действием АПФ, отщепляющего два аминокислотных остатка от декапептида; 3 - ангиотензин II стимулирует синтез и секрецию альдостерона; 4 - ангйотензин II вызывает сужение сосудов периферических артерий; 5 - альдостерон стимулирует реабсорбцию Na+ и экскрецию К+; 6, 7, 8, 9 - торможение секреции ренина и альдостерона по механизму отрицательной обратной связи. Пунктирные линии - регуляция по принципу обратной связи. 601 и ГМК, вызывает изменение внутриклеточной концентрации диацилглицерола и инозитолтрифосфата. Инозитолтрифосфат стимулирует высвобождение из ЭР ионов кальция, совместно с которым активирует протеинкиназу С, опосредуя тем самым специфический биологический ответ клетки на действие ангиотензина П. При участии аминопептидаз ангиотензин II превращается в ангиотензин III - гептапептид, проявляющий активность ангиотензина II. Однако концентрация гептапептида в плазме крови в 4 раза меньше концентрации октапептида, и поэтому большинство эффектов являются результатом действия ангиотензина П. Дальнейшее расщепление ангиотензина II и ангиотензина III протекает при участии специфических протеаз (ангиотензиназ). Ангиотензин II оказывает стимулирующее действие на продукцию и секрецию альдостерона клетками клубочковой зоны коры надпочечников, который, в свою очередь, вызывает задержку ионов натрия и воды, в результате чего объём жидкости в организме восстанавливается. Кроме этого, ангиотензин II, присутствуя в крови в высоких концентрациях, оказывает мощное сосудосуживающее действие и тем самым повышает АД. 3. Восстановление объёма крови при обезвоживании организма Уменьшение общего объёма жидкости, например в результате кровопотери, при обильной рвоте, диарее вызывает высвобождение ренина. Этому способствует также снижение импульсации от барорецепторов предсердий и артерий в результате уменьшения внутрисосудистого объёма жидкости. В результате увеличивается продукция ангиотензина II, наиболее мощного стимулятора секреции альдостерона. Повышение концентрации альдостерона в крови вызывает задержку ионов натрия, что является сигналом для осморецепторов гипоталамуса и секреции из нервных окончаний передней доли гипофиза АДГ, стимулирующего реабсорбцию воды из собирательных трубочек. Ангиотензин II, оказывая сильное сосудосуживающее действие, повышает АД и, кроме этого, усиливает жажду. Поступающая с питьём вода в большей мере, чем это происходит в норме, задерживается в организме. Увеличение объёма жидкости а, также повышение АД приводят к устранению стимула, который вызвал активацию ренинангиотензиновой системы, секрецию альдостерона и восстановление объёма крови (рис. 11-35). 4. Гиперальдостеронтм Гиперальдостеронизм - заболевание, вызванное гиперсекрецией альдостерона надпочечниками. Причиной первичного гиперальдостеронизма (синдром Кона) примерно у 80% больных является аденома надпочечников, в остальных случаях - диффузная гипертрофия клеток клубочковой зоны, вырабатывающих альдостерон. При первичном гиперальдостеронизме избыток альдостерона усиливает реабсорбцию натрия в почечных канальцах. Увеличение концентрации Na+ в плазме служит стимулом к секреции АДГ и задержке воды почками. Кроме того, усиливается выведение ионов калия, магния и протонов. В результате развиваются гипернатриемия, вызывающая, в частности, гипертонию, гипер-волемию и отёки, а также гипокалиемия, ведущая к мышечной слабости, возникают дефицит магния и лёгкий метаболический алкалоз. Вторичный гиперальдостеронизм встречается гораздо чаще, чем первичный, и может быть связан с рядом состояний (например, сердечная недостаточность, хронические заболевания почек, а также сопровождающиеся нарушением кровоснабжения опухоли, секретирующие ренин). При вторичном гиперальдостеронизме у больных наблюдают повышенный уровень ренина и ангиотензина II, что стимулирует кору надпочечников продуцировать и секретировать избыточное количество альдостерона. Клинические симптомы менее выражены, чем при первичном альдостеронизе. Одновременное определение концентрации альдостерона и активности ренина в плазме позволяет окончательно дифференцировать первичный (активность ренина в плазме снижена) и вторичный (активность ренина в плазме повышена) гиперальдостеронизм. В. Предсердный натриуретический фактор (ПНФ) Это пептид, содержащий 28 аминокислот с единственным диеульфидным мостиком. ПНФ синтезируется, главным образом, в кардиомио-цитах предсердий, и хранится в виде препро-гормона, состоящего из 126 аминокислотных остатков. 602 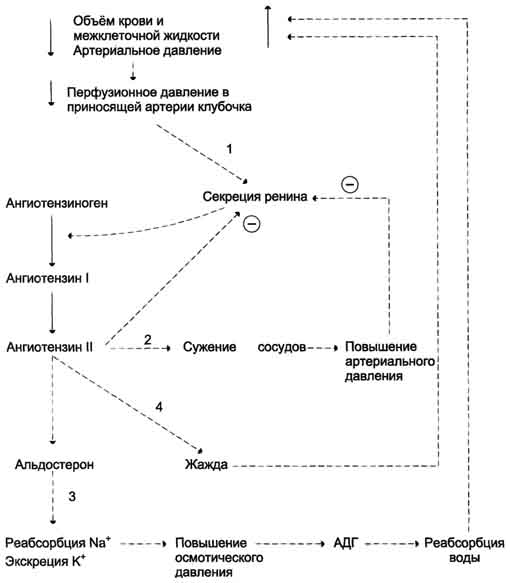 Рис. 11-35. Схема восстановления объёма крови при кровопотере и обезвоживании организма. 1 - уменьшение объёма жидкости и снижение АД активируют систему ренинангиотензинальдостерон; 2 - ангиотензин II вызывает сужение сосудов, что является экстренной мерой для поддержания АД; 3 - альдостерон стимулирует задержку натрия, вследствие чего происходит высвобождение вазопрессина и усиливается реабсорбция воды; 4 - ангиотензин II вызывает также чувство жажды, что способствует увеличению жидкости в организме. Основным фактором, регулирующим секрецию предсердного натрийуретического фактора, является увеличение АД. Другие стимулы секреции - увеличение осмолярности плазмы, повышение частоты сердцебиений, повышенный уровень катехоламинов и глюкокортикоидов в крови. Основные клетки-мишени ПНФ - почки, периферические артерии. В почках ПНФ стимулирует расширение приносящих артериол, усиление почечного кровотока, увеличение скорости фильтрации и экскреции ионов натрия. В периферических артериях ПНФ снижает тонус гладких мышц и соответственно расширяет артериолы (рис. 11-36). Таким образом, суммарным действием ПНФ является увеличение экскреции Na+ и понижение АД. Механизм передачи сигнала ПНФ не включает актвивацию G-белка. Рецептор ПНФ имеет доменное строение: домен связывания с лигандом, 603 локализованный во внеклеточном пространстве, и один домен, пронизывающий мембрану и обладающий активностью гуанилатциклазы. В отсутствие ПНФ его рецептор находится в фосфорилированном состоянии и неактивен. Связывание ПНФ с рецептором вызывает кон-формационные изменения и возрастание гуанилатциклазной активности рецептора. В результате ГТФ превращается в циклический ГМФ (цГМФ), который активирует протеинкиназу G (см. раздел 5). ПНФ обычно рассматривают как физиологический антагонист ангиотензина II, поскольку под его влиянием возникают не сужение просвета сосудов и задержка натрия, а, наоборот, расширение сосудов и увеличение почечной экскреции соли. 87. Регуляция обмена ионов кальция и фосфатов. Строение, биосинтез и механизм действия паратгормона, кальцитонина и кальцитриола. Причины и проявления рахита, гипо- и гиперпаратиреодизма. В организме взрослого человека содержится в среднем 1000 г кальция. Основным депо кальция в организме (99% всего кальция от общей массы) являются кости. В костях около 99% кальция присутствует в малорастворимой форме кристаллов гидроксиапатита [Са10(РО4)6(ОН)2Н2О]. В виде фосфатных солей в костях находится лишь 1% кальция, который может легко обмениваться и играть роль буфера при изменениях концентрации кальция в плазме крови. Другой фонд кальция (1% от общей массы кальция) - кальций плазмы крови. В плазму крови кальций поступает из кишечника (с водой и пищей) и из костной ткани (в процессе резорбции). Кальций - не только структурный компонент костной ткани. Ионы кальция играют ключевую роль в мышечном сокращении, увеличивают проницаемость мембраны клеток для ионов калия, влияют на натриевую проводимость клеток, на работу ионных насосов, способствуют секреции гормонов, участвуют в каскадном механизме свёртывания крови. Кроме этого, они служат важнейшими посредниками во внутриклеточной передаче сигналов. Концентрация кальция внутри клеток зависит от его концентрации во внеклеточной жидкости. Пределы колебаний общей концентрации Са2+ в плазме крови здоровых людей составляют 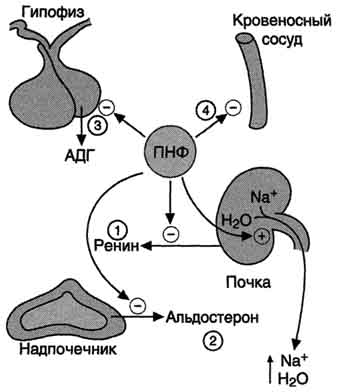 Рис. 11-36. Биологическое действие ПНФ. 1 - ингибирует выделение ренина; 2 - ингибирует секрецию альдостерона; 3 - ингибирует секрецию АДГ; 4 - вызывает релаксацию сосудов. 2,12-2,6 ммоль/л, или 9-11 мг/дл. Кальций плазмы крови представлен в виде:
Биологически активной фракцией является ионизированный кальций, концентрация которого поддерживается в пределах 1,1-1,3 ммоль/л. Изменение уровня кальция может привести к нарушению многих процессов: изменению порога возбудимости нервных и мышечных клеток, нарушению функционирования кальциевого насоса, снижению активности ферментов и нарушению гормональной регуляции метаболизма. Концентрация Са2+ в плазме регулируется с высокой точностью: изменение её всего на 1% приводит в действие гомеостатические механизмы, восстанавливающие равновесие. 604 Основными регуляторами обмена Са2+ в крови являются паратгормон, калыщтриол и каль-цитонин. |
