Значение биохимии в подготовке врача. Биологическая химия
 Скачать 8.33 Mb. Скачать 8.33 Mb.
|
|
2. Классификация гормонов по биологическим функциям По биологическим функциям гормоны можно разделить на несколько групп. Эта классификация условна, поскольку одни и те же гормоны могут выполнять разные функции. Например, адреналин участвует в регуляции обмена жиров и углеводов и, кроме этого, регулирует частоту сердечных сокращений, АД, сокращение гладких мышц. Кортизол не только стимулирует глюконеогенез, но и вызывает задержку NaCl. Классификация гормонов по биологическим функциям
81. Клетки-мишени и клеточные рецепторы гормонов. Рецепторы цитоплазматических мембран, рецепторы, локализованные в цитоплазме. Регуляция количества и активности рецепторов. Механизмы трансдукции сигналов рецепторами мембран, G-белок. Клетки-мишени - это клетки, которые специфически взаимодействуют с гормонами с помощью специальных белков-рецепторов. Эти белки-рецепторы располагаются на наружной мембране клетки, или в цитоплазме, или на ядерной мембране и на других органеллах клетки. Механизмы действия гормонов на клетки-мишени. В зависимости от строения гормона существуют два типа взаимодействия. Если молекула гормона липофильна, (например, стероидные гормоны), то она может проникать через липидный слой наружной мембраны клеток-мишеней. Если молекула имеет большие размеры или является полярной, то ее проникновение внутрь клетки невозможно. Поэтому для липофильных гормонов рецепторы находятся внутри клеток-мишеней, а для гидрофильных - рецепторы находятся в наружной мембране. Для получения клеточного ответа на гормональный сигнал в случае гидрофильных молекул действует внутриклеточный механизм передачи сигнала. Это происходит с участием веществ, которых называют вторыми посредниками. Молекулы гормонов очень разнообразны по форме, а "вторые посредники" - нет. Надежность передачи сигнала обеспечивает очень высокое сродство гормона к своему белку-рецептору. Что такое посредники, которые участвуют во внутриклеточной передаче гуморальных сигналов? Это циклические нуклеотиды (цАМФ и цГМФ), инозитолтрифосфат, кальций-связывающий белок - кальмодулин, ионы кальция, ферменты, участвующие в синтезе циклических нуклеотидов, а также протеинкиназы - ферменты фосфорилирования белков. Все эти вещества участвуют в регуляции активности отдельных ферментных систем в клетках-мишенях. Регуляция количества и активности рецепторов Концентрация рецепторов внутри клетки или на её поверхности и их сродство к данному гормону в норме регулируются различными способами, а также могут меняться при заболеваниях или при использовании гормонов или их агонистов в качестве лекарственных средств. Например, при воздействии β-адренергических агонистов на клетки в течение нескольких минут в ответ на новое добавление агониста прекращается активация аденилатциклазы, и биологический ответ исчезает. Такое снижение чувствительности рецептора к гормону (десенситизация) может происходить в результате изменения количества рецепторов по механизму понижающей регуляции. Гормон связывается с рецептором, комплекс гормон-рецептор путём эндоцитоза проникает в клетку (интернализуется), где часть рецепторов подвергается протеолитическому расщеплению под действием ферментов лизосом, а часть инактивируется, отделяясь от других мембранных компонентов. Это приводит к уменьшению количества рецепторов на плазматической мембране. Например, в случае инсулина, глюкагона, катехоламинов это происходит в течение нескольких минут или часов. При снижении концентрации гормона рецепторы возвращаются на поверхность клетки, и чувствительность к гормону восстанавливается. Активность рецептора, т.е. его сродство к гормону, может изменяться также в результате ковалентной модификации, главным образом путём фосфорилирования. Концентрация внутриклеточных рецепторов может также регулироваться по механизму индукции и репрессии. G-белки (ГТФ-связывающие белки) - универсальные посредники при передаче сигналов от рецепторов к ферментам клеточной мембраны, катализирующим образование вторичных посредников гормонального сигнала. G-белки - олигомеры, состоящие из α, β и γ-субъединиц. Состав димеров βγ незначительно различаются в разных тканях, но в пределах одной клетки все G-белки, как правило, имеют одинаковый комплект βγ-субъединиц. Поэтому G-белки принято различать по их α-субъединицам. Выявлено 16 генов, кодирующих различные α-субъединицы G-белков. Некоторые из генов имеют более одного белка,, вследствие альтернативного сплайсинга РНК. Каждая α-субъединица в составе G-белка имеет специфические центры:
В структуре G-белков отсутствуют α-спиральные, пронизывающие мембрану домены. G-белки относят к группе "заякоренных" белков. 82. Циклические АМФ и ГМФ как вторичные посредники. Активация протеинкиназ и фосфорилирование белков, ответственных за проявление гормонального эффекта. Если сигнал воспринимается мембранными рецепторами, то схему передачи информации можно представить так:
Несмотря на огромное разнообразие сигнальных молекул, рецепторов и процессов, которые они регулируют, существует всего несколько механизмов трансмембранной передачи информации: с использованием аденилатциклазной системы, инозитолфосфатной системы, каталитических рецепторов, цитоплазматических или ядерных рецепторов. Гуанилатциклаза катализирует образование цГМФ из ГТФ, одного из важных посредников внутриклеточной передачи сигнала (рис. 5-32, 5-33). Гуанилатциклаза находится в клетке, как в мембранносвязанном состоянии, так и в цитозольном. Соотношения этих двух форм фермента в различных тканях разное. Например, в клетках тонкого 251 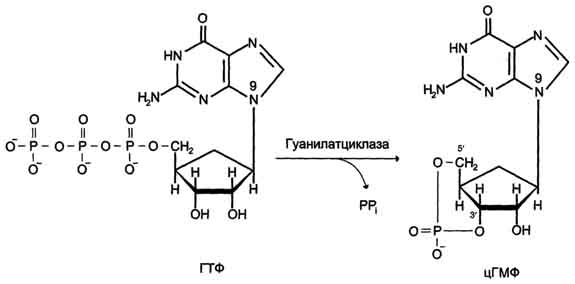 Рис. 5-32. Образование 3',5'-циклического ГМФ (цГМФ). 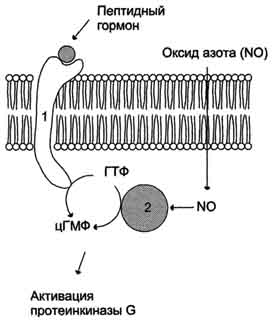 Рис. 5-33. Регуляция активности мембранной (1) и цитозольной (2) гуанилатциклазы. кишечника 90% гуанилатциклазы находится в мембранах, а в лёгких и печени - лишь 20%. Цитозольная и мембранносвязанная гуанилатциклазы различаются не только по локализации, но и по молекулярной массе, активности, способу регуляции. Цитозольная форма гуанилатциклазы состоит из двух субъединиц (α и β) и содержит в своём составе простетическую группу - гем. В области гема связывается активатор этой формы гуанилатциклазы - оксид азота (NO), образующийся из аргинина под действием фермента синтазы оксида азота (см. раздел 9). Мембраннсювязанная гуанилатциклаза - трансмембранный гликопротеин. Внутриклеточный домен гуанилатциклазы проявляет каталитическую активность, внеклеточный домен служит рецептором. Присоединение активатора к рецептору вызывает изменение конформации в мембранном и цитозольном доменах и, как следствие, активацию гуашиатциклазы. В тканях человека присутствуют 3 типа мембранносвязанных гуанилатциклаз, в активации которых принимают участие специфические регуляторы - предсердный натрийуретический фактор (ПНФ), натрийурети-ческий пептид из мозга и кишечный пептид гуанилин. В клетках тканей выявлены 3 основных типа внутриклеточных рецепторных белков, с которыми взаимодействует цГМФ: цГМФ-зависимая протеинкиназа (протеинкиназа G), цГМФ-регулируемые ионные каналы и цГМФ-регулируемая фосфодиэстераза, специфичная к цАМФ (катализирует превращение цАМФ в АМФ). цГМФ играет важную роль в регуляции Са2+-гомеостаза в различных типах клеток. Повышение концентрации цГМФ приводит к понижению концентрации Са2+ как в результате активации Са2+-АТФ-аз, так и за счёт подавления 252 рецепторзависимого поступления этого иона в цитоплазму клетки. Эти эффекты опосредованы действием протеинкиназы G на мембранные белки, участвующие в обмене Са2+. Аденилатциклаза Фермент аденилатциклаза, катализирующий превращение АТФ в цАМФ (рис. 5-36), - ключевой фермент аденилатциклазной системы передачи сигнала. Аденилатциклаза обнаружена во всех типах клеток. Фермент относят к группе интегральных белков клеточной мембраны, он имеет 12 трансмембранных доменов. Внеклеточные фрагменты аденилатциклазы гликозилированы. Цитоплазматические домены аденилатциклазы имеют два каталитических центра, ответственных за образование цАМФ - вторичного посредника, участвующего в регуляции активности фермента протеинкиназы А. На активность аденилатциклазы оказывают влияние как внеклеточные, так и внутриклеточные регуляторы. Внеклеточные регуляторы (гормоны, эйкозаноиды, биогенные амины) осуществляют регуляцию через специфические рецепторы, которые с помощью α-субъединиц G-белков передают сигналы на аденилатциклазу. αs-Субъединица (стимулирующая) при взаимодействии с аденилатциклазой активирует фермент, α-субъединица (ингибирующая) ингибирует фермент. В свою очередь, аденилатциклаза стимулирует проявление ГТФ-фосфатазной 254 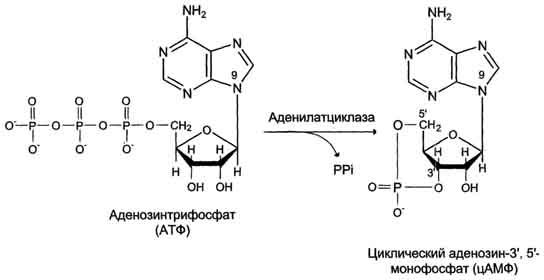 Рис. 5-36. Образование циклического аденозинмонофосфата (цАМФ). активности α-субъединиц. В результате дефосфорилирования ГТФ образуются субъединицы αs-ГДФ и αi-ГДФ, не комплементарные аденилатциклазе. Из 8 изученных изоформ аденилатциклазы 4 - Са2+-зависимые (активируются Са2+). Регуляция аденилатциклазы внутриклеточным кальцием позволяет клетке интегрировать активность двух основных вторичных посредников цАМФ и Са2+. Активация протеинкиназы А (ПКА)
Большую роль в регуляции внутриклеточной сигнальной системы играет белок AKAPs. "Заякоренный" белок AKAPs участвует в сборке ферментных комплексов, включающих не только 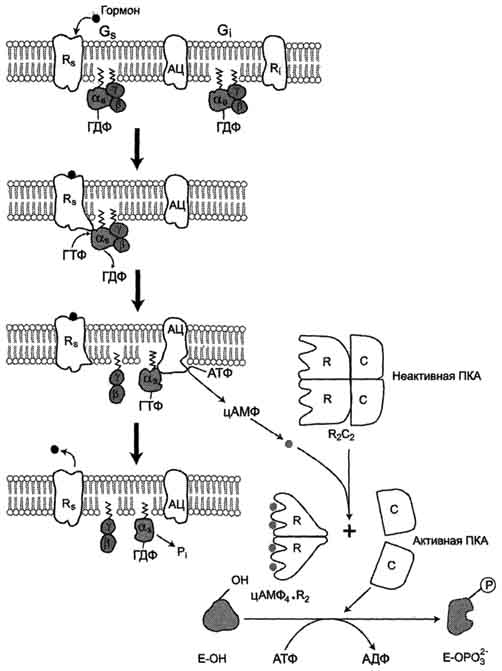 Рис. 5-41. Аденилатциклазная система. протеинкиназу А, но и фосфодиэстеразу и фосфопротеинфосфатазу. Каскадный механизм усиления и подавления сигнала.Передача сигнала от мембранного рецептора через G-белок на фермент аденилатциклазу служит примером каскадной системы усиления этого сигнала. Одна молекула, активирующая рецептор, может "включать" несколько G-белков, и затем каждый активирует несколько молекул аденилатциклазы с образованием тысяч молекул цАМФ. На этом этапе сигнал усиливается в 102-103 раз. Образующийся цАМФ "включают" другой фермент - протеинкиназу А, усиливая сигнал ещё в 1000 раз. Фосфорилирование ферментов протеинкиназой А ещё больше усиливает сигнал, в результате суммарное усиление равно 106-107 раз. Таким образом, по механизму каскадного усиления одна молекула регулятора способна изменить активность миллионов других молекул. Но для любой из систем трансмембранной передачи сигнала клетка имеет другую еистему, подавляющую этот сигнал. Каждый из этапов в ферментном каскаде находится под контролем специальных подавляющих этот сигнал механизмов. Например, длительное действие гормона приводит к десенсибилизации мембранных рецепторов: они либо инактивируются, либо вместе с гормоном погружаются в клетку посредством эндоцитоза. В результате десенсибилизации рецепторов степень активации аденилатциклазной системы снижается. Если в клетке длительное время повышена концентрация цАМФ (повышена активность протеинкиназы А), может происходить фосфорилирование кальциевых каналов, что приводит к повышению концентрации Са2+ в клетке. Кальций активирует Са2+-зависимую фосфодиэстеразу, катализирующую превращение цАМФ в АМФ. В результате инактивации протеинкиназы А (R2C2) снижается скорость фосфорилирования специфических ферментов. Завершает "выключение" системы фосфопротеинфосфатаза, дефосфорилирующая фосфопротеины. 83. Фосфатидилнозитольный цикл как механизм внутриклеточных коммуникаций. Инозитол 1,4,5-трифосфат и диацилглицерол – вторичные посредники передачи сигнала. Иона кальция как вторичные посредники, кальмадулин. Функционирование инозитолфосфатной системы трансмембранной передачи сигнала (рис. 5-42) обеспечивают: R (рецептор), фосфолипаза С, Gplc - белок, активирующий фосфолипазу С, белки и ферменты мембран и цитозоля. Последовательность событий, приводящих к активации фосфолипазы С:
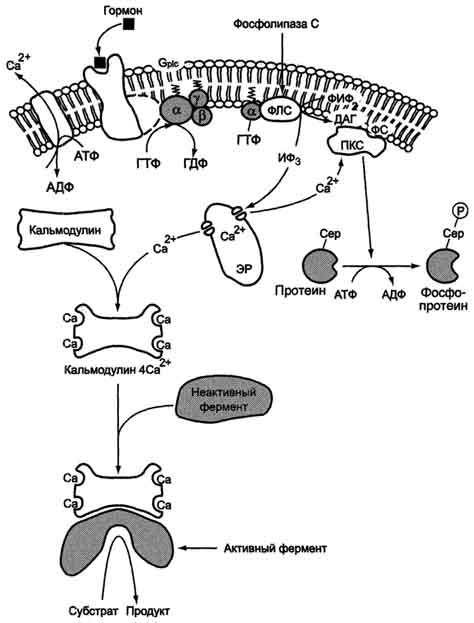 Рис. 5-42. Инозитолфосфатная система.
Активация протеинкиназы С
Участие белка кальмодулина в инозитолфосфатной передаче сигнала В клетках многих тканей присутствует белок кальмодулин, который функционирует как внутриклеточный рецептор Са2+, он имеет 4 центра для связывания Са2+. Комплекс [кальмодулин] -[4 Са2+] не обладает ферментативной активностью, но взаимодействие комплекса с различными белками и ферментами приводит к их активации. Как и большинство систем трансмембранной передачи сигналов, инозитолфосфатная система имеет не только механизм усиления, но и механизм подавления сигнала. Присутствующие в цитозоле инозитол-1,4,5-трифосфат (ИФ3) и диацилглицерол (ДАТ) в мембране могут в результате серии реакций опять превращаться в фосфатидилинозитол-4,5-бисфосфат (ФИФ2). Ферменты, катализирующие восстановление фосфолипида, активируются фосфорилированием протеинкиназой С. Концентрация Са2+ в клетке снижается до исходного уровня при действии Са2+-АТФ-аз цито-плазматической мембраны и ЭР, а также Na+/Ca2+-и Н+/Са2+-транслоказ (активный антипорт) клеточной и митохондриальной мембран.
диацилглицерола в мембране приводит к изменению конформации протеинкиназы С, снижению её сродства к фосфатидилсерину, фермент диссоциирует в цитозоль (неактивная форма). Фосфорилированные протеинкиназой С ферменты и белки под действием фосфопротеинфосфатазы переходят в дефосфорилированную форму. 84. Передача сигналов через внутриклеточные рецепторы. Образование комплекса гормон-рецептор и его взаимодействие с ДНК, гормон чувствительные элементы (HRE). Передача сигналов через рецепторы сопряженные с ионными каналами. Строение рецептора ацетилхолина. Передача сигналов через внутриклеточные рецепторы Стероидные и тиреоидные гормоны связываются с рецепторами внутри клетки и регулируют скорость транскрипции специфических генов (рис. 11-5). В отсутствие гормона внутриклеточные рецепторы связаны обычно с другими белками в цитозоле или ядре. Например, рецепторы глюкокортикоидов образуют в цитозоле комплекс с шапероном, что препятствует связыванию рецептора с молекулой ДНК (рис. 11-6). Взаимодействие гормона с центром связывания на С-концевом участке полипептидной цепи рецептора вызывает конформационные изменения и освобождение рецептора от шаперона. Происходит объединение 2 молекул рецептора с образованием гомодимера. Димер рецептора узнаёт специфическую последовательность нуклеотидов, которая расположена в промоторной области гена. Взаимодействие со специфическим участком ДНК HRE (от англ, hormone response element, элемент, реагирующий на воздействие гормона) обеспечивает центральный домен рецептора. Этот домен содержит аминокислотную последовательность, образующую 2 "цинковых пальца". В каждом "цинковом пальце" атом цинка связан с 4 остатками цистеина (рис. 11-7). В структуре одного "цинкового пальца" имеется последовательность аминокислот, отвечающая за связывание с ДНК, а второй "цинковый 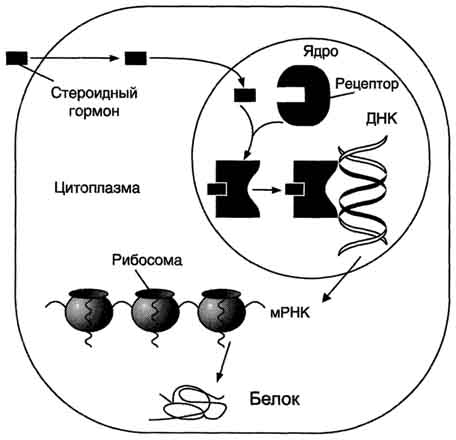 |
