|
|
Шпаргалка по оптике. 1. Геометрическая оптика
Эффект Комптона. Рассеяние рентгеновского излучения веществом.
В 1923 г. американский физик А. Комптон (1892—1962) обнаружил, что при рассеянии монохроматических рентгеновских лучей «легкими» веществами* наряду с исходной длиной волны Я в рассеянных лучах содержатся также лучи с большей длиной волны Я' (эффект Комптона). Схема опыта Комптона показана на рис. 9.9. Узкий пучок лучей, выделяемый диафрагмами di и D2, падал на мишень из рассеивающего вещества. С помощью рентгеновского спектрографа измерялись длина волны К' рассеянных под углом 0 лучей и их интенсивность. Было установлено, что разность ДЯ = Я' — Я не зависит ни от природы рассеивающего вещества, ни от длины Я падающих лучей, а зависит только от угла рассеяния б, образуемого/направлениями падающих и рассеянных лучей. Эта экспериментально найденная зависимость имеет следующий вид:
—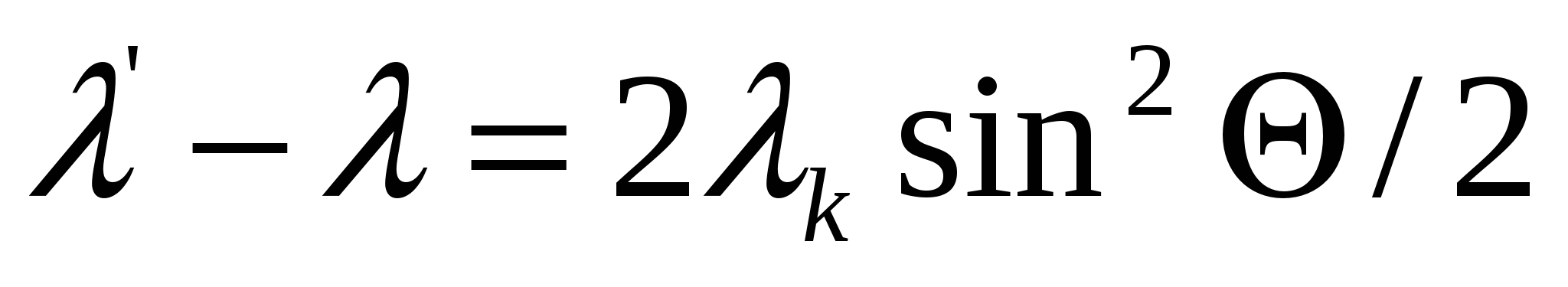 эффект Комптона, эффект Комптона,
λк—комптоновская длина волны.
Было также замечено, что интенсивность рассеянных лучей больше для веществ с малой атомной массой и меньше для веществ с большой атомной массой. Интенсивность рассеянного пучка растет с увеличением угла рассеяния Θ.
Э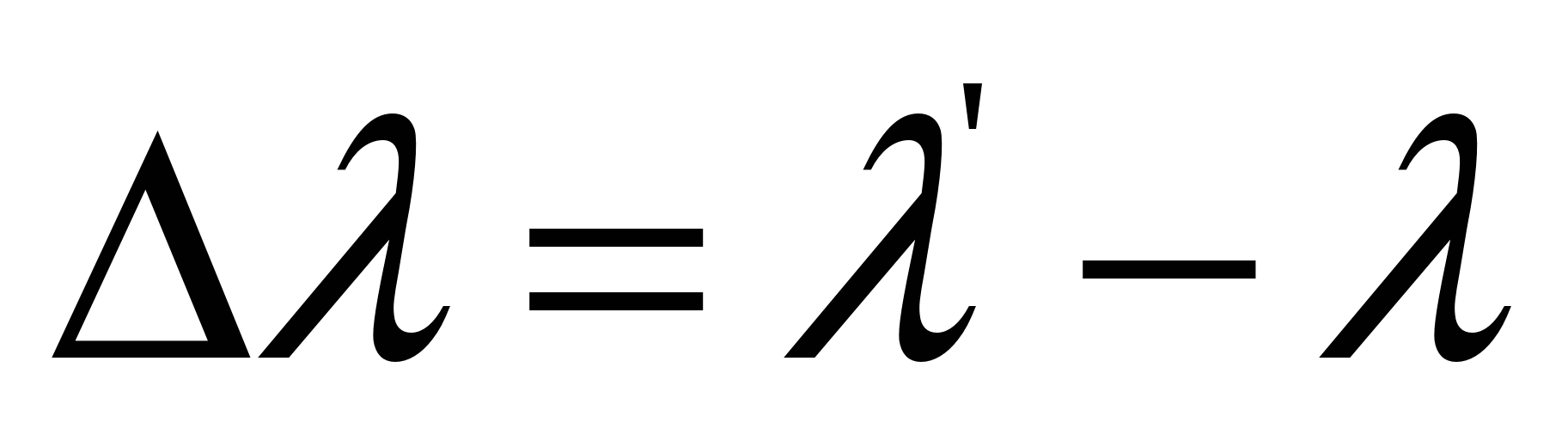 лементарная теория эффекта Комптона. лементарная теория эффекта Комптона.
О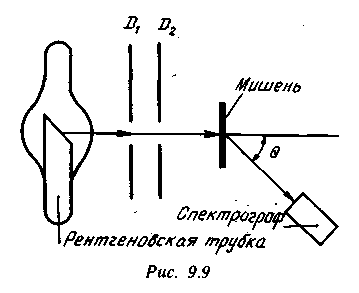 бнаруженная на опыте независимость величины от рода вещества указывает на то, что рассеяние рентгеновских лучей происходит на внешних электронах атомов, которые слабо связаны с атомами рассеивающего вещества. Оценки показывают, что энергия рентгеновских квантов значительно больше энергии связи внешних электронов в атомах. Поэтому с достаточной степенью точности можно считать, что рассеяние рентгеновских квантов происходит на «свободных» электронах в отличие от фотонов, которые при фотоэффекте рассеиваются на «связанных» электронах (для фотона hv бнаруженная на опыте независимость величины от рода вещества указывает на то, что рассеяние рентгеновских лучей происходит на внешних электронах атомов, которые слабо связаны с атомами рассеивающего вещества. Оценки показывают, что энергия рентгеновских квантов значительно больше энергии связи внешних электронов в атомах. Поэтому с достаточной степенью точности можно считать, что рассеяние рентгеновских квантов происходит на «свободных» электронах в отличие от фотонов, которые при фотоэффекте рассеиваются на «связанных» электронах (для фотона hv
A, A— работа выхода).
Для вывода формулы (9.31) предположим, что налетающий рентгеновский фотон упруго взаимодействует с покоящимся «свободным» электроном мишени (рис. 9.10, а). Поскольку энергия налетающего фотона сравнима с энергией покоя электрона hv
m0c2), при использовании законов сохранения нужно энергию и импульс электрона определять по формулам релятивистской механики
после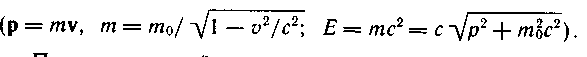 ввзаимодействия электрон начинает двигаться с некоторой скоростью (его называют электроном отдачи) под углом ф к направлению налетающего фотона (рис. 9.10, б), а рассеянный на угол 0 фотон будет иметь импульс РФ = М'. ввзаимодействия электрон начинает двигаться с некоторой скоростью (его называют электроном отдачи) под углом ф к направлению налетающего фотона (рис. 9.10, б), а рассеянный на угол 0 фотон будет иметь импульс РФ = М'.
В соответствии с законами сохранения импульса и энергии в системе фотон — электрон запишем систему двух уравнений (закон сохранения импульса графически иллюстрируется на рис. 9.10, в): — закон сохранения импульса;
(9.32) 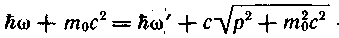 — закон — закон
сохранения энергии.
Если из первого и второго уравнений системы выразить квадрат импульса электрона отдачи, то получатся следующие два уравнения:
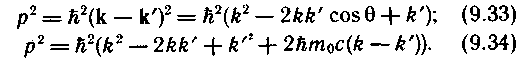
Приравнивая эти выражения, получаем
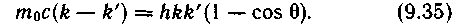
Поскольку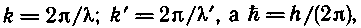 из формулы (9.35) после простых преобразований получим из формулы (9.35) после простых преобразований получим
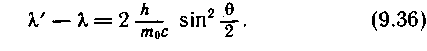
Из сопоставления с зависимостью (9.31) получаем выражение для комптоновской длины волны при рассеянии на электронах:
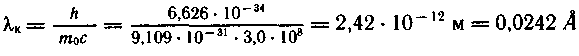
Из приведенных расчетов следует, что в эффекте Комптона отчетливо проявляются корпускулярные свойства света.
Давление света. Опыты Лебедева
К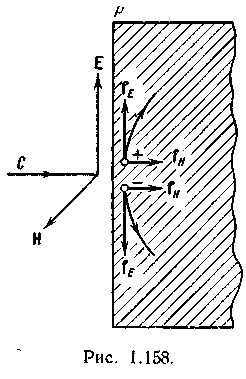 ачественно механизм давления света можно пояснить следующим образом. Пусть на плоскую поверхность Р тела, сечение которого показано на рис. 1.158, падает перпендикулярно к ней ачественно механизм давления света можно пояснить следующим образом. Пусть на плоскую поверхность Р тела, сечение которого показано на рис. 1.158, падает перпендикулярно к ней
электромагнитная волна. Векторы Е и Н лежат в плоскости Р. Рассмотрим, как они будут воздействовать на электрические заряды, составляющие тело. Под действием силы fE =qEположительный заряд начнет смещаться вдоль поверхности по направлению Е, а отрицательный — против. Такое смещение зарядов представляет собой поверхностный ток j, параллельный Е. В телах со свободными зарядами (проводники) это будет то'к про-
в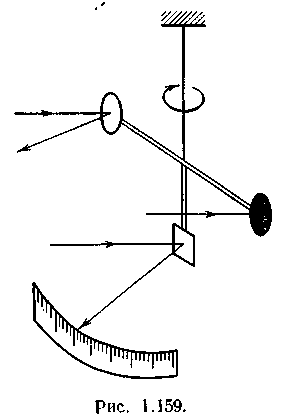 одимости, а в диэлектриках—поляризационный ток смещения. Магнитные силы fH, действующие на ток j, будут по закону Ампера (т. II, §31) направлены перпендикулярно к j и Н, т. е. внутрь тела. Независимо от их знака, заряды, расположенные на поверхности тела и связанные с его атомами, «вдавливаются» в тело. Ускорение и скорость v этих зарядов пропорциональны величине Е. Магнитные же силы пропорциональны [vXH], т. е., в конечном счете, произведению [ЕхН], а оно в свою очередь пропорционально плотности электромагнитной энергии падающей волны w. Точный расчет величины давления света р по теории Максвелла природит к выражению p=(1+ρ)ω (39.1) одимости, а в диэлектриках—поляризационный ток смещения. Магнитные силы fH, действующие на ток j, будут по закону Ампера (т. II, §31) направлены перпендикулярно к j и Н, т. е. внутрь тела. Независимо от их знака, заряды, расположенные на поверхности тела и связанные с его атомами, «вдавливаются» в тело. Ускорение и скорость v этих зарядов пропорциональны величине Е. Магнитные же силы пропорциональны [vXH], т. е., в конечном счете, произведению [ЕхН], а оно в свою очередь пропорционально плотности электромагнитной энергии падающей волны w. Точный расчет величины давления света р по теории Максвелла природит к выражению p=(1+ρ)ω (39.1)
где р — коэффициент отражения от данной поверхности.
Для развития электромагнитной теории света было чрезвычайно важно получить прямое экспериментальное доказательство этого эффекта. Однако обнаружение его осложнялось целым рядом побочных явлений. Частичное поглощение падающего света приводит к нагреванию поверхности. Тепло в свою очередь 'передается молекулам окружающего газа, в силу чего их движение, а следовательно, и оказываемое ими давление возрастают, причем этот «радиометрический эффект» легко перекрывает искомое световое давление.
Впервые преодолеть все экспериментальные трудности сумел П. Н. Лебедев. Идея опыта заключалась в том, что свет направлялся на одно из крылышек легкой вертушки (рис. 1.159), причем ее поворот измерялся по отклонению зайчика, отбрасываемого маленьким, укрепленным на вертушке зеркальцем.
Использование очень тоненьких крылышек привело к тому, что
температура на обеих их поверхностях была практически тождественная, что при малом давлении свело радиометрический эффект почти к нулю. Для зеркального крылышка р«1, а для зачерненного р
0. Позже он доказал давление света и на газы.
9. Фотохимическое действие света.Фотохимическое действие света. Законы фотохимии. Сенсибилизаторы Физические основы фотографии. Цветная фотография. Голография. Физические принципы и техническая реализация голографии.
Фотохимические явления.
Поглощение фотонов молекулами вещества может привести и некоторых случаях и к химическим превращениям. Эйнштейн и 1905 г. указал, что при таких фотохимических превращениях пещества каждый поглощенный квант света вызывает превращение одной молекулы. Опыт подтвердил этот закон. Легко понять, что свет может вызвать такие превращения вещества, которые в обычных условиях требовали бы весьма высокой температуры. Действительно, комнатной температуре 290° К отвечает энергия поступательного движения молекул
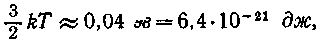
в то время как энергия фотона зеленого излучения
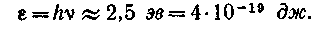
Таким образом, поглощение фотонов видимого излучения эквивалентно нагреванию до многих тысяч градусов. Понятно также, что чем меньше длина волны излучения, тем оно должно быть химически более активным.
Если для расщепления молекулы нужна энергия А, то для того, чтобы расщепление можно было произвести воздействием излучения, необходимо, чтобы энергия одного фотона была не меньше А.
Следовательно, наименьшая частота химически активного
излучения v0 равна
Излучение меньших частот будет химически неактивно. Примером реакции такого типа является разложение бромистого водорода светом
Свободные атомы водорода и брома затем соединяются:
Часто фотохимическое разложение молекул сопровождается вторичными реакциями. Примером реакций такого типа является реакция смеси водорода и хлора. Известно, что в темноте эти газы остаются механически смешанными, не вступают в химическое соединение. Мгновенная вспышка света приводит к бурнойреакции — взрыву. Суть дела в том, что каждый поглощенный фотон приводит к реакции не одной молекулы, но длиннейшей последовательной цепочки превращений многих тысяч и даже миллионов молекул, служит началом «цепной реакции», как показано в работах Н. Н. Семенова.
Фоторасщепление начинает превращения:
Далее каждый свободный атом хлора вызывает цепочку превращений:
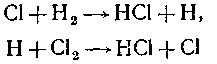
и опять:
Важнейшей для всего живущего на Земле является фотохимическая реакция образования органических веществ из неорганических. Эта реакция идет с помощью катализатора—хлорофилла в листьях растений при поглощении света. До сих пор эта сложная реакция не изучена в деталях и не может быть повторена в лабораторных условиях (т. е. без живых растений).
В заключение этого параграфа отметим, что зрение объясняется также особыми фотохимическими реакциями, происходящими в сетчатке глаза.
Фотография
Важным применением фотохимических превращений является фотография.
Процесс фотографирования широко известен. На фотографическую пластинку проектируется при помощи специальной оптики изображение предмета. После этого пластинку проявляют, закрепляют и получают негатив — изображение предметов с обратным по отношению к естественному распределением света и тени (на негативе светлые места предмета изображаются темными и наоборот). Повторение этого процесса (с другой оптикой, что несущественно) с переносом изображения на фотобумагу дает изображение с правильным распределением света и тени.
Сущность процессов, происходящих в пластинке.
В фоточувствительном слое пластинки содержатся соли серебра. Под действием света происходит фоторасщепление этих молекул, причем выделяются свободные атомы серебра. При правильной экспозиции (выдержке на свету) число выделившихся атомов серебра в данном элементе пластинки будет пропорционально ее освещенности.
Количество выделившегося при этом свободного серебра столь незначительно,что заметить его в обычных условиях совершенно невозможно: на квадратный сантиметр фотопластинки приходится всего несколько стомиллиардных долей грамма свободного серебра. Полученное на пластинке изображение называется «скрытым» или «латентным».
Проявление изображения состоит в том, что фотопластинка подвергается действию реактивов (они могут быть разные, и на их перечислении мы не останавливаемся), под влиянием которых происходит дальнейшее выделение свободного серебра из кристалликов его соли. Речь идет именно о дальнейшем выделении, так как оно происходит только там, где имеются уже атомы свободного серебра. Таким образом, выделившиеся в результате фоторасщепления атомы серебра начинают цепочку превращений, в результате которых выделяются уже заметные количества серебра — десятки миллионов атомов на исходный свободный атом Ag. В результате пластинка чернеет тем быстрее, чем больше в данном месте было свободных атомов Ag, т. е. чем интенсивнее был поток вызвавшего фоторасщепление света. После того как нужное почернение достигнуто, необходимо предохранить пластинку от последующих возможных изменений. Для этого ее промывают в растворе гипосульфита, в котором растворяются все не успевшие разложиться соли серебра. Этим дальнейшие изменения в пластинке исключаются, изображение оказывается «закрепленным».
Голография
Голография (т. е. «полная запись», от греческого: голос — весь, графо — пишу) есть особый способ фиксирования на фотопластинке структуры световой волны, отраженной предметом. При освещении этой пластинки (голограммы) пучком света зафиксированная на ней волна восстанавливается в почти первоначальном виде, так что при восприятии восстановленной волны глазом зрительное ощущение бывает практически таким, каким оно было бы при наблюдении самого предмета.
Голография была изобретена в 1947 г. английским физиком Д. Табором. Однако полное осуществление идеи Габора стало возможным только после появления в 1960 г. источников света высокой степени когерентности — лазеров. Исходная схема Габора была усовершенствована американскими физиками Э. Лейтом и Ю. Упатниексом, которые получили в 1963 г. первые лазерные голограммы. Советский ученый Ю. Н. Денисюк предложил в 1962 г. оригинальный метод фиксирования голограмм на толстослойной эмульсии. Этот метод, в отличие от голограмм на тонкослойной эмульсии, дает цветное изображение предмета.
10. Элементы атомной физики. Строение атома. Опыты Резерфорда. Постулаты Бора. Теория водородного атома. Спектральные серии и уровни энергии. Недостатки теории Бора. Гипотеза де Бройля Волновая функция. Уравнение Шредингера. Квантование энергии на примере частицы в бесконечно глубокой потенциальной яме. Спонтанное и вынужденное излучение. Лазеры. Свойства лазерного излучения и его применение в технологических процессах. Элементы нелинейной оптики.
Теория водородного атома. Спектральные серии и уровни энергии.
Закономерности в атомных спектрах.
Бальмер проводил исследование спектров излучения атомов водорода. Экспериментально было установлено, что атомы водорода (как и атомы других элементов) излучают электромагнитные волны строго определённых частот, другими словами, спектр атома водорода состоит из спектральных линий, длины волн которых строго определены. При этом оказалось, что величину, обратную длине волны спектральной линии, можно рассчитать, как разность, некоторых двух величин, которые называются спектральными термами:
1/λ = Тn1 – Tn2 (1)
Для атома водорода терм можно записать следующим образом:
Tn= Rн/ n2 (2)
где n = 1,2,3... принимает ряд положительных значений,
Rh - постоянная Ридберга, численно равная:
Rh = (1,097373177 ± 0,000000083) 107м -1.
Тогда длину волны любой спектральной линии водорода можно рассчитать по обобщенной Формуле Бальмера: 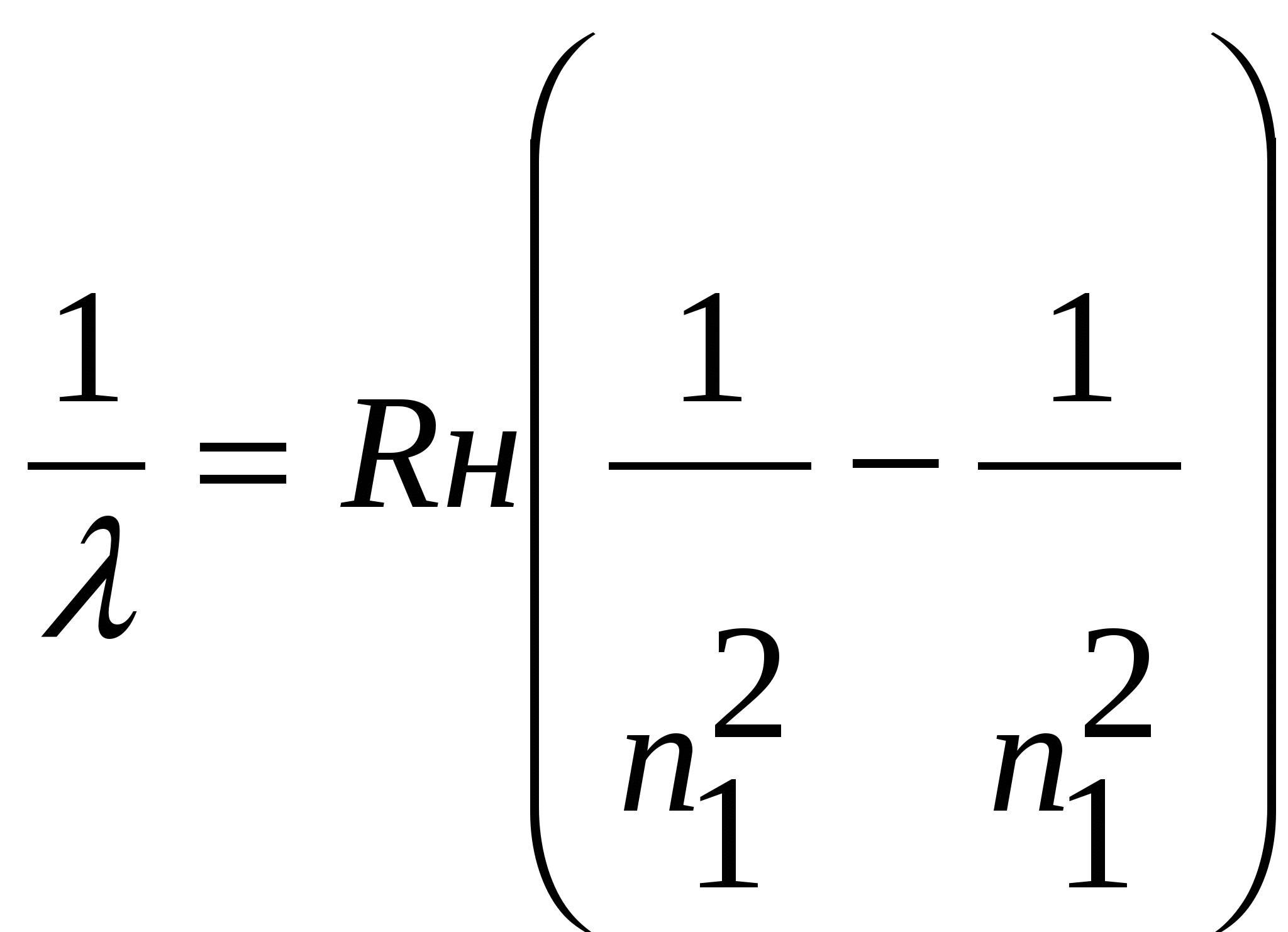 (3) (3)
(n1 = 1,2,3...) (n2=n1, n1+1, n1+2 …)
Длины волн, рассчитанные по формуле (3), совпали с экспериментально измеренными величинами.
Постулаты Бора.
Наличие резких спектральных линий, испускаемых атомами химических элементов, указывает на то, что процессы внутри атомов должны быть дискретны. Законы же классической физика приспособлены для описания непрерывных процессов. Нильс-Бор в 1913 году ясно понял это противоречие и сформулировал два постулата:
1) Атом (и всякая атомная система) может находиться не во всех состояниях, допускаемых классической механикой, а только в некоторых избранных (квантовых) состояниях, характеризующихся определёнными дискретными значениями E1,E2,E3... . В этих состояниях, вопреки классической электродинамике, атом не излучает. Поэтому они называются стационарными состояниями.
2) При переходе из стационарного состояния с большей энергией En2 в стационарное состояние с меньшей энергией En1 энергия атома изменяется на En2 – En1. При этом испускается один фотон с энергией
hν = ħω = En2 – En1 (4)
Такое же соотношение справедливо и для случая поглощения. Соотношение (4) называется правилом частот Бора и объясняет комбинационный принцип Ритца. Сравнивая (1) и (4), находим:
Tn = - E n / С h (5)
Т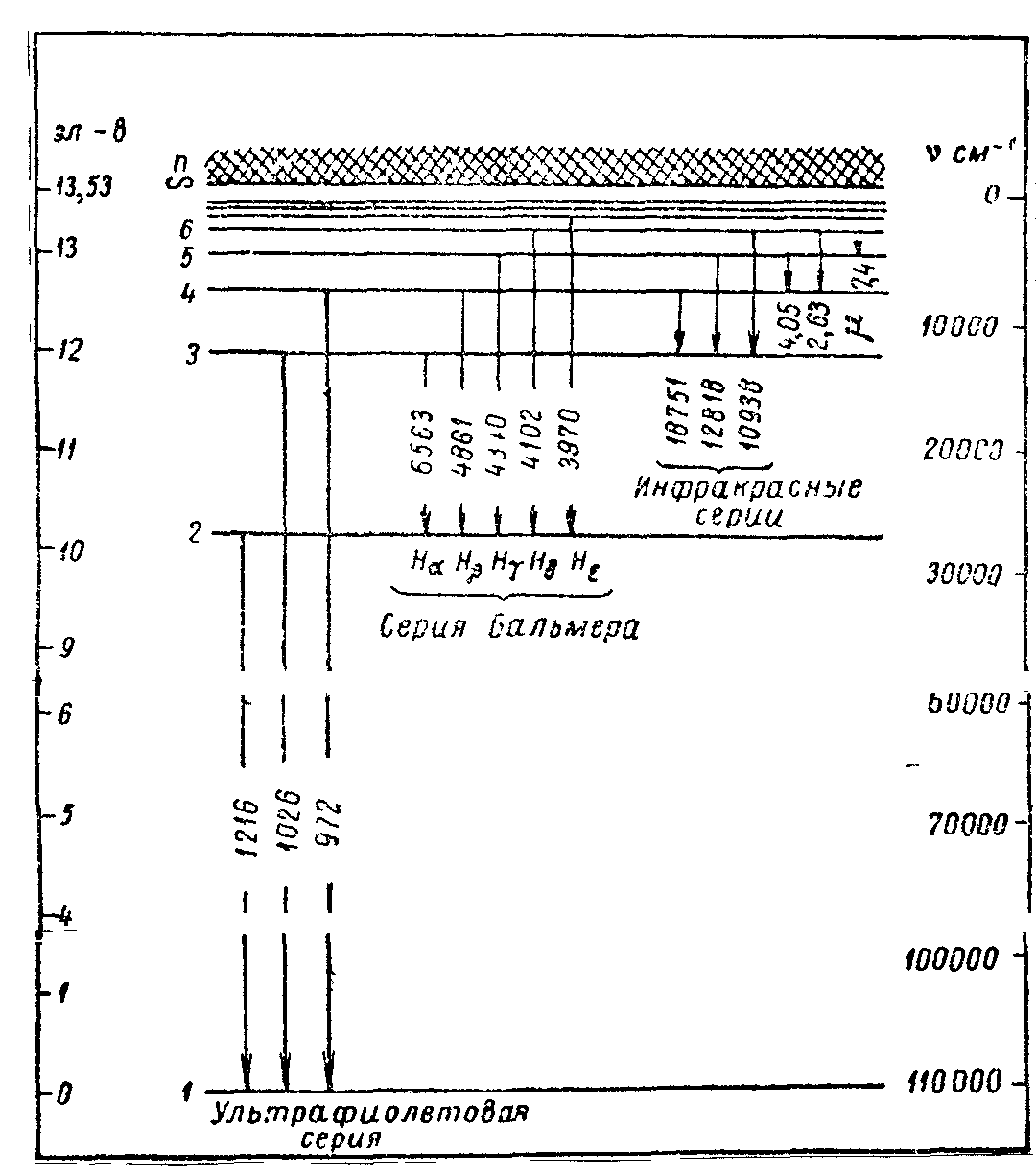
ем самым раскрывается физический смысл термов. Они определяются энергетическими уровнями атомов. Совокупность значений энергии стационарных состояний атома E1, E2, Е3... образует энергетический спектр атома.
В спектроскопии спектральные термы и уровни энергий принято изображать горизонтальными линиями, а переходы между ними стрелками. Стрелкам, направленным от высших уровней к низшим, соответствуют линии изучения, стрелкам, проведенным в обратных направлениях, линии поглощения. На рис.1 изображён спектр водорода.
Уровни энергии здесь нумеруются квантовым числом. За нуль принята энергия уровня с n = ∞ . Все энергетические уровни, расположенные ниже, дискретны. Им соответствуют отрицательные значения полной энергии атома. Выше линий n = ∞ энергия не квантуется, т.е. энергетический спектр непрерывен. Но при Е<0 движение электрона ограничено, а при Е > 0 не ограничено, т.е. при непрерывном энергетическом спектре атома электрон может, как угодно далеко удаляться от ядра и атом ионизируется.
Таким образом, ядро и электрон образуют связанную систему атом-электрон только в случае дискретного энергетического спектра.
Если понимать под атомом только связанные состояния, то можно сказать,что уровни энергии атома всегда дискретны, как это и постулировал Бор. В квантовой механике строго доказывается, что дискретный энергетический спектр является следствием ограничения области пространства, в которой электрон совершает движение. В случае атома это ограничение области движения электрона вызвано силой притяжения его к ядру. рис.1.Энергетический спектр атома водорода
Двух постулатов Бора, конечно, недостаточно для построения полной теории. Они должны быть дополнены, прежде всего правилами квантования, с помощью которых могут быть вычислены уровни атома. |
|
|
 Скачать 1.22 Mb.
Скачать 1.22 Mb.
 бнаруженная на опыте независимость величины от рода вещества указывает на то, что рассеяние рентгеновских лучей происходит на внешних электронах атомов, которые слабо связаны с атомами рассеивающего вещества. Оценки показывают, что энергия рентгеновских квантов значительно больше энергии связи внешних электронов в атомах. Поэтому с достаточной степенью точности можно считать, что рассеяние рентгеновских квантов происходит на «свободных» электронах в отличие от фотонов, которые при фотоэффекте рассеиваются на «связанных» электронах (для фотона hv
бнаруженная на опыте независимость величины от рода вещества указывает на то, что рассеяние рентгеновских лучей происходит на внешних электронах атомов, которые слабо связаны с атомами рассеивающего вещества. Оценки показывают, что энергия рентгеновских квантов значительно больше энергии связи внешних электронов в атомах. Поэтому с достаточной степенью точности можно считать, что рассеяние рентгеновских квантов происходит на «свободных» электронах в отличие от фотонов, которые при фотоэффекте рассеиваются на «связанных» электронах (для фотона hv  ачественно механизм давления света можно пояснить следующим образом. Пусть на плоскую поверхность Р тела, сечение которого показано на рис. 1.158, падает перпендикулярно к ней
ачественно механизм давления света можно пояснить следующим образом. Пусть на плоскую поверхность Р тела, сечение которого показано на рис. 1.158, падает перпендикулярно к ней одимости, а в диэлектриках—поляризационный ток смещения. Магнитные силы fH, действующие на ток j, будут по закону Ампера (т. II, §31) направлены перпендикулярно к j и Н, т. е. внутрь тела. Независимо от их знака, заряды, расположенные на поверхности тела и связанные с его атомами, «вдавливаются» в тело. Ускорение и скорость v этих зарядов пропорциональны величине Е. Магнитные же силы пропорциональны [vXH], т. е., в конечном счете, произведению [ЕхН], а оно в свою очередь пропорционально плотности электромагнитной энергии падающей волны w. Точный расчет величины давления света р по теории Максвелла природит к выражению p=(1+ρ)ω (39.1)
одимости, а в диэлектриках—поляризационный ток смещения. Магнитные силы fH, действующие на ток j, будут по закону Ампера (т. II, §31) направлены перпендикулярно к j и Н, т. е. внутрь тела. Независимо от их знака, заряды, расположенные на поверхности тела и связанные с его атомами, «вдавливаются» в тело. Ускорение и скорость v этих зарядов пропорциональны величине Е. Магнитные же силы пропорциональны [vXH], т. е., в конечном счете, произведению [ЕхН], а оно в свою очередь пропорционально плотности электромагнитной энергии падающей волны w. Точный расчет величины давления света р по теории Максвелла природит к выражению p=(1+ρ)ω (39.1)