история. 1. понятие биотрансформации. Виды биокатализаторов
 Скачать 4.48 Mb. Скачать 4.48 Mb.
|
8.СПОСОБЫ ВНЕСЕНИЯ СУБСТРАТА В РЕАКЦИОННУЮ СМЕСЬНа эффективность биокаталитического процесса существенное влияние оказывает способ обеспечения контакта субстрата и биокатализатора. Способ внесения субстрата в реакционную смесь выбирается в зависимости от его свойств: Физического состояния (жидкость, твердость или газообразное) Способности растворяться в воде или органических растворителях Степени токсичности для биокатализатора Нетоксичные субстраты можно вносить в реакционную смесь в их естественном физическом состоянии. Так, газообразные субстраты обычно барботируют через жидкую реакционную смесь. Биокатализатор взаимодействует с молекулами субстрата, растворившимися в жидкости. 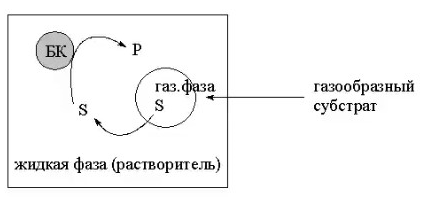 Хорошо растворимые твердые или жидкие субстраты образуют гомогенные растворы в используемом растворителе. При этом все молекулы внесенного субстрата становятся доступными для биокатализатора. 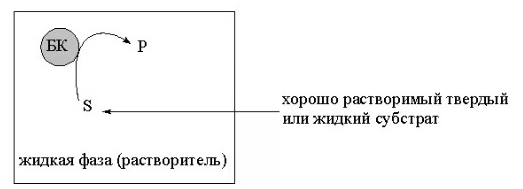 Плохо растворимые твердые субстраты образуют суспензии, а жидкие субстраты присутствуют в виде второй жидкой фазы. В этом случае обеспечивается плохой контакт субстрата с биокатализатором, поскольку доступной является только часть субстрата, перешедшая в растворитель, в котором находится биокатализатор. 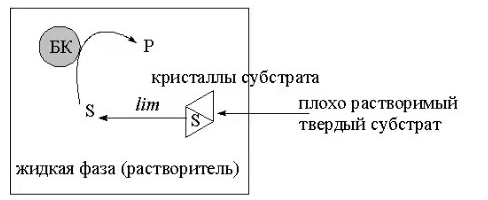 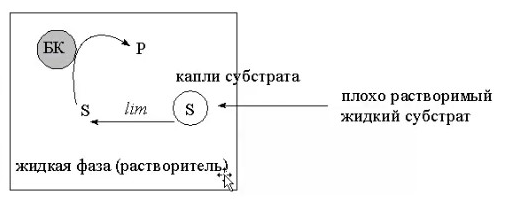 Насыщение жидкой фазы субстратом лимитируется ограниченной поверхностью контакта этих веществ. Для ее увеличения твердые субстраты можно измельчать ультразвуком, или жидкие субстраты интенсивность перемешивать с основной жидкой фазой. Например, внесение субстрата в микрокристаллическом виде оказалось оптимальным способом в процессе трансформации гидрокартизона в преднизалон в воде с помощью микобактерий. Микрокристаллы субстрата прилипали к гидрофобной поверхности бактерий и постепенно поглощались клеткой, минуя растворитель.  Но в большинстве случаев для интенсификации трансформации в нерастворимых субстратах требуется увеличение их растворимости в используемом растворителе. Для этого могут быть использованы следующие подходы: Субстрат можно химически модифицировать, то есть придать растворимую форму Субстрат можно включать внутрь другой более крупной молекулы, обладающей более высокой растворимостью в используемом растворителе. Зачастую субстрат включают внутрь молекулы циклодекстрина, представляющей собой циклический олигомер глюкозы.  (где + - это субстрат) (где + - это субстрат)Циклодекстрины получают трансформацией крахмала микробными ферментами циклодекстрин:гликозидтрансферазами. Внутренняя поверхность молекулы циклодекстрина гидрофобная, а наружная – гидрофильная, что позволяет получать водорастворимые комплексы с гидрофобными веществами. Можно увеличить растворяющие свойства самого растворителя путем введения в него различных добавок. Чаще всего добавляют от 5 до 10% дополнительного растворителя, который с одной стороны хорошо смешивается с основным растворителем, а с другой стороны хорошо растворяет субстрат. Так, многие субстраты вносят в реакционную смесь в идее концентратов в этаноле, метаноле, ацетоне, 1,2-пропандиоле. Кроме того, растворимость субстрата в воде можно увеличить с помощью поверхностно активных веществ. Их вносят в реакционную смесь от 0,5 до 4%. При работе с токсичными субстратами, напротив, необходимо обеспечить низкий уровень субстрата вблизи биокатализатора. Этого можно достичь, если субстрат в натуральном виде вносить небольшими порциями так, чтобы концентрация в реакционной смеси не превысило допустимого значения. 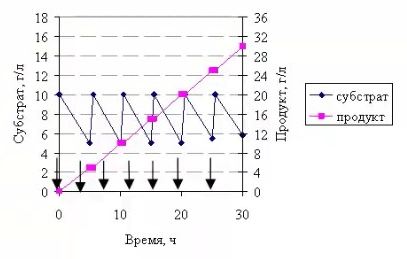 (стрелки – это моменты времени, при которых вносится субстрат) Однако, при этом необходимо постоянно контролировать состав реакционной смеси. Это не всегда удобно. Более удобно использовать физически-модифицированный субстрат. Физическую модификацию можно осуществлять: С помощью жидкости, несмешивающейся в основным растворителем. Можно использовать как простые двухфазные системы, так и эмульсии. 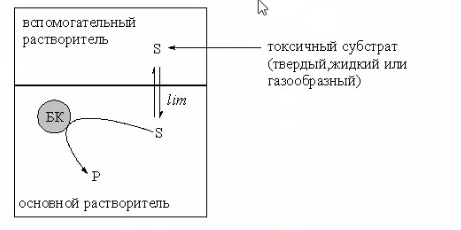 В этом случае, субстрат будет переходить в жидкую фазу с биокатализатором непрерывно по мере его утилизации. В результате вокруг биокатализатора будет постоянно поддерживаться нужная концентрация токсичного субстрата. Для модификации токсичных субстратов можно использовать вспомогательные твердые фазы – сорбенты. В качестве сорбентов используют активированный уголь, различные ионообменные смолы, гидрофобные резины и другие материалы. Субстраты предварительно сорбируют на твердых носителях, а затем вводят в реакционную смесь. 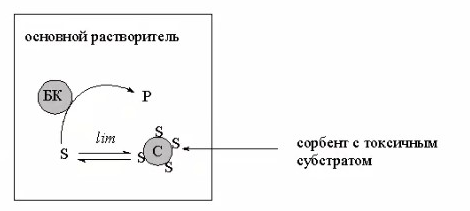 В ходе трансформации субстрат медленно десорбируется, что обеспечивает его постоянно низкую концентрацию в растворителе. Модификацию субстрата можно осуществлять с помощью веществ, образующих с ним нетоксичные комплексы. Обычно в качестве комплексообразователей используется циклодекстрин. 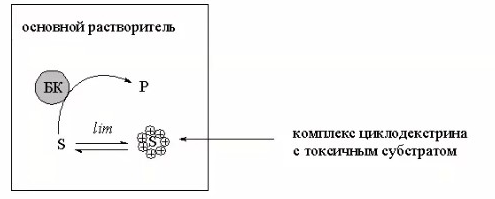 9.СПОСОБЫ УДАЛЕНИЯ ТОКСИЧНЫХ ПРОДУКТОВ ИЗ РЕАКЦИОННОЙ СМЕСИ IN SITUЭффективность биокаталитического процесса можно ограничиваться накоплением в реакционной смеси продуктов трансформации. Токсичные продукты могут подавлять реакцию уже при низких концентрациях (примерно от 100 до 1000 мг/л). Для увеличения выхода токсичных продуктов необходимо предусмотреть возможность выведения их из реакционной смеси in situ, то есть одновременно с процессом трансформации субстрата. Этого можно достичь несколькими способами. Некоторые из них используются также при работе с токсичными субстратами. Во-первых, токсинные продукты можно адсорбировать на подходящих твердых сорбентах, которые вводят в реакционную смесь. Для удаления органических растворителей из водной фазы часто используют активированный уголь, ионнообменные смолы, гидрофобнрые резины. Для удаления воды из органических растворителей обычно применяют циалиты. 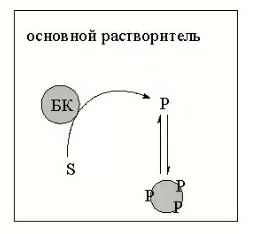 Во-вторых, продукты можно экстрагировать с помощью второй жидкой фазы. 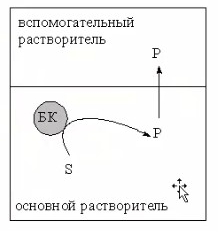 В-третьих, органические продукты можно связывать в нетоксичные комплексы, например с циклодекстринами. 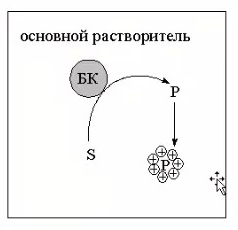 Воду для удаления из органических растворителей можно включать в кристаллогидраты. Например, в безводном сульфате натрия. В-четвертых, летучие продукты можно вакуумировать. 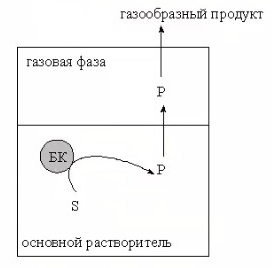 В-пятых, при трансформации в водной фазе токсичные продукты можно удалять через полупроницаемую мембрану во вспомогательную водную фазу. 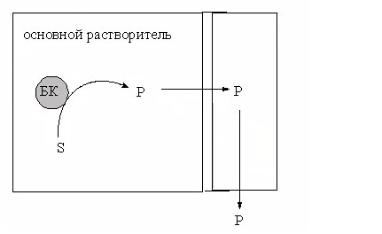 В-шестых, для выведения продуктов из воды можно использовать вспомогательную водную фазу несмешивающуюся с основной фазой. В качестве такой вспомогательной фазы используют водный раствор водорастворимого полимера, например, полиэтиленгликоля. Полимер значительно увеличивает вязкость раствора, в отсутствии принудительного перемешивания такой раствор не будет самопроизвольно смешиваться с водой. Таким образом, все представленные способы выведения продукта из реакционной смесии in situ позволяет поддерживать его низкую концентрацию вблизи биокатализатора, а,следовательно, предотвращать его ингибирование. 10.ПОТЕНЦИАЛ ФЕРМЕНТОВ ДЛЯ ПОЛУЧЕНИЯ БАВ В БИОКАТАЛИТИЧЕСКИХ ПРОЦЕССАХФерменты классифицируются в соответствии с типами реакции, которые они катализируют. По международной классификации ферментов они разделены на 6 основных классов. 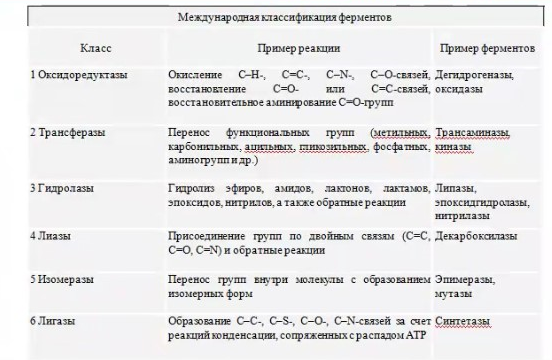 Ферменты почти всех классов играют важную синтетическую роль в органической химии. В качестве исключения можно рассматривать ферменты 6 класса – лигазы. Поскольку регенерация кофактора АТФ in situ до сих пор является затруднительной. Лигазы находят ограниченное применение в качестве катализаторов in vitro в органическом синтезе. В противоположность этому ферменты первых 5 классов оказались высокоэффективными катализаторами, широко применяемыми в органическом синтезе, и в частности для промышленного применения. Оксидоредуктазы. Многие окислительно-восстановительные процессы были успешно реализованы с участием оксидоредуктаз. 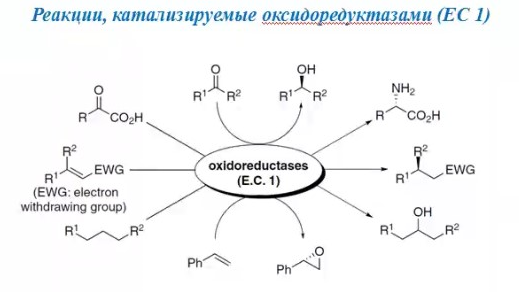 Восстановление карбонильной группы до спиртовой при использовании, например, алкогольдегидрогеназы или дегидрогены – альфа-гидроксикислот в качестве катализаторов или функциональной аминогруппы при использовании дегидрогены – альфа-гидроксикислот в качестве катализаторов при восстановительном амминировании уже нашло широкое применение как в органическом синтезе, так и в промышленности. В последнее время наблюдается растущая тенденция применения оксидоредуктаз также для восстановления двойной С=С связи. Основными преимуществами использования оксидоредуктаз в качестве катализаторов в окислительно-восстановительных процессах является отличительная селективность ферментов даже при использовании соединений не содержащих функциональных групп. Например, использование в качестве субстрата алканов и циклоалканов. Вторым преимуществом является использование молекулярного кислорода в качестве усточивого и дешевого окислительного агента Селективное окисление функционально замещенных алканов затруднительно для хемокатализа и существует лишь ограниченное число эффективных катализаторов для таких превращений. В то время, как с промышленной точки зрения существует высокий спрос на этот тип реакций. На сегодняшний день в промышленности гидроксилирование стероидов осуществляется биокаталитическими, а не химическими методами. Наряду с гидроксилированием другие окислительные процессы с участием осидоредуктаз также представляют интерес в органическом синтезе. Такие как, например, реакция Баэра-Вилигера с участием монооксигеназ (окисление по реакции Баэра-Вилигера с образованием лактонов из кетонов) и стиролмонооксигеназные реакции (эпоксидирование стиролов). Трансферазы. Они также являются универсальными катализаторами для трансформаций в органическом синтезе. В частности, трансаминазы применяют в синтезе аминокислот и аминов. 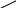 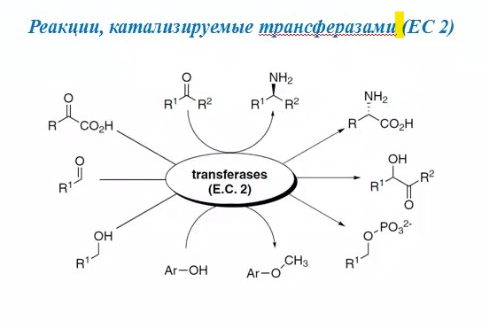 (ошибка в продукте R1 должно быть – 3 реакция слева) Гидролазы. Ферменты этого класса являются наиболее часто используемыми ферментами в органическом синтезе. Это связано с тем, что: Во-первых, многие гидролазы являются коммерчески доступными, например, в случае применения пищевой промышленности. Во-вторых, их применение не требует введения дополнительных кофакторов или использование методов регенерации кофатора. В-третьих, гидролазы находят широкое применение благодаря их способности модифицировать карбоксильную группу, например, в процессах разделения рацемических смесей и D-семетеризации. В-четвертых, гидролазы, особенно в случае липаз, способны осуществлять биотрансформации в органических растворителя, применяемых в качестве реакционной среды, часто используемых в органической химии. Типичными примерами гидролаз являются протеазы, липазы и эстеразы. Типичные превращения включают гидролиз сложных эфиров и амидов, а также обратные реакции – этерификацию и амидирование. 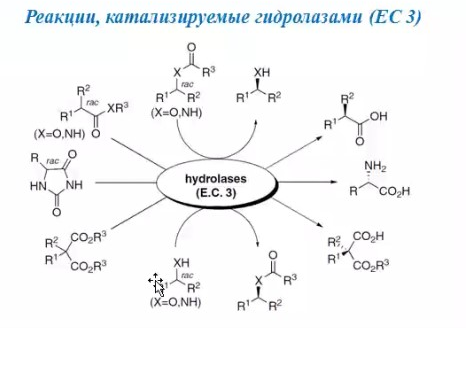 Еще одним типом стериоселективных процессов, представляющих интерес, является реакция десимметеризации прохиральных соединений в хиральные, например, прохиральных и мезодиэфиров. Лиазы. Лиазы характеризуются способностью образовывать новые связи СХН, где в качестве атома Х может выступать углерод, азот или кислород в реакции присоединения небольшой молекулы по двойной связи СХ. Такой малой молекулой может быть, например, вода, аммиак, а также углеродный нуклеофил. Например, ферменты, которые инициируют присоединение воды по двойной связи С=С называются гидротазами, а ферменты инициирующие присоединение аммиака – аммиаклиазами. Кроме того, использование углеродных нуклеофилов позволяет стериоселективно сформировать одинарную С-С связь. Широко используются такие углеродные нуклеофили, как например, цианид в реакции гидроцианирования альдегидов, а также альдегиды в реакциях инверсии полярности, таких как бензоиновые конденсации. 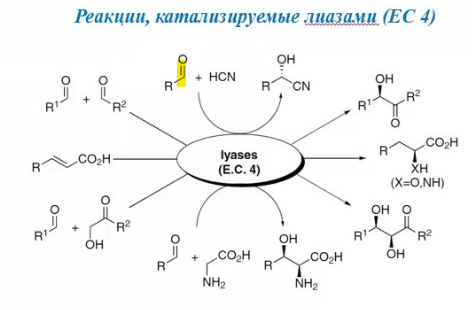 Изомеразы. К ферментам этого класса, способные катализировать реакции изомеризации. Например, рацимизация, 1,2-перемещение функциональных групп, например аминогрупп, и цис-, транс- изомеризация. 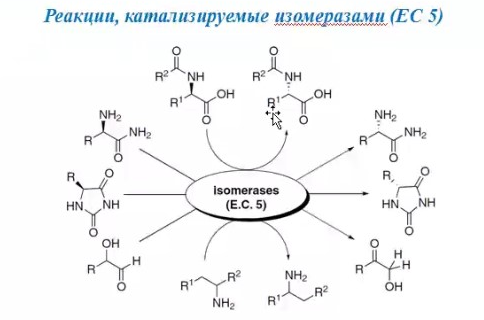 До промышленного уровня доведен процесс производства кукурузного сиропа с высоким содержанием фруктозы с помощью ферментативного превращения глюкозы во фруктозу. Объемы этого производства более 1 млн тонн. В области органической химии использование рацемаз привлекает наибольший интерес, так как применение рацемазы совместно с еще одним биокатализатором, способным разделять рацемические смеси, позволяет разработать процессы динамического кинетического разделения рацемических смесей. Как правило, такие процессы разделения протекают в сочетании с рацемазами и реакциями, катализируемыми гидролазами. Лигазы. Этот класс ферментов пока что не находит области применения. Это связано с тем, что реакции, катализируемые лигазами, требуют вовлечения АТФ в качестве кофакторов которые эффективно регенирируются в процессах, протекающих в живой клетке, но его регенерация in situ в условиях проведения реакции in vitro остается нерешенной. Хотя были разработаны некоторые методы регенерации, применение в процессах органического синтеза, в частности, в крупномасштабных процессах по-прежнему ограничено и разработано эффективных и экономически привлекательных методов регенерации АТФ in situ является перспективным направлением для исследований. |
