история. 1. понятие биотрансформации. Виды биокатализаторов
 Скачать 4.48 Mb. Скачать 4.48 Mb.
|
11.ВЛИЯНИЕ ХИРАЛЬНОСТИ НА БИОЛОГИЧЕСКУЮ АКТИВНОСТЬ ВЕЩЕСТВЯвление хиральности широко распространено в природе и оказывает существенное влияние на нашу жизнь. Следствием хиральности является существование энантиомеров. Чаще всего источником хиральности служит ассиметричный центр. Молекула с одним ассиметричным центром имеет одну пару зеркальных энантиомеров. Чаще всего ассиметричным является атом углерода с 4-мя разными заместителями. Однако, фосфор, сера, бор, кремний и реже азот тоже могут быть ассиметричными центрами. Если в молекуле есть несколько ассиметричных центров, количество пар энантиомеров увеличивается. Энантиомеры каждой пары обладают идентичными химическими и физическими свойствами, за исключением способности вращать плоскость поляризованного света в разных направлениях и различной реакционной способностью по отношению к другим оптически активным соединениям. Все живые организмы имеют в своем составе хиральные биомолекулы такие, как аминокислоты, углеводы, белки и нуклеиновые кислоты. Более того, природные макромолекулы гомохеральны, то есть содержать ассиметричные центры с одинаковой конфигурацией. Белки состоят из L-аминокислот, в то время как углеводы представлены D-сахаридами. К биологически активным веществам, имеющим важное практическое значение, относятся, прежде всего, лекарственные соединения, широко использующиеся в медицине и ветеринарии. Хиральность – свойство соединения существовать в виде пары несовместимых между собой зеркальных изображений. Стереоизомеры – это изомеры, которые обладают идентичным строением, но отличаются расположением атомов в пространстве. Энантиомеры – пара стереоизомеров, представляющих собой зеркальные отражения друг друга, не совмещаемые в пространстве. Диастереомеры – стереоизомеры, которые не относятся к зеркальным отражениям. Диастереомеры характеризуются различиями в физических свойствах и некоторыми различиями в химическом поведении по отношению к ахиральным, а также хиральным реагентам. 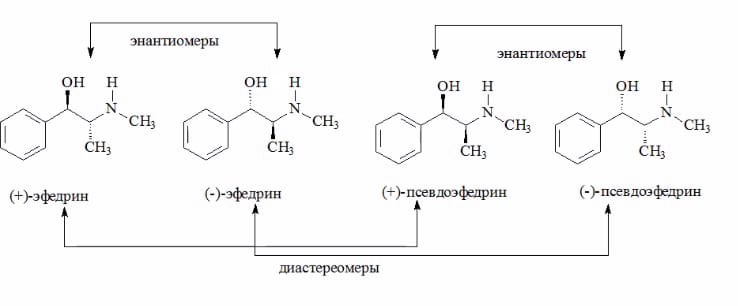 Несмотря на идентичный химический состав, энантиомеры хиральных биологически активных соединений зачастую обладают различной биологической активностью. D-пропоксифен (коммерческое название Darvon) обладает болеутоляющим действием, L-пропоксифен (коммерческое название Norvad) является средством от кашля. (+)-Аскорбиновая кислота обладает противоцинготным действием, (-) -Аскорбиновая кислота неактивна. S,S-аспартам имеет сладкий вкус, а его R,R-изомер является горьким. R-(-)-Лимонен имеет аромат апельсина, S-(-)-лимонен дает лимонный вкус S-(+) – Карвон пахнет тмином, а R-(-) – карвон – мятой. D-Берметрин является мощным инсектицидом, L-берметрин почти неактивен. Принцип действия биологически активных молекул основан на связывании со специфическими биологическими участками – сайтами связывания: белками (рецепторами, ферментами), нуклеиновыми кислотами (ДНК, РНК) и биомембранами (фосфолипидами и гликолипидами), присутствующими в организме. Сайты связывания биологически активных молекул состоят из гомохиральных биомолекул, имеющих сложные трехмерные структуры, способные распознавать хиральность молекулы биологически активных веществ. Благодаря своей сложной энантиоселективной структуре биологические рецепторы взаимодействуют с биологически активными молекулами, как правило, высоко стереоселективным. Только один энантиомер хирального препарата преимущественно взаимодействует с сайтом связывания рецептора, в то время как другой энантиомер практически неспособен связываться с ним. В то же время второй энантиомер препарата в ряде случаев может взаимодействовать с каким-либо другим рецептором или рецепторами в организме. Рассмотрим молекулярный механизм взаимодействия хирального биологически активного вещества с его специфическим биологическим участком или сайтом. Для того, чтобы биологически активная молекула обладала необходимым фармакологическим действием участки молекулы обозначенные как А, В и С должны взаимодействовать с соответствующими сайтами связывания рецептора 1, обозначенные как a,b и c соответственно. Только один энантиомер биологически активной молекулы имеет трехмерную структуру, которая может быть совмещена со всеми соответствующими сайтами связывания, то есть A-a, B-b и С-с. Другой энантиомер этой биологически активной молекулы не может связываться с сайтом 1, независимо от того как он вращается в пространстве и, следовательно, не будет проявлять биологическую активность, характерную для первого энантиомера. Однако, при наличии для второго энантиомера своего специфического участка – сайта 2 – он будет оказывать альтернативное биологическое действие на организм. 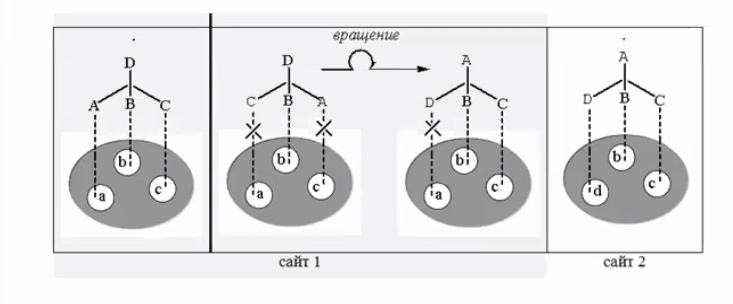 Фармакологическая активность лекарственных соединений, главным образом, зависит от их взаимодействия с этими биологическими участками. Энантиомер, обладающий необходимым терапевтическим эффектом, называют эутомером, а его антипод – менее активный, либо неактивный, либо даже обладающий серьезным побочным действием или токсичностью, называют дистомером. Рассмотрим примеры:
13.11.2021 Лекция | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
