1. Предмет и методы химической термодинамики. Взаимосвязь между процессами обмена веществ и энергии в организме. Химическая термодинамика как теоретическая основа биоэнергетики
 Скачать 29.04 Mb. Скачать 29.04 Mb.
|
|
1.Предмет и методы химической термодинамики. Взаимосвязь между процессами обмена веществ и энергии в организме. Химическая термодинамика как теоретическая основа биоэнергетики. предметом изучения химической термодинамики являются превращения различных видов энергии при протекании химических реакций, процессов растворения, испарения, кристаллизации, адсорбции. Химическая термодинамика количественно определяет тепловые эффекты вышеперечисленных процессов, выясняет возможность самопроизвольного их протекания в том или ином направлении и условия, при которых химические реакции будут находиться в состоянии равновесия. Причем изучение происходящих превращений не требует, с позиций термодинамики, сведений об их механизмах, представлений о строении молекул, участвующих в реакциях веществ. Достаточно только знать начальное состояние системы и те внешние условия, в которых она находится. Следует подчеркнуть также, что термодинамика не может ответить на вопросы о том, с какой скоростью и по какому механизму будет протекать тот или иной процесс, какое количество времени потребуется для достижения в нем химического равновесия. В настоящее время термодинамический метод исследования является одним из наиболее надежных и эффективных средств для изучения обмена веществ и энергии, происходящего в клетках животных, растений и человека. Живые организмы усваивают поступающие к ним из окружающей среды вещества, перерабатывают их, синтезируют и накапливают новые высокомолекулярные соединения для создания и обновления клеток и тканей, аккумулирования больших запасов химической энергии. Совокупность всех процессов называют ассимиляцией или анаболизмом Одновременно в организме протекают противоположные процессы – диссимиляция или катаболизм, сводящиеся к разложению сложных органических соединений, окислению их до Н2О, СО2 и высвобождению при этом энергии. В раннем периоде развития в организме человека, как и во всем живом, процессы ассимиляции превалируют над диссимиляцией, но по мере приближения к старости начинают доминировать процессы диссимиляции, что приводит к уменьшению в организме запасов химической энергии. Изучением и решением всех этих вопросов занимается биоэнергетика, которую можно рассматривать одновременно и как часть биохимии и как часть биофизики. Теоретической же основой биоэнергетики и инструментом, с помощью которого она решает свои задачи, является химическая термодинамика. 2. Основные понятия термодинамики. Внутренняя энергия. Работа и теплота - две формы передачи энергии. Понятия термодинамики:             Система – любой объект природы, состоящий из большого числа молекул (структурных единиц) и отделённый от других объектов природы реальной или воображаемой граничной поверхностью (границей раздела). Состояние системы – совокупность свойств системы, позволяющих определить систему с точки зрения термодинамики. Внутренняя энергия системы – сумма энергий теплового движения молекул и энергии взаимодействия между ними или функция состояния системы, приращение которой равно теплоте Qv. полученной системойв изохорном процессе. Внутреннюю энергию нельзя определить, поскольку у системы нельзя отнять всю энергию. Фаза - гомогенная часть гетерогенной системы (вода и лед в стакане) Фазовый переход - превращения фаз (таяние льда, кипение воды). Функции состояния - свойства, величины которых при переходе системы из одного состояния в другое зависят только от начального и конечного состояния системы и не зависят от пути перехода, получили название функций состояния. К ним относятся, например, давление, объем, температура системы. Термодинамические функции: состояния системы: применяются для определения изменения энергии в тех или иных условиях.(например ΔЕ – внутренняя энергия системы) Изменение ΔЕ обусловлено работой W, которая совершается при взаимодействии системы со средой, и передачей теплоты Q между средой и системой 3 Типы термодинамических систем (изолированные, закрытые, открытые). Типы термодинамических процессов (изотермические, изобарные, изохорные). Стандартное состояние. При изложении основных положений термодинамики пользуются набором определенных строго сформулированных понятий, начальное из которых – понятие термодинамической системы, являющейся объектом исследования в термодинамике. Под термодинамической системой подразумевают избранную совокупность тел или веществ, состоящую из большого числа структурных единиц (молекул, атомов, ионов) и отделенную от окружающей внешней среды определенной границей или поверхностью раздела. Внешнюю среду или внешний мир представляет собой то, что находится вне оболочки системы. В зависимости от свойств поверхности раздела, термодинамические системы делятся, в первую очередь, на изолированные, закрытые иоткрытые (рис. 2). Изолированные системы не могут обмениваться с окружающей средой ни веществом, ни энергией. Закрытые системы обмениваются с внешним миром только энергией, а открытые – и веществом, и энергией. 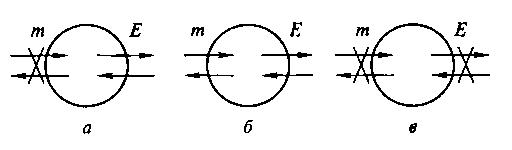 Рис. 2. Примеры закрытой (а), открытой (б) и изолированной (в) систем Следует подчеркнуть, что реальные системы никогда не бывают абсолютно изолированными, они лишь в той или иной степени приближаются к данному понятию, но полностью с ним не совпадают. Существуют такие процессы, в ходе протекания которых остаются неизменными только один или несколько параметров системы, а все остальные меняются. Так, процесс, протекающий при постоянной температуре, называется изотермическим, при постоянном давлении – изобарным, а при постоянном объеме – изохорным. Если неизменными остаются температура и давление или температура и объем, то такие процессы называются, соответственно, изобарно-изотермическими или изохорно-изотермическими. Так, например, химические реакции, протекающие в живых организмах, являются изобарно-изотермическими. Большинство реакций, применяемых для промышленных и технических целей, осуществляется в условиях практически постоянного давления, т.е. является изобарными. Примерами изохорных реакций могут быть реакции, идущие в закрытом сосуде, реакции между твердыми телами и жидкостями без образования газа, реакции между газами, при протекании которых число молекул газа остается постоянным: Для сравнения свойств термодинамических систем необходимо точно указать их состояние. С этой целью введено понятие – стандартное состояние, за которое для индивидуальной жидкости или твердого тела принимается такое физическое состояние, в котором они существуют при давлении в 1 атм (101315 Па) и данной температуре. Для газов и паров стандартное состояние отвечает гипотетическому состоянию, в котором газ при давлении в 1 атм подчиняется законам идеальных газов, при данной температуре. Величины, относящиеся к стандартному состоянию, пишутся с индексом «о» и нижним индексом указывается температура, чаще всего это 298К. Станда́ртные состоя́ния в химической термодинамике - условно принятые состояния индивидуальных веществ и компонентов растворов при оценке термодинамических величин. 4. Первое начало термодинамики. Формулировка. Математическое выражение. Энтальпия. Применение первого начала термодинамики к биосистемам  Частным случаем закона сохранения энергии в применении к процессам, сопровождающимся тепловыми явлениями, выступает первое начало (или первый закон) термодинамики, который можно сформулировать следующим образом: подведенное к системе тепло Q идет на увеличение ее внутренней энергии ΔU и на совершение системой работы А против внешних сил: Q = Δ U + АСистема может переходить из одного состояния в другое различными путями. Но в соответствии с законом сохранения энергии изменение внутренней энергии ΔU системы не зависит от пути перехода: оно одинаково во всех случаях, если одинаковы начальное и конечное состояния системы. Количество же теплоты и количество работы зависят от этого пути. Однако, как бы не менялись значения Q и А при разных путях перехода системы из одного состояния в другое, их алгебраическая сумма будет всегда одинаковой, если только одинаковы начальное и конечное состояния системы.  На основании первого начала термодинамики можно сделать несколько важных выводов.1. В изолированной системе сумма всех видов энергии есть величина постоянная.2. Невозможно создать вечный двигатель первого рода, который производил бы работу без подведения энергии извне, т.к. производимая системой работа будет всегда меньше, чем теплота, затраченная на ее производство. в термодинамике используют новую величину – энтальпию или теплосодержание системы Н, определяемую соотношением: Н = U + рVЭнтальпия больше внутренней энергии на величину работы расширения, совершенной при изменении объема системы от 0 до V. Как и внутренняя энергия, энтальпия является функцией состояния и определить ее абсолютное значение нельзя. Можно только измерить изменение ΔН при переходе системы из одного состояния в другое: ΔН = Н2– Н1= (U2+рV2) – (U1+ рV1) = U2– U1+ (рV2– рV1) = ΔU + р(V2– V1) = ΔU + рΔVПо первому закону во всех явлениях природы энергия не может исчезнуть бесследно или возникнуть из ничего. Энергия может только превращаться из одной формы в другую в строго эквивалентных соотношениях. Этот закон является универсальным и подтверждается всем опытом человечества. Поступление пищи обеспечивает энергию, которая используется для выполнения различных функций организма или сохраняется для последующего использования. Энергия высвобождается из пищевых продуктов в процессе их биологического окисления, которое является многоступенчатым процессом. Пищевые вещества окисляются вплоть до конечных продуктов, которые выделяются из организма. Например, углеводы окисляются в организме до углекислого газа и воды. Такие же конечные продукты образуются при сжигании углеводов в калориметре: C6H12O6 + 6O2 = 6CO2 + 6H2O Величина энергии, высвобождаемой из каждого грамма глюкозы в этой реакции, составляет 4,1 килокалории (кКал). Столько же энергии, образуется при окислении глюкозы в живых клетках, несмотря на то, что процесс окисления в них является многоступенчатым процессом и происходит в несколько стадий. Этот вывод основан на принципе Гесса, который является следствием первого закона термодинамики: тепловой эффект многоступенчатого химического процесса не зависит от его промежуточных этапов, а определяется лишь начальным и конечным состояниями системы. Таким образом, исследования с помощью калориметра показали среднюю величину физиологически доступной энергии, которая содержится в 1 грамме трех пищевых продуктов (в килокалориях): углеводы - 4,1; белки - 4,1; жиры - 9,3. С другой стороны, в конечном итоге вся энергия, поступившая в организм, превращается в теплоту. Также при образовании АТФ лишь часть энергии запасается, большая - рассеивается в форме тепла. При использовании энергии ATФ функциональными системами организма большая часть этой энергии также переходит в тепловую. Оставшаяся часть энергии в клетках идёт на выполнении ими функции, однако, в конечном счёте, превращается в теплоту. Например, энергия, используемая мышечными клетками, расходуется на преодоление вязкости мышцы и других тканей. Вязкое перемещение вызывает трение, что приводит к образованию тепла. Другим примером является расход энергии, передаваемой сокращающимся сердцем крови. При течении крови по сосудам вся энергия превращается в тепло вследствие трения между слоями крови и между кровью и стенками сосудов. Следовательно, по существу вся энергия, потраченная организмом, в конечном счете, преобразуется в теплоту. Из этого принципа существует лишь единственное исключение: в случае, когда мышцы выполняют работу над внешними телами. Если человек не выполняет внешней работы, то уровень высвобождения организмом энергии можно определить по величине общего количества теплоты, выделенной телом. Для этого применяют метод прямой калориметрии, для реализации которого используют большой, специально оборудованный калориметр. Организм помещают в специальную камеру, которая хорошо изолирована от среды, то есть не происходит обмена энергией с окружающей камеру средой. Количество теплоты, выделенной исследуемым организмом, можно точно измерить. Эксперименты, выполненные этим методом, показали, что количество энергии, поступающей в организм, равно энергии, выделяющейся при проведении калориметрии. Прямая калориметрия в проведении трудоёмка, поэтому в настоящее время используют метод непрямой калориметрии, который основан на вычислении энергетического выхода организма по использованию им кислорода. 5. Стандартная энтальпия образования вещества, стандартная энтальпия сгорания вещества. Стандартная энтальпия реакции. Закон Гесса. Формулировка. Математическое выражение. Следствия из закона Гесса.  Стандартная энтальпия сгорания ΔHoсгор – тепловой эффект реакции сгорания одного моля вещества до образования высших оксидов. Для органических веществ –до CO2(г) и H2O(ж). Теплота сгорания негорючих веществ принимается равной нулю. Теплота сгорания топлива характеризует его теплотворную способность. Стандартная энтальпия образования вещества (ΔfH0) – увеличение или уменьшение энтальпии, сопровождающее образование 1 моль вещества из простых веществ, при условии, что все участники реакции находятся в стандартном состоянии Стандартная энтальпия сгорания вещества (ΔсH0) – уменьшение энтальпии при окислении в избытке кислорода 1 моль вещества, взятого в стандартном состоянии, до конечных продуктов окисления. Закон Гесса – энергия не создаётся и не уничтожается, а лишь переходит из одного вида энергии в другой. 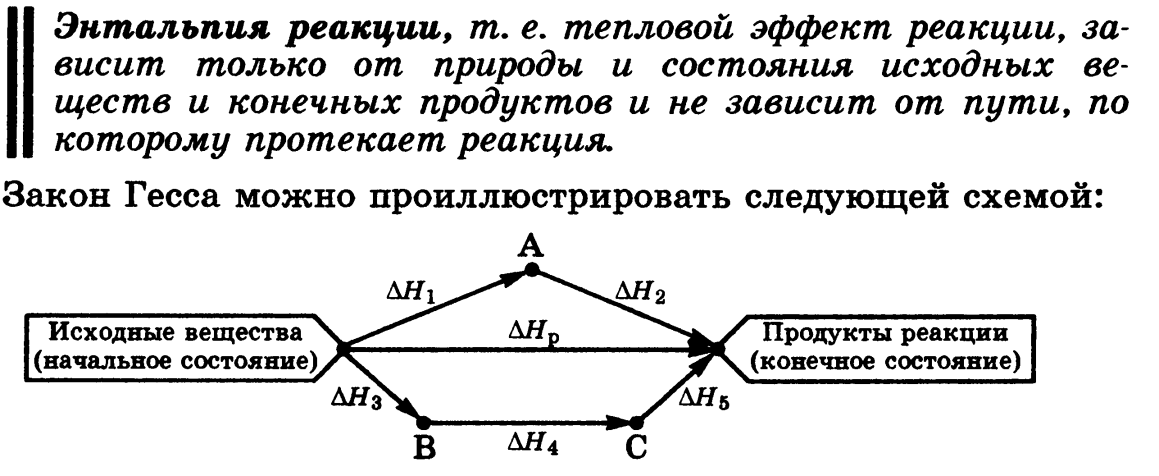 Закон Гесса Тепловой эффект реакции зависит только от природы и состояния исходных вещ-в и не зависит от пути, по которому реакция протекает Следствие 1. Тепловой эффект химической реакции равен разности сумм теплот образования (ΔHf) продуктов реакции и исходных веществ, умноженных на стехиометрические коэффициенты (ν): ΔHof,i - стандартная энтальпия образование веществ vi – стехиометрические коэффициенты Следствие 2. Тепловой эффект химической реакции равен разности сумм теплот сгорания (ΔHc) исходных веществ и продуктов реакции, умноженных на стехиометрические коэффициенты (ν): ΔHoс,i- стандартная энтальпия сгорания веществ vi – стехиометрические коэффициенты Следствие 3. Энтальпия реакции равна разности сумм энергий связей Eсв исходных и конечных реагентов с учетом их стехиометрических коэффициентов. В ходе химической реакции энергия затрачивается на разрушение связей в исходных веществах (ΣEисх) и выделяется при образовании продуктов реакции (–ΣEпрод). Отсюда
Следовательно, экзотермический эффект реакции свидетельствует о том, что образуются соединения с более прочными связями, чем исходные. В случае эндотермической реакции, наоборот, прочнее исходные вещества. При определении энтальпии реакции по энергиям связей уравнение реакции пишут с помощью структурных формул для удобства определения числа и характера связей. Следствие 4. Энтальпия реакции образования вещества равна энтальпии реакции разложения его до исходных веществ с обратным знаком. Следствие 5. Энтальпия гидратации равна разности энтальпий растворения безводной соли (ΔHoраств.б/с)и кристаллогидрата (ΔHoраств.крист) 6.Второе начало термодинамики. Формулировка. Обратимые и необратимые в термодинамическом смысле процессы. Энтропия как критерий возможности протекания самопроизвольных процессов. Второе начало термодинамики: В изобарно-изотермических условиях (р, Т = const) в системе самопроизвольно могут протекать только такие процессы, в результате которых энергия Гиббса системы уменьшается (ΔG < 0). В состоянии равновесия G = const, G = 0  Обратимый процесс (то есть равновесный) — термодинамический процесс, который может проходить как в прямом, так и в обратном направлении, проходя через одинаковые промежуточные состояния, причем система возвращается в исходное состояние без затрат энергии, и в окружающей среде не остается макроскопических изменений. Обратимый процесс можно в любой момент заставить протекать в обратном направлении, изменив какую-либо независимую переменную на бесконечно малую величину. Необратимым называется процесс, который нельзя провести в противоположном направлении через все те же самые промежуточные состояния. Все реальные процессы необратимы.  Энтропия – энтропия – функция состояния, приращение которой ΔS равно теплоте Qмин подведённой к системе в обратимом изотермическом процессе, делённой на абсолютную температуру T, три которой осуществляется процесс: ΔS = Qмин/ T или мера вероятности пребывания системы в данном состоянии – мера неупорядоченности системы.  7. Энергия Гиббса – главный критерий возможности протекания самопроизвольных про цессов. Прогнозирование направления самопроизвольно протекающих процессов в изолированной и закрытой системах; роль энтальпийного и энтропийного факторов.   Критериями направления самопроизвольного протекания необратимых процессов являются неравенства ΔG < 0 (для закрытых систем), ΔS > 0 (для изолированных систем). Если величина ΔG имеет отрицательный знак (ΔG < 0), то реакция самопроизвольно может протекать только в прямом направлении. Причем абсолютное значение разности ΔH – TΔS = ΔG будет определять движущую силу данного процесса. Если же ΔG > 0, то в условиях, для которых были измерены ΔH и TΔS, в прямом направлении данная реакция протекать не может. Зато осуществимой окажется обратная реакция, для которой ΔG будет иметь отрицательное значение. Реакции, для которых ΔH < 0, а ΔS > 0, могут самопроизвольно протекать в прямом направлении при любых температурах, т.к. ΔG у них всегда будет меньше нуля. Примером такой реакции может служить гидролиз пептидов или белков. Если для химической реакции ΔH > 0, а ΔS < 0, то ее самопроизвольное протекание в прямом направлении всегда неосуществимо, т.к. энергия Гиббса в данном случае возрастает. Примером такой реакции может служить процесс фотосинтеза – образование глюкозы и кислорода из углекислого газа и воды, – который невозможен без участия солнечной энергии. В случае ΔH > 0 и ΔS > 0 самопроизвольному протеканию реакции в прямом направлении способствует энтропийный фактор. При низких температурах отрицательное значение ΔH – TΔS может быть невозможно, но при нагревании – оно возможно и реакция становится осуществимой в прямом направлении. Например, тепловая денатурация белковых молекул. Если ΔH < 0 и ΔS < 0, то отрицательное значение ΔG такой химической реакции наблюдается только при достаточно низких температурах. При вычислении ΔG в химической реакции можно использовать следствие из закона Гесса, применяемое для расчета ее теплового эффекта (изменения энтальпии). В данном случае оно будет звучать следующим образом. В ходе самопроизвольного процесса в закрытых системах G уменьшается до определенной величины, принимая минимально возможное для данной системы значение Gmin. Система переходит в состояние химического равновесия (ΔG= 0). Самопроизвольное течение реакций в закрытых системах контролируется как энтальпийным (ΔrH), так и энтропийным (TΔrS) фактором. Для реакций, у которых ΔrH< 0 иΔrS> 0, энергия Гиббса всегда будет убывать, т.е.ΔrG< 0, и такие реакции могут протекать самопроизвольно при любых температурах В изолированных системах энтропия приобретает максимально возможное для данной системы значение Smax; в состоянии равновесияΔS= 0 Под стандартной энергией Гиббса образования ΔG°, понимают изменение энергии Гиббса при реакции образования 1 моль вещества, находящегося в стандартном состоянии. Это определение подразумевает, что стандартная энергия Гиббса образования простого вещества, устойчивого в стандартных условиях, равна нулю. В самопроизвольной реакции: ∆G<0 (G2-G1<0) ∆S>0 (S2-S1>0) реакция пойдет → ∆G>0 ∆S<0 реакция пойдет ← Формула для I и II т/д: ∆Gт=∆H0хр - Т∆S Энтальпийный и энтропийный факторы Из приведенного выражения следует, что самопроизвольное течение реакции может контролироваться как энтальпийным (∆H), так и энтропийным фактором (T∆S). Очевидно, что для реакций, характеризующихся ∆Hr< 0 и ∆Sr> О, энергия Гиббса должна обязательно убывать, т. е. ∆Gr< 0, и такие реакции могут протекать самопроизвольно при любых температурах, так как оба фактора способствуют протеканию процесса. Пример такой реакции — гидролиз белка. Наоборот, при ∆Hr> 0 и ∆Sr< 0 самопроизвольное течение реакций всегда невозможно, так как энергия Гиббса должна обязательно возрастать. Оба фактора препятствуют протеканию реакции. Пример — фотосинтез, т. е. образование глюкозы и кислорода из углекислого газа и воды. Несогласованное действие факторов наблюдается в двух случаях: 1) ∆Hr> 0 и ∆Sr> 0 — самопроизвольному протеканию реакции способствует энтропийный фактор, отрицательное значение изменения энергии Гиббса возможно при соотношении |∆Sr |> |∆Hr|, т. е. при достаточно высоких температурах. Примером процессов этого типа является тепловая денатурация белков; 2) ∆Hr< О и ∆Sr< О — благоприятствующим фактором является энтальпийный, соотношение AGT< 0 наблюдается при |∆Hr| >|∆Sr |, т. е. при достаточно низких температурах. Пример процессов этого типа — гидратация белков. 8 . Термодинамические условия равновесия. Стандартная энергия Гиббса образования вещества, стандартная энергия Гиббса биологического окисления вещества. Стандартная энергия Гиббса реакции. Примеры экзергонических и эндергонических процессов, протекающих в организме. Принцип энергетического сопряжения.   Под стандартной энергией Гиббса биологического окисления ΔG°, понимают изменение энергии Гиббса при реакции биологического окисления 1 моль вещества, находящегося в стандартном состоянии.Под стандартной энергией Гиббса образования ΔG°, понимают изменение энергии Гиббса при реакции образования 1 моль вещества, находящегося в стандартном состоянии   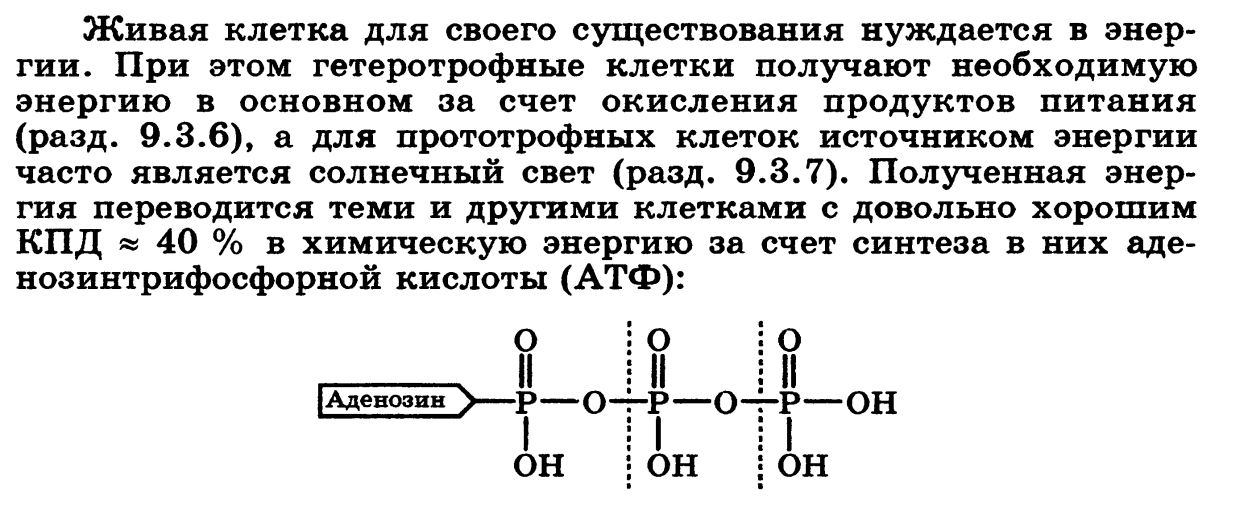  Принцип энергетического сопряжения: Сопряженные реакции – это реакции, в которых протекание одной реакции обусловлено протеканием другой, невозможной в отсутствии первой. Принцип энергетического сопряжения заключается в том, что энергия необходимая для протекания эндергонической реакции поступает за счет осуществление экзэргонической реакции , причем в двух реакциях присутствует общее веществ- интермедиан.
     11.Химическая кинетика как основа для изучения скоростей и механизмов биохимических процессов. Скорость реакции, средняя скорость реакции в интервале, истинная скорость. Факторы, влияющие на скорость реакции. 11.Химическая кинетика как основа для изучения скоростей и механизмов биохимических процессов. Скорость реакции, средняя скорость реакции в интервале, истинная скорость. Факторы, влияющие на скорость реакции.Химическая кинетика изучает скорости химических реакций, их зависимость от различных факторов и механизмы реакций. Последо вательность и характер стадий химических реакций называют меха низмом реакции.  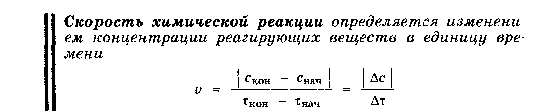 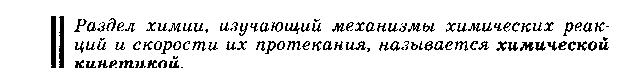  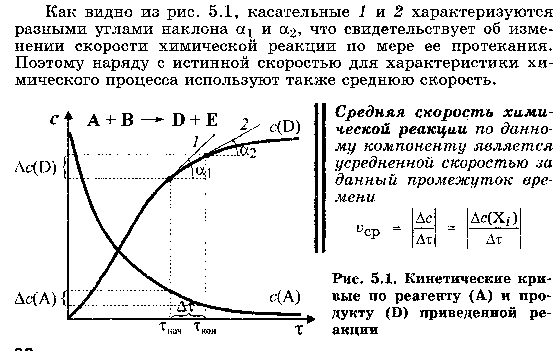 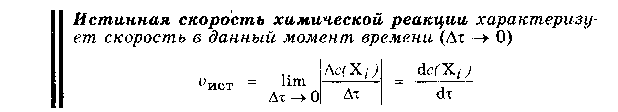  Факторы влияющие на протекание реакции 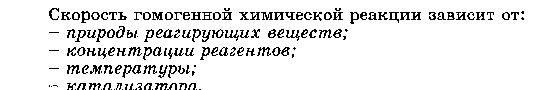 В организме человека протекают тысячи ферментативных реакций, проходящих в живой клетке. Однако в многостадийной цепи процессов достаточно велика разница между скоростями отдельных реакций. Так, синтезу в клетке молекул белка предшествует, по крайней мере, еще две стадии: синтез транспортной РНК и синтез рибосом. Но время, за которое удваивается концентрация молекул т-РНК, составляет 1,7 мин., молекулы белка - 17 мин., а рибосом - 170 мин. Скорость суммарного процесса медленной (лимитирующей) стадии, в нашем примере - скорость синтеза рибосом. Наличие лимитирующей реакции обеспечивает высокую надежность и гибкость управления тысячами реакций, происходящих в клетке. Достаточно держать под наблюдением и регулировать лишь наиболее медленные из них. Такой способ регулирования скорости многостадийного синтеза носит название принципа минимума. Он позволяет существенно упростить и сделать более надежной систему авторегулирования в клетке. Скорость реакций в зависимости от молекулярности будет выражаться уравнениями: а) V = к • СА - для мономолекулярной реакции; б) V = к • СА • Св или в) V = к • С2А - для бимолекулярной реакции; г) V = к • С • Св • С э д) V = к • С2А • Св или е) V = k • С3А- для тримолекулярной реакции. 12. Классификации реакций, применяющиеся в кинетике: реакции, гомогенные, гетерогенные и микрогетерогенные; реакции простые и сложные (параллельные, последовательные, сопряженные, цепные). Молекулярность элементарного акта реакции. Кинетические уравнения. Порядок реакции. Период полупревращения  Микрогетерогенные реакции – 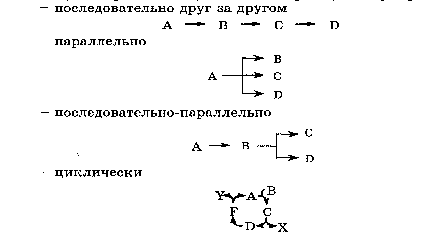  Молекулярность реакции– это количество молекул, которые принимают участие единовременно в одном акте столкновений. Молекулярность можно определить, лишь установив механизм реакции. В зависимости от числа реагирующих молекул (частиц), участвующих в элементарном акте, различают одномолекулярные (мономолекулярные), двухмолекулярные, тримолекулярные реакции. К одномолекулярнымреакциям типа А→Р относятся процессы распада молекулы на более простые составные части и реакции изомеризации. Двухмолекулярныминазываются элементарные реакции вида: А+В→Р и 2А→Р (Н2+J2=2HJ,HJ+HJ=H2+J2,CH3COOCH3+H2O=CH3COOH+CH3OHи т.д.). Значительно реже встречаютсятрехмолекулярныереакции А+2В→Р или 3А→Р. Во всех случаях вид и количество образующихся продуктов реакции не имеет значения, так как молекулярность определяется только числом молекул веществ, реагирующих в элементарном акте. Порядок реакции устанавливается экспериментально. Молекулярность и порядок реакции могут совпадать, а могут и различаться. Молекулярность и порядок реакции совпадаюттолько для простых реакций, протекающих только в одну элементарную стадию без участия посторонних молекул. Молекулярность и порядок реакции не совпадаютв трех основных случаях: 1) для сложных реакций; 2) для гетерогенных реакций; 3) для реакций с избытком одного из реагирующих веществ. Период полупревращения– это время, в течение которого прореагирует половина взятого вещества. Кинетическое уравнение выражает зависимость скорости хим. реакции от концентраций компонентов реакционной смеси Молекулярность-число молекул, реагирующих в в одном элементарном химическом акте. Молекулярность реакции определяется числом молекул, вступающих в химическое взаимодействие в элементарном акте реакции. По этому при знаку реакции разделяются на мономолекулярные, бимолекулярные и тримолекулярные. Тогда реакции типа А —>В будут являться мономолекулярными, например: а) С16Н34 (t°C) —>CgH18 + С8Н16 - реакция крекинга углеводородов; б) CaC03 (t°C) —>СаО + С02 - термическое разложение карбоната кальция. Реакции типа А + В —> С или 2А —> С - являются бимолекулярными, например: а) С + 02 -> С02; б) 2Н202 -> 2Н20 + 02 и т. д. Тримолекулярные реакции описываются общими уравнениями типа: а) А + В + С Д; б) 2А + В Д; в) 3А Д. Например: а) 2Н2 + 02 2Н20; б) 2NO + Н2N20 + Н20. Скорость реакций в зависимости от молекулярности будет выражаться уравнениями: а) V = к • СА - для мономолекулярной реакции; б) V = к • СА • Св или в) V = к • С2А - для бимолекулярной реакции; г) V = к • С • Св • С э д) V = к • С2А • Св или е) V = k • С3А- для тримолекулярной реакции.    Нередко молекулярность реакции трудно установить, поэтому используют более формальный признак - порядок химической реакции. Порядок реакции равен сумме показателей степеней концентраций в уравнении, выражающем зависимость скорости реакции от концентрации реагирующих веществ (кинетическом уравнении). Порядок реакции чаще всего не совпадает с молекулярностью ввиду того, что механизм реакции, т. е. "элементарный акт" реакции (см. определение признака молекулярности), трудно установить. Рассмотрим ряд примеров, иллюстрирующих указанное положение.
2Н202 —> 2Н20 + О э т. е. является бимолекулярной.  13.Зависимость скорости реакции от концентрации. Кинетические уравнения реакций первого, второго и нулевого порядков. Экспериментальные методы определения скорости и константы скорости реакций. Элементарный акт химической реакции осуществляется в момент столкновения реагирующих частиц. Увеличение концентрации реагентов соответствует увеличению числа частиц в объеме, что приводит к более частым столкновениям, а следовательно к увеличению скорости реакции. Количественная зависимость скорости реакции от концентрации выражается законом действующих масс: Скорость простой гомогенной реакции при постоянной температуре пропорциональна произведению концентраций реагирующих веществ, возведенных в степени, численно равные их стехиометрическим коэффициентам.  , где а и б - стехиометрические коэффициенты реагентов, с(А) и с(В) – молярные концентрации реагентов, к- константа скорости реакции. Порядок реакции по реагенту равен показателю степени, в которую надо возвести концентрацию данного реагента в кинетическом уравнении сложной реакции, чтобы вычисленная по этому уравнению скорость была равна скорости, найденной экспериментально. |
