5 Глава Гипертоническая болезнь (эссенциальная гипертензия) и симптоматические гипертензии
 Скачать 2.67 Mb. Скачать 2.67 Mb.
|
|
3.2.1. Электрокардиографическая диагностика инфаркта миокарда Локализация очаговых изменений (ишемии, повреждения и некроза) определяется по стандартным отведениям, усиленным и грудным отведениям (см. главу 2, рис. 2.2). В настоящее время инфаркт миокарда разделяется на крупноочаговый или Q(+) и мелкоочаговый или Q(-) (см. рис. 3.1.). 3.2.1.1. Крупноочаговый инфаркт миокарда I стадия – острая. Она подразделяется на период повреждения (Iа стадия) и формирование некроза (Iб стадия). Iа стадия - повреждение. На электрокардиограмме, зарегистрированной в течение 10-30 минут после острого нарушения коронарного кровоснабжения, в большинстве случаев отмечается картина, характерная для субэндокардиальной ишемии: над зоной инфаркта миокарда наблюдаются высокие положительные симметричные зубцы Т. Однако в этот период развития инфаркта такие электрокардиографические изменения регистрируются редко, преимущественно врачами скорой и неотложной медицинской помощи. В среднем через 20-30 минут после острого нарушения коронарного кровотока наблюдается подъем сегмента ST в виде монофазной кривой, при чем этот сегмент сливается с зубцом Т. Реже наблюдается подъем сегмента ST в виде плато. Эта стадия продолжается от нескольких часов до 3 суток. Специфичность и чувствительность элевации сегмента ST у больных с болями в грудной клетке для диагностики инфаркта миокарда составляет 91% и 46% соответственно. Смертность возрастает с увеличением числа отведений, отражающих элевацию сегмента ST. Iб стадия - формирование некроза сердечной мышцы. Эта стадия характеризуется уменьшением зоны повреждения: часть мышечных волокон некротизируется, но в то же время на периферии обмен веществ в зоне повреждения восстанавливается и переходит в ишемию, а функция кардиомиоцитов постепенно нормализуется. Зона некроза приводит к появлению на электрокардиограмме патологического зубца Q: QS или qR с одновременным подъемом сегмента ST. 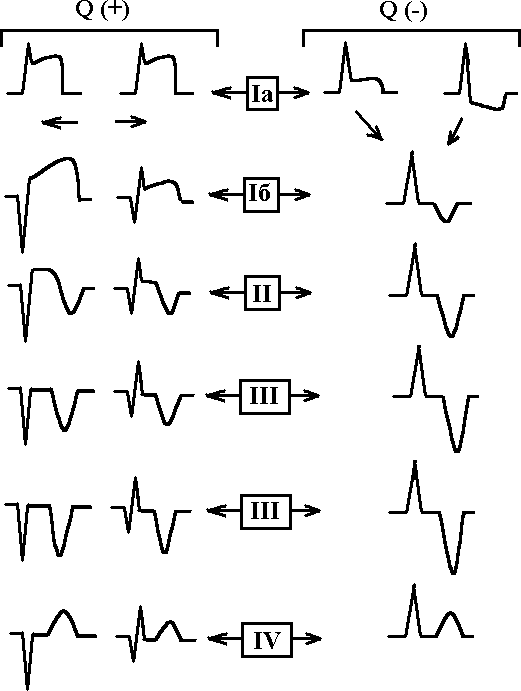  Рис. 2.12. Сопоставление продолжительности положительного клинического эффекта у больных стенокардией III-IV функционального класса при проведении лазеротерапии и аортокоронарного шунтирования. Лазеротерапия использовалась в терапевтических дозах. ия - рубцовая. Рубцовая ткань ведет себя так же, как зона некроза, т.е. не возбуждается и не создает электрического потенциала. На электрокардиограмме отмечается наличие патологического зубца Q(QS) с отрицательным зубцом Т, который может продолжать постепенно углубляться. Критерием выписки из стационара является отсутствие динамики электрокардиограммы, т.е. отсутствие изменения патологического зубца Q(QS) и отрицательного зубца Т при их регистрации трижды с интервалом 2-3 дня. IV стадия – период обратного «ремоделирования» миокарда левого желудочка. В настоящее время с применением ингибиторов АПФ, адекватной гипотензивной терапии и т.д. через 0,5-1,5 года после перенесенного инфаркта миокарда отрицательные зубцы Т в области сформировавшегося рубца трансформируются в положительные, что косвенно свидетельствует об обратном «ремоделировании» миокарда левого желудочка, а также об адекватной терапии после выписки из стационара (Rayn B., 1996). 3.2.1.2. Мелкоочаговый инфаркт миокарда I стадия – острая. Она подразделяется на период повреждения (Iа стадия) и формирование некроза (Iб стадия). Iа стадия - повреждение. На электрокардиограмме, зарегистрированной в течение 10-30 минут после острого нарушения коронарного кровоснабжения, в большинстве случаев изменения отсутствуют. В среднем через 30 минут после острого нарушения коронарного кровотока наблюдается подъем или депрессия сегмента ST. Реже выявляется подъем сегмента ST в виде плато. Эта стадия продолжается, также как при крупноочаговом инфаркте миокарда, от нескольких часов до 3 суток. Iб стадия - формирование некроза миокарда. Эта стадия характеризуется уменьшением зоны повреждения: часть мышечных волокон некротизируется, но размер некроза небольшой (как правило, не превышает 1/3 толщины стенки левого желудочка), при этом на периферии обмен веществ в зоне повреждения восстанавливается и переходит в ишемию, а функция кардиомиоцитов постепенно нормализуется. На электрокардиограмме, при развитии некроза сердечной мышцы, сегмент ST нормализуется и в области поражения формируется только отрицательный зубец Т. Патологического зубца Q (QS) или qR не наблюдается. Клиническое разделение между нестабильной стенокардией и инфарктом миокарда (с зубцом Q или без него) может быть проведено только ретроспективно, после серий электрокардиограмм и определения плазменных маркеров инфаркта. Больные с элевацией ST имеют большую вероятность коронарного тромбоза. Следует отметить, что не каждый инфаркт с элевацией ST приводит к формированию некроза с зубцом Q. Согласно результатам ангиографии, окклюзирующий тромбоз венечных артерий у больных с инфарктом миокарда и элевацией ST представлен более чем в 90% случаев, в то время как только оккюзирующий стеноз или тромбоз коронарных артерий встречается только у 1% больных со стабильной стенокардией и около 35-75% - с нестабильной стенокардией или инфарктом без зубца Q. II стадия - подострая. В этой стадии на электрокардиограмме сегмент ST находится на изолинии, и происходит постепенное углубление отрицательного зубца Т. Критерием диагностики подострой стадии мелкоочагового инфаркта миокарда является только углубление отрицательного зубца Т. III стадия - рубцовая. На электрокардиограмме при мелкоочаговом инфаркте миокарда отмечается наличие только отрицательного зубца Т, который может продолжать постепенно углубляться. Критерием выписки из стационара является отсутствие динамики на серии электрокардиограмм, т.е. отсутствие изменения отрицательного зубца Т, как минимум, на двух электрокардиограммах, зарегистрированных с интервалом 2-3 дня. IV стадия – период обратного «ремоделирования» миокарда левого желудочка. Также как при крупноочаговом инфаркте миокарда, при применении ингибиторов АПФ, адекватной гипотензивной терапии и т.д. через 1-3 месяца (до 1 года) после перенесенного инфаркта миокарда отрицательные зубцы Т в области сформировавшегося рубца трансформируются в положительные, что также косвенно свидетельствует об обратном «ремоделировании» миокарда левого желудочка, а также об адекватной терапии после выписки из стационара (Rayn B., 1996). 3.2.1.3. Атипичные формы первого инфаркта миокарда При атипичных формах инфаркта миокарда могут наблюдаться следующие электрокардиографические признаки (на рис. 3.2. представлена изменение зубца R в грудных отведениях в норме): 1 – «Провал» зубца R электрокардиограммы в грудных отведениях. Чаще наблюдается в отведениях V2,V3,V4, реже в отведении V5 (см. рис. 3.3.). 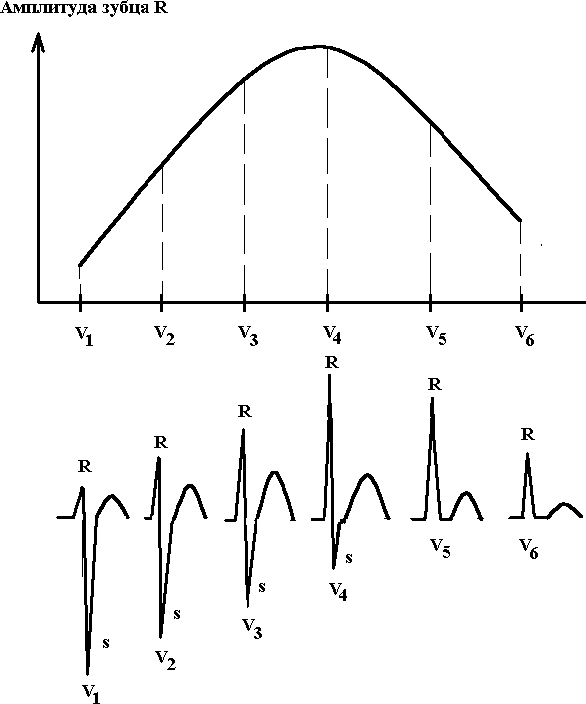 Рис.3.2. Схема динамики зубца R в грудных отведениях в норме. 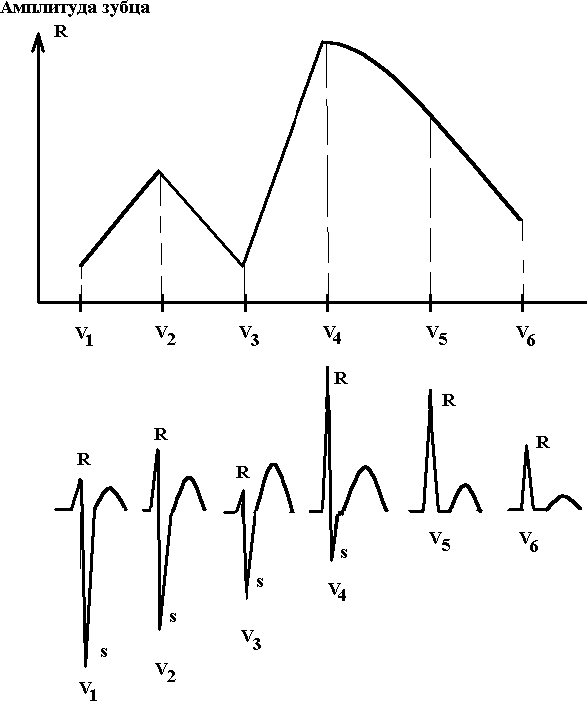 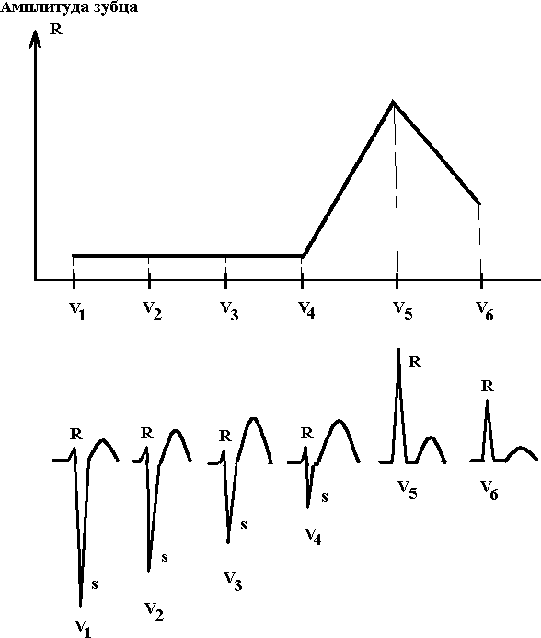 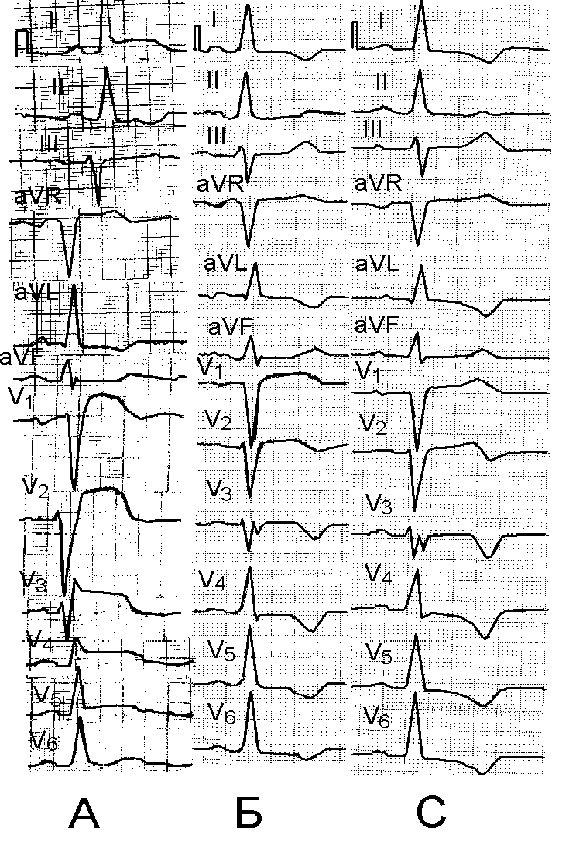 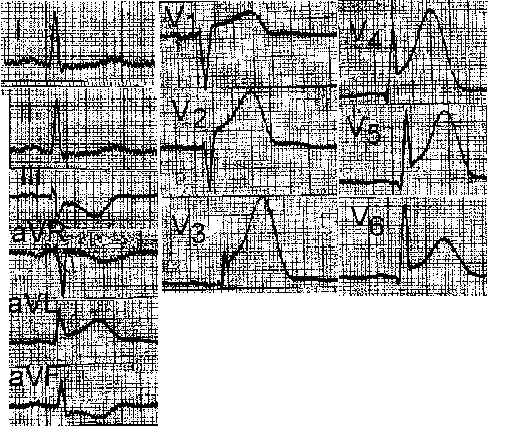 Рис. 3.4. Схема динамики зубца R в грудных отведениях при атипичной форме инфаркта миокарда (отсутствие нарастания зубца R с V1 по V4 ). Зубец “r” в грудных отведениях обычно составляет 1-2 мм. Отсутствие нарастания зубца R в грудных отведениях с V1 по V4-V5. 2 - Отсутствие нарастания зубца R в грудных отведениях с V1 по V4-V5 (cм. рис. 3.4.). На рисунках 3.5.-3.7. для иллюстрации представлены электрокардиограммы больных инфарктом миокарда с локализацией в области передней и задней стенки левого желудочка.  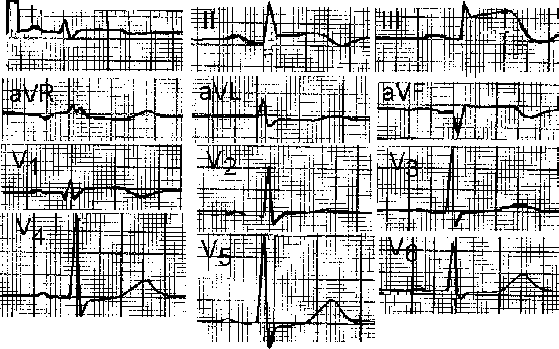  Рис. 3.6а. Ээектрокардиограмма при передне-перегородочном инфаркте миокарда с вовлечением верхушки и боковой стенки левого желудочка, острая стадия. 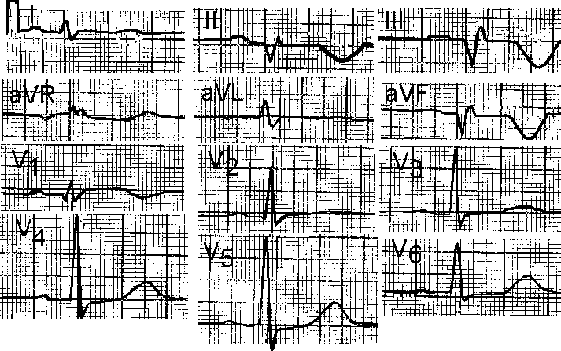 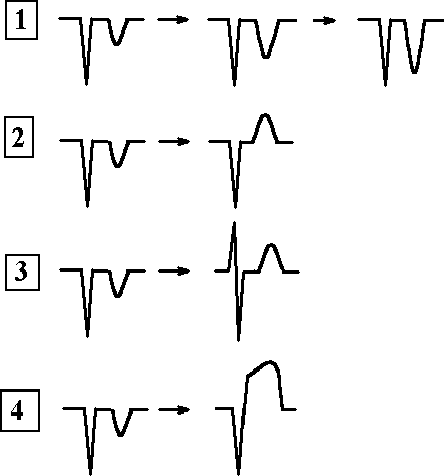 Рис. 3.6б. Электрокардиограмма при передне-перегородочном инфаркте миокарда с вовлечением верхушки и боковой стенки левого желудочка, подострая стадия. Рис. 3.7а. Электрокардиограмма при задне-диафрагмальном инфаркте миокарда левого желудочка, острая стадия. Рис. 3.7б. Электрокардиограмма при задне-диафрагмальном инфаркте миокарда левого желудочка, подострая стадия. Рис. 3.7в. Электрокардиограмма при задне-диафрагмальном инфаркте миокарда левого желудочка, стадия рудцевания. 3.2.1.4. Изменения электрокардиограммы при повторных инфарктах миокарда При повторных инфарктах миокарда могут наблюдаться следующие изменения (см. рис.3.8.): 1. Внезапная «положительная» динамика зубца «Т» в области рубцов: внезапное увеличение отрицательного зубца «Т» по сравнению с электрокардиограммой после предшествующего инфаркта миокарда. Эти изменения могут наблюдаться как в первые часы, так и в течение 10-17 дней от начала сильного ангинозного приступа. 2. Нормализация зубца «Т» в области рубцов, т.е. из отрицательного он становится положительным. 3. Внезапная полная нормализация электрокардиограммы, т.е. вместо рубцовых изменений у больного при развитии повторного инфаркта миокарда электрокардиограмма полностью нормализуется. 4. Старые «очаговые» изменения перекрываются «свежими» изменениями, характерными для острой фазы инфаркта миокарда. Например, после старого инфаркта миокарда наблюдался QS и инверсия зубца Т, а при повторном инфаркте в этой же зоне – QS с подъемом сегмента ST. 5. На электрокардиограмме наблюдаются изменения, характерные для первого инфаркта миокарда, а на противоположной стенке – рубцовые очаговые изменения. 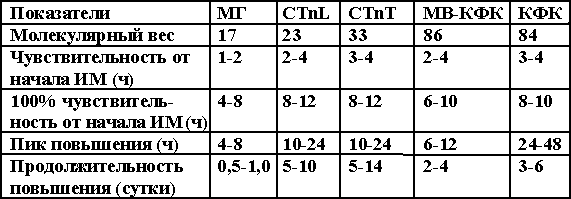 Рис. 3.8. Электрокардиограмма при повторных инфарктах миокарда. 1- Внезапная «положительная» динамика зубца «Т» в области рубцов: внезапное увеличение отрицательного зубца «Т» по сравнению с электрокардиограммой после предшествующего инфаркта миокарда. Эти изменения могут наблюдаться как в первые часы или сутки, так и в течение 10-17 дней от начала сильного ангинозного приступа; 2 - Нормализация зубца «Т» в области рубцов, т.е. из отрицательного он становится положительным; 3 - Внезапная полная нормализация электрокардиограммы, т.е. вместо рубцовых изменений у больного при развитии повторного инфаркта миокарда электрокардиограмма полностью нормализуется; 4 - Старые «очаговые» изменения перекрываются «свежими» изменениями, характерными для острой фазы инфаркта миокарда. Например, после старого инфаркта миокарда наблюдался QS и инверсия зубца Т, а при повторном инфаркте в этой же зоне – QS с подъемом сегмента ST. 3.2.2. Биохимическая диагностика инфаркта миокарда Идеальный плазменный маркер инфаркта миокарда, по критериям ВОЗ, должен быть представлен высокой концентрацией в сердечной мышце, появляться рано (в первые 1-2 ч от начала симптомов заболевания), отсутствовать в немиокардиальной ткани и плазме. Кроме того, обязательно должно быть стойкое соответствие между уровнем маркера в плазме и степенью поражения миокарда. Он должен регистрироваться в крови достаточно долго, а определение его быть простым, быстрым и дешевым. По критериям ВОЗ для диагностики инфаркта миокарда рекомендуется использовать миоглобиновую фракцию креатинкиназы, кардиоспецифичный тропонин Т и тропонин L, миоглобин и креатинкиназу, причем достоверным диагностическим критерием этого заболевания считается повышение активности ферментов сыворотки крови на 50% от верхней границы их нормальныхзначений. В настоящее время миоглобиновая фракция креатинкиназы является стандартным лабораторным тестом для диагностики инфаркта миокарда, хотя его значение не совсем совершенно. Его недостатки включают недостаточную специфичность, что может приводить к ложноположительным результатам, невозможность определить инфаркт миокарда с достаточной точностью в первые 6-8 часов от начала заболевания. Уровень миоглобиновой фракции креатинкиназы быстро понижается и не определяется в крови более чем через 72 часа от начала заболевания. Различают две изоформы миоглобиновой фракции креатинкиназы: «миоглобиновая фракция креатинкиназы-1» и «миоглобиновая фракция креатинкиназы-2». Абсолютный уровень миоглобиновой фракции креатинкиназы-2 больше, чем 2 ммоль/л, а соотношение миоглобиновой фракции креатинкиназы-2/миоглобиновой фракции креатинкиназы-1, составляющее в норме 1:5, повышает чувствительность и специфичность диагностики инфаркта миокарда в течение первых 6 ч в сравнении с суммарным определением миоглобиновой фракции креатинкиназы. Кардиоспецифичный тропонин «Т» и тропонин «L» являются новыми маркерами инфаркта миокарда. Повышение уровня тропонина «Т» и «L» происходит рано после повреждения миокарда и может сохраняться в крови в течение нескольких дней (до 10 дней для «L-формы» и 10-14 дней для «Т-формы»). Повышение уровеня тропонина «T» более, чем на 0,1 ng/mL указывает на повреждение миокарда и наблюдается у больных инфарктом миокарда уже в первые 0,5-1 ч с момента возникновения симптомов заболевания. Миоглобин, низкомолекулярный протеин, обнаруживаемый в сердечной и скелетной мышце, высвобождается более быстро, чем миоглобиновая фракция креатинкиназы, но быстрее выводится почками. Хотя повышение миоглобина может появиться через 2 часа после инфаркта, низкая его специфичность предполагает использование других добавочных тестов, таких как определение миоглобиновой фракции креатинкиназы или кардиоспецифичного тропонина (табл.3.1). Креатинкиназа, кардиоспецифический фермент, обнаруживаемый в сердечной и скелетной мышце, высвобождается в среднем через 4 ч с максимумом повышения в течение 24 – 48 ч от начала инфаркта миокарда. Измерение биохимических маркеров миокардиального некроза должно быть интерпритировано в контексте время-зависимых процессов при инфаркте миокарда. Некоторые маркеры, такие, как миоглобин и другие, могут быть диагностически значимы в ранние сроки развития инфаркта миокарда, а в более поздний период - кардиоспецифичный тропонин «Т» и «L», креатинкиназа. Большой трудностью для интерпретации исследований по биохимическим маркерам является отсутствие единого золотого стандарта. Критерии ВОЗ оказываются неадекватными для многих случаев инфаркта миокарда, особенно когда уровень креатинкиназы или ее миоглобиновой фракции повышается чуть выше нормальных значений. 3.2.3. Сцинтиграфия миокарда В настоящее время наиболее часто применяются сцинтиграфические методы исследования, основанные на накоплении радиоактивных изотопов в неизменененном миокарде (таллий-201 или Tl201) и в области повреждения или некроза (технеций-99-пирофосфат или Tc99–пирофосфат). Tl201 является аналогом иона калия и накапливается в интактном миокарде в зависимости, с одной стороны, от степени регионарной перфузии, с другой – от экстракции этого препарата через клеточную мембрану кардиомиоцитов вследствие активизации Na,K-АТФаз. Кроме того, используется сочетанное применение радионуклеоидов для негативной (Tl201) и позитивной (Tc99-пирофосфат) визуализации зоны инфаркта миокарда (Чазов Е.И., 1992). В нормальной сердечной мышце при введении Tc99-пирофосфата накапливается 6-8%, при развитии ишемии и повреждения – до 20%, а в случае некроза – более 20% от дозы вводимого препарата в сравнении с его распространением в окружающих тканях. В настоящее время, согласно данным рандомизированных исследований, клиническое применение радиоизотопного сканирования для выявления острого инфаркта миокарда должно быть ограничено только теми клиническими ситуациями, при которых оценка анамнеза, электрокардиографических изменений и лабораторных показателей оказывается невозможной или малоинформативной. Таблица 3.1. Плазменные маркеры острого инфаркта миокарда Примечание: ИМ – инфаркт миокарда, МГ – миоглобин, cTnT и cTnL - кардиоспецифичный тропонин «Т» и тропонин «L», МВ-КФК – миоглобиновая фракция креатинкиназы, КФК - креатинкиназа. У больных, поздно поступивших в стационар (более 24 часов, но менее 7 суток), без диагностических электрокардиографических изменений, а также у пациентов в ранний период после аортокоронарного шунтирования используется сцинтиграфия миокарда с использованием технеция-99-пирофосфат (препарат накапливается в зоне некроза сердечной мышцы), которая имеет высокую чувствительность (88%) и специфичность (77%) для диагностике острого инфаркта миокарда. Недавно предложенная инфаркт-поглощаемая сцинтиграфия с антимиозиновыми антителами была описана как альтернатива сцинтиграфии с пирофосфатом. Следует отметить, что серийные измерения накопления радиоизотопных препаратов с использованием либо Tl201, либо Tc99-пирофосфат с одновременной регистрацией перфузии миокарда выявляют очаговые поражения сердечной мышцы, однако при проведении этих исследований невозможно отличить зону ишемии от области повреждения и некроза. Тс99-пирофосфат является уникально подходящим для точного измерения размеров миокарда, находящегося в состоянии риска (повреждения с дальнейшим переходом в некроз). Из-за малого перераспределения фармакопрепарата, визуализация миокарда может быть отсроченной (в течение несколько часов) после его инъекции. Сцинтиграфия миокарда с Tl201 и Tc99–пирофосфат может быть использована для оценки размеров инфаркта. Недавно Tc99–пирофосфат был использован для этой цели при выполнении томографии (Rayn B., 1994). Размеры инфаркта, оцененные Tc99–пирофосфат, тесно коррелировали с другими показателями, отражающими размер инфаркта (r = 0,82-0,87), включая фракцию выброса левого желудочка, индекс сократимости локальной стенки, показателями кретинкиназы и размером дефекта по данным сцинтиграфии с Tl201. 3.2.4. Эхокардиографическая диагностика Признаками очаговых поражений миокарда при инфаркте являются: - пассивное парадоксальное движение межжелудочковой перегородки и снижение ее систолической экскурсии менее 0,3 см, - уменьшение амплитуды задней стенки левого желудочка менее 0,3 см, - акинезия или дискинезия одной из стенок левого желудочка. 3.3. Дифференциальная диагностика инфаркта миокарда Основной клинический синдром – внезапное появление болей в грудной клетке длительностью более 1 ч, не купирующихся приемом нитроглицерина. Дифференциальную диагностику следует проводить со спонтанным пневмотораксом, расслаивающейся аневризмой аорты, тромбоэмболией легочной артерии, острой межреберной невралгией, острой пневмонией, острым сухим перикардитом. r Спонтанный пневмоторакс. Спонтанный пневмоторакс может развиваться при туберкулезе легких, бронхоэктатической болезни, абсцессе, гангрене, раке легкого, буллезной эмфиземе, прорыве эхинококового пузыря и воздушной кисты легкого. Заболевание начинается остро с сильных болей в грудной клетке или за грудиной, удушья инспираторного характера, цианоза. При осмотре больной бледен, покрыт холодным потом, пульс частый, нитевидный. Пораженная половина грудной клетки отстает при дыхании, голосовое дрожание отсутствует. В области поражения перкуторно определяется тимпанический звук, при аускультации дыхание резко ослаблено или совсем не выслушивается. Симптоматика этого заболевания обусловлена спадением части или всего легкого (правого или левого), причем болевой синдром развивается из-за смещения органов средостения. Диагностика: а) клиническая картина заболевания - внезапное начало с болей в грудной клетке или за грудиной, удушье инспираторного характера, цианоз, перкуторно над легкими в области поражения - тимпанический звук, резко ослабленное или совсем не выслушиваемое дыхание; б) электрокардиографическое исследование – признаки острого легочного сердца: синдром SI-QIII, отклонение оси вправо, смещение переходной зоны к отведениям V5, V6; в) рентген грудной клетки – отсутствует легочный рисунок в области поражения, отчетливо выявляются контуры поджатого легкого, смещение тени сердца, крупных сосудов в противоположную сторону. Обычно отличить спонтанный пневмоторакс не трудно, если помнить о возможности наличия этого заболевания. Лечение – хирургическое. Устранение пневмоторакса проводят путем облитерации плевральной щели (с помощью введения в полость плевры стерильных раздражающих веществ, например, талька), резекция пораженной части легкого. r Расслаивающаяся аневризма аорты. Заболевание характеризуется внезапными, острыми и резкими болями в грудной клетке, длящихся более 1 ч, не купируемые нитроглицерином, сопровождающиеся снижением артериального давления, одышкой инспираторного характера, реже - обморочным состоянием. Боли при расслаивающейся аневризме чаще иррадиируют в спину. Расслаивающаяся аневризма аорты чаще наблюдается у лиц с высокой и стойкой артериальной гипертензией. Разрыв аорты в подавляющем большинстве случаев происходит дистальнее отхождения от нее левой подключичной артерии. Снижение артериального давления связано с воздействием на барорецепторы в результате надрыва эндотелиальных отделов аневризмы аорты. При этом заболевании наблюдается лейкоцитоз, повышение температуры и увеличение скорости оседания эритроцитов. На электрокардиограмме при расслаивающейся аневризме отмечаются снижение сегмента S-Т и высокие остроконечные зубцы Т, указывающие на субэндокардиальную ишемию. Отсутствие электрокардиографической картины, типичной для инфаркта миокарда в течение нескольких дней после тяжелого приступа болей в грудной клетке, сопровождающихся повышением температуры и лейкоцитозом, отсутствие увеличения ферментов сыворотки крови или незначительное их активности (не более, чем на 10-20% от верхней границы нормы), - все это указывает в пользу расслаивающей аневризмы аорты, а не инфаркта миокарда (см. ниже). Лечение расслаивающей аневризмы аорты хирургическое: протезирование аорты. r Тромбоэмболия легочной артерии. Заболевание развивается остро, причем клиническая картина зависит от калибра легочной артерии, окклюзированной тромбом. При окклюзии крупной ветви легочной артерии, например, общего ствола, смерть наступает практически мгновенно или в течение нескольких минут. При обтурации ветвей легочной артерии среднего калибра развиваются: - сильные боли в грудной клетке, постоянного характера, длительностью более 1 ч, не купирующиеся нитратами, - удушье инспираторного характера, - цианоз, - через несколько часов или дней от начала клинической картины заболевания - кашель с прожилками крови. При обследовании отмечается притупление перкуторного звука на стороне поражения, ослабленное дыхание, причем в первые часы заболевания отмечаются вначале сухие рассеянные, реже свистящие, а затем влажные звучные мелкопузырчатые хрипы. Изменение электрокардиограммы при эмболии легочной артерии При тромбоэмболии легочной артерии возникает острая перегрузка правых отделов сердца, которая в большинстве случаев (в 40-60%) находит отражение на электрокардиограмме. Электрокардиографические признаки тромбоэмболии легочной артерии: 1. Синдром SI – QIII. В III, avF отведениях определяется разной степени выраженности зубец q(Q), не превышающий 0,03 сек и глубиной до 25% зубца R комплекса QRS в этих отведениях. Иногда в III, aVF отведениях отмечается подъем сегмента S-T в виде монофазной кривой, когда сегмент S-T сливается вместе с положительным зубцом Т. Формирование зубца q в III, aVF отведениях сопровождается появлением зубца S в I, aVL отведениях, причем сегмент S-T может располагаться ниже изолинии; 2. Отсутствует зубец Q во II стандартном отведении. 3. Отклонение оси вправо, смещение переходной зоны к отведениям V5, V6. 4. Признаки перегрузки правого предсердия – электрокардиографические признаки, характерные для «P-pulmonale»; Аналогичные изменения электрокардиограммы наблюдаются при развитии инфаркта миокарда в области задней стенки левого желудочка. Дифференциально-диагностические электрокардиографические признаки отличия тромбоэмболии легочной артерии от инфаркта миокарда в области задней стенки левого желудочка: 1. При тромбоэмболии легочной артерии отсутствует патологический зубец Q во II отведении, который должен быть при инфаркте миокарда; 2. При тромбоэмболии легочной артерии в III, avF отведениях определяется разной степени выраженности зубец q(Q), не превышающий по продолжительности 0,03 сек и по глубине 25% зубца R в этих отведениях; 3. Наблюдается выраженный зубец S в I, aVL отведениях, который не характерен для неосложненного инфаркта миокарда в области задней стенки левого желудочка; 4. При тромбоэмболии легочной артерии появляются электрокардиографические признаки, характерные для остро возникшей перегрузки правых отделов сердца: 4.1. Отклонение электрической оси вправо; 4.2. Признаки перегрузки правого предсердия – электрокардиографические критерии, характерные для «P-pulmonale»; 4.3. Увеличивается амплитуда зубца R во II, III и aVF отведениях; 4.4. Отмечается электрическая ось сердца типа синдрома SI > SII > SIII ; 4.5. Наблюдаются признаки гипертрофии или перегрузки правого желудочка в грудных отведениях; 4.6. Увеличение амплитуды или появление высокого зубца R в правых грудных отведениях V1, V2, причем ЭКГ в этих отведениях может иметь вид R, Rs, qR; 4.7. Появление зубца S в отведениях V5, V6; 4.8. Развитие признаков полной или неполной блокады правой ножки пучка Гиса; 4.9. Увеличение времени внутреннего отклонения в отведениях V1, V2 более 0,03 сек; 4.10. Регистрация позднего зубца R в отведении aVR; 4.11. Смещение переходной зоны вправо – равенство соотношения R и S в отведениях V5 или V6; 4.12. Появление отрицательного зубца «Т» в отведениях V1-V3; 4.13. Увеличение амплитуды зубца «Р» в отведениях V1-V5. Следует отметить, что помимо тромбоэмболии легочной артерии, к развитию аналогичной электрокардиографической картины может приводить острая дыхательная недостаточность, спонтанный пневмоторакс, массивные пневмонии. При рентгенографии грудной клетки определяется увеличение правого желудочка сердца, выбухание конуса и дуги легочной артерии, повышение прозрачности легочной ткани в зоне разветления затромбированной легочной артерии, симптом «ампутации» корня с его расширением проксимальнее тромбоза. При развитии инфаркта легких и инфаркт-пневмонии рентгенологически определяется характерный участок затемнения легочной ткани в виде треугольника, обращенного основанием к плевре или так называемая «клиновидная тень» в области поражения. Критерии диагностики тромбоэмболии легочной артерии: а) клиническая картина заболевания - внезапное начало с болей в грудной клетке или за грудиной постоянного характера, длительностью более 1 ч, не купирующихся нитроглицерином, удушье инспираторного характера, цианоз, кашель с прожилками крови, тимпанический звук, притупление перкуторного звука, ослабленное дыхание, влажные звучные мелкопузырчатые хрипы в области поражения; б) электрокардиографические признаки острого легочного сердца: SI, QIII, отклонение оси вправо, смещение переходной зоны к отведениям V5, V6, признаки перегрузки правого предсердия, характерные для «P-pulmonale»; в) рентген грудной клетки – увеличение правого желудочка сердца, выбухание конуса и дуги легочной артерии, повышение прозрачности легочной ткани в зоне разветвления затромбированной легочной артерии, симптом «ампутации» корня с его расширением проксимальнее тромбоза, «клинивидная тень» в области поражения. При окклюзии ветвей легочной артерии мелкого калибра в большинстве случаев болевой синдром отсутствует, а заболевание проявляется одышкой инспираторного характера и (или) кровохарканьем. В большинстве случаев наблюдаются электрокардиографические признаки перегрузки правых отделов сердца или острого легочного сердца (см. выше), причем в среднем в 80% случаев при рентгенологическом исследовании можно не выявить патологических изменений. С целью уточнения диагноза в ряде случаев прибегают к ангиографическому исследованию. r Остро возникшая межреберная невралгия. Боли развиваются внезапно, чаще в левой половине грудной клетки, усиливаются при дыхании, движении, изменении положения тела. Отмечается выраженная болезненность при пальпации паравертебральной области, по ходу межреберных промежутков. Результаты физикального, электрокардиографического исследования, данные клинического и биохимического исследованийкрови не выходят за пределы нормы. r Острая пневмония. Острая пневмония, сопровождающаяся вовлечением плевры и сухим плевритом, может быть причиной ошибочной диагностики инфаркта миокарда. Это заболевание в большинстве случаев начинается остро с болей в левой половине грудной клетки, длящихся более 1 ч, усиливающихся при дыхании, кашле, уменьшающихся в покое (нитроглицерином не купируются). Боли в грудной клетке при этом заболевании сопровождаются повышением температуры, кашлем с мокротой, может наблюдаться одышка инспираторного характера, цианоз, тахикардия. При физикальном обследовании отмечается укорочение перкуторного звука в области поражения, звучные влажные хрипы и шум трения плевры над этим участком, указывающие на наличие инфильтративного фокуса, подтверждаемого результатами рентгенологического исследования. Кроме того, отмечается лейкоцитоз с палочкоядерным сдвигом влево, увеличение скорости оседания эритроцитов, активность ферментов сыворотки крови не выходят за пределы нормы. На электрокардиограмме очаговые изменения не выявляются. Появление и усиление болей в левой половине грудной клетки при дыхании, кашле, острое начало заболевания, сопровождающееся лихорадкой, кашлем с мокротой, данные физикального обследования, указывающие на наличие инфильтративного фокуса, подтвержденного результатами рентгенологического исследования, при отсутствии очаговых изменений на электрокардиограмме, лейкоцитоз, увеличение скорости оседания эритроцитов - совокупность этих симптомов является достаточным основанием для диагностики острой пневмонии. r Острый перикардит. Заболевание начинается остро с болей в левой половине грудной клетки, возникающих в покое и усиливающиеся при движении, дыхании, изменении положения тела больного: он старается принять сидячее положение, при котором боль беспокоит меньше. Боль в грудной клетке при перикардите появляется одновременно с лихорадкой, лейкоцитозом и увеличением скорости оседания эритроцитов, реже повышением активности ферментов крови, не превышающих 50% от верхней границы нормы. При физикальном обследовании выслушивается громкий и разлитой шум трения перикарда. На электрокардиограмме при остром перикардите наблюдается подъем сегмента S-Т во всех трех стандартных отведениях, без патологического зубца Q, характерного для инфаркта миокарда. При эхокардиографическом исследовании отмечается однонаправленное движение перикарда и миокарда в момент систолы. Сухой перикардит обычно развивается как осложнение ревматизма, туберкулеза, уремии, пневмонии, иногда острых инфекций дыхательных путей. Следует отметить, что при выпотном перикардите боли в грудной клетке отсутствуют, а симптоматика проявляется прогрессирующей недостаточностью кровообращения. Критерии диагностики перикардита - боли в левой половине грудной клетки, шум трения перикарда, повышение температуры, лейкоцитоз, повышение скорости оседания эритроцитов, подъем сегмента S-Т во всех трех стандартных отведениях, без патологического зубца Q, однонаправленное движение перикарда и миокарда в момент систолы. По совокупности этих признаков диагностируют сухой перикардит. r Диагностика инфаркта миокарда Анамнез и клиническая картина инфаркта миокарда считается типичной при: - наличие тяжелого и продолжительного приступа загрудинных болей длящихся более 1 ч и не купирующихся нитратами. На догоспитальном этапе инфаркт миокарда диагностируется при исключении всех остальных заболеваний, которые могут сопровождаться сходным болевым синдромом (см. раздел дифференциальная диагностика инфаркта миокарда), - при внезапном появлении сердечной астмы, в том числе впервые в жизни, на фоне предшествующего относительного благополучия или предшествующей стенокардии. В остальных случаях (гастралгическая и атипичные формы этого заболевания) врачу необходимо для диагностики инфаркта миокарда проанализировать электрокардиограмму, оценить клинический анализ крови и активность кардиоспецефических ферментов сыворотки крови (креатинкиназы, миоглобиновой фрации креатинкиназы, тропонина «Т» и «L», миоглобина и т.д.), а, при необходимости, в том числе, если вышеуказанные исследования малоинформативны, провести эхокардиографию и сцинтиграфию миокарда с технецием-99-пирфотех. r Диагностика инфаркта миокарда в остром и начале подострого периода Диагноз крупноочагового инфаркта миокарда (Q(+) устанавливается при наличии типичной клиники заболевания и патогномоничных изменений электрокардиограммы (наличия патологическогозубца Q или QS). При атипической клинической картине начала этого заболевания инфаркт диагносцируется на основании выявления патологического зубца Q(QS) на электрокардиограмме в сочетании с гиперферментемией, акинезией (дискинезией) или гипокинезией, со снижением систолической экскурсии миокарда левого желудочка менее чем на 0,3 см при эхокардиографическом исследовании или увеличении накопления миокардом технеция-99-пирфотех более, чем на 20% от введенной дозы препарата. Диагноз мелкоочагового Q(-) инфаркта миокарда устанавливается при типичных или нетипичных клинических формах заболевания при развивающихся в динамике подъема или депрессии сегмента S-T и (или) постоянным углублением зубца Т при наличии типичных изменений активности ферментов сыворотки крови или в сочетании с пассивным парадоксальным движением межжелудочковой перегородки, снижением ее систолической экскурсии менее 0,3 см или уменьшением амплитуды движения задней стенки левого желудочка менее чем на 0,3 см. r Диагностика инфаркта миокарда в подостром и периоде рубцевания Диагноз крупноочагового инфаркта миокарда или Q(+) устанавливается при наличии типичной или атипичной клиники заболевания и патогномоничных изменений электрокардиограммы (патологический зубец Q(QS) в сочетании с акинезией, дискинезией или гипокинезией (амплитуда сокращения менее 0,3 см) стенок левого желудочка при эхокардиографическом исследовании. Диагноз мелкоочагового Q(-) инфаркта миокарда устанавливается при типичных или нетипичных клинических формах заболевания при развивающихся в динамике постоянного углубления зубца Т в сочетании с гипокинезией (амплитуда сокращения менее 0,3 см) стенок левого желудочка. r Течение инфаркта миокарда В большинстве случаев выделяют следующие периоды течения инфаркта миокарда: прединфактное состояние, остро-острейший период – с первых часов до конца 12 часов, острый период – с первых 12 часов по 7-10 день, подострый период – с 7-10 по 20-25 день и период выздоровления или рубцевания, длящийся 3-5 и более месяцев от начала заболевания. Выделяют два типа течения: неосложненное и осложненное течение инфаркта миокарда. 3.4. Неосложненный инфаркт миокарда Под неосложненным течением инфаркта миокарда понимают отсутствие клинически значимых осложнений в течение 1-2 месяцев от начала заболевания (госпитальный и санаторный периоды). Чаще всего осложнения наблюдаются в первые 7-14 дней от начала заболевания (период формирования некроза и рубца сердечной мышцы). При неосложненном инфаркте миокарда в остро-острейший период заболевания может наблюдаться синусовая брадикардия, тахикардия, единичная (до 1 в час) предсердная и желудочковая экстрасистолия. Возможно также появление кратковременной гипотонии рефлекторного происхождения (в момент развития болевого синдрома). Эти нарушения кратковременны, быстро устраняются при проведении адекватной терапии и не оказывают существенного влияния на течение и прогноз неосложненного инфаркта миокарда. 3.4.1. Резорбционно-некротический синдром при инфаркте миокарда В остром и подостром периоде инфаркта миокарда исчезает болевой синдром, причем сохранение ангинозного синдрома связано, как правило, с выраженной ишемией периинфарктной зоны или с присоединившимся эпипристеночным перикардитом. Перкуссия – границы сердца расширены влево, аускультация – ослабление I тона, короткий (мягкий) систолический шум на верхушке, обусловленный относительной недостаточностью митрального клапана. В подостром периоде и стадии рубцевания исчезает или уменьшается систолический шум на верхушке, ослабление I тона, а в остальном при исследовании сердечно-сосудистой системы отклонения практически не выявляются. Лабораторные данные в остром и подостром периоде отражают резорбционно-некротический синдром, развивающийся вследствие резорбции некротических масс, асептического воспаления и выхода ферментов из поврежденных кардиомиоцитов. Показатели резорбционно-некротического синдрома при инфаркте миокарда представлены в таблице 3.2. Таблица 3.2. Показатели резорбционно-некротического синдрома при инфаркте миокарда __________________________________________________________________________________ Показатели Начало Максимум Длительность Нормальные повышения повышения сохранения значения изменений __________________________________________________________________________________ Температура 1-2 сут. 2-4 сут 7-10 сут до 37о __________________________________________________________________________________ Лейкоцитоз, х109/л 1-2 сут. 3-7 сут 3-7 дней 4-8 __________________________________________________________________________________ СОЭ, мм/ч 2-3 сут. 8-12 сут. 3-4 недели Мужчины 1-10 Женщины 2-15 __________________________________________________________________________________ СРБ 1-2 сут. 13-18 дней 28-56 сут отсутствует __________________________________________________________________________________ Глюкоза, ммоль/л 2-3 ч 1-2 сут. 7-10 дней 3,3-5,5 __________________________________________________________________________________ Миоглобин, пкг/л 2 ч 6-10 ч 28-32 ч 5,0-8,5 __________________________________________________________________________________ МВ-КФК, % 2-4 ч 18-24 ч 5-8 дней от 0 до 6 __________________________________________________________________________________ КФК, ммоль Р/ч.л 4 ч 24-48 ч 5-6 дней до 1,2 __________________________________________________________________________________ ЛДГ, ммоль/ч.л 8 ч 2-3 сут 10-12 дней от 0,8 до 4,0 __________________________________________________________________________________ АсАТ, ммоль/ч.л 8-12 ч 2-3 сут 7-8 дней от 0,1 до 0,4 __________________________________________________________________________________ АлАТ, ммоль/ч.л 8-12 ч 72 ч 5-6 дней от 0,1 до 0,68 __________________________________________________________________________________ Продолжение таблицы 3.2. __________________________________________________________________________________ Показатели Начало Максимум Длительность Нормальные повышения повышения сохранения значения изменений __________________________________________________________________________________ Альдолаза, мкмоль/ч.л 10-20 ч 48 ч 7-8 дней от 0,2 до 1,2 __________________________________________________________________________________ Сиаловые кислоты, 24 ч 5-10 сут 1-2 мес от 0,13 до 0,2 ед.опт. плотн. __________________________________________________________________________________ Фибриноген, г/л 48 ч 3-5 сут 1-2 нед от 2 до 4 __________________________________________________________________________________ Серомукоид, г/л 1-2 сут. 10 –14 сут 22-26 дней 22-28 __________________________________________________________________________________ -2-глобулины, % 48 ч 3-5 день 20-21 день 4-8 __________________________________________________________________________________ ДНК, г/л 1-2 ч 3-5 день 10-14 дней 0,12-0,20 __________________________________________________________________________________ Гаптоглобин, г/л 1-2 сут. 3-4 день 10-14 дней 0,20-0,40 __________________________________________________________________________________ Примечание: СОЭ - скорость оседания эритроцитов, СРБ - С-реактивный белок, МВ-КФК - миоглобиновая фракция креатинкиназы, КФК - креатинкиназа, ЛДГ - лактатдегидрогеназа, АсАТ - аспартатаминотронсфеназа, АлАТ - аланиламинотрансфераза, ДНК - дезоксирибонуклеиновая кислота. 3.4.2. Лечение неосложненного инфаркта миокарда Лечение неосложненного инфаркта миокарда представлено в таблице 3.3. Таблица 3.3. Лечение неосложненного инфаркта миокарда ____________________________________________________________________________________ Дни <6 ч 6-24ч 1-3 с 3-7 с 7-14 с 14-21 с 21-35 с > 35 c наблюдения ____________________________________________________________________________________ Купирование анги- нозного синдрома ____________________________________________________________________________________ Оксигенотерапия + - - - - - - - ____________________________________________________________________________________ Тромболитики + - - - - - - - ____________________________________________________________________________________ Внутривенно нитроглицерин + + + + - - - - 0,1%-1,0 мл на 1,5 –2,0 g KCL и 2,5-3,0 g MgSO4 в разведении на 200,0 физиологического раствора ____________________________________________________________________________________ Аспирин + + + + + + + + ____________________________________________________________________________________ Гепарин + + + + - - - - ____________________________________________________________________________________ Продолжение таблицы 3.3. ____________________________________________________________________________________ Дни <6 ч 6-24ч 1-3 с 3-7 с 7-14 с 14-21 с 21-35 с > 35 c наблюдения ____________________________________________________________________________________ Ингибиторы АПФ + + + + + + + + ____________________________________________________________________________________ Нитраты пролонги- рованного действия + + + + + + + + ____________________________________________________________________________________ -адреноблокаторы или антагонисты кальция ____________________________________________________________________________________ Примечание: «+» - обязательное проведение терапии, «-» терапия не проводится или противопоказана, «» - показана, но только по строгим показаниям к конкретному виду лечения. r Комментарии к лечению больных неосложненным инфарктом миокардаКогда больной с подозреваемым инфарктом миокарда поступает в отделение неотложной терапии, первоначальная оценка и лечебные мероприятия должны проводиться немедленно, так как реперфузионная терапия эффективна только в первые часы развития заболевания. В идеале начальная оценка состояния больного должна быть завершена в течение 10 минут после его прибытия в отделение и до начала лечения должно пройти не более 20 минут. На отделениибольному с подозреваемым инфарктом миокарда должны провести следующие мероприятия: 1) кислород через носовой катетер, 2) сублингвально нитроглицерин (если артериальное давление не менее 90 мм.рт.ст., а частота сердечных сокращений не более 100 и не менее 50 ударов в 1 мин.), 3) адекватную анальгезию (таламонал, морфин-сульфат или меперидин, см. ниже), 4) аспирин от 160 до 325 мг per os и 5) регистрацию электрокардиограммы в 12 отведениях. Элевация сегмента ST 1 мм в одном или нескольких отведениях, является достоверным признаком тромботической окклюзии коронарной артерии. Этим пациентам показано восстановление коронарного кровотока с помощью проведения тромболитической терапии или с помощью коронарной ангиопластики. Если имеются симптомы инфаркта миокарда и впервые выявленная полная блокада левой ножки пучка Гиса, ведение больных должно быть как с элевацией сегмента ST. И наоборот, больным без элевации ST на электрокардиограмме не должна проводиться тромболитическая терапия, так как ее положительный эффект в этой ситуации является неопределенным (Rayn B., 1996, Грацианский Н.А., 2000, Голиков А.П. и соавт., 2000). Оксигенотерапия Повсеместно стало универсальной практикой назначать кислород, обычно через носовой катетер, всем больным с возможным инфарктом миокарда или ишемическим дискомфортом в грудной клетке, хотя не известно, влияет ли эта терапия на повреждение миокарда или на снижение заболеваемости и смертности. Экспериментальные данные показывают, что вдыхаемый кислород может ограничивать ишемическое повреждение миокарда, причем у больных инфарктом миокарда назначение кислорода уменьшает элевацию сегмента ST электрокардиограммы (Rayn B. еt al., 1996). Рациональное использование кислорода основано на том положении, что даже при неосложненном инфаркте миокарда, некоторые больные изначально испытывают гипоксемию из-за снижения вентеляционно-перфузионного отношения и задержки воды в легких. У больных с выраженной сердечной недостаточностью, застоем в легких или механическими осложнениями инфаркта миокарда значительная гипоксемия может не коррегироваться назначением кислорода. Для больных без осложнений нужно отметить, что излишнее назначение кислорода может привести к системной вазоконстрикции. Кроме того, повышенный ток кислорода может быть вреден для больных с обструктивными заболеваниями легких. С другой стороны, поскольку назначение нитроглицерина приводит к дилатации сосудистого русла легких и повышает вентиляционно-перфузионные нарушения, выглядит разумным назначение дополнительного кислорода, по крайней мере, в течение первых часов для больных с вероятным или развивающимся инфарктом миокарда. Применение кислорода через 2-3 часа от начала заболевания не показано (Rayn B. еt al., 1996). r Наблюдение за больными инфарктом миокардаРанние мероприятия заключаются в наблюдении за больными инфарктом миокарда, профилактике возможных осложнений и их лечении, если они появились. Компьютерные алгоритмы обеспечивают помощь медицинскому персоналу в определении и интерпритации нарушений ритма. Однако, выбор отведений и техники наложения электродов (подготовка кожи и использование геля) зависит от качества обучения персонала. Артериальное давление должно измеряться все больным вне зависимости от тяжести состояния пациента. Инвазивный артериальный мониторинг предпочтителен у больных с гипотонией, а остальным пациентам - неинвазивный контроль артериального давления. Неинвазивное определение артериального давления с использованием автоматических устройств, которые измеряют давление с запрограммированными интервалами, является не всегда точным (из-за неподходящего размера манжетки, контрактуры мышц и т.п.), а периферичекая вазоконстрикция может привести к ошибочно низкому результату измерения. Более того, многие больные жалуются, что это устройство раздражает их и нарушает покой. Пульсовая оксиметрия должна проводиться всем больным инфарктом миокарда для продолжительного наблюдения за насыщением крови кислородом, обеспечивающего раннее предотвращение гипоксемии. r Уровень активности больных инфарктом миокардаПрофилактика осложнений инфаркта миокарда включает различные меры, направленные на снижение повреждения миокарда путем поддержания баланса между доставкой кислорода и его потребностью. Ограничение ранней физической нагрузки и уменьшение симпатической стимуляции являются методами ограничения потребности миокарда в кислороде, которая, в свою очередь, может увеличить зону повреждения миокарда в условиях сниженного коронарного кровотока. В 60-80 гг. продолжительность постельного режима у больных инфарктом миокарда составляла несколько дней. Однако в последние годы стало известно, что долгая неподвижность вредна, так как физическая детренированность появляется через 6 часов после пребывания в положении лежа, а в первые сутки строго постельного режима уменьшается преднагрузка из-за потери объема плазмы. Изменение наполнения желудочков активизирует компенсаторные механизмы, которые направлены наувеличение давление и объема. Сердечно-сосудистая дисфункция после постельного режима может быть более функциональной при небольших движениях, чем детренированность после физической пассивности. Короткий период (примерно 12 часов) строгого постельного режима показан большинству пациентов в остром периоде инфаркта миокарда с последующим разрешением садиться и пользоваться прикроватным столиком. Продолжительный постельный режим не является необходимым и для больных, которые гемодинамически нестабильны. Низкий уровень активности, такой, как туалет, умывание с посторонней помощью, легкие передвижения в постели, должен использоваться для предотвращения физиологической детринерованности. «Коронарная предосторожность», объявленная для ограничения физических нагрузок и стимуляции симпатической нервной системы, была стандартом ведения больных инфарктом миокарда только в 60-70-х годах. Холодные и горячие блюда были ограничены так же, как стимулирующие напитки, ректальные измерения температуры и регулярный осмотр per rectum, энергичные растирания спины, помощь при приеме пищи были общеприняты и насильный покой был нормой. Недавние рандомизированные обзоры показали, что «коронарная предосторожность» все еще практикуется во многих странах, несмотря на тот факт, что многоцентровые исследования не поддерживают ее использование. Избегание натуживания является универсальной мерой предосторожности. Форсированный выдох при закрытой глотке вызывает внезапные и интенсивные изменения систолического артериального давления и частоты сердечных сокращений. Изменение нагрузки на левый желудочек в течение пробы Вальсальвы могут влиять на регионарную миокардиальную реполяризацию и способствовать развитию желудочковых аритмий. У больных молодого и среднего возраста ослабляется автономный сердечный ответ. Поэтому следует избегать проведение приема Вальсальвы, особенно у лиц моложе 45 лет. Рекомендуется использование «мягких» слабительных средств для предотвращения запоров, причем прикроватный стульчак обычно предпочтительней судна, в том числе и для большинства гемодинамически нестабильных пациентов. Следует отметить, что артериальное давление и частота сердечных сокращений повышаются после приема кофе, однако клинически незначимое изменение этих показателей наблюдаются при приеме до 400 мг кофеина (от 2 до 4 чашек кофе, например Nescafe, в зависимости от крепости и способа приготовления). У людей, принимающих регулярно кофеин-содержащие напитки, развивается толерантность после 1-4 дней в зависимости от ранее используемой дозы этих напитков. При полном отказе от кофе появляются головные боли и повышается частота сердечного ритма. Любители этого напитка могут сохранить прием нескольких (3-4 в сутки) чашек кофе, даже в палате интенсивной терапии. |
