Глик Молекулярная биотехнология. Глик Б., Пастернак Дж. Молекулярная биотехнология. Принципы и применение. Пер с англ. М. Мир, 2002. 589 с
 Скачать 9.74 Mb. Скачать 9.74 Mb.
|
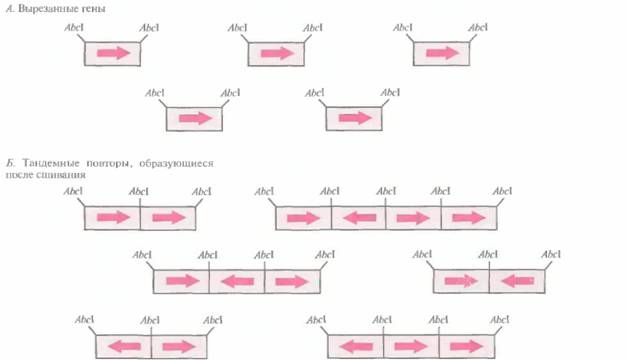
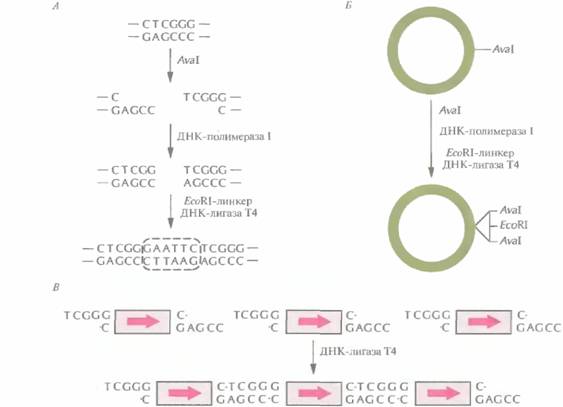
Однонаправленное тандемное расположение геновОбычно уровень генной экспрессии пропорционален числу копий транскрибируемого гена в хозяйских клетках. Отсюда следует, что с увеличением числа копий плазмиды должно увеличиваться и количество продукта встроенного в эту плазмиду гена. Однако помимо клонируемого гена плазмида содержит и другие транскрибируемые последовательности, например гены устойчивости к антибиотикам, и по мере увеличения ее копийности энергетические ресурсы клетки будут во все большей степени направляться на образование белков, кодируемых плазмидой, и метаболическая активность хозяйской клетки упадет. Выходом из этой ситуации могло бы стать встраивание в малокопийную плазмиду нескольких копий интересующего исследователя гена. Однако при этом возникает одна техническая проблема — расположение генов в такой ориентации, чтобы все они могли правильно транскрибироваться и транслироваться. Простое сшивание «конец-в-конец» приводит к случайной ориентации генов, так что одни из них экспрессируются, а другие, находящиеся в противоположной ориентации, — нет (рис. 6.11). Чтобы решить эту проблему можно использовать рестрицирующий фермент AvaI, который узнает последовательность CTCGGG и разрезает ДНК с 5'-конца от остатка Т. Процедура состоит в следующем. Плазмиду, содержащую эту последовательность, разрезают с помощью AvaI и. используя ДНК-полимеразу I, достраивают липкие концы. Затем к обоим ее тупым концам пристраивают EcoRI-линкер (GAATTC), вновь замыкая кольцо. Получившаяся плазмида содержит сегмент ДНК с двумя AvaI-сайтами, фланкирующими EcoRI-сайт и перекрывающимися с ним (рис. 6.12, А и Б), т. е. последовательность CTCGGG AATTCTCGGG (здесь подчеркнутые основания — сайты узнавания для AvaI). Нужный ген вместе с трансляционными старт-и стоп-сигналами встраивают в EсоRI-сайт и затем вырезают из плазмиды с помощью AvaI (рис. 6.12, В). Такие фрагменты имеют неидентичные липкие концы, и поэтому при последующем сшивании соединяются в одной ориентации. Подобный набор однонаправленных тандемных копий гена может быть встроен в экспрессирую-щий вектор. При этом тандемная последовательность может находиться в двух ориентациях относительно промотора, так что ее экспрессия будет происходить только в 50% случаев. 118 ГЛАВА 6
Другой подход основан на использовании синтетических ориентированных адаптеров -коротких олигодезоксинуклеотидов, присоединенных к концам линеаризованной плазмидной ДНК и к концам фрагментов ДНК с клонируемым геном. При лигировании эти фрагменты располагаются только в одной ориентации. Описанная процедура технически значительно более проста, чем та, в которой используется ре-стрицирующая эндонуклеаза AvaI; кроме того, она не требует, чтобы в гене-мишени отсутствовали AvaI- и EcoRI-сайты. Уже показано экспериментально, что уровень экспрессии генов интерферона действительно увеличивается пропорционально числу тандемных копий гена, по крайней мере до четырех копий на плазмиду. Однако тандемные повторы иногда оказываются нестабильными и со временем некоторые из них или даже все утрачиваются плазмидой. Трансляционные экспрессирующие векторыНаличие сильного регулируемого промотора -это очень важное, но недостаточное условие максимизации количества продукта клонированного гена. Большую роль играют также эффективность трансляции и стабильность самого продукта. В прокариотических клетках разные мРНК не всегда транслируются с одинаковой эффективностью. Различие может составить несколько сотен раз, и в результате в клетке будут присутствовать сотни или даже тысячи копий одних белковых молекул и лишь несколько копий других. Различия в трансляции связаны — по крайней мере частично — со свойствами имеющегося в транскрибированной РНК сигнала инициации трансляции, называемого сайтом связывания рибосомы. Сайт связывания рибосомы — это Оптимизация экспрессии генов, клонированных в прокариотических системах 119
|