ВКР Сотина. Исследование фазовых эффектов и методов разделения азеотропных смесей, утверждена приказом ргу имени С. А. Есенина от 20 г
 Скачать 1.21 Mb. Скачать 1.21 Mb.
|
1.3. Диаграммы фазового равновесия азеотропных системСостояние двухфазной бинарной системы жидкость пар определяется двумя независимыми переменными. Парожидкостное равновесие (ПЖР) обычно изучают при изобарических (при постоянном давлении) или изотермических условиях (постоянной температуре). На рис. 7-9 схематически представлены основные типы диаграмм равновесия жидкость пар бинарных систем. 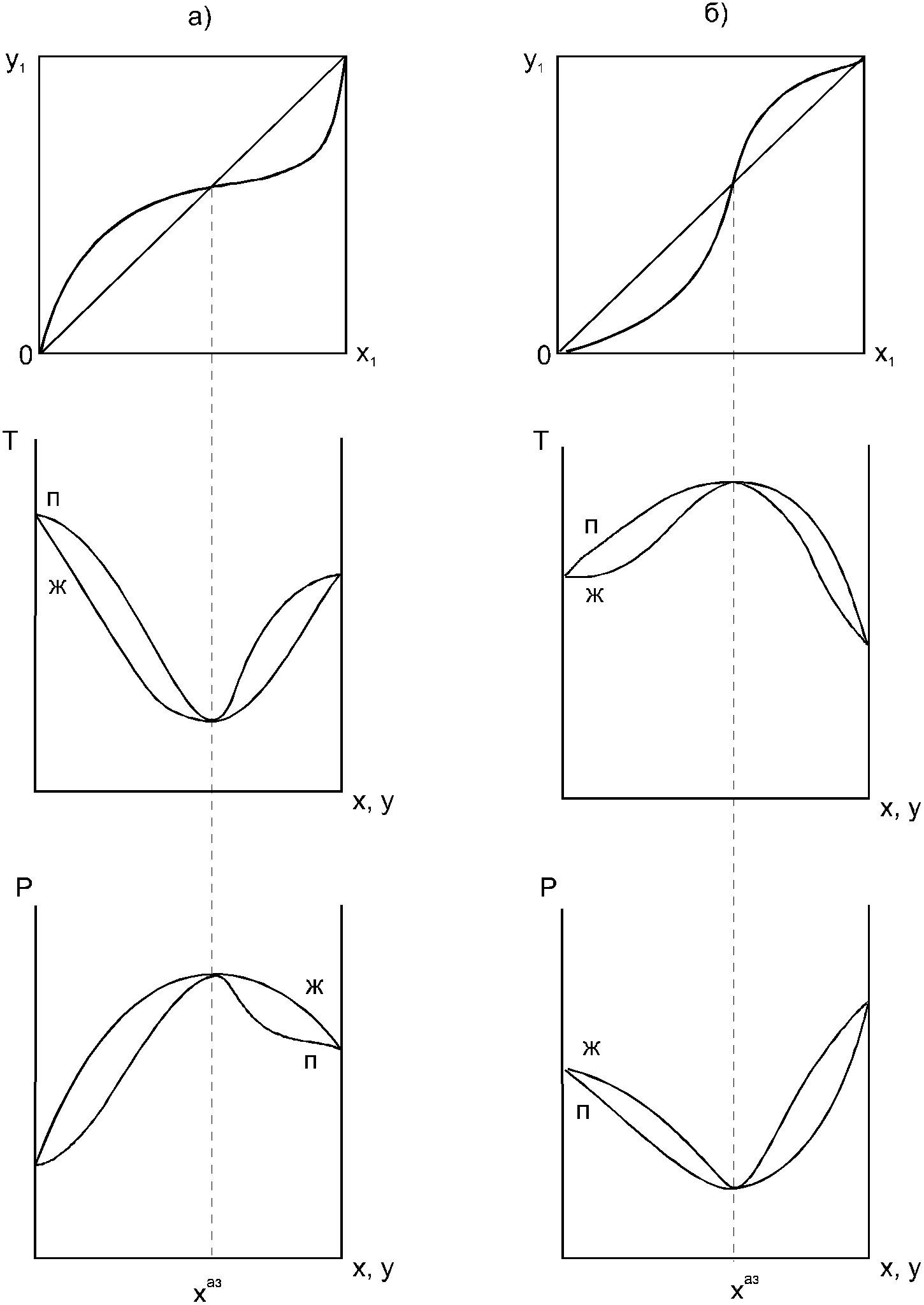 Рис. 7. Диаграммы фазового равновесия жидкостьпар гомогенных азеотропных систем: а - положительный азеотроп, б - отрицательный азеотроп. При изучении гомогенных систем (рис. 7) в качестве параметров состояния выбирают температуру, давление и концентрацию одного из компонентов (обычно компонент 1 имеет меньшую температуру кипения). Данные системы являются двухфазными, т. е. состоят из двух фаз: жидкой и паровой. 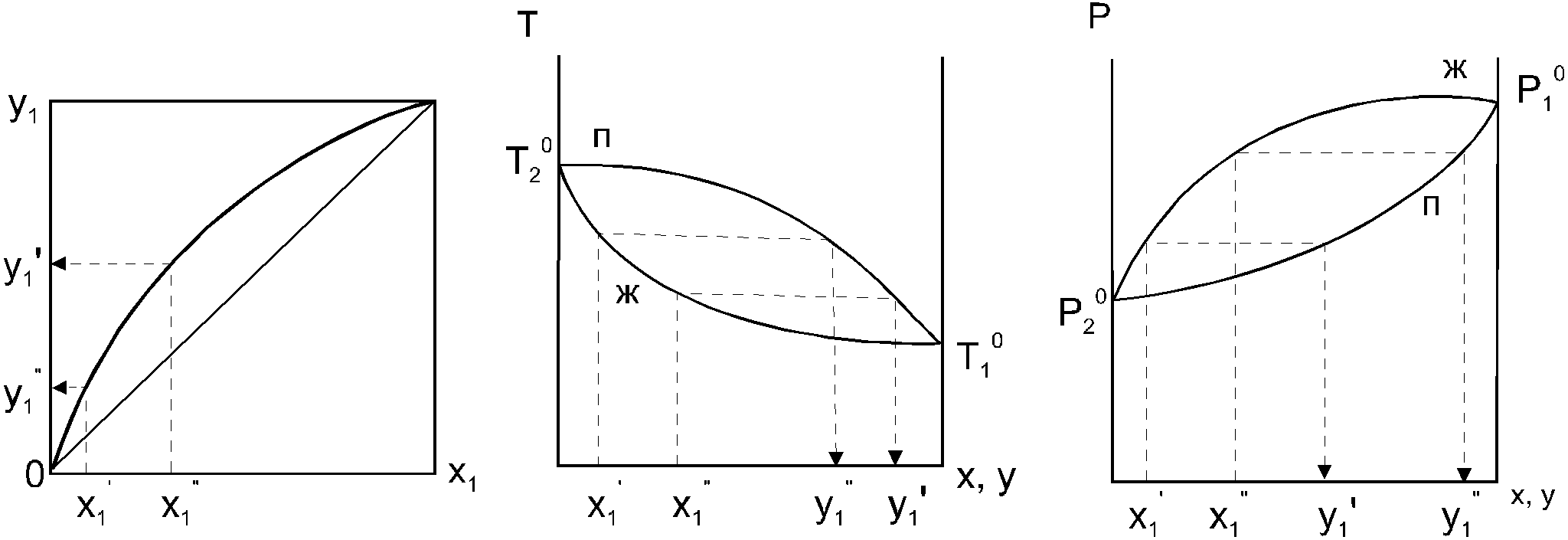 Рис. 8. Диаграммы фазового равновесия жидкостьпар зеотропной гомогенной системы. При ограниченной взаимной растворимости компонентов бинарная система характеризуется наличием областей с тремя равновесными фазами: две жидкие и одна паровая (рис.8). Такая трехфазная система имеет только одну степень свободы, т. е. состояние системы определяется заданием одного из параметров температуры, давления или состава равновесной фазы. По характеру отклонения от идеального поведения бинарные смеси подразделяются на системы с положительными, отрицательными и смешанными отклонениями [11]. Идеальные системы описываются законом Рауля: yiP = xiPi0 (49) Отклонения от идеальности учитываются введением соответствующих коэффициентов: активности (γi) для жидкой фазы и летучести (φi) для паровой фазы. Поведение паровой фазы обычно принимают идеальным (φi = 1), тогда уравнение (49) для реальных систем имеет вид: yiP = xiPi0γi (50) Для положительных отклонений γi > 1, lnγi > 0, для отрицательных 0 < γi < 1, lnγi < 0, для смешанных отклонений lnγi имеет разные знаки. Азеотроные системы можно разделить также на зеотропные (рис. 8, 9а) и азеотропные (рис. 7, 9б-г). Гетероазеотропные системы имеют азеотроп в области сосуществования двух равновесных жидких фаз, который реализуется только при положительных отклонениях от идеального поведения. 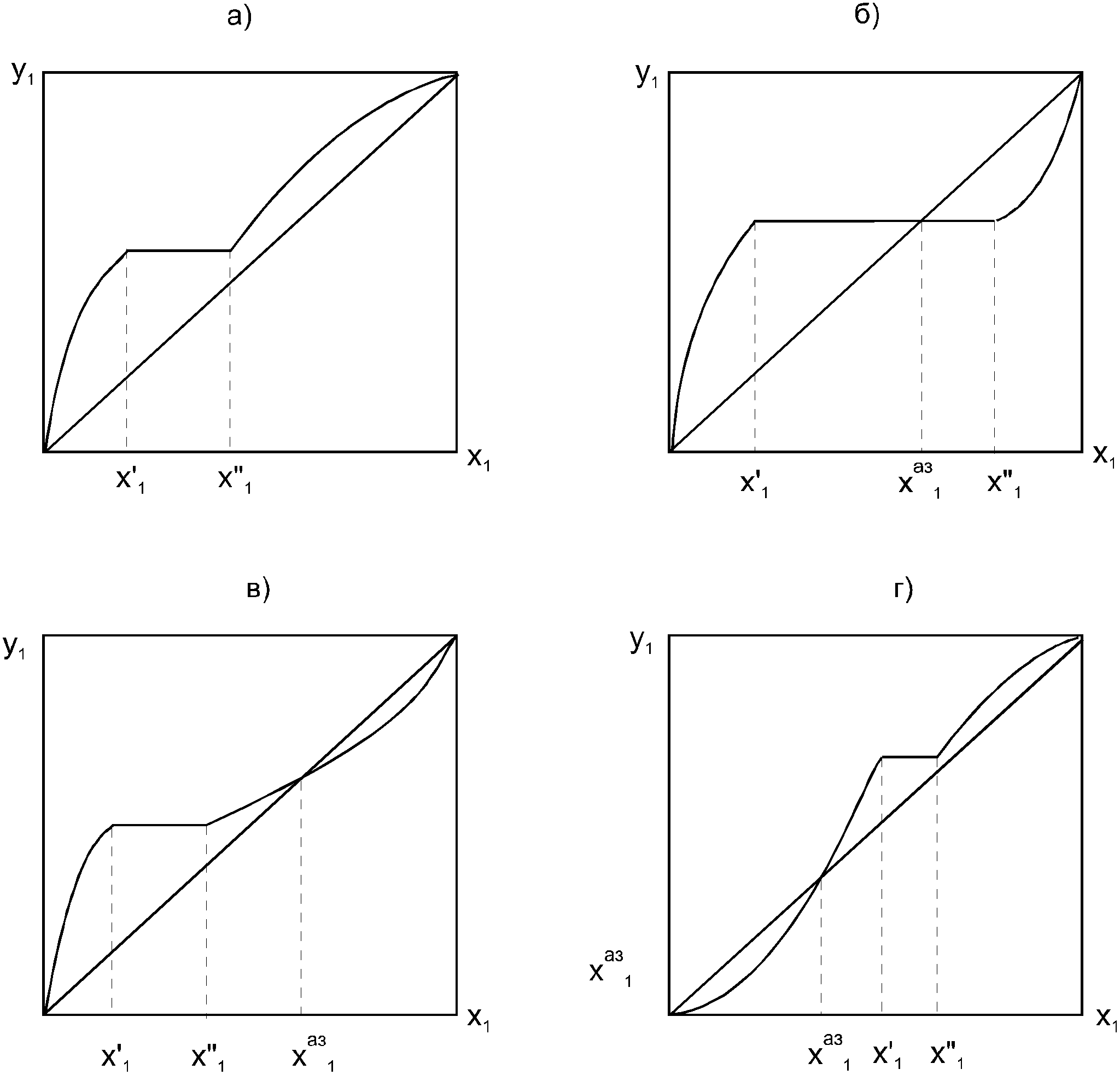 Рис. 9. Диаграммы фазового равновесия бинарных расслаивающихся систем: а) зеотропная, б) гетероазеотропная, в) с гомогенным азеотропом, г) со смешанными отклонениями от идеального поведения(расслаивание и отрицательный азеотроп). Азеотроп характеризуется равенством составов паровой и жидкой фаз и наличием экстремума по температуре (в изобарических условиях) или давлению (в изотермических условиях), что вытекает, как будет показано далее, из первого закона Коновалова. В точке азеотропа наблюдается равенство единице коэффициента распределения компонентов ki и коэффициента относительной летучести αij: kiаз = yi/xi = 1 (51) αiаз = ki/ kj = 1 (52) где ki,j - коэффициент равномерного распределения компонента i, j между паровой и жидкой фазами. Соотношения (51)-(52) используют для определения параметров азеотропной точки при интерполяции экспериментальных данных по ПЖР. Фазовые диаграммы графически отображают состояния равновесной системы в пространстве термодинамических переменных, например: температуры, давления и состава. Число фаз в бинарных системах может быть различно. Состояние двухфазной бинарной системы жидкость пар определяется двумя независимыми переменными, в качестве которых обычно выбирают концентрацию одного компонента и внешний параметр (температуру Т или давление Р). Примеры даны на рис. 10. 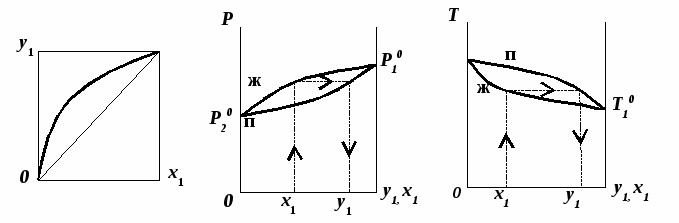 Рис. 10. Диаграммы фазового равновесия жидкость - пар бинарных зеотропных систем: а) у - х, б)Р - х - у; в)Т - х - у. Фазовые равновесия жидкость – жидкость и жидкость – твердое тело экспериментально исследуют при постоянном давлении, в качестве независимых переменных выступают состав и температура (рис. 11). Состояние трехфазной бинарной системы жидкость жидкость – пар в области расслаивания определяется одной независимой переменнойf=1 (Т,Р или состав). На рис. 11 представлены наиболее распространенные примеры фазовых диаграмм жидкость – твердая фаза и жидкость – жидкость – пар. Их полные множества включают большее число типов. 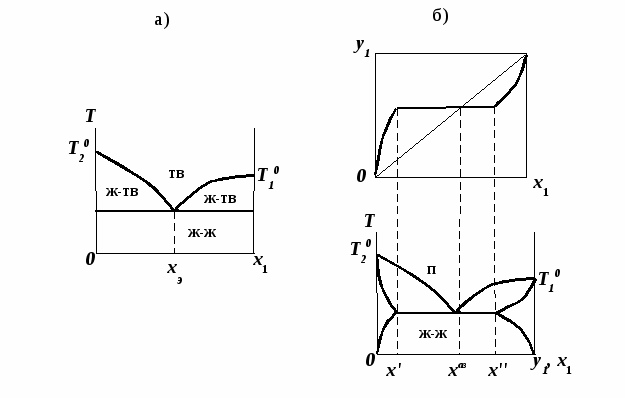 Рис. 11. Примеры фазовых диаграмм бинарных систем с ограниченной взаимной растворимостью компонентов в изобарических условиях: а) жидкость - твердая фаза; б) жидкость - жидкость - пар. На рис. 12 приведены более сложные диаграммы бинарных расслаивающихся систем. 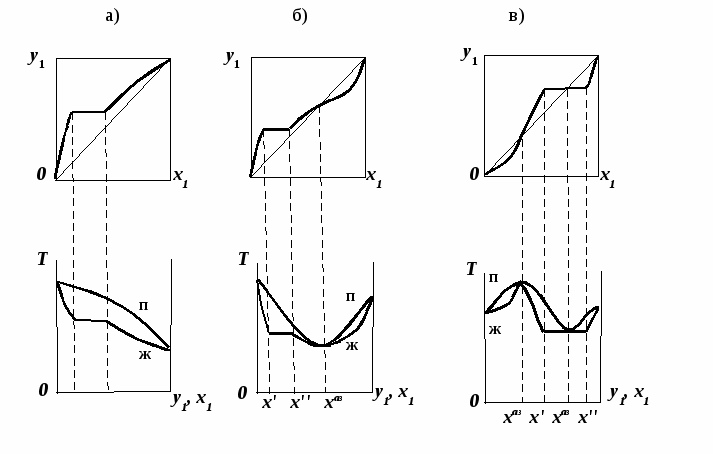 Рис. 12. Примеры фазовых диаграмм жидкость - жидкость - пар бинарных систем в изобарических условиях: а) зеотропная система; б) расслаивание жидкой фазы и гомогенный азеотроп; в) отрицательный азеотроп и гетерогенный азеотроп. Здесь x', x'' – составы равновесных жидких фаз. Диапазоны условий, в которых изучают фазовые равновесия, ограничены критическими точками [11]. Это предельные точки на кривых равновесия фаз, в окрестностях которых фазовое равновесие нарушается, происходит потеря термодинамической устойчивости и фазы становятся неразличимыми. Условие устойчивости фазы приведено ниже: 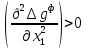 (53) (53)Критическая точка фазового равновесии жидкость – пар является конечной точкой на кривой испарения и характеризуется критическими значениями температуры Тс, давления Рс и объема Vc. Фазовый переход твердая фаза – жидкость характеризуется критической температурой плавления. Парожидкостное равновесие существует в диапазоне условий (Р, Т), ограниченном этими критическими точками. 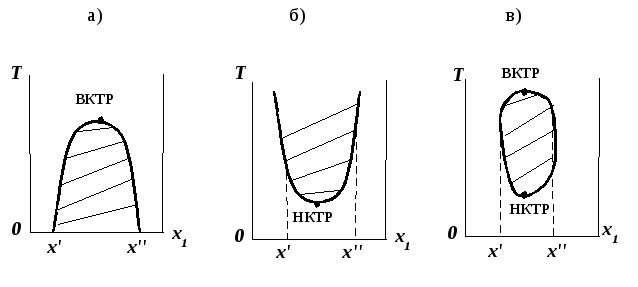 Рис. 13. Критические точки растворимости бинарных систем (Р=const): а) верхняя критическая точка растворимости; б) нижняя критическая точка растворимости; в) две критические точки растворимости. На рис. 13 приведены диаграммы фазового равновесия жидкость – жидкость. Линии, соединяющие составы равновесных фаз (x' ,x''), называются нодами жидкость-жидкость. Бинодаль – линия составов равновесных жидких фаз, отделяющая расслаивающуюся часть диаграммы от гомогенной (рис. 13).[45] В большинстве бинарных систем взаимная растворимость компонентов увеличивается при повышении температуры (рис. 13а). В верхней критической точке растворимости (ВКТР) жидкие фазы становятся неразличимыми, при дальнейшем повышении Т смесь является гомогенной. В системах с нижней критической точкой растворимости (НКТР) увеличение температуры приводит к уменьшению взаимной растворимости (рис. 13б). Смеси с двумя критическими точками растворимости встречаются значительно реже (рис. 13в). Данные фазовых равновесий жидкость – пар (гомогенная жидкая фаза) и жидкость – жидкость – пар (ограниченная взаимная растворимость компонентов) используются для расчетов ректификации бинарных смесей. Диаграммы жидкость – жидкость необходимы при разработке экстракционного разделения и комплексов, сочетающих ректификацию и расслаивание жидкой фазы. Диаграммы жидкость – твердая фаза необходимы при разработке комплексов разделения бинарных смесей, сочетающих ректификацию и кристаллизацию [20]. |
