|
Рабочая лекционная тетрадь по Контролю качества. Лекарственные средства, производные спиртов Спирт этиловый
Лекарственные средства, производные парааминобензойной кислоты
Бензокаин
Анестезин
|
Прокаина гидрохлорид
Новокаин
|
Тетракаина гидрохлорид
Дикаин
|
Benzocaine *
Anaesthesinum
|
Procaini hydrochloridum
Novocainum
|
Tetracaini hydrochloridum
Dicainum
|
 NH2 NH2
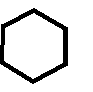
 


C – O - C2H5
||
O
|
NH2
 
 
• HCl HCl

C – O - CH2-СН2-N-C2H5
|| |
O C2H5
|
NH – CH2– CH2– CH2– CH3
 
 
• HCl HCl

C – O - CH2-СН2-N-CH3
|| |
O CH3
|
Этиловый эфир парааминобензойной кислоты
|
β- диэтиламиноэтилового эфира парааминобензойной кислоты гидрохлорид
|
β- диметиламиноэтилового эфира п-бутиламинобензойной кислоты гидрохлорид
|
Свойства
|
Белые кристаллические порошки без запаха.
|
Мало растворим в воде, легко в спирте, эфире, хлороформе. Трудно растворим в жирных маслах.
|
Очень легко растворимы в воде, в спирте, эфире и мало растворимы в хлороформе
|
|
|
Горького вкуса, на языке вызывают чувство онемения.
|
Подлинность
|
р-ция на аминогруппу - образование азокрасителя → вишнево- красное окрашивание или осадок от оранжево- желтого до оранжево- красного цвета
 NH2 N≡N NH2 N≡N
+ NaNO2 + 2 HCl → Cl + NaCl + 2 H2O
R R
 NaO NaO
N≡N N=N
OH
NaOH
Cl + →
R β- нафтол R
|
5 и 7
|
10.
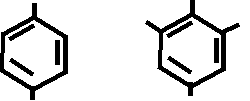 NH – C4 H9 NH – C4 H9 NH – C4 H9 NH – C4 H9
O2N NO2
HNO3 KOH
→ →
C – O - R C – O - R
|| ||
O N – C4H9 O
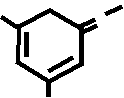 || O- || O-
O2N N - OK
→
COOR кроваво- красный
|
лигниновая проба на газетной бумаге → желтое или оранжевое пятно
  NH2 N=CHR NH2 N=CHR
+ R – C = O → + H2O
|
H
R R
|
11. с роданидом аммония → роданид дикаина. Осадок высушивают, отфильтровывают и определяют t плавления.
|
бромирование → дибромпроизводная белый осадок
NH2 NH2
 Br Br Br Br
+ 2 Br2 → ↓ + 2 HBr
R R
|
|
|
С р-ром хлорамина + HCI + эфир → слой хлороформа окрашивается в оранжевый цвет.
|
|
t плавления
|
6. йодоформная проба → осадок желтого цвета трийодметан и запах
  NH2 NH2 NH2 NH2
+ NaOH → + C2H5OH
COOC2H5 COONa
C2H5OH + 4 I2 + 6 NaOH → CHI3↓ + HCOONa + 5 NaI + 5 H2O
|
7. Р - ция осаждения на хлорид ион
|
R3N • HCl + AgNO3 → AgCl↓ + R3N •HNO3
Белый творожистый осадок
|
|
8. Экспресс- анализ подлинности р-ция вытеснения → белый маслянистый осадок
R3N • HCl + NaOH → NaCl + + R3N ↓ + H2O
|
|
|
|
|
9. Р- ция окисления с KMnO4 + H2SO4 → обесцвечивание р-ра
|
|
Количественное определение
|
По ГФ – метод нитритометрии
|
Метод основан на способности препаратов за счет аминогруппы вступать в р-цию диазотирования.
|
Метод основан на способности препарата за счет аминогруппы вступать в реакцию нитрозирования
|
Методика: Тн пр-та растворяют в воде + HCI + катализатор кристаллический KBr и титруют при 18-20 `C 0,1 н р-ром NaNO2
|
Индикаторы: нейтральный красный → от красного в желтый
тропеалин ОО малиновый → синий
тропеалин + метиленовый синий → голубой.
Можно определить окраску с помощью потенциометра.
|
индикатор –
|
 NH2 N≡N NH2 N≡N
+ NaNO2 + 2 HCl → Cl + NaCl + 2 H2O
R R
Соль диазония
|
 NH- C4H9 NH- C4H9
+ NaNO2 + 2 HCl →
R
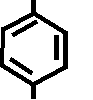 O=N – N – C4O9 O=N – N – C4O9
→
+ NaCl + 2 H2O
R нитрозодикаин
|
2 NaNO2 + 2 KI + 4 HCl → I2 + 2 NO↑ + + 2 KCl + 2 NaCl + 2 H2O
|
fэкв. = 1 M1/z = М
|
Для анестезина и новокаина – метод броматометрии
|
Для анестезина и новокаина - метод йодхлорметрии
|
Метод алкалиметрии
|
|
Вариант вытеснения, прямого титрования (экспресс)
|
Метод основан на вытеснении более слабого органического основания сильным минеральным.
|
Методика: Тн пр-та растворяют в воде + ф/ф + спиртохлороформная смесь (для извлечения органического основания) и титруют 0,1 н р-ром NaOH до слабо розового окрашивания водного слоя.
|
R3N • HCl + NaOH → NaCl + R3N + H2O
1 моль 1 экв. fэкв. = 1 M1/z = М
|
Метод аргентометрия по Фаянсу
|
Метод основан на осаждении хлорид ионов катионами серебра.
|
Методика: Тн пр-та растворяют в воде + разведенную уксусную к-ту + индикатор бромфеноловый синий и титруют 0,1 н р-ром AgNO3 до фиолетового окрашивания.
|
R3N • HCl + AgNO3 → AgCl↓ + R3N •HNO3
1 моль 1 экв.
fэкв. = 1 M1/z = М
|
Метод фотоколориметрии
|
|
Применение
|
Местноанестезирующие пр-ты
|
Мази, свечи, присыпки, «Меновазин».
|
Для спинномозговой и проводниковой анестезии. Ампулы, свечи, субстанции, мази, инъекционные р-ры с 0,1 н р-ром HCI.
|
Поверхностная анестезия. Пленки глазные, капли глазные. Дозы превышать нельзя, применяется однократно.
|
Хранение
|
Список Б. В ХУТ, защищенном от света месте, т.к окисляется за счет аминогруппы.
|
Список А. В ХУТ.
|
Лекарственные средства, производные сульфаниламидов
Общая характеристика сульфаниламидных препаратов
САП – сульфаниламидные препараты, амиды сульфаниловой к-ты

H2N SO3H H2N SO2 – NH2
сульфаниловая кислота амид сульфаниловой кислоты
Общие формулы САП и их натриевых солей можно представить следующим образом:
R ΄ R R΄ R ΄ R R΄ R
H - N SO2 – N - H H N SO2 – N - Na
САП – кислота САП – соль
САП классифицируют по характеру радикалов R и R΄. Большинство САП являются первичными ароматическими аминами (R΄= Н). Водород в амидной группе может быть замещен на радикал R (алифатический или гетероциклический).
Свойства
Белые кристаллические порошки без запаха. Обладают амфотерными св-ми.
САП - соли (сульфацил Na, стрептоцид растворимый) – растворимы в воде, плохо растворимы в органических растворителях.
САП - кислоты (норсульфазол, сульфодимезин, стрептоцид, фталазол) – нерастворимы в воде, растворимы в органических растворителях.
Химические свойства обусловлены наличием следующих функциональных групп:
Первичной ароматической аминогруппой – основные св-ва - растворимы в кислотах
Сульфамидной группой – кислотные св-ва - растворимы в гидроксидах щелочных металлов
O O
 || || || ||
H2 N S - N - R ↔ H2N S= N - R
|| | |
O H OH
аци-форма
Ароматическое ядро – р-ция галоидирования, электрофильное замещение - фенильный радикал.
Подлинность
Реакции на первичную ароматическую аминогруппу
Если аминогруппа закрыта – то открывают путем гидролиза (кипятят ЛС в HCI)
А) р-ция образования азокрасителя
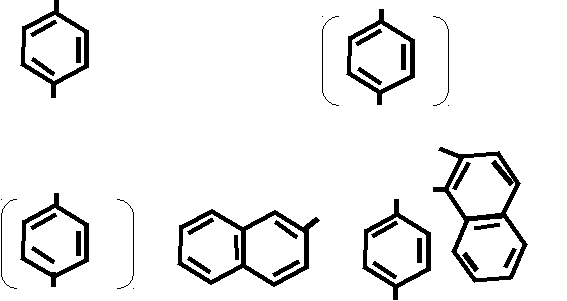 NH2 N≡N NH2 N≡N
+ NaNO2 + 2 HCl → Cl + NaCl + 2 H2O
SO2 –NH - R SO2 –NH - R
NaO
N≡N N=N
OH
NaOH
Cl + →
SO2 –NH - R SO2 –NH - R
Б) лигниновая проба → желто- оранжевое пятно
 NH2 N=CHR NH2 N=CHR
+ R – C = O → + H2O
|
H
SO2 –NH - R SO2 –NH –R
В) с нитропруссидом натрия → окрашенные продукты р-ции
Реакции на сульфамидную группу
А) р-ция с CuSO4 за счет подвижного атома H сульфамидной группы натриевые соли образуют окрашенные комплексные соединения
Если САП- кислота – то добавляем 0,1 н р-р NaOH
Норсульфазол – грязно- фиолетовое
Сульфацил натрия – голубовато- зеленый осадок
Сульфодимезин – желто- зеленый, переходящий в коричневый
 NH2 NH2 NH2 NH2
+ NaOH → + CuSO4 →
- H2O
O = S–NH - R O = S = N –R
|| |
O ONa
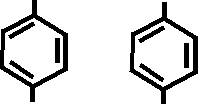 NH2 NH2 NH2 NH2
↓ Это реакция отличия!!!!!!!!!!!
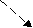  O = S=N - R R –N=S = O O = S=N - R R –N=S = O
| |
O – Cu – O
Б) р-ция минерализации на сульфогруппу → белый осадок
САП + HNO3 → SO42-
SO42- + BaCl2 → BaSO4 ↓ + 2 Cl –
|
|
|
 Скачать 1.99 Mb.
Скачать 1.99 Mb.
 ΄ R R΄ R
΄ R R΄ R || ||
|| ||  NH2 N≡N
NH2 N≡N NH2 N=CHR
NH2 N=CHR NH2 NH2
NH2 NH2 NH2 NH2
NH2 NH2
 O = S=N - R R –N=S = O
O = S=N - R R –N=S = O