фармакология. Лекция 1 Общая фармакология Фармакология
 Скачать 0.87 Mb. Скачать 0.87 Mb.
|
Лекция 2Общая фармакология (продолжение). Фармакокинетика - это раздел фармакологии, который изучает различные этапы прохождения лекарства в организме: всасывание (абсорбция), биотранспорт (связывание с транспортными белками), распределение по органам и тканям, биотрансформация (метаболизм), выведение (экскреция) ЛС из организма. Пути введения ЛС в организм.От пути введения зависит: Скорость и полнота доставки ЛС в очаг болезни. Эффективность и безопасность (рациональное применение лекарств без осложнений фармакотерапией.). 1. Энтеральный путь введения – путь поступления лекарств в организм через ЖКТ. Достоинства:Удобство Безопасность Проявление местного и резорбтивного эффекта. К энтеральному пути относится: Пероральный (per os) – через рот (внутрижелудочный; приём лекарств внутрь) Сублингвальное (под язык). Интрадуоденальное. Ректальный(per rectum). 2.Парентеральный путь введения – введение, минуя ЖКТ. Достоинства: 1. Достижение точной дозировки. 2. Быстрое достижение эффекта. К парентеральным путям относится: Внутривенное введение. Внутриартериальное введение. Внутримышечное введение. Подкожное введение. Интратрахеальное введение. Интравагинальное введение. Внутрикостное введение. Этапы фармакокинетики. I. Всасывание (абсорбция) - процесс поступления лекарства из места его введения в системный кровоток при внутрисосудистом введении. Скорость всасывания зависит от: Лекарственной формы препарата. От степени растворимости в жирах или в воде. От дозы или концентрации. От пути введения. От интенсивности кровоснабжения органов и тканей. Скорость всасывания при per os применении зависит от: РН среды в различных отделах ЖКТ. Характера и объёма содержимого желудка. От микробной обсеменённости. Активности пищевых ферментов. Состояния моторики ЖКТ. Интервала между приемом лекарства и пищей. Процесс всасывания характеризуется следующими фармакокинетическими параметрами:Биодоступность (f) – относительное количество препарата, которое поступает из места введения в кровь (%). Константа скорости всасывания (К01) – это параметр, который характеризует скорость поступления ЛС из места введения в кровь (ч -1, мин -1). Период полуабсорбции (t ½α) – время, необходимое для всасывания из места введения в кровь ½ введенной дозы (ч, мин). Время достижения максимальной концентрации (tmax) – это время, за которое достигается максимальная концентрация в крови (ч, мин). Процессы всасывания у детей достигают состояния абсорбции лекарственного уровня взрослых лишь к трём годам жизни. До трех лет абсорбция лекарств снижена главным образом из-за недостатка обсемененности кишечника, а также из-за недостатка желчеобразования. У людей старше 55 лет также снижена всасывательная способность. Им нужно лекарства дозировать с учетом возрастных особенностей. II. Биотранспорт – после всасывания лекарств в кровь они вступают в обратное взаимодействие с т.н. транспортными белками, к которым относятся белки сыворотки крови. Подавляющее число лекарства (90%) вступает в обратимые взаимодействия с человеческим сывороточным альбумином. А также взаимодействует с глобулинами, липопротеидами, гликопротеидами. Концентрация связанной с белком фракции соответствует свободной, т.е.: [Ссвяз] = [Ссвоб]. Фармакологической активностью обладает лишь свободная, несвязанная с белком фракция, а связанная является своего рода резервом препарата в крови. Связанная часть ЛС транспортным белком определяет: 1. Силу фармакологического действия лекарства. 2. Продолжительность его действия. Места связывания белка являются общими для многих веществ. Процесс обратимого взаимодействия лекарств с транспортными белками характеризуется следующими фармакокинетическими параметрами: Касс (ЛС + белок) – характеризует степень сродства или силу обратимого взаимодействия препарата с белком сыворотки крови (моль-1). N – показатель, который свидетельствует о количестве мест фиксации на молекуле белка для молекулы конкретного препарата. III. Распределение лекарств в организме. Как правило, лекарства в организме распределяются по органам и тканям неравномерно с учетом их тропности (сродства). На характер распределения лекарств в организме влияют следующие факторы: Степень растворимости в липидах. Интенсивность регионарного или местного кровоснабжения. Степень сродства к транспортным белкам. Состояние биологических барьеров (стенок капилляров, биомембран, гематоэнцефалических и плацентарных). Основными местами распределения ЛС в организме являются: Внеклеточная жидкость. Внутриклеточная жидкость. Жировая ткань. Параметры: Объем распределения (Vd) - степень захвата ЛС тканями из крови (л, мл). IV. Биотрансформация. Один из центральных этапов фармакокинетики и основной путь детоксикации (обезвреживания) ЛС в организме. В биотрансформации принимают участие: Печень Почки Легкие Кожа Плацента Биотрансформация осуществляется в 2 фазы. Реакции 1 фазы: Гидроксилирование, окислительно-восстановтиельные реакции, дезаминарование, дезалкилирование и т.д. В процессе реакций этой фазы происходит изменение структуры молекулы препарата так, что он становится более гидрофильным. Это обеспечивает более легкую экскрецию из организма с мочой. Реакции I фазы осуществляются с помощью ферментов эндоплазматического ретикулума (микросомальные или ферменты монооксигеназной системы, основным из которых является цитохром Р450). Лекарства могут как усиливать, так и уменьшать активность этого фермента. ЛС, прошедшие I фазу, структурно подготовлены к реакциям II фазы. В процессе реакций II фазы образуются коньюгаты или парные соединения препарата с одним из эндогенных веществ (например, с глюкуроновой кислотой, глутатионом, глицином). Образование коньюгатов происходит при каталитической активности одного из одноименных ферментов, например (препарат +глюкуроновая кислота – образуется при помощи глюкуронидтрансферазы). Образовавшиеся коньюгаты являются фармакологически неактивными веществами и легко выводятся из организма с одним из экскретов. Однако не вся введенная доза ЛС подвергается биотрансформации, часть её выводится в неизмененном виде. V. Выведение (экскреция). Является завершающим этапом фармакокинетики, в процессе которого лекарство в виде метаболитов или в неизмененном виде выводится из организма с одним из экскретов. Чаще всего ЛС выводятся из организма с мочой, желчью, выдыхаемым воздухом, слюной, потом, грудным молоком. Наибольший удельный вес приходится на почки. При этом реализуются следующие механизмы: Клубочковая фильтрация. Канальцевая секреция. Канальцевая реабсорбция. Основные фармакокинетические параметры: 1. Константа экскреции (Кех) –– характеризует скорость выделения лекарства из организма с каким-либо экскретом (ч-1, мин-1). 2. Период полуэлиминации (t1/2) – это время исчезновения из организма лекарства путем биотрансформации и экскреции половины введенной или поступившей и всосавшейся дозы (ч, мин.). 3. Константа элиминации (Кel) – характеризует скорость исчезновения препарата из организма путем экскреции и биотрансформации (ч-1, мин-1). Лекции 3-5. ФАРМАКОЛОГИЯ ВЕГЕТАТИВНОЙ НЕРВНОЙ СИСТЕМЫ (ВНС) ВНС – автономная система, состоящая из двух отделов: симпатического и парасимпатического. Сюда же можно отнести и соматический отдел, по строению похожий на симпатический и парасимпатический отделы. Особенности анатомического строения ВНС. Волокна симпатической нервной системы выходят из спинного мозга в грудных и поясничных его отделах. Ганглии СНС располагаются по бокам позвоночника – паравертебрально, у них длинные постганглионарные волокна и короткие преганглионарные. Парасимпатические волокна выходят из краниального отдела (3-я пара черепно-мозговых нервов – ими иннервируются внутренние мышцы глаза, 7-8 пара – лицевой нерв имеет вегетативные волокна, которые иннервируют слюнные железы, 10-я пара – nervus vagus – иннервирует все органы брюшной полости и органы дыхания). Из сакрального отдела выходят нервы, иннервирующие нижнюю часть толстого кишечника и органов брюшного таза. Мышцы радужной оболочки представлены круговой, циркулярной и радиальной мышцами. Круговая мышца иннервируется парасимпатической системой, радиальная – симпатической. Сужение зрачка – миоз – круговая мышца сокращается. Расширение – мидриаз – радиальная мышца сокращается. Саливация – усиление слюноотделения. При возбуждении симпатических отделов – слюны мало, она густая, вязкая, много плотного остатка. При возбуждении парасимпатического отдела – много жидкой слюны, без остатка. Влияние на сердце – раздражение блуждающего нерва – урежение сердечных сокращений (брадикардия), снижение силы сердечных сокращений – отрицательное инотропное действие. При увеличении тонуса симпатического отдела – учащение сердечных сокращений (тахикардия), повышение силы сердечных сокращений. ЖКТ – повышение тонуса парасимпатического отдела – повышение перистальтики и усиление деятельности пищеварительных желез; повышение тонуса симпатического отдела – угнетение перистальтики, снижение активности пищеварительных желез. Органы дыхания – при активации парасимпатического отдела – бронхоспазм, бронхорея. Активация симпатической системы – улучшение газообмена. Парасимпатической иннервации в сосудах нет, следовательно все сосудистые реакции (расширение, сужение) регулируются только симпатическим отделом ВНС. Для управления органами необходима передача импульсов с нервных волокон на рабочие органы. Передача импульса происходит за счет химических компонентов. Длительность периода передачи импульсов – 0,000002 сек. В тканях, где синтезируется медиатор, также синтезируется и фермент, который разрушает этот медиатор, из-за этого получается такая скорость передачи импульсов. Медиатор парасимпатической нервной системы быстро разрушается. Для его сохранения, выделения, показа его функции применили лекарственный препарат – физостигмин. Этот препарат блокирует фермент, разрушающий медиатор. Медиатор в парасимпатическом отделе – ацетилхолин (АХ), фермент, который его разрушает – холинэстераза (ХЭ); физостигмин относится к группе антихолинэстеразных средств – разрушает его активность. Этапы передачи импульса Синтез и депонирование в пресинаптическом волокне; Включение механизма освобождения медиатора в синаптическую щель; Взаимодействие медиатора с рецепторами постсинаптической мембраны; Включение механизма сопряжения активированных рецепторов постсинаптической мембраны с обменом и функциями клетки; Ферментная инактивация медиатора или его реабсорбция в пресинаптических окончаниях и восстановление исходного состояния клетки. 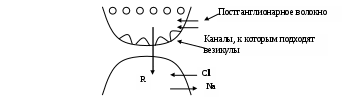 1. Здесь происходит синтез и депонирование медиатора. Для синтеза АХ необходима активность фермента холинацетилазы и большого количества аминокислоты холина. Увеличение содержания холина происходит после прихода рабочего импульса и в присутствии холинацетилазы происходит синтез медиатора. Медиатор, который синтезируется в ретикулах, соединяется с белком, АТФ – эти компоненты являются защитой медиатора от действия ферментов, которые могут его разрушить. Фракции медиатора: стратегическая – часть медиатора, которая не может сразу включиться в передачу импульса; мобилизационная – более активно готова к передаче импульса; горячая – непосредственно принимает участие в передаче импульса. Все эти фракции находятся в динамическом равновесии. 2. В пресинаптической мембране существуют каналы, к которым изнутри обратимо подходят везикулы с медиатором. После появления рабочего импульса в клетку входят ионы Na, которые увлекают за собой ионы К, который попав в клетку, захватывается белком – кальмодулином и приносится ферменту, который расположен на сократительных элементах клетки. Этим ферментом является Са-зависимая АТФ-аза (фосфатаза). Под влиянием Са активность фермента увеличивается, а функция этого фермента сводится к деформированию АТФ. При деформации АТФ выделяется энергия, которая идет на сокращение актиновых и миозиновых нитей, везикулы сокращаются и медиатор выходит в синаптическую щель. 3. В постсинаптической мембране есть рецепторы, с которыми реагирует медиатор. Это взаимодействие основано на электросилах: у медиатора, который поступает на постсинаптическую мембрану есть положительный заряд (катионная головка). Рецептор имеет анионный центр, представленный карбонильными белками и имеющий отрицательный заряд. При передаче импульса медиатор и рецептор взаимно подстраиваются друг к другу и при наличии разности зарядов взаимодействуют друг с другом. 4. После взаимодействия медиатора и рецептора идет ответная реакция со стороны рабочих органов, эта реакция может быть или положительной или отрицательной, при действии одного и того же медиатора. Например, АХ резко возбуждает перистальтику кишечника и может быть диарея, т.е. один и тот же медиатор может вызывать различные эффекты. Если будет усиление ответной реакции – будет вхождение Na, Са, повышение внутриклеточной активности. Са является биокатализатором обменных процессов в клетке. При торможении – в клетке открываются каналы для Cl, и в клетку входит Cl, вместо деполяризации развивается суперполяризация – отсутствие возможности передачи импульса, одновременно включаются насосы, которые выводят из клетки Na и Са. 5. 75% АХ уходит из синаптической щели и не разрушается ХЭ, а разрушается в крови – это объясняет кратковременность действия медиатора. Количество ХЭ достаточно (5% для разрушения АХ, который ушел в кровь). Медиатором симпатического отдела является адреналин (А). Передача импульса в ганглиях Во всех ганглиях симпатической и парасимпатической нервных систем заложены одни и те же рецепторы – Н-холинореактивные биохимические системы (н-хрбс). Рецепторы – гликопротеидные комплексы – комплекс биохимических соединений. Некоторые ганглии в организме переродились – мозговой слой надпочечников. Если количество АХ повышается, то возбуждаются рецепторы мозгового слоя надпочечников, а, следовательно, выделяется большое количество адреналина. Перерожденные ганглии – каротидные клубочки. Парасимпатическая: Холиномиметики – повторяют эффекты медиатора. Холиноблокаторы – препятствуют действию медиатора. Симпатическая: Адреномиметики. Адреноблокаторы. Рецепторы по-разному реагируют на яды: Н-хрбс – реагируют на никотин (табак). М-хрбс – реагируют на мускарин (грибы). Яд Кураре – вызывает расслабление поперечно-полосатой мускулатуры. Миорелаксанты – производные кураре. Передача импульса в ЦНС Идет по синаптическому типу, как и в ганглиях. Введение атропина меняет активность ЦНС, что говорит о наличии н-хрбс, также там есть и м-хрбс. Симпатическая нервная система также подвержена действию ядов. Если ввести эрготоксин – возбуждающие эффекты не появляются, тормозные не страдают. В симпатической нервной системе принимают участие α и β-рецепторы. α-рецепторы – рецепторы, которые воспринимают возбуждающие и сосудосуживающие импульсы. β-рецепторы – воспринимают тормозные и сосудорасширяющие импульсы. Н-ХОЛИНОМИМЕТИКИ, Н-ХОЛИНОБЛОКАТОРЫ Каротидные клубочки – это начало рефлекторной дуги, импульсы передаются на дыхательный центр – повышение тонуса дыхательной системы. Кордиамин – действует на сосуды, улучшает гемодинамику. При большом разведении выделение адреналина увеличивается в 6 раз. У кроликов, которые курили 250 дней в году была атрофия сетчатки глаза. У самцов – атрофия половых желез, у самок – выкидыши, выраженные явления атеросклероза. Механизм развития сосудистых поражений – большие количества адреналина приводили к спазму сосудов, нарушению трофики внутренней оболочки сосудов, изъязвление, замещение этих участков соединительной тканью, на ней отлагались фибрины, тромбоциты – образование тромбов. Точно такой процесс происходит и в организме человека. «Цититон» - 0,15 % раствор цитизина, получают из травы мышатника. Препарат рефлекторно возбуждает дыхательный центр, поэтому если есть угнетение дыхательного центра (передозировка морфином), то этот препарат НЕ ЭФФЕКТИВЕН! «Лобелин» - также рефлекторно возбуждает дыхательный центр. Отрицательная черта – вызывает гипергликемию, следовательно, требуется дополнительное количество кислорода для нормализации углеводного обмена. Эти препараты повторяют строение алкалоида никотина, поэтому для облегчения отвыкания от курения предложены таблетки «Табекс» и «Лобесил», которые по химическому строению близки к никотину, восполняют никотиновый голод. Ганглиоблокаторы (н-холиноблокаторы) Резкой разницы в препаратах миоблокаторах и миорелаксантах нет. Если ганглиоблокаторы взять в большой дозе они могут оказать блокаду н-хрбс поперечнополосатых мышц. Особенность химического строения не выявлена. Ганглиоблокирующее действие могут оказывать снотворные, производные тиобарбитуровой кислоты. Барбитал натрия в дозе 1/2 - 1/3 – снотворные дозы, оказывают выраженное ганглиоблокирующее действие, поэтому целесообразно применять при нарушении ночного сна и при необходимости блокады ганглиев. Ганглиоблокаторы не оказывают одинакового действия на ганглии симпатического и парасимпатического отделов. Всегда есть большая склонность к блокаде одного из отделов. Если заблокированы ганглии парасимпатического отдела, то поток импульсов по постганглионарным волокнам будет меньше, следовательно, и возбуждение м-хрбс будет меньше, действие блуждающего нерва на сердце будет меньше, поэтому будет тахикардия и повышение силы сердечных сокращений. Если заблокированы ганглии симпатического отдела – поток по постганглионарным волокнам уменьшается, количество адреналина снижается, малые количества медиатора взаимодействуют с β-адренореактивными системами, происходит расширение сосудов – гипотензивный эффект. Бензогексоний действует на ганглии симпатического отдела и меньше на ганглии парасимпатического отдела. Снижает АД, но при ГБ его не рекомендуют, т.к. для обеспечения эффективности лечения дозу препарата необходимо постоянно увеличивать. «Пирилен» - ганглиоблокатор, проникает через ГЭБ, применяется при ГБ, при эндартериите, при токсикозе беременных. «Пентамин» - при кишечных коликах, бронхиальной астме, отеке легких. «Гигроний» - для управляемой гипотонии во время оперативного вмешательства. Миорелаксанты – расслабляют поперечно-полосатые мышцы. Используются для проведения хирургических вмешательств, менее выражена интоксикация организма. Миорелаксанты: Антидеполяризующие – фиксируют состояние покоя. Количество импульсов в норме, в н-хрбс – 400-600 имп/с, если меньше – мышечное расслабление – эффект миорелаксации. Препятствуют деполяризации и передаче импульсов. Деполяризующие – наблюдается одиночное вздрагивание поперечно-полосатых мышц. Фиксируют период деполяризации и препятствуют восстановлению исходного состояния. При передозировке антидеполяризующих – введение антихолинэстеразных средств для блокирования ХЭ. Если передозировка деполяризующих – переливание крови – увеличение количества бутирилхолинэстеразы. Классификация лекарственных групп для воздействия на рецепторы парасимпатической системы: М -, Н - холиномиметики: «Ацетилхолина хлорид» - используется только в экспериментальных опытах для выявления наличия рецепторов; «Карбохолин» - устойчив к действию ХЭ, поэтому может применяться и перорально, повторяет все эффекты АХ, возбуждает м-хрбс, угнетает работу сердца, брадикардия, снижение силы сердечных сокращений, снижение систолического АД. Для лечения гипертонии не применяется. Антихолинэстеразные средства: а. Обратимого действия: Прозерин Калимин Галантамин б. Необратимого действия: Армин После применения препаратов обратимого типа действия – активность фермента восстанавливается, после применения необратимого типа – длительное восстановление. Реактиваторы ХЭ: Дипироксим Изонитрозин Аллоксим После введения этих ЛС вводится 2-3 мл 0,1% р-ра атропина сульфата. М-холиномиметики: Пилокарпин Ацеклидин М-холиноблокаторы (группа атропина): Атропин Скополамин Экстракт красавки Метацин Ипротропиума бромид Н-холиномиметики (дыхательные аналептики): Лобелин Миорелаксанты: Антидеполяризующие (тубокурарин, мелликтин, ардуан) Деполяризующие (дитилин) Ганглиоблокаторы: Бензогексоний Пирилен Пентамин Гигроний Классификация препаратов, применяемых в симпатическом отделе: α–β- Адреномиметики: Адреналин Норадреналин Эфедрин α– Адреномиметики: Мезатон Нафтизин Ксилометазолин Деконгестанты – препараты адреномиметического типа действия, способствуют активации адренергической передачи, уменьшают отек, заложенность носа, облегчают носовое дыхание. α-Адреномиметики – ограничивают приток крови к слизистой носа, снижают наполнение кавернозных синусов. Они используются местно в виде капель или аэрозолей. Для перорального приема деконгестанты используют в комбинации с антигистаминными препаратами. Недостатки: длительное применение деконгестантов может вызвать медикаментозный ринит. Пероральный прием вызывает бессонницу, тахикардию, повышение АД. β-Адреномиметики: Изадрин Сальбутамол Адреноблокаторы: α-Адреноблокаторы (пирроксан, празозин, фентоламина гидрохлорид) β-блокаторы (талинолол, атенолол, ацебуталол, анаприлин) Симпатолитики: Октадин Резерпин Лекция 6. Наркотические анальгетики. Анальгетические средства (от греч. аn – отрицание, logus - боль ) – это группа ЛС, которые избирательно подавляют болевую чувствительность без выключения сознания и других видов чувствительности (тактильная, барометрическая и др.) Механизмы генерации и подавления боли в организме. Боль возникает, когда происходит раздражение болевых рецепторов (ноцицепторов). Это окончания афферентных нервных волокон, расположенные в коже, слизистых оболочках, мышцах и внутренних органах. В передаче болевых импульсов большую роль играют медиаторы боли (пептиды, которые синтезируются в организме): - вещество Р; соматостатин; холецистокинин. Путь следования болевого импульса. 1. Ноцицептор (б R) 2. Афферентное нервное волокно 3. Задние рога спинного мозга (вставочные нейроны) 4. Продолговатый мозг 5. Средний мозг 6. Ретикулярная формация 7. Гипоталамус 8. Таламус 9. Лимбическая система 10. Кора головного мозга. Все эти структуры, участвующие в восприятии, генерации и проведении болевого импульса, образуют ноцицептивную систему. В организме существует система, которая обладает анальгетической способностью, т.е. антиноцицептивной активностью. Это антиноцицептивная система, которая представлена эндопептидами (эндоопиатами): - энкефалины; эндорфин; неоэндорфин; динорфин. Они взаимодействуют с опиатными рецепторами, при этом происходит подавление боли в организме (происходит процесс угнетения восприятия и проведения импульсов в ЦНС).
|
