Курсовая по МФТ Бабина. Маркетинговые исследования муколитических средств с углубленным анализом лекарственного препарата ацц
 Скачать 1.64 Mb. Скачать 1.64 Mb.
|
2.1.3. Характеристика лекарственного средства.АЦЦ является оригинальным препаратом фирмы «HEXAL AG» Таблетки шипучие впервые были зарегистрированы: «АЦЦ®Актив» - 28.09.2018, дата окончания действия регистрационного удостоверения – 28.09.2023; «АЦЦ®200» - 11.01.2009, дата переоформления регистрационного удостоверения – 18.09.2014; «АЦЦ®100» - 29.12.2008, дата переоформления регистрационного удостоверения – 18.09.2014. Сироп для приема внутрь впервые был зарегистрирован 21.10.2014, дата окончания действия регистрационного удостоверения – 21.10.2019.[30] Порошок для приготовления раствора впервые был зарегистрирован: «АЦЦ®Лонг» - 31.08.2010, дата переоформления регистрационного удостоверения – 24.09.2014; «АЦЦ» - 16.11.2009, дата переоформления регистрационного удостоверения – 30.05.2017 Международный номер CAS - 616-91-1 В России зарегистрировано три лекарственные формы:
2.1.3.1. Перечень синонимов и аналогов, зарегистрированных в России, выбор одного из них для оценки конкурентоспособности.Синонимы – препараты с одним и тем действующим веществом, МНН/составом.
Оценка конкурентоспособности будет производиться в сравнении с лекарственным препаратом «Викс Актив ЭкспектоМед» таблетки шипучие. Аналоги – препараты, близкие по механизму действия, относящиеся к одной фармакологической подгруппе
Оценка конкурентоспособности будет производиться в сравнении с лекарственным препаратом «Амброксол» таблеки. 2.1.4. Качество лекарственного средства.Федеральный закон от 12 апреля 2010 г. N 61-ФЗ «Об обращении лекарственных средств» - нормативный документ регламентирующий качество.[1] Препарат производится в соответствии с требованиями системы GMP. 2.1.5. Влияние различных факторов на потребительские свойства и качство лекарственного средства и лекарственных форм на его основе, способы защиты товаров по этапам жизненного цикла.
Получение ацетилцистеина основано на основных свойствах аминогруппы, которая способна ацилироваться. В качестве ацилирующего агента чаще всего берут уксусный ангидрид, можно использовать ацетилхлорид. Рисунок 2 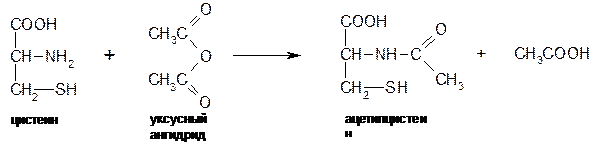 Рис. 2 - ацитилирование
Ацетилцистеин меняет свои свойства под действием влаги, повышенной температуры, при попадании солнечных лучей. Легко окисляется на воздухе, образуя цистеин. Упаковка шипучих таблеток состоит из картонной коробки (вторичная упаковка) и полипропиленовой тубы (первичная упаковка). Коробка полностью защищает препарат от воздействия неблагоприятных внешних факторов. Туба дает защиту от воздействия света, влажности, кислорода воздуха, реакций окисления и гидролиза. Порошок для приготовления раствора упакован в картонную коробку и в пакетики из трехслойного материала (алюминиевая фольга/бумага/ полиэтилен). Первичная и вторичная упаковки отвечают за сходные функции с упаковками шипучих таблеток. Сироп также состоит из вторичной упаковки (картонной коробки) и из флакона из темного стекла, с укупоренными белыми крышками с уплотнительной мембраной, с функцией защиты от вскрытия детьми, с защитным кольцом. У каждой лекарственной формы вторичная упаковка несет информационную функцию, в которую входят: наименование производителя, страна – производитель, торговое название, международное непатентованное название, дозировка, торговый знак, форма выпуска, состав препарата, дата производства, срок годности, номер серии, условия отпуска, способ применения, меры предосторожности, условии хранения. Препарат хранится в защищенном от света месте, при температуре не выше 25°, в недоступном для детей месте. Препарат хранят в соответствии с Приказом МЗ и СР РФ от 23 августа 2010 г. N 706н «Об утверждении правил хранения лекарственных средств»[7]
При одновременном применении ацетилцистеина и противокашлевых средств из-за подавления кашлевого рефлекса может возникнуть застой мокроты. При одновременном применении с антибиотиками для перорального применения (в т.ч. пенициллины, тетрациклины, цефалоспорины) возможно их взаимодействие с тиоловой группой ацетилцистеина, что может привести к снижению их антибактериальной активности. Поэтому интервал между приемом антибиотиков и ацетилцистеина должен составлять не менее 2 ч (кроме цефиксима и лоракарбефа). Одновременный прием с вазодилатирующими средствами и нитроглицерином может привести к усилению сосудорасширяющего действия последнего.
Индивидуальная тара должна быть газо- и паронепроницаемой, индифферентной к организму человека и ингредиентам лекарственного средства, светонепроницаемой, должна обладать барьерной устойчивостью к микроорганизмам и другим показателям. Тара и упаковочные материалы не должны абсорбировать лекарственное вещество, а также вспомогательные вещества в количестве, влияющем на их содержание в лекарственном средстве сверх установленных норм; не должны содержать канцерогенных и токсичных веществ, а также постороннего запаха и вкуса, воспринимаемого лекарственными веществами. Тара и упаковка должны обеспечивать предохранение лекарственной формы от воздействия неблагоприятных факторов внешней среды; обеспечивать удобство пользования, защиту от преднамеренного вскрытия до попадания лекарства к потребителю и употребления детьми; создавать рациональные единицы для транспортировки, хранения и реализации; также тара и упаковка являются носителями информации[14]
Ацетилцистеин является производным аминокислоты цистеина. Оказывает муколитическое действие, облегчает отхождение мокроты за счет прямого воздействия на реологические свойства мокроты. Действие обусловлено способностью разрывать дисульфидные связи мукополисахаридных цепей и вызывать деполимеризацию мукопротеидов мокроты, что приводит к уменьшению ее вязкости. Препарат сохраняет активность при наличии гнойной мокроты. Оказывает антиоксидантное действие, основанное на способности его реактивных сульфгидрильных групп (SH-группы) связываться с окислительными радикалами и таким образом нейтрализовать их. Кроме того, ацетилцистеин способствует синтезу глутатиона, важного компонента антиокислительной системы и химической детоксикации организма. Антиоксидантное действие ацетилцистеина повышает защиту клеток от повреждающего действия свободнорадикального окисления, свойственного интенсивной воспалительной реакции. При профилактическом применении ацетилцистеина отмечается уменьшение частоты и тяжести обострений бактериальной этиологии у пациентов с хроническим бронхитом и муковисцидозом.
Абсорбция высокая. Быстро метаболизируется в печени с образованием фармакологически активного метаболита — цистеина, а также диацетилцистеина, цистина и смешанных дисульфидов. Биодоступность при приеме внутрь составляет 10% (из-за наличия выраженного эффекта первого прохождения через печень). Tmax в плазме крови составляет 1–3 ч. Связь с белками плазмы крови — 50%. Выводится почками в виде неактивных метаболитов (неорганические сульфаты, диацетилцистеин). T1/2 составляет около 1 ч, нарушение функции печени приводит к удлинению T1/2 до 8 ч. Проникает через плацентарный барьер. Данные о способности ацетилцистеина проникать через ГЭБ и выделяться с грудным молоком отсутствуют.[21]
Лекарственные средства, пришедшие в негодность, или с истёкшим сроком годности подлежат изъятию из обращения и последующему уничтожению в полном объёме. Продажа указанных лекарственных средств запрещается. Порядок изъятия из обращения определён Приказом МЗ и СР РФ от 23 августа 2010 г. N 706н «Об утверждении правил хранения лекарственных средств». [7] Порядок уничтожения лекарственных средств с просроченным сроком годности определён Приказом МЗ РФ от 26.12.2016 N 998н «Об утверждении Административного регламента Федеральной службы по надзору в сфере здравоохранения по исполнению государственной функции по осуществлению федерального государственного надзора в сфере обращения лекарственных средств посредством организации и проведения проверок соблюдения субъектами обращения лекарственных средств требований к доклиническим исследованиям лекарственных средств, клиническим исследованиям лекарственных препаратов, хранению, перевозке, отпуску, реализации лекарственных средств, применению лекарственных препаратов, уничтожению лекарственных средств»; Письмом Министерства ФинансовРФ, Федеральной Налоговой Службой от 16 июня 2011 г. N ЕД-4-3/9486 «О порядке совершения операций с лекарственными средствами с истёкшим сроком хранения». Для недоброкачественных, фальсифицированных и контрафактных лекарственных средств порядок уничтожения определяется Постановлением Правительства от 3 сентября 2010 г. N 674 «Об утверждении правил уничтожения недоброкачественных лекарственных средств, фальсифицированных лекарственных средств и контрафактных лекарственных средств» (с изменениями на 16 января 2016 года). Утилизацию полимерной и металлической упаковки, содержащей остатки вредных веществ, нужно производить только на специализирующихся предприятиях занимающихся утилизацией отходов. Бумажные упаковки сжигают, а металлическую тару переплавляют.[2] Основные нормативные документы в области обращения с опасными отходами (с отходами фармацевтической продукции) являются:
|
