Местное лечение гнойных ран лица и шеи - В.В.ПОЛЯКОВА. Методическое пособие Смоленск, 2004 оглавление введение 3 патогенез раневого процесса 3
 Скачать 1.28 Mb. Скачать 1.28 Mb.
|
ВОЛОКНИСТО-ПОРИСТЫЕ ПЕРЕВЯЗОЧНЫЕ МАТЕРИАЛЫ (ВГШМ)НА ОСНОВЕ ВЫСОКОМОЛЕКУЛЯРНЫХ ГЛИКАНОВ ЖИВОТНОГО И МИКРОБНОГО ПРОИСХОЖДЕНИЯВ патогенезе раневого процесса важное место занимают местные ферментативные процессы. В I фазе раневого процесса выраженная воспалительная реакция обусловлена активностью ферментативных процессов. Чрезмерная их стимуляция может оказывать повреждающее действие на ткани и способствовать распространению воспалительного процесса. Принципиально новым подходом к решению проблемы лечения гнойно-воспалительных заболеваний считается лечение таких больных в условиях регулируемой активности раневых энзимов и коррекции местной ферментативной активности волокнисто-пористыми препаратами на основе полисахаридов -коллапора и аубазипора (Балин В.Н. и соавт., 1996) (рис. 2), и гликана-аубазидана и хонсурида (Мадай Д.Ю., 1998). Авторами предложен прибор и способ определения суммарной активности раневых протеолитических энзимов с помощью засвеченной и проявленной фотопленки, экспонированной в рану на 6 часов. По степени просветления фотопленки и показаниям миллиамперметра с помощью колибровочной кривой определяли активность раневых протеаз. Ими из гликана-аубазидана и хонсурида создана гамма перевязочных препаратов, разрешенных для клинического применения:
На основании экспериментально-клинических исследований авторы рекомендуют при острых гнойных поражениях тканей и органов челюстно-лицевой области, протекающих с низкой активностью раневых протеаз, для активации пекролиза местно применять коллапор (ежедневные перевязки в течение 2-3 дней), а после повышения активности последних - аубазипор и хонсурид. При высокой активности раневых протеаз (более 130 МЕ/л) в комплекс местного лечения необходимо включать волокнисто-пористые препараты с антиферментной активностью (иммобилизованная форма контрикала). Рис.2 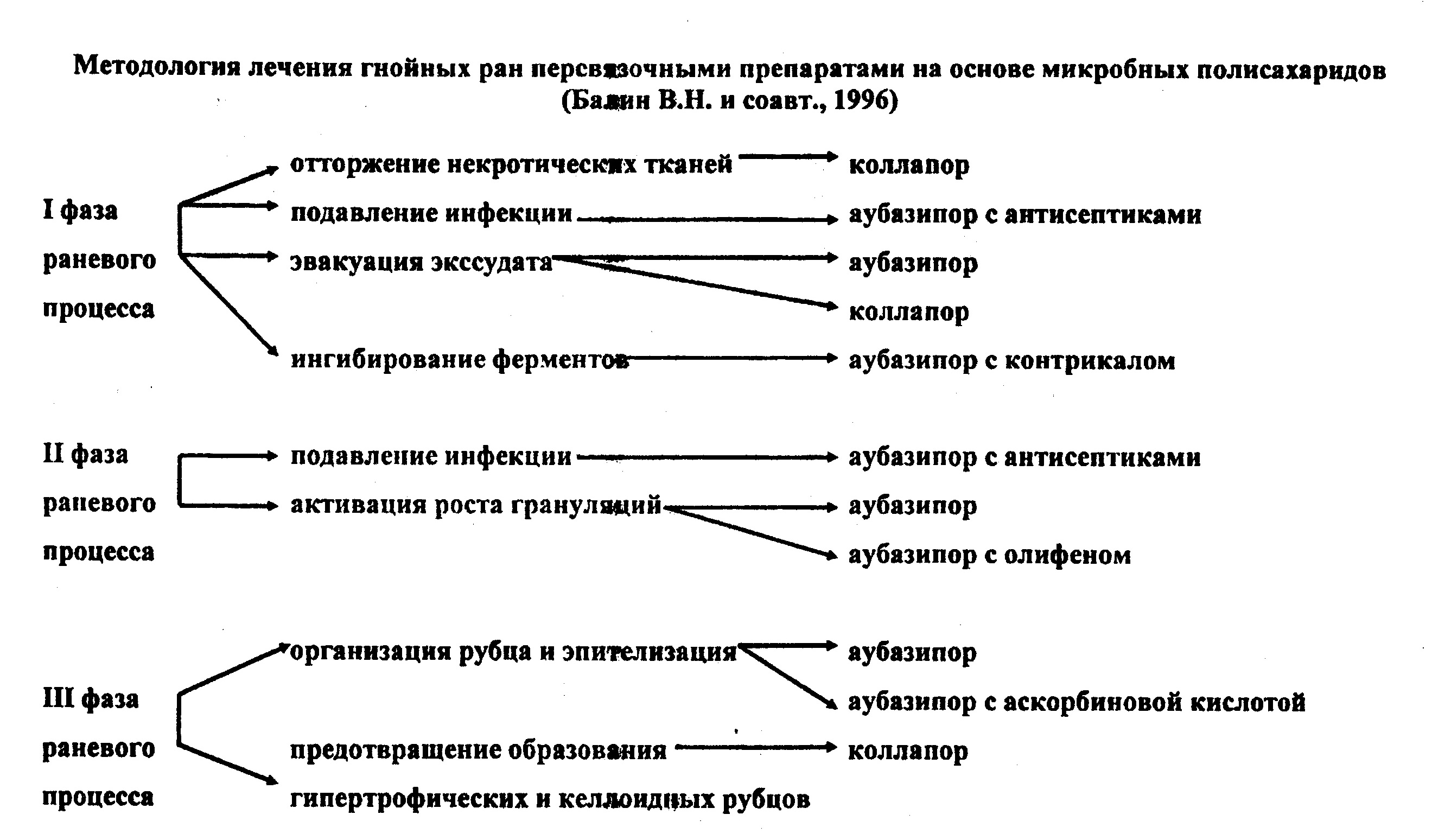 При наличии обширных некрозов показано включение в комплекс биорегулирующей терапии полисахаридных препаратов с антиоксидантной и антиги-поксантной активностями, в частности – местно - ежедневные перевязки с помощью волокнисто-пористых препаратов с проферментной антиоксидантной и антигипоксантной активностями (иммобилизованные формы контрикала, аскорбиновой кислоты и цитохрома С) до стабилизации воспалительного процесса. При благоприятном течении раневого процесса (активность раневых про-теаз 80 - 130 МЕ/л) достаточно назначать волокнисто-пористые препараты с антисептиками. Во II фазе раневого процесса при высокой активности раневых протеаз назначают препараты с антиферментной активностью. Для стимуляции фибрино-генеза - иммобилизованные формы натриевой соли аскорбиновой кислоты и цитохрома С. В III фазе раневого гистогенеза при высокой активности ферментов плазмы крови - ВППМ, оптимизирующие эпителизацию ран и организацию рубца (иммобилизованные формы натриевой соли витамина С и цитохрома С), а при низкой - препараты, предотвращающие образование гипертрофических и кел-лоидных рубцов (коллапор). Выше изложенная разработка показаний, теоретическое и патоморфологи-ческое обоснование комплексного применения полисахаридов или биологически активных препаратов, изготовленных на их основе с учетом оценки активности раневых протеаз, при лечении гнойно-воспалительных заболеваний че-люстно-лицевой области приобретает особую актуальность и имеет не только большое медицинское, но и социально-экономическое значение. ЛОКАЛЬНАЯ АУТОЦИТОКИНОТЕРАПИЯБольшое значение в развитии и течении воспалительных заболеваний отводится иммунной системе, В клинической иммунологии активно изучается новая система пептидов иммунной системы, получивших название цитокины. Особенность цитокинов в том, что они являются секретируемыми продуктами всех клеток, принимающих активное участие в иммунных процессах (лимфоциты, фагоцитарные, тучные клетки и др.), а также ряда клеточных элементов организма (фибробласты, клетки эндотелия и другие). Они играют важную роль в иммунных и воспалительных реакциях как медиаторы межклеточного взаимодействия, регулируют активность фагоцитов, опосредуют взаимодействие с клетками нелимфоидной природы. По своей природе цитокины - белки или гликопротеиды средней молекулярной массы (15 - 60 кД). Действуют они кас-кадно, то есть один или несколько цитокинов какого-либо клеточного источника запускают цитокиновую систему в других клеточных элементах. Определенный комплекс цитокинов, включающий ИЛ-1, ФНОα, ИЛ-6, ГМ-КСФ (фактор, стимулирующий образование колоний гранулоцитов / моноцитов), ФАТ (фактор, с активирующий тромбоциты) и другие определяют течение воспаления в гнойной ране. На основе цитокинов в последние годы разрабатываются эффективные фармакокинетические препараты, с успехом применяемые в лечении больных с воспалительными заболеваниями. На кафедре иммунологии Российского государственного медицинского университета разработан оригинальный метод локальной аутоцитокинотера-пии, основанный на местном применении естественной композиции цитокинов, секретируемых лимфоцитами периферической крови пациента. Этот метод имеет ряд преимуществ перед применением рекомбинантных цитокинов. Комплекс цитокинов представлен их естественной комбинацией, не оказывает токсического действия и регулируюет течение всех стадий раневого процесса. Предпосылкой для использования в лечебной практике локальной цитокиноте-рапии явились результаты экспериментальных исследований. Комплекс аутоло-гичных цитокинов ускоряет процесс заживления инфицированных ран у кроликов и препядствует развитию гнойных осложнений, снижая бактериальную об-семененность (Ковальчук Л.В., Ганковская Л.В., 1993). Нами (Полякова В.В. и соавт., 1998) проведено лечение и обследование больных с одонтогенными флегмонами, где в комплексное лечение включали локальную аутоцитокинотерапию. Цитокины получали из периферической крови больного по методу Л.В. Ковальчука и Л.В, Ганковской (1995). После промывания гнойных ран раствором фурацилина проводили дополнительное орошение раны аутоцитокинами и оставляли турунды, смоченные этим препаратом. Обработку раны цитокинами проводили со 2-х суток до момента ее очищения и появления розовых грануляций. Перевязка больных проводилась 2 раза в сутки. Уже после 2-3 раз использования локальной аутоцитокинотерапии отмечалось полное исчезновение болей в ране, нормализовывалась температура тела, улучшалось общее самочувствие больных. На 3 - 5 сутки лечения прекращалось гноетечение из ,пан, появлялись розовые грануляции, уменьшались отек и инфильтрация мягких тканей. Это дало возможность накладывать первично-отсроченные швы, что сокращало сроки лечения больных. У больных контрольной группы, лечение которых проводилось традиционным способом гноетечение из ран продолжалось до 6 - 8 суток после операции. В это время начинали уменьшаться отек и инфильтрация мягких тканей, появлялись грануляции. Вторичные швы накладывались на 7 - 8 сутки. К окончанию лечения у больных этой группы оставалось повышенным СОЭ и лейкоцитоз. Большинство из них выписывалось из клиники с улучшением на амбулаторное долечивание. Полученные нами результаты лечения дают основание считать, что использование локальной аутоцитокинотерапии в комплексной терапии больных с одонтогенными флегмонами оказывает благоприятное влияние на раневой процесс, ускоряя очищение ран от гнойно-некротических масс и появление розовых грануляций. Это позволяет накладывать первично-отсроченные швы, что дает хорошие косметические и функциональные результаты, сокращает сроки стационарного лечения больных. |
