Методичні вказівки для студентів 2 курсу фармацевтичного факультету
 Скачать 2.54 Mb. Скачать 2.54 Mb.
|
Заняття № 11ДІАЗО- ТА АЗОСПОЛУКИ. ТЕОРІЯ КОЛІРНОСТІАКТУАЛЬНІСТЬ ТЕМИ Азобарвники є найбільш розповсюдженим класом барвників. Їх застосовують для фарбування вовняних та штучних тканин, шкіри, паперу та ін. Забарвлення деяких азобарвників змінюється у залежності від рН середовища, що дозволяє використовувати їх як індикатори. Прикладом такого азобарвника є метиловий оранжевий. Діазосполуки мають велике значення в синтезі барвників, лікарських препаратів, у фармацевтичному синтезі та ін. З огляду на те, що всі азосполуки є забарвленими речовинами, реакція азосполучення широко застосовується у фармацевтичному аналізі для підтвердження справжності лікарських препаратів, що містять у своєму складі первинну ароматичну аміногрупу. Багато азосполук використовуються як хіміотерапевтичні засоби, наприклад салазопіридазин і салазодиметоксин. Таким чином, уміння інтерпретувати хімічну будову і властивості діазо- та азосполук необхідні для вивчення таких дисциплін, як фармацевтична хімія, токсикологічна хімія, фармакологія та фармакогнозія. ЦІЛІ НАВЧАННЯ Загальна ціль: Вміти визначати хімічні властивості діазо- та азосполук для застосування у фармацевтичних і токсикологічних дослідженнях. Досягнення цієї мети забезпечується конкретними цілями, що є уміннями. Конкретні цілі Вміти:
Зміст навчання Основні теоретичні питання:
3. Фізичні та хімічні властивості солей діазонію: - будова катіона арилдіазонію; - вплив рН середовища на будову діазосполук - реакції, які проходять з виділенням азоту ( механізм нуклеофільного і радикаль- ного заміщення ) - реакції, які проходять без виділення азоту ( азосполучення, відновлення). 4. Хімічні властивості азосполук: - основні властивості - відновлення - окислення. 5. Основні положення теорії колірності. Хромофори та ауксохроми. Азобарвники. Граф логічної структури ДІАЗО- ТА АЗОСПОЛУКИ  БУДОВА МОЛЕКУЛ СПОСОБИ ОТРИМАННЯ   СИНТЕЗ ПОХІДНИХ ХІМІЧНІ ВЛАСТИВОСТІ    СИНТЕЗ БАРВНИКІВ СОЛІ ДІАЗОНИЮ АЗОСПОЛУКИ    реакціі з виді лен ням азоту Основнівлас тивості   реакціі без виділення азоту відновлення    окислення.  ІДЕНТИФІКАЦІЯ   ВИКОРИСТАННЯ ДІАЗО- ТА АЗОСПОЛУК В СИНТЕЗІ ЛІКАРСЬКИХ ЗАСОБІВ Джерела інформації Обов'язкова література:
Додаткова література:
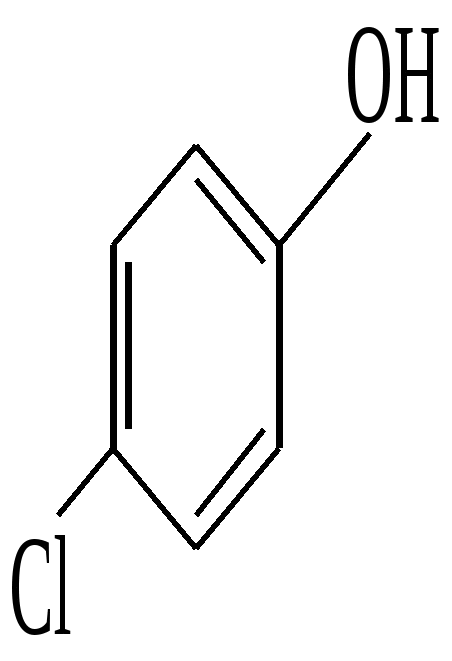
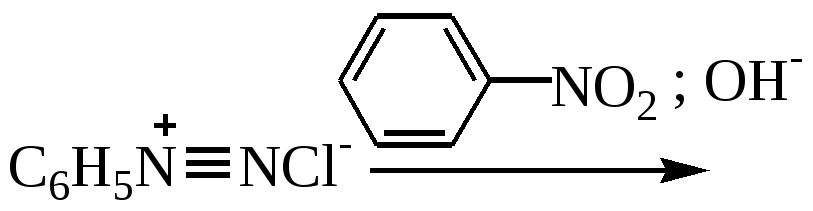
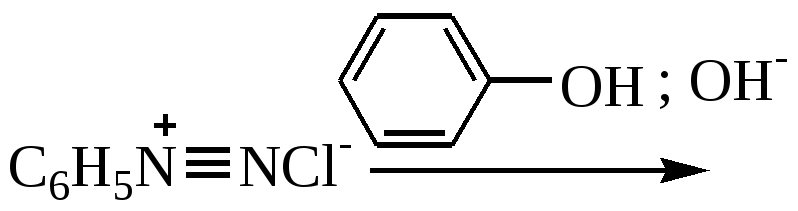
ОРІЄНТОВНА ОСНОВА ДІЇ (ООД) Інструкція з виконання лабораторних дослідів Хімічні властивості діазо- та азосполук Принцип методу: наявність в молекулах азосполук хромофорних груп може бути використана для реакцій ідентифікації нітросполук, амінів та лікарських засобів з відповідними функціональними групами. Ціль: за допомогою характерних реакцій практично довести хімічні властивості представників класів діазо- та азосполук. Обладнання та реактиви: штатив з пробирками, склянки 25 мл, пальник, універсальний індикаторний папір, йодкрохмальний папір, льодова суміш, скляні палички, пробка з газовідвідною трубкою, конц. HCl, 10 %-ний р-н HCl, 30 %-ний р-н NaNO2, анілін, N,N-диметиланілін, 1 %-ний р-н FeCl3, лужний розчин -нафтолу, 5 %-ний р-н CH3COONa. Методика виконання: Опит 34. Діазотування аніліну У велику пробірку поміщають 1 мл аніліну, 7-8 мл води і 2,5 мл концентрованої хлоридної кислоти. Суміш охолоджують в склянці з льодом до 0°С. Потім при частому струшуванні пробірки по краплях додають 1 мл 30 %-ного розчину натрия нітриту. Температура суміші не повинна підніматися вище 5 °С (регулюють шляхом додавання в реакційну суміш шматочків льоду). Після збільшення розчину натрію нітриту скляної паличкою наносять краплю розчину на йодкрохмальний папір (фільтровальний папір, оброблений калію йодидом і крохмалем). При нанесенні проби, що містить азотисту кислоту, виділяється вільний йод, який з крохмалем утворює комплекс синє-фіолетового кольору. Поява забарвлення на йодкрохмальному папері свідчить про завершення реакції діазотування. Якщо забарвлення йодкрохмального паперу не змінюється, то в реакційну суміш додатково підливають декілька крапель 30%-ного розчину натрію нітриту. Суміш перемішують і знову беруть пробу. Діазотування припиняють, коли в суміші з’являється надлишок азотистої кислоти, не зникаючий при струшуванні впродовж декількох хвилин. Отриманий прозорий розчин солі фенилдіазонию розділяють на три частини і використовують для проведення наступних дослідів. Опит 35. Розкладання солі діазонію при нагріванні У пробірку поміщають 1 мл розчину бензолдіазонію хлориду, отриманого в попередньому опиті, і злегка нагрівають в полум'ї пальника. Спостерігають бурхливе виділення бульбашок газу – азоту, яке триває надалі і без нагрівання. Після закінчення реакції пробірку закривають пробкою з газовідвідною трубкою, кінець якої опускають в суху пробірку. Розчин в пробірці нагрівають. Фенол, що утворюється в процесі розкладання солі діафонію, переганяється з водяною парою: Відчувають характерний запах фенолу. При додаванні до розчину фенолу 1 краплі 1 %-ного розчину ферруму (III) хлориду спостерігають появу фіолетового забарвлення (див. опит 56). Опит 36. Отримання кислого азобарвника (судан I) В пробірку поміщають декілька кристалів -нафтолу і додають 2-3 краплі 10 %-ного розчину натрію гідроксиду. До прозорого лужного розчину -нафтола підливають 1 мл розчину солі діазонію, отриманого в опиті 34. Спостерігають утворення оранжево-червоного осаду азобарвника -фенилазо--нафтолу (судан I) : Опит 37. Отримання основного азобарвника п-диметиламино-азобензола і його індикаторні властивості У пробірку поміщають 1 краплю N,N-диметиланіліну, 5 крапель води і додають по краплях концентровану хлоридну кислоту до утворення прозорого розчину. Вміст пробірки охолоджують, підливають 1 мл розчину солі діазонію, отриманого в опиті 34, і енергійно струшують. При додаванні в пробірку 2-3 крапель 5 %-ного розчину натрію ацетату спостерігають утворення жовто-помаранчевого осаду основного барвника – п-диметиламиноазобензолу. У пробірці змішують декілька крапель розчину утвореного азобарвника і 5-6 мл води. При наступному додаванні в пробірку декількох крапель 10 %-ного розчину хлоридної кислоти жовте забарвлення розчину зникає і з'являється червоне. При підлуговуванні знову відновлюється жовте забарвлення розчину : Хід роботи:
завдання для перевірки досягнення конкретних цілей навчання Тест 1 Для назв органічних сполук використовують замісникову номенклатуру ІUРАС? Виберіть хімічну назву, відповідно запропонованій номенклатурі, для приведеної сполуки:  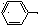  NN NН2 NN NН2
Тест 2 Згідно з номенклатурою ІUРАС укажіть серед запропонованих формул 4-гідроксіазобензол:
Тест 3 Солі діазонію є формою існування діазосполук із загальною формулою ArN2X. За допомогою якої реакції можна одержати такі солі з аріламінів?
Тест 4 Представником азосполук є азобензол, що має формулу: 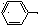  NN NNЗазначте, за допомогою якої реакції можна одержати цю сполуку?
Тест 5 Діазосполуки можуть існувати у двох формах : солі діазонію й діазотати. Вони будуть мати іонну будову [Ar-N+N]X-, якщо:
Тест 6 Представником азосполук є азобензол, що має формулу: 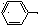  NN NNЯка з наведених реакцій використовується для одержання цієї сполуки? А 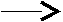  . C6H5NO2 [H ; HCl . C6H5NO2 [H ; HCl В 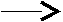 . C6H5NH2 KNO2+ HCl . C6H5NH2 KNO2+ HCl С 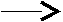 . C6H5NO2 [H ; KOH . C6H5NO2 [H ; KOH D 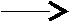 . C6H5NH2 CH3COCl . C6H5NH2 CH3COCl Е 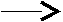 . C6H5NH2 НNO3 конц . C6H5NH2 НNO3 конц Тест 7 Соли діазонію можуть вступати у реакції з виділенням азоту и без виділення азоту. Вкажіть, яка із запропонованих реакцій проходить із виділенням азоту? А 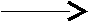 . С6Н5-N+ºNCl- KCN; t; CuCN . С6Н5-N+ºNCl- KCN; t; CuCN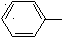 В 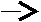 . С6Н5-N+ºNCl- + N(CH3)2 H+ . С6Н5-N+ºNCl- + N(CH3)2 H+С 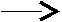 . С6Н5-N+ºNCl-+ C2H5OH t . С6Н5-N+ºNCl-+ C2H5OH t  D 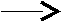 . С6Н5-N+ºNCl- + OH OH- . С6Н5-N+ºNCl- + OH OH-Е. С6Н5-N+ºNCl- + CH3-NH2 ® Тест 8 Зазначте, в результаті якої із запропонованих реакцій утворюється похідне азобензолу?
Тест 9 За участю азогрупи азосполуки вступають у реакції окислення та відновлення. Укажіть, які сполуки утворюються при відновлені азосполук хлоридом олова (II) в середовищі хлороводневої кислоти:
Тест 10 За участю азогрупи азосполуки вступають у реакції окислення та відновлення. Укажіть, які сполуки утворюються при окислені азосполук пероксикислотами:
Тест 11 Ауксохроми – це групи атомів в молекулі, які самі не спроможні викликати забарвлення, але при наявності хромофорів здатні посилювати колір. Зазначте, яка із запропонованих груп є ауксохромом?
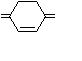
Тест 12 Хромофорами називаються групи атомів, наявність яких в молекулі дає забарвлення речовині. Зазначте, яка із запропонованих груп є хромофором?
Еталони відповідей: 1.A, 2.D, 3.A, 4.E, 5.D, 6.C, 7.C, 8.C, 9.B, 10.C, 11.E, 12.A. КОРОТКІ МЕТОДИЧНІ ВКАЗІВКИ ДО ПРОВЕДЕННЯ ПРАКТИЧНОГО ЗАНЯТТЯ На занятті перевіряється підготовка студентів до проведення практичного заняття, проводиться інструктаж з техніки безпеки при роботі з хімічними реактивами. Під керівництвом викладача виконуються завдання для самостійної роботи. Потім студенти приступають до виконання лабораторної роботи, використовуючи інструкцію робочого журналу. Після виконання лабораторної роботи студенти оформлюють протокол, роблять висновки до роботи, що перевіряється і контролюється викладачем. Проводиться підсумковий тестовий контроль за темою, підводяться підсумки заняття. |