Методичка-Органічна хімія. Методичні вказівки для студентів до практичних занять. Заняття Тема Основи будови органічних сполук. Техніка безпеки. Ізомерія, номенклатура, класифікація органічних сполук
 Скачать 1.57 Mb. Скачать 1.57 Mb.
|
Властивостями моносахаридівДослід 1. Оксидація альдоз і кетоз йодом. У дві пробірки окремо прилити по 5 крапель розчинів глюкози =0,5% і фруктози і =0,5%, долити по 1-2 краплі розчину йоду =2% та краплями розчину лугу (до знебарвлення розчинів). Зазначити час додавання лугу. Залишити обидві пробірки на 7-8 хвилин а потім у кожну пробірку прилити 2-3 краплі розчину сульфатної кислоти. Що спостерігається? Написати рівняння оксидації глюкози. Дослід 2. Загальна реакція на вуглеводи (проба Моліша). У пробірку внести 1 см3 0,5%-го розчину глюкози і додати 2 краплі спиртового розчину -нафтолу. Потім обережно приливати по стінці пробірки 2 см3 конц. сульфатної кислоти. Що спостерігається на межі поділу рідин? Через деякий час суміш змішати, а через 1 хвилину долити воду. Що змінилося? Чому? Дослід 3. Реакція “срібного дзеркала” (проба Толенса). У пробірку налити 2 краплі 0,2н розчину аргентум нітрату (краплями) і 2 краплі 2н розчину лугу. До одержаної суміші прилити 3-4 краплі 2н розчину аміаку (до повного розчинення осаду) і 1-2 краплі 0,5% розчину глюкози. Суміш нагріти на водяній ванні. Що при цьому спостерігається? Написати рівняння реакції. Дослід 4. Відновлення купрум (ІІ) гідроксиду моносахаридами (проба Троммера). У пробірку прилити 2-3 краплі 0,5% розчину глюкози і 6-8 крапель 2н розчину лугу і краплями додати 0,2н розчину купрум (ІІ) сульфату. Вміст пробірки нагріти на водяній бані. Що спостерігається? Написати рівняння реакції. Дослід 5. Реакція Селіванова на кетози. У дві пробірки помістити по 1-2 краплі реактиву Селіванова (резорцин + луг + конц. хлоридна кислота). В одну з них прилити 2 краплі 0,5% розчину глюкози, а в другу 2 краплі 0,5% розчину фруктози. Пробірки нагріти на водяній банні. Які зміни відбулися в пробірці з фруктозою? Дослід 6. Якісна реакція на пентози. У пробірку внести шар тирси, змоченої окремо приготовленою сумішшю конц. НСl і води (1:1). Все перемішати і прокип’ятити. Смужку фільтрувального паперу, попередньо змочену сумішшю 2 краплями аніліну і 4 краплями 2н ацетатної кислоти, опустити у пробірку з киплячою сумішшю. Як змінилось забарвлення? Написати рівняння реакції одержання фурфуролу. Дослід 7. Якісна реакція на глюкозу як багатоатомний спирт. До 1-2 крапель 5% розчину глюкози долити 2-4 краплі розчину купрум (ІІ) сульфату і лугу. Вміст пробірки струсити. Що спостерігається? Написати рівняння реакції утворення комплексної сполуки. Дослід 8. Взаємодія глюкози з розчином Cа(OH)2. До 2 см3 20% розчину глюкози прилити, перемішуючи, вапняне молоко (СаСl2 + NaOH). Спостерігати за розчиненням осаду. Написати рівняння утворення кальцій глюконату. Дослід 9. Відношення глюкози до фуксинсульфітної кислоти. У дві пробірки внести по 1 см3 розчину фуксинсульфітної кислоти. В одну долити 1 см3 10% глюкози, а в другу 1 см3 10% розчину формальдегіду. Через деякий час у пробірці з формаліном утвориться фіолетово-рожеве забарвлення, а з глюкозою – ні. Чому? Відповідь обмотивуйте. Дослід 10. Фармакопейна проба на ідентичність глюкози. До 1 см3 розчину препарату прилити 5 см3 реактиву Фелінга 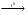 цегляно-червоний осад. цегляно-червоний осад.ЗАНЯТТЯ №33 Тема:Вуглеводи. Ди- і полісахариди. Актуальність теми:Полісахариди – це природні біополімери, які складаються з великої кількості молекул моносахаридів. До полісахаридів відносяться багато продуктів рослинного походження (крохмаль, целюлоза, пектинові речовини), тваринного (глікоген, хітин) і бактеріального (декстрани). Всі вони відіграють важливу біологічну роль і використовуються як лікарські препарати. Навчальні цілі:Теоретичне і практичне засвоєння будови молекул, властивостей та застосування ди- і полісахаридів. Малий практикум. Знати:
Вміти:
Самостійна позааудиторна робота
Контрольні питання
Самостійна аудиторна робота
Теоретична частинаДисахаридами називають вуглеводи, молекули яких складаються з двох залишків моносахаридів однакової або різної природи, з’єднаних між собою глікозидним зв’язком. Будучи О-глікозидами, дисахариди легко гідролізуються в кислому середовищі, з утворенням двох молекул моносахаридів. У залежності від способу утворення глікозидного зв’язку, дисахариди поділяються на дві групи – відновні та невідновні. Представниками відновних дисахаридів є мальтоза, целобіоза та лактоза, а до невідновних відноситься сахароза. Молекула мальтози складається із двох залишків D-глюкопіранози з’єднаних 1,4-глюкозидним зв’язком. Лактоза - з залишків D-галактопіранози та D-глюкопіранози, сполучених 1,4-глікозидним зв’язком, целобіоза складається з двох залишків D- глюкопіранози, зв’язаних 1,4-глікозидним зв’язком. Залишок глюкози напівацитального гідроксилу має β-кофігурацію. Невідновний дисахарид – сахароза складається з залишків α-D-глюкопіранози і β-D-фруктофуранози. Дисахариди проявляють властивості моносахаридів, які утворюються при їх гідролізі. До полісахаридів відносять сполуки, молекули котрих містять більше десяти моносахаридних ланок, сполучених О – глікозидним зв’язком. Вони поділяються на гомополісахариди і гетерополісахариди. До гомополісахаридів відносяться крохмаль, який складається з амілози і амілопектину, глікоген (тваринний крохмаль) і целюлоза. До полісахаридів бактеріального походження відносяться декстрани, які використовуються у виробництві плазозамінників, а також пектинові речовини. До гетерополісахаридів відносяться полісахариди сполучної тканини, гіалуронова кислота, гепарин та рослинні камеді. Полісахариди при реакціях гідролізу утворюють моносахариди. Медичні препарати: сахароза, лактоза, крохмаль, поліглюкін, інулін, колодій, карбоксиметилцелюлоза, гепарин, хітін, рослинні камеді та ін. Практична роботаВластивості ди- і полісахаридів. Дослід 1. Відновлююча здатність лактози. У пробірку прилити 1-2 краплі 1% розчину лактози, 4 краплі 10% лугу і 1-2 краплі 2% купрум (ІІ) сульфату . Що спостерігається? Одержану суміш розвести водою і нагріти верхній шар. Як змінюється забарвлення? Чому? Дослід 2. Відсутність відновлюючих властивостей у сахарози. Дослід проробити аналогічно попередньому, тільки замість розчину лактози взяти розчин сахарози. Нагрівати не до кипіння. Чи відбуваються зміни? Чому? Дослід 3. Добування кальцій сахарату. У пробірку прилити по 2 см3 вапняного молока (CaCl2 + NaOH) і розчину сахарози. При нагріванні випадає осад трикальцій сахарату складу: С12Н22О113Са(ОН)2, який малорозчинний у гарячій воді, а при охолодженні розчиняється. Написати рівняння реакції утворення кальцій сахарату. Дослід 4. Добування озазонів дисахаридів (синтез). У дві пробірки внести по ложечці натрій ацетату і гідрохлорид фенілгідразину і прилити до них по 1 см3 розчину сахарози. Вміст пробірок нагріти на водяній бані протягом 5 хвилин Після охолодження розчинів спостерігати за випаданням кристалів озазонів. Кристали розглянути під мікроскопом. Зарисувати їх форму в протоколах. Написати рівняння реакції утворення озазону. Дослід 5. Якісна реакція на сахарозу. До 2 см3 2% розчину сахарози і прилити 2-3 краплі 5% спиртового розчину -нафтолу. Обережно по стінці (подалі від очей) приливати 1 см3 конц. H2SO4. На межі поділу утворюється червоно-фіолетове кільце. Зробити висновок. Дослід 6. Визначення питомого обертання розчину сахарози. Трубку поляриметра сполоснути 2-3 рази розчином сахарози, а потім заповнивши трубку розчином, визначити знак і кут обертання. Розчин сахарози залишити в трубці і через годину повторити визначення. Кут залишається сталим, що означає, що сахароза в розчині не здатна до мутаротації. Дослід 7. Виявлення крохмалю з допомогою йоду. У пробірці змішати 1 см3 розчину крохмалю з 1-2 краплями розчину Люголя. Суміш нагріти і знову охолодити. Дослід повторити декілька раз. Які зміни відбуваються в пробірці? Пояснити суть процесу. Дослід 8. Відношення крохмалю до реактиву Фелінга. У пробірці змішати 1 см3 1% крохмального клейстеру з 1 см3 реактиву Фелінга. Вміст пробірки нагрівати на водяній бані. Пояснити причину відсутності зміни забарвлення. Зробити висновки. Дослід 9. Ферментний гідроліз крохмалю. У пробірці змішати 5 см3 крохмального клейстеру з невеликою кількістю власної слини. Після нагрівання пробірки в руці протягом 5 хвилин випробувати суміш реактивом Люголя. Пояснити суть процесу. Написати рівняння гідролізу крохмалю. Дослід 10. Кислотний гідроліз целюлози. У пробірці змішати кусочки фільтрувального паперу з конц. сульфатною кислотою. Добре перемішувати скляною паличкою до повного розчинення паперу і утворення в’язкого розчину. До частини одержаного розчину прилити води, прокип’ятити 20 хвилин і долити по декілька крапель реактиву Фелінга, і 10% розчину лугу. Нагріти. Спостерігати за зміною забарвлення. Гідролізована клітковина проявляє відновні властивості. Гідроліз проходить за схемою: (C6H10O5)n (C6H10O5)n C12H22O11 C6H12O6 целюлоза амілоїд целобіоза глюкоза ЗАНЯТТЯ №33 Тема. Омилювані ліпіди. Жири. Воски. Актуальність теми. Омилювані ліпіди є структурними компонентами клітинних мембран та служать резервним енергетичним матеріалом, а також можуть бути попередниками у синтезі інших біологічно-активних сполук, виконувати роль барєру, який захищає організм від термічного та механічного впливів. Навчальні цілі: Знати:
Вміти:
Самостійна позааудиторна робота 1. Теоретично підготуватись по контрольних питаннях даної теми. 2.Який об'єм водню (н.у.) необхідний для одержання 2 т твердого тристеаринового жиру з триолеату?. 3.Пояснити миючі властивості мила. 4. Поверхнево – активні речовини, їх значення і застосування. 5. Напишіть рівняння лужного гідролізу триацилгліцерину, до складу якого входять ліноленова, лінолева, пальмітинова кислоти. Назвіть продукти реакції. 6. Напишіть рівняння реакції триолеїну з такими реагентами: Вr2; НІ. Поясніть значення цих реакцій. 7. Що таке кислотне число, йодне число, число омилення? 8. До якого класу сполук належать жири і воски? Що являє собою бджолиний віск? 9. Напишіть структурні формули таких сполук: 1) 1-пальмітоїлдистеароїлгліцерину; 2) триолеїну. 10. Оформити три графи протоколу. Контрольні питання 1. Ліпіди, їх класифікація та біологічне значення. 2. Номенклатура та ізомерія жирів. 3. Прості ліпіди. Воски. Бджолиний віск. Спермацет. 4. Жири, їх склад та властивості. Продукти оксидації жирів. 5. Омилення жирів, їх гідроліз. Мило, синтетичні миючі засоби (СМЗ). 6. Гідрування жиру. Штучні жири. Твіни. 7. Аналітичні характеристики жирів (число омилення, йодне число). 8. Вищі жирні кислоти – структурні компоненти омилюванних ліпідів. 9. Насичені вищі жирні кислоти. Стеарин. 10. Ненасичені вищі жирні кислоти. Лінетол. Самостійна аудиторна робота 1. Проробити досліди передбачені у методичній вказівці. 2. Результати спостережень і висновки внести у протокол. 4. Написати тестовий контроль або самостійне індивідуальне завдання. 5. Оформити протокол і захистити його у викладача 6. Виписати з даної теми медичні препарати вказати їх фарма-кологічну дію та застосування. 7. Написати формули твердого і рідкого жирів, мила. 8. Синтетичні миючі засоби. Теоретична частинаЛіпіди – це природні органічні сполуки, похідні вищих аліфатичних кислот і спиртів. Жири – це естери, утворені триатомним спиртом гліцерином і вищими карбоновими кислотами. Жири, що містять однакові залишки кислот (R=R/=R// ), називають простими, а з різними залишками – змішаними. Більшість природних жирів відрізняються відносно невеликим набором жирних кислот (приблизно 5-8). Найважливіші з них є дві насичені кислоти – пальмітинова і стеаринова та дві ненасичені – олеїнова і ліноленова. Насичені кислоти входять до складу твердих (тваринних) жирів – яловичий, свинячий, а ненасичені – до рідких (рослинних) – жирів, які називають оліями, наприклад, соняшникова, оливкова, лляна та ін. Способи добування:
Жири легші за воду і в ній не розчиняються, проте добре розчинні в органічних розчинниках, зокрема в петролейному ефірі. Жири, за хімічними властивостями подібні до естерів, проте мають свої особливості. Найважливішою реакцією є гідроліз жирів, який відбувається під дією кислот, лугів або ферментів. За наявності лугу проводять лужний гідроліз (омилення жирів) за температури 220-2600С. Солі вищих жирних кислот називають милами, а реакцію лужного гідролізу жирів, при якій утворюються мила, - омиленням. Воски – це естери вищих карбонових кислот і високомолекулярних спиртів, які містять парну кількість атомів Карбону в кислотних і спиртових залишках. Воски поділяють:
Воском прийнято вважати також озокерит (гірський віск). Воски бувають м’які і тверді. До м’яких належить ланолін і спермацет. Ідентифікацію проводять за допомогою фізичних та хімічних методів. Медичні препарати: жири, твіни, спермацет, віск та ін. Практична робота |
