Микробиология. Общая микробиология
 Скачать 476.77 Kb. Скачать 476.77 Kb.
|
|
Бактериофаги. Взаимодействие фага с бактериальной клеткой. Умеренные и вирулентные фаги. Лизогения и фаговая конверсия. Бактериофаги– вирусы бактерий. История открытия бактериофага связана с именами Н.Ф. Гамалеи, наблюдавшего спонтанный лизис сибиреязвенных бактерий в 1898г.Французский ученый Ф.Д, Эррель подробно изучил взаимодействие фага и бактерий и сделал заключение, что открытый им литический агент является вирусом бактерий и назвал его «бактериофагом» - пожирателем бактерий. Бактериофаги широко распространены: они выявлены у большинства бактерий, а также у других микроорганизмов, например, у грибов и поэтому их часто называют фагами. Наиболее детально изучена структура крупных фагов, к которым относятся фаги E. Coli (Т2, Т4, Т6). Классификация бактериофагов Нитевидные фаги с длинным отростком и сокращающимся чехлом с длинным отростком без сокращающегося чехла с коротким отростком с аналогом отростка без отростка Они состоят из головки икосаэдрического типа, в которой заключена или ДНК, или РНК. Большинство фагов содержат двунитевую ДНК, замкнутую в кольцо. Хвостовой отросток имеет внутри полый цилиндрический стержень, сообщающийся с головкой, а снаружи – чехол, способный к сокращению наподобие мышцы. Чехол присоединен к воротничку, окружающему стержень около головки. Хвостовой отросток заканчивается шестиугольной базальной пластинкой с шипами, от которых отходят нитевидные структуры – фибриллы. 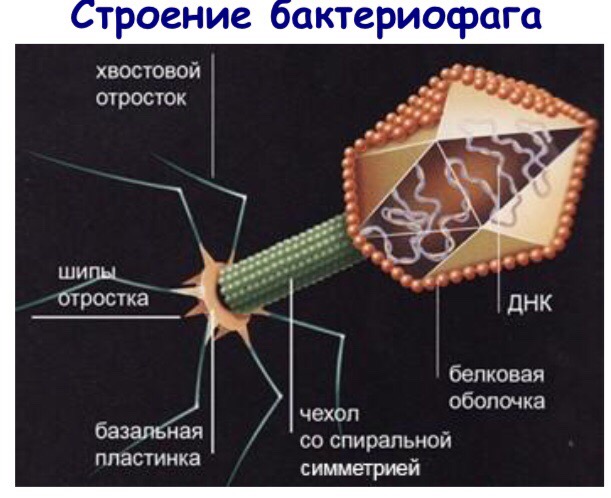 Вирулентные бактериофаги: продуктивный тип; литический цикл Умеренные бактериофаги: интегративный тип; лизогения; фаговая конверсия. Вирулентные (литические), вызывающие продуктивную инфекцию и лизис бактериальной клетки; Умеренные бактериофаги - вызывают латентную инфекцию и ассоциацию генома вируса с бактериальной хромосомой. Умеренные фаги, в отличие от вирулентности, не вызывают гибели бактериальных клеток и при взаимодействии с ней переходят в неинфекционную форму фага, называемую профагом. Профаг — геном фага, ассоциированный с бактериальной хромосомой. Лизогения-это взаимодействие может происходить по интегративному типу. Отражает потенциальную способность лизогенных бактерий к лизису при освобождении профага из состава бактериального генома и перехода в вирулентный фаг, способный репродуцироваться. Фаговая конверсия- изменение фенотипа бактериальной клетки (антигенной характеристики, токсинообразования, чувствительности к другим фагам и т. п.), обусловленное включением в ее хромосому генома умеренного фага. Методы обнаружения бактериофагов: метод Аппельмана, метод Грация. Фаготипирование бактерий. Применение фагов в медицине и биотехнологии. Получение препаратов бактериофагов. Метод Аппельмана: метод определения литической активности фага на жидких питательных средах путем установления его максимального разведения, вызывающего полный лизис бульонной культуры чувствительных бактерий. Метод Грация метод титрования фага, заключающийся в определении количества активных фаговых частиц в 1 мл субстрата путем внесения образца в полужидкий агар (0,7%), содержащий чувствительную к фагу культуру, с последующим наслоением смеси на плотный агар (1,5%) в чашке Петри, термостатированием и подсчетом количества негативных колоний. Фаготипирование- способ определения принадлежности выделенной и идентифицированной до вида культуры к тому или иному фаговару. Используют 2 подхода. Сущность первого состоит в установлении свойств, полученных из лизогенной культуры фагов (литического спектра, антигенной специфичности и др.). Сущность второго, более распространенного, подхода базируется на выявлении спектра чувствительности выделенной культуры к набору стандартных типовых фагов. Если фаговар культуры соответствует типовому фагу, наступает лизис культуры, проявляющийся в отсутствии роста, в то время как на месте нанесения др. фагов наблюдается сплошной рост микробов. Для Ф. необходимы молодая (4 - 6-часовая) культура исследуемого штамма, идентифицированного до вида или подвида; набор стандартных типовых фагов в критических тест-разведениях (в максимальном разведении фага, вызывающем сплошной лизис гомологичной культуры); чашки Петри со стандартной свежеприготовленной и хорошо высушенной средой. Применение фагов с лечебными и профилактическими целями проводится сравнительно редко. Это связано с большим количеством отрицательных результатов, которые объясняются следующими причинами: 1) Строгой специфичностью фагов, лизирующих только те клетки бактериальной популяции, которые снабжены соответствующими рецепторами, вследствие чего фагорезистентные особи, имеющиеся в каждой популяции, полностью сохраняют свою жизнеспособность. 2) Широким применением более эффективных этиотропных средств- антибиотико, не обладающих специфичностью бактериофагов. В настоящее время препараты бактериофагов применяются для лечения дизентирии, сальмонеллеза, гнойной инфекции, вызванных антибиотико-резистентными бактериями. Культуру засевают сплошным газоном на чашку с питательной средой, дают ей впитаться в агар и на поверхность посева пастеровской пипеткой, штампом-репликатором или калиброванной петлей наносят типовые фаги. На второй день учитывают спектр чувствительности культуры к фагам. Результаты используют для эпидемиологического анализа. Микрофлора организма человека. Биотопы. Понятие об аутохтонных, аллохтонных, резидентных и транзиторных микроорганизмах. Значение нормальной микрофлоры. Организм человека заселен (колонизирован) более чем 500 видов микроорганизмов, составляющих нормальную микрофлору человека, находящихся в состоянии равновесия (эубиоза) друг с другом и организмом человека. Микрофлора представляет собой стабильное сообщество микроорганизмов, т.е. микробиоценоз. Она колонизирует поверхность тела и полости, сообщающиеся с окружающей средой. Место обитания сообщества микроорганизмов называется биотопом. В норме микроорганизмы отсутствуют в легких и матке. Различают нормальную микрофлору кожи, слизистых оболочек рта, верхних дыхательных путей, пищеварительного тракта и мочеполовой системы. Среди нормальной микрофлоры выделяют резидентную и транзиторную микрофлору. Резидентная (постоянная) облигатная микрофлора представлена микроорганизмами, постоянно присутствующими в организме. Транзиторная (непостоянная) микрофлора не способна к длительному существованию в организме. Микрофлора кожи имеет большое значение в распространении микроорганизмов в воздухе. На коже и в ее более глубоких слоях (волосяные мешочки, просветы сальных и потовых желез) анаэробов в 3—10 раз больше, чем аэробов. Кожу колонизируют пропионибактерии, коринеформные бактерии, стафилококки, стрептококки, дрожжи Pityrosporum, дрож-жеподобные грибы Candida, редко микрококки, Мус. fortuitum. На 1 см2 кожи приходится менее 80 000 микроорганизмов. В норме это количество не увеличивается в результате действия бактерицидных стерилизующих факторов кожи. В верхние дыхательные пути попадают пылевые частицы, нагруженные микроорганизмами, большая часть которых задерживается в носо- и ротоглотке. Здесь растут бактероиды, коринеформные бактерии, гемофильные палочки, пептококки, лактобактерии, стафилококки, стрептококки, непатогенные нейссерии и др. Трахея и бронхи обычно стерильны. Микрофлора пищеварительного тракта является наиболее представительной по своему качественному и количественному составу. При этом микроорганизмы свободно обитают в полости пищеварительного тракта, а также колонизируют слизистые оболочки. В полости рта обитают актиномицеты, бактероиды, бифи-цобактерии, эубактерии, фузобактерии, лактобактерии, гемофильные палочки, лептотрихии, нейссерии, спирохеты, стрептококки, стафилококки, вейлонеллы и др. Обнаруживаются также грибы рода Candida и простейшие. Ассоцианты нормальной микрофлоры и продукты их жизнедеятельности образуют зубной налет. Микрофлора желудка представлена лактобациллами и дрожжами, единичными грамотрицательными бактериями. Она несколько беднее, чем, например, кишечника, так как желудочный сок имеет низкое значение рН, неблагоприятное для жизни многих микроорганизмов. При гастритах, язвенной болезни желудка обнаруживаются изогнутые формы бактерий — Helicobacter pylori, которые являются этиологическими факторами патологического процесса. В тонкой кишке микроорганизмов больше, чем в желудке; здесь обнаруживаются бифидобактерии, клостридии, эубактерии, лактобациллы, анаэробные кокки. Наибольшее количество микроорганизмов накапливается в толстой кишке. В 1 г фекалий содержится до 250 млрд микробных клеток. Около 95 % всех видов микроорганизмов составляют анаэробы. Основными представителями микрофлоры толстой кишки являются: грамположительные анаэробные палочки (бифидобактерии, лактобациллы, эубактерии); грамположительные спорообразующие анаэробные палочки (клостридии, перфрингенс и др.); энтерококки; грамотрицательные анаэробные палочки (бактероиды); грамотрицательные факультативно-анаэробные палочки (кишечные палочки и сходные с ними бактерии. Микрофлора толстой кишки — своеобразный экстракорпоральный орган. Она является антагонистом гнилостной микрофлоры, так как продуцирует молочную, уксусную кислоты, антибиотики и др. Известна ее роль в водно-солевом обмене, регуляции газового состава кишечника, обмене белков, углеводов, жирных кислот, холестерина и нуклеиновых кислот, а также продукции биологически активных соединений — антибиотиков, витаминов, токсинов и др. Морфокинетическая роль микрофлоры заключается в ее участии в развитии органов и систем организма; она принимает участие также в физиологическом воспалении слизистой оболочки и смене эпителия, переваривании и детокси-кации экзогенных субстратов и метаболитов, что сравнимо с функцией печени. Нормальная микрофлора выполняет, кроме того, антимутагенную роль, разрушая канцерогенные вещества. Пристеночная микрофлора кишечника колонизирует слизистую оболочку в виде микроколоний, образуя своеобразную биологическую пленку, состоящую из микробных тел и экзополи-сахаридного матрикса. Экзополисахариды микроорганизмов, называемые гликокаликсом, защищают микробные клетки от разнообразных физико-химических и биологических воздействий. Слизистая оболочка кишечника также находится под защитой биологической пленки. Важнейшей функцией нормальной микрофлоры кишечника является ее участие в колонизационной резистентности, под которой понимают совокупность защитных факторов организма и конкурентных, антагонистических и других особенностей анаэробов кишечника, придающих стабильность микрофлоре и предотвращающих колонизацию слизистых оболочек посторонними микроорганизмами. Нормальная микрофлора влагалища включает бактероиды, лактобактерии, пептострептококки и клостридии. Представители нормальной микрофлоры при снижении сопротивляемости организма могут вызвать гнойно-воспалительные процессы, т.е. нормальная микрофлора может стать источником аутоинфекции, или эндогенной инфекции. Она также является источником генов, например генов лекарственной устойчивости к антибиотикам. Дисбактериоз, причины его возникновения и методы коррекции (пробиотики, пребиотики и симбиотики). Эубиоз (от греч. еu – хорошо и bios – жизнь) – состояние динамического равновесия между компонентами экосистемы «внешняя среда – макроорганизм – микрофлора» и связанное с ним состояние здоровья. Дисбактериоз (от греч. dys – приставка, означающая отрицание, и bacteria) – изменения количественного и качественного состава нормальной микрофлоры. Дисбактериоз приводит к состоянию нарушенного функционирования составных частей экосистемы «внешняя среда – макроорганизм – бактериальная микрофлора», в результате чего развивается заболевание, усугубляется болезнь и даже может наступить смерть макроорганизма. Иногда используется более широкое понятие дисбиоз, характеризующее нарушение равновесия между макроорганизмом и всеми группами микроорганизмов, населяющих его, включая вирусы, грибы, простейшие, гельминты. Под это понятие подпадают такие широко распространенные заболевания, как рота- и энтеровирусные заболевания, вирусные гепатиты, грипп, ОРВИ и другие вирусные инфекции, туберкулез, микозы, описторхоз, лямблиоз, гельминтозы и т. д. В настоящее время условно выделяют четыре степени кишечного дисбактериоза: 1-я степень, или латентная, компенсированная форма – наблюдаются незначительные количественные изменения в аэробной части микрофлоры, увеличение или уменьшение количества эшерихий. 2-я степень (субкомпенсированная форма) – наряду с количественными, наблюдаются качественные изменения эшерихий, снижается количество бифидобактерий, увеличивается количество условно-патогенных бактерий, псевдомонад, грибов. 3-я степень – значительно снижен уровень бифидо- и лактобактерий, резко изменено количество эшерихий. Создаются условия для развития условно-патогенной флоры. Тяжесть клинических симптомов, кишечные дисфункции, а также степень декомпенсации нарастают. 4-я степень – бифидофлора резко снижена или отсутствует, значительно уменьшено количество лактофлоры, значительные количественные и качественные изменения эшерихий, растет число условно-патогенных микробов в различных ассоциациях. Функциональные расстройства со стороны различных органов желудочно-кишечного тракта могут сопровождаться деструктивными изменениями кишечной стенки, что чревато развитием бактериемии и сепсиса. Микрофлора может выявляться в других органах и биологических средах, которые в норме стерильны (кровь, моча и др.), появляются дополнительные очаги инфекции. Основные причины дисбактериоза. Экзогенные причины: • Ухудшение экологического состояния антропогенного генеза; воздействие ксенобиотиков (промышленных и бытовых загрязнителей, биохимически чужеродных соединений, пестицидов, гербицидов, нитратов, нитритов, стимуляторов роста и т. д.) • Воздействие радиации, в том числе в малых дозах; избыточное ультрафиолетовое облучение • Несбалансированное питание (дефицит пищевых волокон, микро- макроэлементов, избыток консервированных и рафинированных продуктов, недостаток витаминов и т. д.) • Неадекватное использование антибиотиков • Кишечные инфекции как бактериальной, так и вирусной этиологии (сальмонеллез, шигеллез, иерсиниоз, кампилобактериоз, рота- и энтеровирусные заболевания и т. д.) • Высокая степень урбанизации и связанная с ней высокая вероятность передачи и быстрого распространения различных инфекционных заболеваний • Физический и эмоциональный стресс («медвежья болезнь») • Резкая смена климатических и географических поясов («диарея путешественника»), сезонные колебания • Химио- и гормонотерапия; лечение цитостатиками и иммунодепрессантами; регулярное употребление слабительных раздражающего действия • Гиподинамия • Злоупотребление алкоголем Эндогенные причины: • Возраст (младенческий и старческий) • Хронические воспалительные заболевания ЖКТ, особенно с секреторной недостаточностью; стойкие дискинезии ЖКТ • Аномалии строения ЖКТ, врожденные и приобретенные вследствие травм, заболеваний и операций • Иммунодефицитные состояния различного происхождения, хронические инфекции • Заболевания обмена веществ (в том числе сахарный диабет, атеросклероз и другие) • Аллергии, особенно связанные с ЖКТ • Онкологические заболевания 3. Санитарная микробиология Санитарная микробиология. Методы и задачи. Понятие о санитарно-показательных микроорганизмах. Главной задачей санитарной микробиологии является раннее обнаружение патогенной микрофлоры в окружающей среде. Выделяемые в этих случаях микробы служат показателями санитарного неблагополучия, потенциальной опасности исследуемых объектов, и поэтому названы «санитарно-показательными». Однако не все микробы, входящие в состав нормальной флоры тела человека или животных, могут быть признаны санитарно-показательными. На основании многочисленных исследований были сформулированы требования, которым должны отвечать санитарно-показательные микроорганизмы: 1.Они должны постоянно содержаться в выделениях человека и теплокровных животных и поступать в окружающую среду в больших количествах. 2.Они не должны иметь другого природного резервуара, кроме организма человека и животных. 3.После выделения в окружающую среду они должны сохранять жизнеспособность в течение сроков, близких к срокам выживания патогенных микробов, выводимых из организма теми же путями. 4.Они не должны размножаться в окружающей среде. 5.Они не должны сколько-нибудь значительно изменять свои биологические свойства в окружающей среде. 6.Они должны быть достаточно типичными, с тем, чтобы их дифференциальная диагностика осуществлялась без особого труда. 7.Индикация, идентификация и количественный учет должны производится современными, простыми, легко доступными и экономичными микробиологическими методами. Микрофлора воздуха. Факторы, влияющие на количество микробов в воздухе. Методы исследования микрофлоры воздуха. Санитарно-показательные микроорганизмы воздуха. В воздух попадают микроорганизмы из дыхательных путей и с каплями слюны человека и животных. Здесь обнаруживаются кокковидные и палочковидные бактерии, бациллы, клостридии, актиномицеты, грибы и вирусы. С целью снижения микробной обсемененности воздуха проводят влажную уборку помещения, очистку поступающего воздуха. Применяют также аэрозольную дезинфекцию и обработку помещений лампами ультрафиолетового излучения. В воздух попадают микроорганизмы из дыхательных путей и с каплями слюны человека и животных. Здесь обнаруживаются кокковидные и палочковидные бактерии, бациллы, клостридии, актиномицеты, грибы и вирусы. Золотистый стафилококк и гемолитические стрептококки являются представителями микрофлоры верхних дыхательных путей и имеют общий путь выделения с патогенными микроорганизмами, передающимися воздушно-капельным путем. Появление в воздухе спорообразующих бактерий — показатель загрязненности воздуха микроорганизмами почвы, а появление грамотрицательных бактерий — показатель возможного антисанитарного состояния. По эпидемиологическим показаниям в воздухе определяют наличие сальмонелл, микобактерий, вирусов. Санитарно-показательные микроорганизмы воздуха. Возбудители воздушно-капельных инфекций имеют общий путь выделения с бактериями (кокками), постоянно обитающими на слизистой оболочке верхних дыхательных путей, выделяющимися в окружающую среду (при кашле, чиханье, разговоре), поэтому в качестве санитарно-показательных бактерий для воздуха закрытых помещений предложены гемолитические стрептококки и золотистые стафилококки. Грамотрицательные бактерии– в связи с распространением госпитальной инфекции в воздухе больничных помещений. Определяют наличие дрожжеподобных и плесневых грибов. По эпидемиологическим показаниям в воздухе определяют наличие сальмонелл, микобактерий, вирусов. Появление в воздухе спорообразующих бактерий — показатель загрязненности воздуха микроорганизмами почвы, а появление грамотрицательных бактерий — показатель возможного антисанитарного состояния. Микробиологический контроль воздуха проводится с помощью методов естественной или принудительной седиментации микробов. Естественная седиментация (по методу Коха) проводится в течение 10 мин путем осаждения микробов на поверхность твердой питательной среды в чашке Петри. Принудительная седиментация микробов осуществляется путем «посева» проб воздуха на питательные среды с помощью специальных приборов. Санитарно-гигиеническое состояние воздуха определяется по следующим микробиологическим показателям: 1. Общее количество микроорганизмов в 1 м воздуха (обсемененность воздуха) — количество колоний микроорганизмов, выросших при посеве воздуха на питательном агаре в чашке Петри в течение 24 ч при 37С. 2. Индекс санитарно-показательных микробов— количество золотистого стафилококка и гемолитических стрептококков в 1 м3 воздуха. Эти бактерии являются представителями микрофлоры верхних дыхательных путей и имеют общий путь выделения с патогенными микроорганизмами, передающимися воздушно-капельным путем. Появление в воздухе спорообразующих бактерий — показатель загрязненности воздуха микроорганизмами почвы, а появление грамотрицательных бактерий — показатель возможного антисанитарного состояния. |
