Фармакогнозия экзамен. Определение фармакогнозии как науки и учебной дисциплины, ее связь с другими дисциплинами. Основные понятия предмета лекарственные растения, лекарственное растительное сырье,
 Скачать 1.68 Mb. Скачать 1.68 Mb.
|
|
Цельное и измельченное сырье. При исследовании цельного сырья берут кусочки пластинки листа с краем и жилкой; у трав берут лист, иногда также кусочек стебля и цветок, у цветков — чашечку и венчик. При исследовании резаного сырья берут несколько различных кусочков. Просветление можно проводить двумя способами. I. Несколько кусочков сырья помещают в колбу или пробирку, прибавляют раствор 25 г/л натрия гидроксида Р и кипятят в течение 1—2 мин. Затем содержимое выливают в чашку Петри (или фарфоровую), жидкость сливают и сырье тщательно промывают водой Р. Из воды кусочки сырья вынимают скальпелем или лопаточкой и помещают на предметное стекло в каплю раствора хлоралгидрата Р1 или раствора глицерина Р. II. Кусочки кипятят в растворе хлоралгидрата Р1, разведенного водой Р (1:1, об/об), в течение 5—10 мин (до просветления). Просветленный кусочек сырья помещают на предметное стекло в каплю раствора хлоралгидрата Р1 или глицерина Р, разделяют скальпелем или препаровальной иглой на две части, одну из них осторожно переворачивают. Объект накрывают покровным стеклом, слегка подогревают до удаления пузырьков воздуха и, после охлаждения, рассматривают лист с обеих сторон под микроскопом сначала при малом, затем при большом увеличении. При приготовлении микропрепаратов из толстых листьев их предварительно раздавливают скальпелем. Для исследования стеблей их отрезки кипятят в растворе 50 г/л натрия гидроксида Р, тщательно промывают водой Р, снимают эпидермис скальпелем или препаровальными иглами и рассматривают его с поверхности; из остальных тканей готовят препарат, раздавливая объект скальпелем на предметном стекле в растворе хлоралгидрата Р1 или растворе глицерина Р. При необходимости приготовления поперечных срезов листьев и стеблей их кипятят в растворе хлоралгидрата Р1 в течение 10 мин и делают срезы, зажимая кусочки листа в пробку или сердцевину бузины. Готовые срезы помещают в воду Р и далее используют для приготовления микропрепаратов, рассматривая их в растворе хлоралгидрата Р1. Исследование при дополнительном измельчении. Для микроскопического испытания лекарственное растительное сырье дополнительно измельчают (355) (2.9.12), если в частной статье не указано иное. Наиболее широко используемой средой для заключения в нее дополнительно измельченного сырья является раствор хлоралгидрата Р. Однако в этом реактиве не всегда хорошо видны некоторые элементы, в таком случае могут быть использованы иные среды, например, 50% (об/об) раствор глицерина Р, позволяющий обнаружить зерна крахмала. При необходимости в частной статье может быть отмечено использование специфических реактивов, например, реактива молочной кислоты Р (использование которого позволяет обнаруживать различные диагностические признаки), раствора рутения красного Р (позволяющий увидеть присутствие слизи в клетках), или глицерина Р (в котором видны крахмал и инулин) и других. Использование раствора хлоралгидрата. 2-3 капли раствора хлоралгидрата Р помещают на предметное стекло. Небольшое количество порошка суспендируют в растворе и накрывают покровным стеклом. Препарат очень аккуратно нагревают на плитке или на газовой микрогорелке до кипения и кипятят в течение непродолжительного времени, при необходимости с помощью пипетки добавляют реактив, охлаждают и просматривают под микроскопом. Нагревание повторяют до тех пор, пока крахмальные зерна и водорастворимое содержимое клеток не станет невидимым. Просматривают полученный препарат под микроскопом. Так как хлоралгидрат склонен к кристаллизации в виде длинных нитей, для предотвращения этого после нагревания удаляют покровное стекло, к препарату прибавляют 1 каплю 10% (об/об) смеси раствора хлоралгидрата Р и глицерина Р, накрывают чистым покровным стеклом и просматривают под микроскопом. Использование 50% (об/об) раствора глицерина. 2 капли 50% (об/об) раствора глицерина Р помещают на предметное стекло. Небольшое количество порошка суспендируют в растворе и накрывают покровным стеклом. Просматривают под микроскопом. Макроскопический и микроскопический анализ. Общие правила и методы исследования группы ЛРС «Корневища», «Корни». Цельное сырье. Готовят поперечные и продольные срезы. Небольшие куски подземных органов помещают в холодную воду Р и выдерживают около суток, затем помещают в смесь спирт Р — глицерин Р (1:1, об/об) на 3 сут. Размоченные объекты выравнивают скальпелем так, чтобы они имели строго поперечное или продольное сечение. Делают срезы и готовят микропрепараты в растворе хлоралгидрата Р1 или растворе глицерина Р и рассматривают диагностические признаки сначала при малом, затем при большом увеличении. Диагностические признаки: особенности строения эпидермы или перидермы, расположение и строение механических, проводящих, секреторных тканей, кристаллы оксалата кальция, запасные вещества. Измельченное сырье. Кусочки подземных органов кипятят в течение 3—5 мин в растворе 50 г/л натрия гидроксида Р, тщательно промывают водой Р и готовят микропрепараты, раздавливая кусочки в растворе глицерина Р или растворе хлоралгидрата Р1. Исследование при дополнительном измельчении. Препарат готовят так же, как указано в разделе «Листья, травы, цветки». Макроскопический и микроскопический анализ. Общие правила и методы исследования группы ЛРС «Трава». См. вопрос 30 Макроскопический и микроскопический анализ. Общие правила и методы исследования группы ЛРС «Плоды». Цельное сырье. Готовят препараты кожуры семени и околоплодника с поверхности или поперечные срезы. Препараты поверхности кожуры и околоплодника. 2-3 семени или плода кипятят в пробирке в растворе 50 г/л натрия гидроксида Р в течение 2—3 мин и тщательно промывают водой Р. Объект помещают на предметное стекло, препаровальными иглами отделяют кожуру семени или ткани околоплодника и рассматривают их в растворе хлоралгидрата Р1 или растворе глицерина Р. Срезы. Для приготовления срезов сухие плоды и семена предварительно размягчают, поместив их на сутки во влажную камеру (влажной камерой служит эксикатор с водой, в которую добавлено несколько капель хлороформа) или водяным паром в течение 15—30 мин или более в зависимости от твердости объекта. Мелкие плоды и семена запаивают в парафиновый блок размером около 0,5 см × 0,5 см × 1,5 см. Кончиком нагретой препаровальной иглы расплавляют парафин и в образовавшуюся ямку быстро погружают объект. Поверхность объекта должна быть сухой. Срезы объекта делают вместе с парафином; срезы выбирают из парафина препаровальной иглой, смоченной жидкостью, и готовят микропрепараты в растворе глицерина Р или растворе хлоралгидрата Р1. Диагностические признаки: форма и строение клеток экзокарпия (эпидермиса), наличие и строение трихом, расположение и форма механических элементов в мезокарпии, число и расположение эфиро-масличных каналов, проводящих пучков, наличие кристаллических включений. Исследование при дополнительном измельчении. Препарат готовят так же, как указано в разделе «Листья, травы, цветки». Макроскопический и микроскопический анализ. Общие правила и методы исследования группы ЛРС «Кора». Цельное сырье и измельченное сырье. Готовят поперечные или продольные срезы коры. Кусочки коры размером около 2—3 см × 0,5—1 см кипятят в колбе или пробирке с водой Р в течение 5 мин. Размягченные куски выравнивают скальпелем так, чтобы они имели строго поперечное или продольное сечение. Делают срезы и готовят микропрепараты в растворе хлоралгидрата Р1 или растворе глицерина Р. При необходимости готовят препараты в соответствующих реактивах для выявления различных структур или веществ. Диагностические признаки: толщина, окраска и характер пробки, наличие колленхимы, толщина первичной и вторичной коры, ширина сердцевинных лучей, особенности расположения и количество лубяных волокон, каменистых клеток, клеток с эфирным маслом, включения кристаллов оксалата кальция, млечники. Соскоб коры или мелкие кусочки кипятят в течение 3—5 мин в растворе 50 г/л натрия гидроксида Р, промывают водой Р и готовят микропрепараты, раздавливая объект скальпелем в растворе глицерина Р или растворе хлоралгидрата Р1. Исследование при дополнительном измельчении. Препарат готовят так же, как указано в разделе «Листья, травы, цветки». Макроскопический и микроскопический анализ. Общие правила и методы исследования группы ЛРС «Цветки». См. Вопрос 30 Макроскопический и микроскопический анализ. Общие правила и методы исследования группы ЛРС «Семена». См. Вопрос 33 Роль и значение ЛРС и препаратов растительного происхождения в современной медицине. Лекарственное растительное сырье (ЛРС) широко используется в медицине для получения различных лекарственных препаратов: настоев и отваров, настоек, экстрактов, суммарных препаратов и т.д. В последнее время увеличился выпуск новых видов продукции из ЛРС (брикеты, фильтр-пакеты, порошки, таблетки и т.д.). В настоящее время в России используются лекарственные средства, которые получают из веществ синтетического, растительного, животного, минерального происхождения. Получают лекарственные средства так же из крови, плазмы крови, органов и тканей человека и животного, используются антибиотики и препараты, получаемые микробиологическим путем. Из лекарственного растительного сырья получают примерно одну треть всех разрешенных к медицинскому применению лекарственных средств. Использование средств растительного происхождения, в первую очередь, обусловлено их высокой биологической активностью, комплексным воздействием на организм больного и безопасностью при лечении различных хронических заболеваний или в целях профилактики. Охрана природных ресурсов. Дикорастущие ЛР и их рациональное использование. Рациональная эксплуатация зарослей дикорастущих лекарственных растений. В рамках решения данной задачи необходимо учет биологических особенностей развития растений и выполнение правил заготовки и сушки сырья для каждого лекарственного растения, предусмотренных инструкциями по сбору, сушке и нормативной документацией на лекарственное растительное сырье. Основные правила заготовки лекарственного растительного сырья: - заготовка должна осуществляться на территориях с повышенным обилием лекарственных растений; - собираться должны только те части растений, которые используются в качестве сырья; - на заготовительном участке должна оставляться часть растений для обсеменения и размножения; - при заготовке листьев с многолетних растений нельзя собирать все листья, часть их нужно оставлять; - при заготовке плодов недопустимы срезка и (или) обламывание ветвей; - сбор коры должен быть осуществлен методом полукольцевых надрезов и только на участках отведенных лесхозами; - сбор сырья должен проходить в периоды максимального накопления им фармакологически активных веществ. Кроме выше перечисленных правил в рамках рационального использования лекарственных растительных ресурсов должны осуществляться: очередность заготовок, учитывающая сроки восстановления зарослей, комплексная переработка и использование лекарственного сырья, введение в культуру, рекультивация земель с использованием лекарственных растений и др. Охрана ресурсов дикорастущих лекарственных растений. Лекарственные растения, находящиеся под угрозой исчезновения, и редкие виды внесенные в Красные книги находятся под охраной государств. К числу редких видов относятся растения, численность и ареал которых имеют постоянную тенденцию к сокращению. Для их восстановления предусматриваются усиление охраны и разработка специальных программ по восстановления. Как говорилось выше, в России существует несколько форм охраны природы и отдельных видов растений и животных. Главной, среди которых, являются заповедники. Помимо этого, охраной лекарственных растений занимаются ботанические и промысловые заказники. На территории ботанических заказников запрещаются промысловые заготовки лекарственных растений и организуются они для сохранения и восстановления численности отдельных или многих видов дикорастущих лекарственных растений. В промысловых заказниках (приписные угодия) разрешено проводить заготовку лекарственного сырья с применением мероприятий, способствующих сохранению популяций лекарственных растений. При этом участки закрепляются за заготовительными организациями, которые обязаны выделять средства для охраны, проведения комплекса мероприятий по окультуриванию и восстановлению естественных зарослей. На территории приписных угодий запрещается заготовка сырья без специальной лицензии и ограничены: распашка земель, выпас скота, сенокошение, осушение болот, использование ядохимикатов, отдых населения, застройка, движение механизированного автотранспорта, разработка полезных ископаемых и др. Культура ЛР. Районы возделывания. При размещении плантаций лекарственных растений по территории России, в первую очередь, необходимо учитывать требования, предъявляемые теми или иными видами растений к почвенно-климатическим факторам. Ряд культур, таких как календула, ромашка, пустырник сердечный, выращиваются в большинстве регионов страны. Другие, например шалфей лекарственный, из-за более высокой потребности в тепле, возделывается только в Южном (включая Северо- Кавказский) и Крымском федеральных округах. В настоящее время в Центральном федеральном округе площади под лекарственными культурами занимают около 10% всей посевной площади лекарственных культур в стране (около 400 га). В Приволжском федеральном округе под лекарственные культуры отведено 44—52% всех посевных площадей занятых лекарственными культурами в стране (более 2100 га). В Сибирском федеральном округе лекарственные культуры занимают 15—20% всей посевной площади лекарственных культур в стране (730-780 га). В Крымском округе лекарственные культуры выращивают на площади 600-700 га, что составляет около 15% посевных площадей лекарственных культур в нашей стране. В Южном федеральном округе (включая Северо-Кавказский), занимавшем в 1970-1990-е гг. лидирующее положение по объему культивированного лекарственного растительного сырья, лекарственные растения выращиваются на небольшой площади — на 3—5% от всех посевных площадей лекарственных культур в стране (160 га). В Дальневосточном федеральном округе посевы лекарственных культур занимают около 2% всей посевной площади лекарственных культур в стране (110 га). Лекарственным растениеводством занимаются сельскохозяйственные предприятия различных форм собственности (государственные, частные) 74—80% и фермерские хозяйства 20—25%. Перспективные лекарственные формы из РС. Преимущества, особенности. Методы анализа. Популярные лекарства и препараты из растительного сырья Чаше всего лекарственные препараты из растительного сырья применяются в нескольких видах: Растительные соки. Речь идет не только о популярной в настоящее время теории о пользе свежевыжатых соков из овощей и фруктов, но и о применении соков из зеленой массы свежих частей растений, в том числе и корней. Соки могут применяться, как свежевыжатыми, так и консервированными. Отвары или водные вытяжки из растений. Изготавливаются из сухого сырья, путем кипячения на водяной бане в течение нескольких минут. Чаще всего такой способ применяется для корней и стеблей. Настои. В отличие от предыдущего типа, вытяжка полезных веществ происходит путем настаивания в течение нескольких дней. К этому же типу относятся многочисленные чаи. Настойки. Делаются из любого типа растительного сырья на основе спирта или спирто-водного раствора. Пасты. Эмульсии, приготавливаемые в лабораторных условиях, по специальной рецептуре. Гос. Контроль на радиационную безопасность ЛРС. Цель и этапы проведения. НД. Отбор проб для радиационного контроля. Радиационный контроль лекарственных средств проводится в соответствии с требованиями закона «О радиационной безопасности населения» и «Правил сертификации лекарственных средств». Радиационный контроль лекарственных средств отечественного и зарубежного производства на территории Российской Федерации осуществляется уполномоченными на это органами. При проведении радиационного контроля ЛРС и ЛРП выполняются следующие основные процедуры: отбор проб из партии ЛРС/серии ЛРП; приготовление счетных образцов с концентрированием удельной активности в случае необходимости; измерение активности стронция-90 и цезия-137 в счетных образцах; расчет результатов измерений и погрешности исследований; определение соответствия ЛРС/ЛРП критериям радиационной безопасности. Отбор проб для радиационного контроля проводят в соответствии с требованиями ОФС «Отбор проб лекарственного растительного сырья и лекарственных растительных препаратов». Подготовку счетных образцов ЛРС/ЛРП для определения удельной активности Sr-90 и Cs-137 проводят на основании настоящей общей фармакопейной статьи. Метрологические характеристики средств измерений должны подтверждаться поверкой органами Государственной метрологической службы в установленные сроки с выдачей свидетельства о поверке. Результатом измерения активности радионуклидов в счетном образце является интервал значений активности от (А — ∆А) до (А + ∆А) , в котором с вероятностью Р=0,95 находится значение измеряемой величины А (Бк): Порядок отбора проб ЛРС/ЛРП Порядок отбора проб ЛРС/ЛРП включает выделение однородной по радиационному составу пробы для приготовления счетных образцов. Отбор проб проводят в соответствии с требованиями ОФС «Отбор проб лекарственного растительного сырья и лекарственных растительных препаратов». Отбор пробы для радиационного контроля от партии ЛРС и от серии ЛРП имеют разные схемы отбора проб и разный объем выборки. Определение содержания остаточных пестицидов в ЛРС. Цель и этапы проведения. НД. Порядок отбора проб. Порядок отбора проб Отбор проб от партии сырья/серии препарата проводят в соответствии с требованиями ОФС «Отбор проб лекарственного растительного сырья и лекарственных растительных препаратов» и настоящей статьей. Отбор проб для проведения испытаний осуществляют в соответствии с действующими санитарно-гигиеническими правилами и условиями, исключающими дополнительное загрязнение сырья. Для обеспечения достоверности полученных результатов анализируемое на содержание остаточных пестицидов лекарственное растительное сырье/препараты, как правило, должно иметь влажность не более 15 %. Основные этапы определения содержания остаточных пестицидов в лекарственном растительном сырье и лекарственных растительных препаратах: отбор пробы для определения остаточных пестицидов, тяжелых металлов и мышьяка (ОФС «Отбор проб лекарственного растительного сырья и лекарственных растительных препаратов»); подготовка пробы к определению; определение содержания остаточных пестицидов в испытуемых образцах; обработка результатов измерений; определение соответствия сырья допустимым нормам. Используемые аналитические методы должны удовлетворять требованиям ОФС «Валидация аналитических методик» и следующим критериям: выбранный метод является подходящим для комбинации остаточный пестицид/лекарственное растительное сырье; при интерпретации результатов необходимо учитывать влияние некоторых компонентов (например, влияние дисульфида у растений семейства Крестоцветных); концентрации испытуемого раствора и раствора сравнения, а также настройки аппаратуры должны быть такими, чтобы аналитический сигнал, используемый для количественного анализа пестицидов, находился в пределах линейного диапазона используемого детектора; каждый пестицид извлекается в диапазоне 70-110 %; повторяемость и воспроизводимость метода: относительное стандартное отклонение (%) не должно превышать значений, указанных в табл. 1. Для определения содержания пестицидов в пробе используется газовая (ГХ/МС) или жидкостная (ВЭЖХ/МС) хроматография с масс-спектрометрическим детектором. При отсутствии масс-спектрометрического детектора можно использовать электронно-захватный или другие селективные детекторы. Определение проводится в соответствии с требованиями ОФС «Хроматография», «Газовая хроматография», «Высокоэффективная жидкостная хроматография» и «Масс-спектрометрия». Упаковка, маркировка и транспортирование ЛРС и ЛР препаратов. Требования к материалам упаковки. Упаковка лекарственного растительного сырья и лекарственных растительных препаратов Упаковка должна обеспечивать защиту лекарственного растительного сырья и лекарственных растительных препаратов в процессе хранения и транспортирования от повреждений, потерь, отрицательного действия факторов окружающей среды (температура, влажность, свет), а также сохранность и неизменность свойств лекарственного растительного сырья и лекарственных растительных препаратов в течение установленного срока его годности. Упаковка должна быть изготовлена в соответствии с действующими в РФ требованиями к данному виду упаковки из материалов, разрешенных к применению в РФ. Упаковка должна быть однородной по типу для каждой партии сырья; чистой, сухой, без посторонних запахов. Материалы, из которых изготавливается упаковка, должны быть прочными, легкими, химически и физически индифферентными при контакте с лекарственным растительным сырьем/препаратом. Для высушенного лекарственного растительного сырья используют следующие виды упаковки: 1) Мешки тканевые, мешки из химических волокон и мешки льно-джуто-кенафные. При упаковывании сырья в двойные мешки предварительно один мешок вкладывают в другой. 2) Мешки бумажные многослойные, пакеты бумажные двойные или одинарные. 3) Полиэтиленовые мешки. Для упаковки лекарственных растительных препаратов (фасованной продукции) используют пачки картонные с внутренним пакетом, пакеты бумажные, фильтр-пакеты бумажные и др. Виды упаковки и масса лекарственного растительного сырья, упакованного в тару, устанавливаются нормативной документацией на конкретные виды лекарственного растительного сырья. Маркировка лекарственного растительного сырья Каждая упаковочная единица с лекарственным растительным сырьем должна быть промаркирована путем нанесения информации непосредственно на упаковку несмывающейся краской либо путем прикрепления этикетки (маркировочного ярлыка). Наносимая информация должна соответствовать требованиям действующего законодательства РФ. Маркировка лекарственных растительных препаратов Маркировку наносят на вторичную упаковку лекарственных растительных препаратов. Наносимая информация должна соответствовать требованиям действующего законодательства РФ. Транспортирование лекарственного растительного сырья и лекарственных растительных препаратов Лекарственное растительное сырье и лекарственные растительные препараты должны транспортироваться в сухих, чистых, не имеющих постороннего запаха, крытых транспортных средствах, либо в контейнерах. Правила хранения различных групп ЛРС и ЛР препаратов. НД. Настоящая общая фармакопейная статья устанавливает требования к условиям хранения лекарственного растительного сырья и лекарственных растительных препаратов. Лекарственное растительное сырье должно храниться в специально оборудованных складских помещениях, имеющих ряд зон: приемное отделение для оформления документов, проверки качества упаковки и маркировки, отбора проб для анализа; помещение для временного хранения лекарственного растительного сырья, зараженного вредителями запасов (изолятор); зону для временного хранения нестандартного сырья; зону для основного хранения сырья; зоны для раздельного хранения различных групп лекарственного растительного сырья и др. Лекарственное растительное сырье и лекарственные растительные препараты должны храниться таким образом, чтобы избежать перекрестной контаминации. Помещения для хранения лекарственного растительного сырья и лекарственных растительных препаратов должны быть чистыми и хорошо проветриваемыми, и, при необходимости, подвергаться дезинфекции, должны быть защищены от проникновения в них насекомых и животных, особенно грызунов. Для контроля температуры и влажности в помещениях для хранения лекарственного растительною сырья должны быть предусмотрены соответствующие средства измерения (например, термометр и психрометр, термогифометр и др.). Лекарственное растительное сырье, требующее хранения при температуре, отличной от комнатной, должны иметь соответствующую маркировку. Лекарственное растительное сырье и лекарственные растительные препараты не должны подвергаться длительному воздействию прямого или яркого рассеянного солнечного света. Лекарственные растительные средства, требующие защиты от света, должны храниться в защищенном от света месте и/или в светозащитной упаковке в соответствии с требованиями. Основная масса лекарственного растительного сырья хранится в зонах для основного хранения сырья. Изолированно от других видов сырья следует хранить: плоды и семена в отдельной зоне для хранения; эфирномасличное сырье, обладающее запахом, в хорошо укупоренной таре (в том числе плотно укупоренные мешки, тюки, кипы тканевые); ядовитое и сильнодействующее сырье (в отдельном помещении или в отдельном шкафу под замком). Хранение лекарственного растительного сырья, содержащего сердечные гликозиды, осуществляется с соблюдением требований ГФ, в частности, требований о повторном контроле на биологическую активность. Лекарственное растительное сырье должно храниться таким образом, чтобы не препятствовать свободной циркуляции воздуха в помещении. Лекарственное растительное сырье при хранении необходимо ежегодно перекладывать, обращая внимание на наличие вредителей запасов и на соответствие длительности хранения сроку годности, указанному в фармакопейной статье или нормативной документации. Определение содержания тяжелых металлов и мышьяка в ЛРС. Этапы и методы. НД. Требования настоящей общей фармакопейной статьи распространяются на методы количественного определения тяжелых металлов: свинца, кадмия, ртути и мышьяка в лекарственном растительном сырье и лекарственных растительных препаратах. Определение содержания тяжелых металлов и мышьяка в лекарственном растительном сырье и лекарственных растительных препаратах проводят с использованием одного из следующих методов: атомно-абсорбционной спектрометрии; атомно-эмиссионной спектрометрии с индуктивно связанной плазмой; масс-спектрометрии с индуктивно связанной плазмой. Результаты, полученные при определении содержания тяжелых металлов и мышьяка в лекарственном растительном сырье, распространяются на лекарственный растительный препарат, произведенный из данной партии лекарственного растительного сырья. Лекарственные растительные препараты подвергаются выборочному контролю на содержание тяжелых металлов и мышьяка не реже одного раза в год (одна серия каждого наименования). Процедура определения содержания тяжелых металлов и мышьяка в лекарственном растительном сырье и лекарственных растительных препаратах состоит из следующих основных этапов: Отбор пробы для определения остаточных пестицидов, тяжелых металлов и мышьяка. Отбор пробы проводится в соответствии с требованиями ОФС «Отбор проб лекарственного растительного сырья и лекарственных растительных препаратов» в условиях, исключающих дополнительное загрязнение сырья. Подготовка пробы. Определение содержания тяжелых металлов и мышьяка в испытуемых пробах. Определение соответствия сырья допустимым нормам. 46.Витамины, их биогеоценоз. Локализация по органам и тканям растительного оранизма. Влияние онтогенетических факторов и условий среды на накопление витаминов в растениях. Витамины — группа низкомолекулярных органических соединений относительно простого строения и разнообразной химической природы. Это сборная по химической природе группа органических веществ, объединённая по признаку абсолютной необходимости их для гетеротрофного организма в качестве составной части пищи. Витамины встречаются в растениях практически всех семейств. Витамины локализуются в зеленых частях растений, цветках, плодах (витамины С, Р, К, каротиноиды) и в семенах (витамины Е и F). Водорастворимые витамины находятся в растворенном состоянии в клеточном соке, жирорастворимые витамины включены в пластиды и алейроновые зерна. Каротиноиды находятся в хлоропластах и хромопластах, они встроены в мембраны тилакоидов или растворены в липидных каплях – пластоглобулах. Влияние факторов внешней среды и онтогенеза на накопление витаминов. Витамином С у травянистых растений наиболее богаты листья, затем в убывающем порядке идут цветки, почки, прилистники, плоды, корни, черешки, стебли. В листьях верхних ярусов витамина С больше, чем в нижних. В плодах наблюдается следующая закономерность накопления витаминов: витамин С и каротиноиды — максимальное количество в фазу полной зрелости; витамин Р — максимум, когда плоды сформировались и достигли половины своего размера, в период формирования семян содержание витамина Р резко уменьшается. Влияние факторов внешней среды на накопление витамина С и каротиноидов. В границах ареала растений в северных районах произрастания накапливается больше аскорбиновой кислоты, а в южных районах — больше каротиноидов. Повышение температуры воздуха способствует накоплению каротиноидов, а при понижении температуры, т.е. в прохладный сезон, накапливается больше витамина С. Увеличение влажности способствует накоплению витамина С и каротиноидов, но избыток влаги действует отрицательно. Накоплению витамина С способствуют увеличение освещенности, азотные и комплексные удобрения, почвы плодородные легкие суглинистые и супесчаные. Культура и селекция приводят к снижению накопления витамина С и каротиноидов. 4 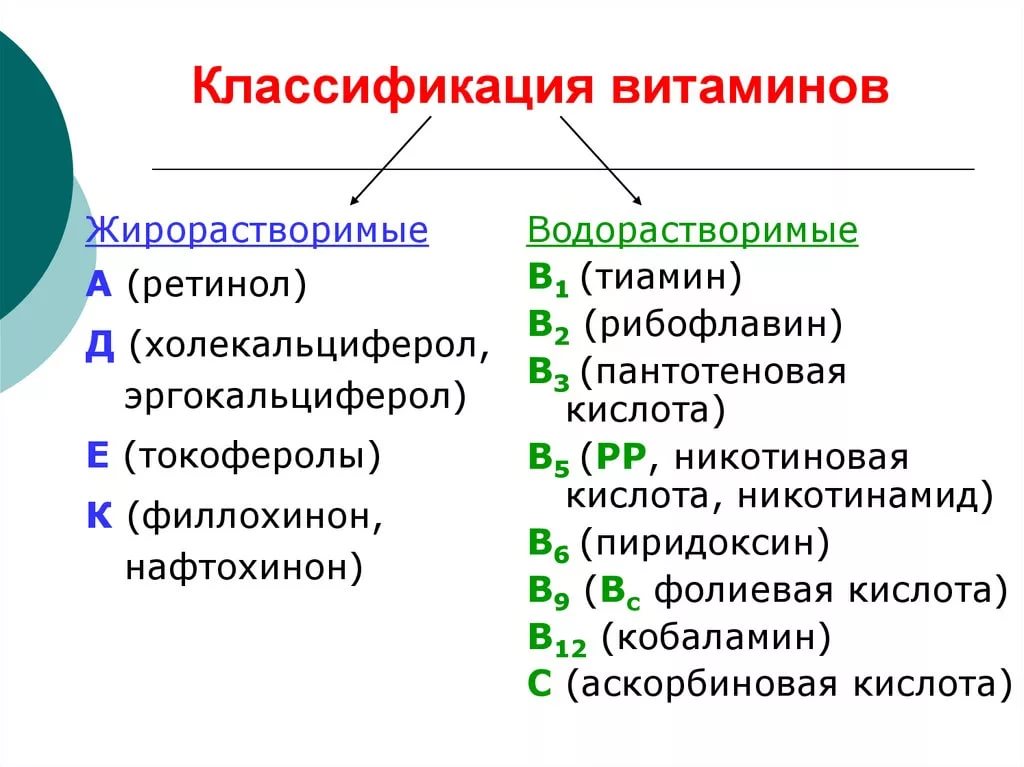 7.Витамины, классификация. Физико-химические с-ва. Распространение в растительном мире. Влияние факторов внешней среды (географический фактор, климатические условия, состав почвы и т.д.) на синтез и накопление витаминов в растениях. 7.Витамины, классификация. Физико-химические с-ва. Распространение в растительном мире. Влияние факторов внешней среды (географический фактор, климатические условия, состав почвы и т.д.) на синтез и накопление витаминов в растениях.Физические свойства. В чистом виде витамины – кристаллические вещества или жидкости белого, желтого, оранжевого или красного цвета, имеющие специфический вкус, без характерного запаха. В основу их первой классификации положена растворимость в воде или жирах. В настоящее время установлено, что витамины – индивидуальные вещества различных химических классов. витамин С: плоды черной смородины, плоды шиповника, плоды рябины, плоды малины, листья крапивы, плоды и листья земляники. в  итамин Р: бутоны и плоды софоры японской, плоды аронии (рябины) черноплодной, плоды черной смородины, кожура плодов цитрусовых, листья чая. итамин Р: бутоны и плоды софоры японской, плоды аронии (рябины) черноплодной, плоды черной смородины, кожура плодов цитрусовых, листья чая.каротиноиды (провитамин А): плоды шиповника, плоды облепихи, плоды рябины, цветки календулы, трава череды, трава сушеницы топяной. витамин К: листья крапивы, трава пастушьей сумки, трава тысячелистника, цветки и листья зайцегуба, кора калины, кукурузные рыльца. витамин Е: плоды облепихи, облепиховое масло, масло шиповника, кукурузное масло, льняное масло, семена тыквы. витамин F: масло кукурузное, масло подсолнечное и другие растительные жирные масла. В лекарственном растительном сырье довольно часто встречаются витамины группы В: В2 — рибофлавин, В5 — пантотеновая кислота, В9 — фолиевая кислота, провитамин витаминов группы D — эргостерол и другие фитостеролы. В высоких концентрациях способны накапливаться только кислота аскорбиновая (витамин С), каротиноиды (провитамин А), витамин К1 (филлохинон) и некоторые флавоноиды (рутин, кверцетин и др.), относимые к витамину Р. 48.Анализ ЛРС, содержащего витамины( определение подлинности и доброкачественности). Для качественного обнаружения витаминов чаще всего используют хроматографию в тонком слое. Витамины на хроматограмме обнаруживают по окраске в видимом свете (у каротиноидов), на флуоресценции в УФ-лучах как до, так и после проявления специальными реактивами. Количественное определение содержания витаминов в ЛРС проводят методом титриметрии, спектрофотометрии, флуореметрии Доброкачественность – характеризуется нормальной влажностью, зольностью и достаточным содержанием действующих веществ, отсутствием плесени и вредителей. Доброкачественность сырья зависит от своевременного и правильного проведения сбора и сушки. Фармакогностический анализ нормативно регулируется документами 2-х типов: с одной стороны – соответствующие общие статьи ГФ ХI, нормирующие правила приемки, методы отбора проб, методы определения подлинности и доброкачественности ЛРС, с другой – НД, определяющие требования к конкретному виду сырья. На анализ сырье может поступать в цельном, резаном, дробленном и порошкообразном виде, в виде таблеток, лекарственных сборов и брикетов. Фармакогностический анализ складывается из ряда последовательно проводимых анализов: макроскопического; микроскопического; биологическим; фитохимического; хроматографическим; товароведческого.рр Выбор метода исследования зависит от формы сырья. 49.Сборка. сушка хранение и переработка ЛРС содержащего витамины. Пути использования применения в медицине. Заготовку сырья ведут в период максимального накопления действующих веществ. Сбор проводят в сухую погоду после обсыхания росы. Сочные плоды собирают в небольшую по объему тару (корзины, ящики с перфорированными стенками) и сразу же доставляют к месту сушки. Перед сушкой сочные плоды подвяливают на воздухе или при температуре 25-30 °С. Трава пастушьей сумки легко поражается мучнистой росой — такое сырье не подлежит заготовке. Сушка для всех видов сырья допускается воздушно-теневая, но предпочтительнее — искусственная. Температурный режим сушки для сырья, содержащего филлохинон (витамин К1) — 40-50 °С, каротиноиды – 60-70 °С. Плоды шиповника, богатые аскорбиновой кислотой, рекомендуется сушить при 80-90 °С, чтобы инактивировать ферменты и сохранить витамин С. Плоды облепихи обычно перерабатывают в свежем виде — не позднее трех дней после сбора. Если заготавливают замороженные плоды, то их перерабатывают не позднее 6 месяцев, не допуская размораживания. При замораживании хорошо сохраняются витамины Е и каротиноиды, а витамин С разрушается. Хранят витаминосодержащее сырье по общему списку. Срок годности сырья, преимущественно, 2-3 года. Для сырья земляники и черной смородины срок годности — 1 год. Очень быстро — за 4-6 месяцев хранения разрушаются витамины С и K1, каротиноиды более устойчивы (срок годности – 1-2 года) Лекарственное растительное сырье, содержащее витамины, используется для получения разнообразных лекарственных форм и препаратов. I. Экстемпоральные лекарственные формы Настои. Отвары:Сборы: III. Препараты, содержащие сумму витаминов. масло шиповника, масло облепиховое, масло из плодов и листьев облепихи; концентрат масла облепихового (полуфабрикат); сиропы шиповника, шиповника с витамином С, шиповника с биоженьшенем, плодово-ягодный (шиповник, рябина); «Холосас» — сироп из сгущенного водного экстракта плодов шиповника; «Каротолин» — масляный экстракт каротиноидов из мякоти плодов шиповника. Лекарственное растительное сырье, содержащее витамины, и лекарственные средства на его основе обладают широким спектром фармакологического действия. Действие обусловлено витаминами и другими биологически активными веществами, содержащимися в сырье: флавоноидами, дубильными веществами и др.. Лекарственное растительное сырье, содержащее витамины, используют как: поливитаминные средства — плоды черной смородины, плоды рябины обыкновенной, плоды шиповника, листья крапивы; кровоостанавливающие средства – цветки и листья зайцегуба, листья крапивы, кора калины, трава пастушьей сумки, трава тысячелистника; ранозаживляющие и противоязвенные средства — масло облепихи и масло шиповника, трава череды, трава сушеницы топяной; противовоспалительное и антисептическое средство — цветки календулы; противовоспалительное и противоаллергическое средство — трава череды; желчегонные средства — кукурузные столбики с рыльцами, плоды шиповника; мочегонные средства — плоды и листья земляники, трава череды. 50. Полисахариды, определение, классификация физ-хим свойства, локализация по органам и тканям, их распространение в растительном мире Полисахариды (гомогликозиды) — это высокомолекулярные продукты конденсации более пяти моносахаридов и их производных, связанных друг с другом О-гликозидными связями, образующие линейные или разветвленные цепи. Молекулярная масса полисахаридов колеблется от нескольких тысяч до нескольких миллионов. Полисахариды делятся на два типа: гомополисахариды (гомополимеры) крахмал клетчатка гетерополисахариды (гетерополимеры). инулин пектиновые вещества камеди слизи |
