Патология системы крови-1. Патология системы крови
 Скачать 0.79 Mb. Скачать 0.79 Mb.
|
|
Симптоматическое лечение Симптоматическая терапия имеет целью облегчение состояния пациента. Для этого устраняют неприятные, тягостные ощущения (болевые, психоэмоциональные и др.), а также проводят мероприятия по устранению недостаточности функции органов и физиологических систем. Профилактика Профилактика повторного развития ДВС — ликвидации или предупреждении возникновения условий, провоцирующих развитие ДВС (терапия основного заболевания, введение гепарина при гиперкоагуляции, повторные трансфузии свежезамороженной плазмы). Прогноз Прогноз во многом зависит от эффективности терапии основного заболевания, своевременности диагностики ДВС-синдрома, адекватности лечебных мероприятий. Летальность при ДВС составляет 40–60%. Основные причины смерти: острая почечная недостаточность, дыхательная недостаточность, кровоизлияние в мозг, надпочечники, острая кровопотеря, приводящая к развитию шока и комы. Гемобластозы Гемобластозы — опухоли, возникающие из кроветворных клеток гемопоэтической ткани. Гемобластозы занимают первое место как причина смерти среди всех болезней системы крови. Гемобластозы подразделяют на лейкозы (опухоли, диффузно — системно –поражающие гемопоэтические клетки костного мозга), лимфомы (внекостномозговые плотные, растущие в виде узла или нескольких узлов, опухоли из лимфопролиферативных кроветворных клеток) и миелопролиферативные новообразования (миеломы). В клинической практике используют не родовое понятие «лейкоз», а названия конкретных нозологических форм лейкоза (разных его стадий и определённых иммуно-, фено- и генотипов), каждая из которых подразумевает конкретную программу лечения. Так, согласно МКБ–10, к злокачественным новообразованиям «лимфоидной, кроветворной и родственных им тканей» (коды МКБ — C81–C96) относятся болезнь Ходжкена (лимфогранулематоз), неходжкенские лимфомы (лимфосаркомы), злокачественные иммунопролиферативные болезни (в том числе макроглобулинемия Вальденстрёма), множественная миелома, лимфоидный лейкоз (лимфолейкоз), миелоидный лейкоз (миелолейкоз), истинная полицитемия и ряд других опухолей. Для лимфоидных гемобластозов предложена классификация REAL (Revised Europian–American classification of Lymphoid neoplasms, см. статью «Классификация REAL» в приложении «Справочник терминов» на компакт диске). В клинической литературе лимфомы (растущих вне костного мозга очаговые опухоли из кроветворных клеток) обозначают как гематосаркомы (син.: лимфосаркомы). К гематосаркомам относят также миело-, эритро-, мегакариосаркомы, а также морфологически недифференцируемые гематосаркомы. При метастазировании гематосарком в костный мозг опухолевый процесс приобретает генерализованный характер. Этот феномен обозначают как лейкемизация гематосарком. Характеристики отдельных лимфом приведены в статье «Лимфомы» приложения «Справочник терминов» на компакт диске. В этом же приложении рассмотрены этиология, патогенез, проявления и принципы терапии других гемобластозов: истинной полицитемии, лимфогранулематоза (болезни Ходжкена), миеломной болезни, макроглобулинемии Вальденстрёма. Общая характеристика лейкозов Лейкоз — системное опухолевое поражение гемопоэтических клеток костномозговой ткани. Для обозначения лейкозов не рекомендуется применять старый, предложенный еще Р. Вирховым, термин «лейкемия» (белокровие) в связи с тем, что к лейкозам относятся, помимо опухолей из лимфо- и миелопоэтических клеток, также и новообразования из клеток эритро- и мегакариоцитарных ростков. Этиология Причины Причинами лейкозов являются те же группы факторов, которые вызывают опухоли (см. главу 17 «Опухоли»). Факторы риска • Наследственное предрасположение. Описаны доминантное и рецессивное наследование хронического лимфолейкоза (ХЛЛ), а также низкая заболеваемость этим лейкозом в одних этнических группах и высокая в других. Чаще в этих случаях наследуется не сам лейкоз, а нестабильность генома — сниженная резистентность хромосом к действию мутагенов, предрасполагающая родоначальные миелоидные или лимфоидные клетки к опухолевой (лейкозной) трансформации. • Применение лекарственных средств с цитостатическим действием. Вероятность возникновения острых лейкозов у больных, лечившихся цитостатиками, повышается в сотни раз. • Воздействие на организм проникающей радиации и/или рентгеновского излучения (в том числе- с лечебной целью). Минимальный интервал времени до возникновения лейкоза после облучения составляет 5–10 лет, а после химиотерапии — 2 года (максимум в течение 6–10 лет). Патогенез Трансформация нормальных гемопоэтических клеток в опухолевые является результатом изменений в генетической прграмме. Основную роль при этом играют хромосомные нарушения. В большинстве случаев они определяют прогноз болезни и тип специфического лечения. Нестабильность генома лейкозных клеток приводит к появлению в первоначальном опухолевом клоне новых субклонов, среди которых в процессе жизнедеятельности организма, а также под воздействием лечения "отбираются" наиболее автономные (этот феномен получил название «опухолевая прогрессия»). Этим феноменом объясняют прогредиентность течения лейкозов, их «уход» из-под контроля цитостатиков и генерализация процесса. Этиология, патогенез, проявления и принципы лечения различных лейкозов (лейкоз острый, миелолейкоз хронический, лимфолейкоз хронический) рассмотрены в разделе «Лейкозы» настоящей главы. Характеристика отдельных видов лимфом приведена в статье «Лимфомы» приложения «Справочник терминов» на компакт диске. В этом же приложении рассмотрены этиология, патогенез, проявления и принципы терапии других гемобластозов: истинной полицитемии, лимфогранулематоза (болезни Ходжкена), миеломной болезни, макроглобулинемии Вальденстрёма. Опухолевый атипизм Атипизм гемобластозов — совокупность существенных качественных и количественных отличий биологических свойств гемобластозных клеток от нормальных и других патологически изменённых (но не трансформированных) клеток и тканей. В основе формирования атипизма гемобластозов лежит процесс опухолевой прогрессии. Опухолевая прогрессия Опухолевая прогрессия по своему существу является механизмом нарастания степени злокачественности клеток гемобластозов в результате изменений их генетической программы. Повышенная и постоянная изменчивость различных свойств гемобластозов, обусловливая их гетерогенность и автономность, создаёт условия для всё большей приспособленности их клеток к условиям среды, включая и возможность «ускользания» от цитостатической терапии. Признаки опухолевой прогрессии гемобластозов Проявления опухолевой прогрессии гемобластозов приведены на рис. 21–34. 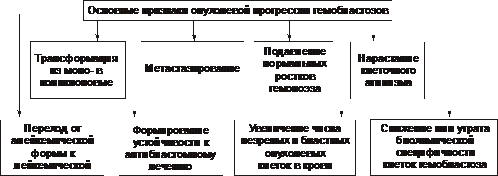 Рис. 21–34. Признаки опухолевой прогрессии гемобластозов. Процесс опухолевой прогрессии ведет к формированию и/или нарастанию степени атипизма роста, обмена, структуры и функции лейкозов. Атипизм роста Проявления атипизма роста лейкозов представлены на рис. 21–35. 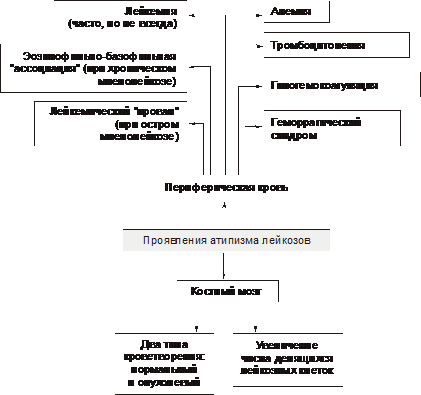 Рис. 21–35. Основные проявления атипизма роста лейкозов. • Костный мозг. † Наличие клеток, относящихся к двум качественно разным типам гемопоэза: нормальному и опухолевому. † Увеличение числа делящихся гемопоэтических клеток («омоложение» состава гемопоэтических клеток). Это сопровождается нарастанием количества атипичных бластных и молодых нормальных клеток гемопоэтической ткани. • Периферическая кровь. † Лейкемия (белокровие, от гр. leukos белый, haima кровь). Наблюдается часто, но не всегда и характеризуется увеличением количества лейкозных клеток различной степени зрелости (бластных, созревающих). В зависимости от общего количества лейкоцитов и наличия бластных клеток в единице объёма крови при лейкозах выделяют четыре формы лейкоза. ‡ Лейкемическая: число лейкоцитов превышает 30–50 ‡ Сублейкемическая: Количество лейкоцитов выше нормы (но до 30–50 ‡ Лейкопеническая: число лейкоцитов ниже нормы, сравнительно небольшое количество бластных лейкозных клеток. ‡ Алейкемическая: количество лейкоцитов в диапазоне нормы, бластные клетки отсутствуют. Атипичные лейкоциты, их бластные и молодые формы находят лишь в ткани костного мозга. † Лейкемический «провал» (лейкемические «ворота» [hiatus leukaemicus], лейкемическое «зияние»). Выявляется при остром миелобластном лейкозе и характеризуется наличием в периферической крови бластных, молодых и зрелых форм лейкозных клеток и отсутствием одной или нескольких переходных форм гемопоэза. С этим и связано название признака — лейкемический «провал». † Анемия. Является спутником большинства лейкозов, в особенности острых. † Тромбоцитопения и снижение свёртываемости крови. † Геморрагический синдром. Характеризуется частыми кровотечениями, в том числе в полости тела и полые органы (желудок, кишечник, пищевод, мочевой пузырь и др.), а также кровоизлияниями. Атипизм обмена Атипизм обмена характеризуется отклонением от нормы биохимических характеристик клеток и/или продуктов их метаболизма. Помимо общих признаков опухолевого атипизма обмена углеводов, белков, липидов, ионов, минералов, КЩР (см. главу 17 «Опухолевый рост»), для лейкозов характерен ряд специфичных признаков. • Прекращение синтеза лейкозными клетками отдельных ферментов (например, кислой фосфатазы, миелопероксидазы) и, как следствие — катализируемых или процессов. • Пара и диспротеинемии. Парапротеинемия наблюдается при миеломной болезни, макроглобулинемии Вальденстрёма, болезни тяжёлых цепей Франклина. Атипизм структуры Характеризуется развитием признаков клеточного (см. главу 17 «Опухолевый рост») и тканевого атипизма (проявляющегося наличием двух типов клеток в гемопоэтической ткани и периферической крови — нормальных и опухолевых). Подробнее характеристику атипизма структуры лейкозов см. в учебниках по патологической анатомии. Атипизм функций При лейкозах нарушаются функции как трансформированных (лейкозных), так и нормальных лейкоцитов. Это приводит к существенным нарушениям фагоцитарной активности, механизмов реализации клеточного и гуморального иммунитета. В совокупности указанные нарушения обусловливают развитие иммунодефицита и в том числе снижение противоинфекционной устойчивости и антибластомной резистентности организма. Характеристика отдельных, наиболее часто встречающихся лейкозов. Ниже рассмотрены острые и хронические формы лейкозов как пример современного подхода к патогенезу, типированию конкретных стадий, проявлениям и принципам лечения онкогематологических заболеваний. Острый лейкоз Клеточным субстратом острых лейкозов являются бластные опухолевые клетки. Острый лейкоз без лечения приводит к смертельному исходу в течение нескольких недель или месяцев. При правильном и своевременном лечении прогноз для детей часто благоприятен. Острые лейкозы подразделяют на миелоидные (острый миелолейкоз), лимфоидные (острый лимфолейкоз ), монобластные (миеломонобластные), эритромиелобластные и мегакариобластные. Хронический лейкоз Морфологический субстрат хронических лейкозов — относительно дифференцированные клетки кроветворной ткани. Больные могут жить без лечения в течение нескольких месяцев и лет. Хронические лейкозы нередко трансформируются в острые формы. Хронические лейкозы подразделяют на миелоидные (хронический миелолейкоз — ХМЛ), лимфоидные (хронический лимфолейкоз — ХЛЛ и волосатоклеточный лейкоз), моноцитарные (миеломоноцитарные), эритроцитарные (истинная полицитемия) и мегакариоцитарные. Острые лейкозы Острые лейкозы — злокачественные заболевания кроветворной системы, морфологический субстрат — бластные клетки. Наиболее часто диагносируются острый лимфобластный лейкоз (ОЛЛ) и острый миелоидный лейкоз. Частота Частота острых лейкозов 13,2:100 000 среди мужчин и 7,7:100 000 среди женщин. ОЛЛ чаще развивается в детском возрасте и после 40 лет. Частота острого миелоидного лейкоза одинакова во всех возрастных группах. Патогенез Патогенез острого лейкоза обусловлен пролиферацией клона опухолевых клеток с характерными цитогенетическими нарушениями, угнетением нормального кроветворения, выходом бластных клеток в кровь, метастазированием их в другие кроветворные (селезёнка, печень, лимфоузлы) и некроветворные (кожа, ЦНС, яички, лёгкие) органы. Виды острого лейкоза Существенный момент диагностики и последующей терапии любого лейкоза — типирование заболевания у конкретного больного. Критерии типирования лейкозов представлены на рис. 21–36. 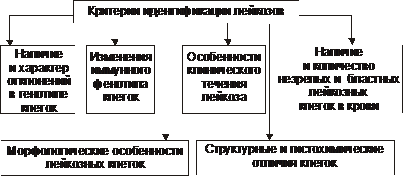 Рис. 21–36. Критерии типирования лейкозов. В основу классификаций острых лейкозов положены внешний вид и цитохимические особенности бластных клеток, их иммунофенотип и генетические особенности. Так, франко-американо-британская (FAB) классификация основана на оценке морфологии лейкозных клеток (строение ядра, соотношение размеров ядра и цитоплазмы). Острый миелоидный лейкоз Виды острого миелоидного лейкоза приведены в табл. 21–6. Таблица 21-6. Варианты острых миелоидных лейкозов (классификация ВОЗ, 1999).
ОМЛ — острый миелоидный лейкоз Об уровне дифференцировки лимфоидных клеток свидетельствует экспрессия на поверхности их ядерной мембраны, в цитоплазме и на цитоплазматической мембране различных Аг, «кластеров дифференцировки», обозначаемых аббревиатурой CD (от англ. cluster of differentiation). Иммунофенотипическая характеристика миелобластных лейкозов приведена в таблице 21-7. Таблица 21–7. Иммунофенотипическая характеристика миелобластных лейкозов.
По: «Внутренние болезни», М: ГЭОТАР–МЕД, 2001. Условные обозначения: «+» — выраженная экспрессия Аг; «+/–» — вариабельная экспрессия Аг; «–» — отсутствие экспрессии Аг |
