Патология системы крови-1. Патология системы крови
 Скачать 0.79 Mb. Скачать 0.79 Mb.
|
|
Рис. 21–23. Изменения в системе гемостаза при тромбоцитопениях. Терапия тромбоцитопений Этиотропный принцип Предусматривает прекращение (уменьшение степени) патогенного действия факторов, вызывающих тромбоцитопению. Для этого проводят спленэктомию и удаляют гемангиомы, необходимы также защита от лучистой энергии; замена вызывающих тромбоцитопению ЛС, предупреждение попадания в организм веществ, обусловливающих тромбоцитопению (этанола, соединений золота и др.), инактивация и элиминация противотромбоцитарных АТ и др. Патогенетический принцип С целью уменьшения «потребления» и/или разрушения тромбоцитов, активации тромбоцитопоэза, нормализации содержания и активности в крови про- и антиагрегантов, факторов свёртывающей, противосвёртывающей и фибринолитической систем проводят трансфузию тромбоцитов, пересадку костного мозга, используют лимфо- и/или плазмоферез (удаление из крови антитромбоцитарных АТ и лимфоцитов), а также иммунодепрессанты; антикоагулянты, антиагреганты. Симптоматический принцип Для нормализации функций органов и их систем, нарушенных вследствие тромбоцитопении, проводят вливание цельной крови и тромбоцитарной массы, а также лечение постгеморрагических состояний. Тромбоцитопатии Тромбоцитопатии — состояния, характеризующиеся нарушением свойств тромбоцитов (адгезивного, агрегационного, коагуляционного) и, как правило, расстройствами гемостаза. Тромбоцитопатиям (в отличие от тромбоцитопений) свойственны стабильные, длительно сохраняющиеся функциональные, биохимические и морфологические изменения в тромбоцитах. Они наблюдаются даже при нормальном количестве тромбоцитов и не исчезают при устранении тромбоцитопении (если таковая имелась). Виды Тромбоцитопатии подразделяют на первичные (наследственные и врождённые) и вторичные (приобретённые). • Первичные тромбоцитопатии. Развиваются при генных дефектах. Примеры: болезнь фон Виллебранда, тромбастения Глянцманна, недостаточность тромбоксан A синтетазы. • Вторичные тромбоцитопатии. Развиваются при воздействии химических и биологических факторов. † Химические факторы. ‡ Избыток продуктов обмена веществ, в норме выводящихся почками. Считают, что они (возможно, креатинин) деполимеризуют крупномолекулярные полимеры фактора VIII. ‡ Некоторые ЛС (подробнее см. в разделе «Этиология» статьи «Тромбоцитопатии» в приложении «Справочник терминов» на компакт диске). ‡ Гиповитаминозы (дефицит аскорбиновой кислоты, цианкобаламина). † Биологические факторы. ‡ Вещества, образующиеся в опухолевых клетках. Они нарушают деление и созревание мегакариоцитов. Это наблюдается при различных формах лейкозов или метастазах солидных опухолей в кроветворную ткань. ‡ Продукты деградации фибриногена и фибрина (ДВС–синдром). ‡ Повышенное содержание в плазме крови нормальных и аномальных белков при болезни Вальденстрёма и миеломной болезни. ‡ Повышенная концентрация в плазме крови факторов свёртывающей системы (например, при переливании больших доз крови, плазмы, концентратов прокоагулянтов). Патогенез тромбоцитопатий В основе развития как первичных, так и вторичных тромбоцитопатий лежит расстройство одного или нескольких процессов (рис. 21–24). 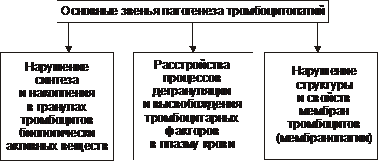 Рис. 21–24. Основные звенья патогенеза тромбоцитопатий. Парциальная или сочетанная реализация указанных механизмов обусловливает либо преимущественное нарушение контактной активности тромбоцитов (их агрегация и/или адгезия), либо преимущественные расстройства их прокоагулянтных свойств. • Нарушение контактной активности тромбоцитов. В большинстве случаев включает одно, а иногда несколько из указанных ниже звеньев: † Нарушения синтеза и/или накопления в гранулах тромбоцитов их содержимого. Эти нарушения ведут к расстройствам гемостаза и состояния эндотелия стенок сосудов. † Расстройства механизма дегрануляции при взаимодействии тромбоцитов с агрегирующими факторами — АДФ, катехоламинами, тромбоксаном А2, коллагеном и др. Эти расстройства, как и нарушения синтеза и/или накопления в гранулах их компонентов, снижают контактную (адгезивную и агрегационную), а также прокоагулянтную активность тромбоцитов (способность инициировать процесс тромбообразования). † Аномалии физико химических свойств и/или химического состава и структуры мембран тромбоцитов. Чаще наблюдаются дефицит гликопротеинов, нарушения структуры и соотношения различных фракций мембранных фосфолипидов. Эти изменения также обусловливают нарушения адгезивно агрегационной активности тромбоцитов. • Нарушения прокоагулянтной активности тромбоцитов включает: † Снижение синтеза, содержания и/или активности фосфолипидного фактора 3 тромбоцитов (фактора коагуляции белков крови). Этот фактор при совместном действии с другими прокоагулянтами обусловливает переход протромбина в тромбин. † Нарушение высвобождения тромбоцитарного фактора 3 из тромбоцитов. Обусловлено наследуемыми, врождёнными или приобретёнными мембранопатиями, аномалиями канальцев и элементов цитоскелета тромбоцитов. Это препятствует взаимодействию фактора 3 тромбоцитов с плазменными факторами гемокоагуляции на поверхности тромбоцитов. Указанные аномалии приводят к нарушениям процесса свёртывания белков крови и тромбообразования. • У ряда пациентов выявляются аномалии механизмов и контактной, и прокоагулянтной активности тромбоцитов одновременно. Так, при синдроме ВискоттаОлдрича отмечается нарушение образования и хранения компонентов плотных гранул различного типа тромбоцитов, а также освобождения их содержимого. Эти изменения сопровождаются расстройством адгезивной, агрегационной и прокоагулянтной активности тромбоцитов. Проявления тромбоцитопатий • Геморрагический синдром. Проявляется внутренними и внешними кровотечениями, а также кровоизлияниями в различные органы, ткани, кожу, слизистые оболочки. • Различные расстройства микрогемоциркуляции: изменения объёма и скорости кровотока в сосудах микроциркуляторного русла, турбулентный его характер и др. Это нередко ведёт к нарушениям обмена веществ в тканях (в связи с развитием капилляро-трофической недостаточности), различным дистрофиям, эрозиям и изъязвлениям. • Значительные изменения функциональных свойств тромбоцитов (адгезивного, агрегационного, прокоагуляционного). • Дефекты гранул тромбоцитов: отсутствие или уменьшение их числа (например, при синдроме серых тромбоцитов), нарушение высвобождения их содержимого. • Отклонения от нормы размера и формы мегакариоцитов и тромбоцитов. Лечение тромбоцитопатий Лечение тромбоцитопатий представляет сложную задачу, и у многих пациентов (особенно с наследственными и врождёнными формами) проводится в течение всей жизни. Этиотропный принцип Направлен на прекращение действия (защиту от воздействия) факторов физического, химического, биологического характера, лечение болезней, патологических процессов и состояний, вызывающих тромбоцитопатию. Патогенетический принцип Для предотвращения (уменьшения степени) нарушений адгезивной, агрегационной и прокоагулянтной активности тромбоцитов необходимо введение проагрегантов, инъекции прокоагулянтов и/или антифибринолитических препаратов ( Симптоматический принцип Для нормализации функций органов и тканей, нарушенных вследствие расстройств микрогемоциркуляции, кровотечений и кровоизлияний при тромбоцитопатии, необходимо вводить растворы, нормализующие реологические свойства крови (плазмозаменители, плазма), остановить кровотечение, лечить постгеморрагические состояния. Нарушения гемостаза Система гемостаза — комплекс факторов и механизмов, обеспечивающих оптимальное состояние агрегатного состояния форменных элементов крови (рис. 21–25). 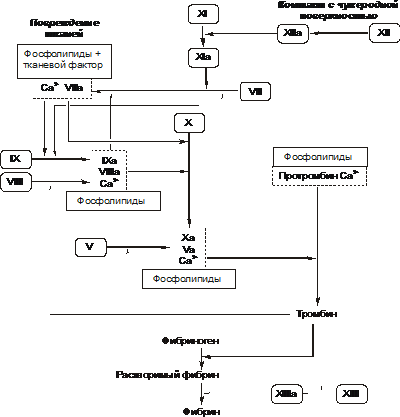 Рис. 21-25. Гемокоагуляционный каскад. Активация фактора XII запускает внутренний механизм; высвобождение тканевого фактора и активация фактора VII запускают наружный механизм коагуляции. Оба пути приводят к активации фактора Х (ДМ Зубаиров, 1995) В узком (прикладном) смысле термин «гемостаз» (от гр. haima кровь, stasis остановка) применяют для обозначения собственно процесса остановки кровотечения. • Система гемостаза включает факторы и механизмы трёх категорий: † обеспечивающие коагуляцию белков крови и тромбообразование (свёртывающая система), † обусловливающие торможение или блокаду коагуляции белков плазмы и процесс тромбообразования (противосвёртывающая система), † реализующие процессы лизиса фибрина (фибринолитическая система). • Биологическая роль системы гемостаза состоит в обеспечении оптимальных реологических свойств крови и реализации процесса гемокоагуляции, адгезии, агрегации и активации форменных элементов крови с образованием тромба при повреждении стенок сосудов или сердца. Это предотвращает или уменьшает потерю крови организмом. • Типовые формы патологии системы гемостаза. Многочисленные нарушения системы гемостаза подразделены на три группы. † Усиление свёртываемости крови и тромбообразования — гиперкоагуляция и развитие тромботического синдрома. † Уменьшение свёртываемости крови и тромбообразования — гипокоагуляция и развитие геморрагических синдромов. † Фазное нарушение состояния системы гемостаза (ДВС-синдром): фаза гиперкоагуляции, сопровождаясь интенсивным потреблением прокоагулянтов, переходит в фазу гипокоагуляции. Развивается коагулопатия потребления и тромбогеморрагический синдром. Тромботический синдром Тромботический синдром, или тромбофилия (от гр. thrombos ком, сгусток, phileo люблю) — состояние, характеризующееся чрезмерной (неадекватной) коагуляцией крови и тромбообразованием, ведущими к ишемии тканей и органов. Основные причины • Повреждение стенок сосудов и сердца (например, при их механической травме, атерогенезе, васкулитах, ангиопатиях у пациентов с СД). • Патология форменных элементов крови (например, тромбоцитопатии, гемолиз эритроцитов, чрезмерное повышение адгезии и агрегации тромбоцитов и эритроцитов). • Патология факторов системы гемостаза. † Абсолютное или относительное преобладание эффектов прокоагулянтных факторов. † Недостаточность антикоагулянтных и фибринолитических факторов (например, при системном атеросклерозе, СД, гипертонической болезни, эндотоксинемиях, шоковых состояниях). Механизмы Механизмы гиперкоагуляции и тромботического синдрома представлены на рис. 21–26.  Рис. 21–26. Основные механизмы гиперкоагуляции и тромботического синдрома. • Чрезмерная активация прокоагулянтов и проагрегантов. Наиболее частые причины. † Гиперлипопротеинемии. Липопротеины активируют фактор Хагемана (фактор свёртывания ХII) и стимулируют активность протромбиназы. † Повышенный уровень антифосфолипидных АТ (IgG, IgM) при антифосфолипидном синдроме. АТ к анионным фосфолипидам стимулирует реакцию высвобождения из тромбоцитов, эндотелиоцитов, кардиомиоцитов и некоторых других клеток прокоагулянтов и их последующую активацию. Такой механизм тромбообразования выявляется, например, при СКВ и ишемической болезни сердца (ИБС). † Массированные травмы мягких тканей (например, при механическом повреждении органов, тканей, конечностей, синдроме длительного раздавливания), ожоги большой площади, шоковые состояния, сепсис. • Увеличение концентрации в крови прокоагулянтов и проагрегантов (фибриногена, протромбина, акцелерина, проконвертина, тромбина, и др.). † Наиболее частые причины. ‡ Гиперкатехоламинемия. Катехоламины активируют процесс синтеза фибриногена (например, при патогенном стрессе или феохромоцитоме). ‡ Гиперкортицизм (с гиперпродукцией глюкокортикоидов). Глюкокортикоиды стимулируют образование протромбина, проакцелерина, фибриногена. ‡ Атеросклеротическое поражение стенок артерий. Потенцирует синтез фибриногена, протромбина, фактора Хагемана, антигемофилических глобулинов и др. ‡ Септицемия. Стимулирует гиперпродукцию тканевого тромбопластина. † Последствия чрезмерной активации и/или увеличения в крови прокоагулянтов и проагрегантов: гиперкоагуляция белков крови, адгезия, агрегация и активация форменных элементов крови, образование единичных тромбов, генерализованный тромбоз (наблюдается при синдроме ДВС). • Снижение содержания и/или угнетение активности прокоагулянтов и проагрегантов. Наиболее частые причины. † Наследственный дефицит антитромбина. Характеризуется снижением синтеза антитромбина III, а также его сродства к гепарину. † Печёночная, почечная или панкреатическая недостаточность. Все эти состояния обусловливают снижение синтеза гепатоцитами антитромбина III. † Гиперлипопротеинемии. Обусловливают снижение уровня гепарина в крови (за счёт его адсорбции на поверхности форменных элементов крови и иммунных комплексов, например при СКВ или пурпуре Шёнляйна Геноха). † Наследственная или приобретённая недостаточность протеинов С и S. Вторичный (приобретённый) дефицит этих белков наблюдается при печёночной недостаточности, СД, лейкозах, массивных травмах, респираторном дистресс синдроме взрослых. • Уменьшение уровня и/или подавление активности фибринолитических агентов. Наиболее частые причины. † Подавление синтеза и выделение клетками в кровь активатора плазминогена. Наблюдается у пациентов с атеросклерозом, инфарктом миокарда, ревматоидным артритом). † Наследственная или приобретённая гиперпродукция антиплазминов. † Снижение продукции фактора ХII (например, при васкулитах или ДВС–синдроме). Именно это послужило причиной смерти больного тромбофилией по фамилии Хагеман (его именем назван фактор ХII). Последствия гиперкоагуляции и тромбоза • Нарушения центральной, органно тканевой и микрогемоциркуляции с исходом в инфаркт. При этом характер и тяжесть нарушений кровообращения определяются видом сосуда, поражённого тромбозом (артерии или вены, микрососуды или магистральные стволы), количеством тромбированных сосудов, наличием коллатералей и условий для их развития, скоростью и масштабом процесса тромбообразования, значимостью для организма, органа или ткани. Наиболее опасны тромбы в сосудах мозга, сердца, лёгкого, поджелудочной железы, надпочечников, кишечника. • Расстройства кровообращения, не завершающиеся инфарктом. Они обусловливают гипоксию тканей и органов (первично циркулярного типа), развитие дистрофических изменений и снижение их функций, гипотрофию и гипоплазию тканевых и клеточных элементов, сдавление ткани дистальнее места пристеночного венозного тромба (расширенной веной и отёчной тканью), образование тромбоэмболов (чаще в связи с разрушением венозного тромба). Геморрагические заболевания и синдромы Геморрагические заболевания и синдромы — патологические состояния, характеризующиеся повышенной кровоточивостью в результате недостаточности одного или несколько элементов гемостаза. Этиология Выделяют наследственные и приобретённые формы геморрагических заболеваний и синдромов. • Наследственные формы связаны с генетически детерминированными патологическими изменениями сосудистой стенки, аномалиями мегакариоцитов, тромбоцитов, адгезионных белков плазмы крови и плазменных факторов свёртывающей системы крови. • Приобрётенные формы в большинстве случаев обусловлены поражением кровеносных сосудов иммунной, иммунокомплексной, токсикоинфекционной и дисметаболической этиологии (различные васкулиты), поражением мегакариоцитов и тромбоцитов различной этиологии (тромбоцитопатии), патологией адгезионных белков плазмы крови и факторов свёртывающей системы крови и многофакторными нарушениями свёртывающей системы крови (острые синдромы ДВС). Виды геморрагических заболеваний По происхождению различают следующие виды геморрагических заболеваний и синдромов: васкулиты, тромбоцитопении, тромбоцитопатии, коагулопатии, ДВС. • Васкулиты. Обусловлены первичным поражением сосудистой стенки с возможным вторичным развитием коагуляционных и тромбоцитарных нарушений. К этой группе относят наследственную геморрагическую телеангиэктазию Рандю–Ослера, синдром Элерса–Данло, синдром Марфана, гигантские гемангиомы при синдроме Казабаха–Мерритт, геморрагический васкулит Шёнляйна–Геноха, эритемы, геморрагические лихорадки, гиповитаминозы С и В и др. • Тромбоцитопении. Развиваются в результате первичного поражения мегакариоцитарно-тромбоцитарного ростка, перераспределения тромбоцитов и их депонирования в селезёнке, повышенного разрушения (например, при СКВ или идиопатической тромбоцитопенической пурпуре), повышенного потребления тромбоцитов и образования тромбов (ДВС, тромботическая тромбоцитопеническая пурпура), применения некоторых ЛС. • Тромбоцитопатии. Характеризуются наличием аномальных тромбоцитов с нарушением их функций. Наиболее распространённые среди них — тромбастения Глянцманна и болезнь фонВиллебранда. • Коагулопатии. Обусловлены нарушениями свёртываемости крови. † Наследственные коагулопатии: гемофилия А, гемофилия В, болезнь фонВиллебранда, дефицит факторов свёртываемости крови; † Приобретённые коагулопатии: витамин К-зависимые коагулопатии (возникают при недостаточности функции печени, нарушении всасывания витамина К, алиментарной недостаточности витамина К, приёме ЛС, таких как кумарин), ДВС, патология печени (приводит к дефициту многих факторов свёртывания), патологические ингибиторы свёртывания (волчаночный антикоагулянт; специфические ингибиторы свёртывания — АТ, специфичные к отдельным коагуляционным белкам); † Нарушения стабилизации фибрина, повышенный фибринолиз, в том числе при лечении прямыми и непрямыми антикоагулянтами, фибринолитиками (стрептокиназой, урокиназой, алтеплазой и др.); † Другие приобретённые расстройства свёртывания: дефицит факторов свёртываемости крови может возникать при соматических заболеваниях (например, при амилоидозе — дефицит фактора Х). • ДВС. Являются следствием комплексных нарушений различных звеньев системы гемостаза. |
