ываыва. Предмет и задачи клинической фармакологии. Основные разделы клинической фармакологии. Виды фармакотерапии
 Скачать 1.13 Mb. Скачать 1.13 Mb.
|
|
Всасывание (абсорбция) – процесс поступления ЛС из места их введения в системный кровоток. МЕХАНИЗМЫ АБСОРБЦИИ (ВСАСЫВАНИЯ) • пассивная диффузия – прохождение низкомолекулярных соединений через биологические мембраны по градиенту концентрации • фильтрация (конвекционный транспорт) – прохождение молекул лекарственного вещества через поры мембран • активный транспорт – прохождение молекул лекарственного вещества через биологические мембраны с участием транспортных систем и потреблением энергии, может протекать против градиента концентрации (характерны избирательность, конкуренция за носитель и «насыщаемость») • облегченный транспорт – подобен активному транспорту, но не сопровождается потреблением энергии • пиноцитоз – сходен с фагоцитозом. Скорость высвобождения из лекарственных форм. В зависимости от степени управления процессом высвобождения различают: I - лекарственные формы с контролируемым высвобождением; II - лекарственные формы пролонгированные. Обе эти группы в зависимости от кинетики процесса могут подразделяться на лекарственные формы: • с периодическим высвобождением; • с непрерывным высвобождением; • с отсроченным высвобождением. Большинство современных лекарственных форм имеет разновидности с модифицированным высвобождением. К формам с модифицированным временем наступления эффекта относятся лекарственные формы: 1 - рапид; 2 - максирапид; 3 - регуляр; 4 - формы с замедленным (отсроченным) действием. К формам с модифицированной продолжительностью действия относятся лекарственные формы: 1 - с продленным действием; 2 - с повторным действием; 3 - с поддерживающим действием. К формам с модифицированной выраженностью действия относятся лекарственные формы: 1 - форте; 2 - семи; 3 - мите. Пути выведения ЛС, их преимущества и недостатки. Энтеральный путь введения ЛС: сублингвальный, пероральный, ректальный. Лекарственные средства чаще всего вводят в желудочный тракт (через рот или прямую кишку). Достоинством этого пути является удобство применения (не требуется помощь медицинского персонала), а также сравнительная безопасность и отсутствие осложнений, характерных для парентерального введения. Лекарственные препараты, вводимые энтерально, могут оказывать как местное (некоторые противомикробные и противоглистные средства), так и системное действие. Прием внутрь через рот (peros). При лечении заболеваний внутренних органов перорально следует назначать лекарственные средства, которые хорошо всасываются слизистой оболочкой желудка или кишечника. Если необходимо создать высокую концентрацию препарата в желудочно-кишечном тракте, наоборот, используют лекарственные средства, которые плохо всасываются, что позволяет получить хороший эффект при отсутствии системных побочных реакций. При тяжелом течении некоторых заболеваний, например, дизентерии, желательно, чтобы концентрация лекарственных средств была высокой как в просвете кишечника, так и в крови. Недостатками перорального пути применения лекарственных средств при необходимости получения системного эффекта являются следующие: относительно медленное развитие терапевтического действия; возможность больших индивидуальных различий в скорости и полноте всасывания; влияние пищи и других лекарственных средств на всасывание; невозможность применения лекарственных веществ, плохо абсорбирующихся слизистой оболочкой желудка и кишечника (например, стрептомицина) и разрушающихся в просвете желудка и кишечника (инсулин, окситоцин и т.д.) или при прохождении через печень (гормоны), а также веществ, оказывающих сильное раздражающее действие. Введение лекарственных средств через рот невозможно или очень неудобно при рвоте и бессознательном состоянии больного. Внутрь лекарственные вещества вводят в форме растворов, порошков, таблеток, капсул, пилюль. Чтобы предотвратить раздражающее действие некоторых лекарственных веществ на слизистую оболочку желудка, используют таблетки, покрытые пленками, устойчивыми к действию желудочного сока, но распадающимися в щелочной среде кишечника. Имеются лекарственные формы (таблетки с многослойными оболочками и т.п.), обеспечивающие постепенное, длительное высвобождение действующего начала, что позволяет пролонгировать терапевтическое действие препарата. Следует помнить о том, что некоторые таблетки и капсулы в случае их приема больными в положении лежа могут задерживаться в пищеводе и вызывать его изъязвление, особенно у пожилых людей, у которых нарушена перистальтика. Для профилактики этого осложнения таблетки и капсулы следует запивать большим количеством воды. Применение под язык (сублингвально). Слизистая оболочка ротовой полости имеет обильное кровоснабжение, поэтому всасывающиеся через нее вещества быстро попадают в системный кровоток и начинают действовать через короткое время. Сублингвально особенно часто применяют нитроглицерин для купирования приступов стенокардии, а такженифедипин и клофелин при гипертонических кризах. При сублингвальном применении лекарственное средство не подвергается действию желудочного сока и попадает в системный кровоток по венам пищевода, минуя печень, что позволяет избежать его биотрансформации. Препарат следует держать под языком до полного рассасывания. Проглатывание его части со слюной снижает преимущества этого пути введения лекарственных средств. При частом сублингвальном применении лекарственных средств может возникнуть раздражение слизистой оболочки ротовой полости. Введение в прямую кишку (ректальное). Прямая кишка имеет густую сеть кровеносных и лимфатических сосудов, поэтому многие лекарственные вещества (особенно неионизированные жирорастворимые соединения) хорошо всасываются с поверхности ее слизистой оболочки. Вещества, абсорбирующиеся в нижней части прямой кишки, через нижние геморроидальные вены попадают в системный кровоток, минуя печень. Ректальное введение препаратов позволяет избежать раздражения желудка. Кроме того, таким образом можно применять лекарственные средства в тех случаях, когда затруднено или неосуществимо их введение per os (тошнота, рвота, спазм или непроходимость пищевода). К недостаткам этого пути относят выраженные индивидуальные колебания в скорости и полноте всасывания препаратов, психологические затруднения и неудобства применения (на работе, в путешествии и т.п.). Ректально вводят свечи (суппозитории) и жидкости с помощью клизм. Этот путь введения используют как для получения местного (например, при язвенном колите), так и системного эффекта. Парэнтеральный путь введения: внутривенное, внутриартериальное, внутримышечное, подкожное введение. Способы применения лекарственных средств, при которых они не вводятся в желудочно-кишечный тракт, называются парентеральными. К парентеральным способам относятся различные виды инъекций, ингаляции, электрофорез и поверхностное нанесение препаратов на кожу и слизистые оболочки. Внутривенное введение. Введение лекарственных веществ в вену обеспечивает быстрое наступление и точное дозирование эффекта; быстрое прекращение поступления препарата в кровяное русло при возникновении побочных реакций; возможность введения веществ, которые не всасываются из желудочно-кишечного тракта или раздражают его слизистую оболочку. При внутривенном введении лекарственных средств следует соблюдать предосторожность. Прежде чем вводить препарат, необходимо убедиться в том, что игла находится в вене. Попадание лекарственного вещества в околовенозное пространство может сопровождаться сильным раздражением, вплоть до некроза тканей. Некоторые препараты, например сердечные гликозиды, вводят очень медленно, так как быстрое повышение их концентрации в крови может быть опасным. Внутриартериальное введение. Для лечения заболеваний некоторых органов (печень, конечности) лекарственные вещества, которые быстро метаболизируются или связываются тканями, вводят в артерию. При этом высокая концентрация препарата создается только в соответствующем органе, а системного действия удается избежать. Следует помнить, что возможный тромбоз артерии является значительно более серьезным осложнением, чем тромбоз вены. Внутримышечное введение. При внутримышечном введении препарата обеспечивается относительно быстрое наступление эффекта (растворимые лекарственные вещества всасываются в течение 10-30 мин). Таким образом можно применять лекарственные средства, оказывающие умеренное раздражающее действие, а также депо-препараты. Объем вводимого вещества не должен превышать 10 мл. После введения препаратов внутримышечно могут появиться местная болезненность и даже абсцессы. Не следует делать инъекции вблизи нервных стволов, так как раздражающие вещества могут повреждать нервные волокна, в результате чего появляются сильные боли, а иногда парез мышц. Опасным может оказаться случайное попадание иглы в кровеносный сосуд. Подкожное введение. При подкожном введении всасывание лекарственных веществ, а следовательно, и проявление терапевтического действия происходит медленнее, чем при внутримышечном и внутривенном введении. Однако эффект сохраняется более длительно. Следует помнить, что подкожно введенные вещества плохо всасываются при недостаточности периферического кровообращения (например, при шоке). Парэнтеральный путь введения: ингаляционный, интратекальный, местное применение, электрофорез. Способы применения лекарственных средств, при которых они не вводятся в желудочно-кишечный тракт, называются парентеральными. К парентеральным способам относятся различные виды инъекций, ингаляции, электрофорез и поверхностное нанесение препаратов на кожу и слизистые оболочки. Ингаляция. Путем ингаляций лекарственные вещества вводят в виде аэрозолей (b-адреномиметики), газов (летучие анестетики) и порошков (хромогликат натрия). При ингаляционном введении лекарственные вещества быстро всасываются и оказывают местное и системное действие. При использовании газообразных веществ прекращение ингаляции ведет к быстрому прекращению их действия (эфир для наркоза, фторотан). При вдыхании аэрозоля достигается высокая концентрация лекарственного средства в бронхах (беклометазон, сальбутамол) при минимальном системном эффекте. Ингаляционным путем невозможно применение раздражающих лекарственных веществ. Следует помнить о возможном действии ингалируемых лекарственных препаратов, например, средств для наркоза, на окружающих людей. Кроме того, при ингаляциях лекарственные вещества поступают сразу в левые отделы сердца через легочные вены и могут оказать кардиотоксическое действие. Интратекальное введение. Для непосредственного действия на ЦНС лекарственные вещества вводят в субарахноидальное пространство. Так применяют местные анестезирующие средства для спинномозговой анестезии. Этот путь используется также в тех случаях, когда необходимо создать высокую концентрацию вещества (например, антибиотика или глюкокортикоида) в субарахноидальном пространстве. Местное применение. Нанесение лекарственных средств на поверхность кожи или слизистых оболочек используется для получения локального эффекта. Однако некоторые вещества при нанесении их на слизистые оболочки носа, глаз и даже кожу могут всасываться и оказывать системное действие. Например, длительное нанесение на кожу глюкокортикоидов приводит к возникновению у больного побочных реакций, подобных таковым при пероральном применении этих препаратов. В последнее время разработаны особые лекарственные формы, которые фиксируются клейким веществом на коже и обеспечивают медленное и длительное всасывание лекарственного средства, за счет чего увеличивается продолжительность его действия. Таким путем вводятся, например, нитроглицерин и скополамин. Электрофорез. Метод основан на использовании гальванического тока для переноса лекарственных веществ с поверхности кожи в глубоко расположенные ткани. Распределение ЛС. Моделирование фармакокинетических процессов, однокамерная фармакокинетическая модель. Фармакокинетическая кривая, площадь фармакокинетической кривой. РАСПРЕДЕЛЕНИЕ - процесс поступления ЛС из кровеносного русла в органы и ткани, характер которого зависит от того, какой фармакокикетической модели соответствует распределение данного ЛС в организме. Выделяют следующие фармакокинетические модели распределения ЛС: 1) Однокамерная модель - при этом подразумевается фармакокинетическая однородность тканей и распределение ЛС в организме является равномерным. 2) Двухкамерная модель - приэтом ЛС, попав в центральную камеру (под которой обьгчно подразумевают кровь, интенсивно кровоснабжаемые органы и межтканевую жидкость) затем переходит в периферическую камеру (которая включает умеренно и слабо кровоенабжаемые органы и ткани). 3) Трехкамерная модель - при этом наблюдается кумуляция ЛС в каком-либо органе или ткани. Фармакокинетическая кривая отображает изменение концентрации лв. в организме с течением времени. 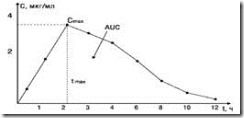 Площадь под кривой “концентрация — время” (A- C) — площадь фигуры, ограниченной фармакокинетической кривой и осями координат (A- C = C0/Kel – константа элиминации). Величина (A- C) связана с другими фармакокинетическими параметрами — объемом распределения, общим клиренсом. При линейности кинетики препарата в организме величина A- C пропорциональна общему количеству (дозе) препарата, попавшего в системный кровоток. Часто определяют площадь под частью кривой (от нуля до некоторого времени t); этот параметр обозначают A- Ct, например, площадь под кривой от 0 до 8 ч — A- C8. Понятие эффекта первичного прохождения через печень. Метаболизм ЛС: несинтетические и синтетические реакции Эффект первого прохождения через печень или ''пресистемная элиминация'' ЭЛИМИНАЦИЯ-1БИОТРАНСФОРМАЦИЯ -2 ВЫВЕДЕНИЕ В НЕИЗМЕННОМ ВИДЕ БИОТРАНСФОРМАЦИЯ- совокупность физико-химических и биохимических процессов, способствующих превращению ЛС в метаболиты, пригодные к удалению из организма. Выделяют два основных типа биотрансформации: 1) микросомальный (катализируемый ферментами, находящимися на мембранах эндоплазматическо-го ретикулума печени и других тканей, способные преобразовываться в везикулы-микросомы); 2) немикросомальный (осуществляемый ферментами другой локализации). В реакциях биотрансформации можно выделить два этапа(ФАЗЫ) : Реакции I фазы (несинтетические) • окисление – гидроксилирование, дезалкилирование, дезаминирование и др. • восстановление – азогруппы, нитрогруппы, дегидрогенизация и др. • гидролиз – эфирный, амидный Реакции II фазы (синтетические) • остатками неорганических и органических кислот, включая аминокислоты – серной, уксусной (ацетилирование), глюкуроновой, глутаминовой, глицином, глутатионом • метильными группами (метилирование) • молекулами воды Выведение ЛС. Понятие клиренса: общий, почечный, печеночный. Экскреция - процесс выделения лс. из организма. Основные пути выведения лекарственных веществ и их метаболитов из организма: почки, потовые железы, лёгкие, кишечник. • Под клиренсом (Clобщ.) понимают объем крови (плазмы, сыворотки), полностью освобождаемый от определенного вещества за единицу времени. • Этот показатель важен для расчета поддерживающей дозы (Dподдерж.) трудно управляемых лекарств: Dподдерж. = CSS´Clобщ где CSS – равновесная концентрация Клиренс выражают в мл/мин или л\ч.Всвязи с тем, что общие пути выведении – почечный и печеночный, общ клиренс складывается из них:почечный отражает выведение ЛП с мочой, печеночный-метаболич.инактивацией ЛС в печени и выведение препарата с желчью (желечный клиренс). Основн физиол.ф-ры, определ-е общий клирес – функцион сост. физиолг.сис-м организма, объем притекающей крови, скорость кровотока в органе. Печеночный клиренс зависит от скорости кровотока в печени и функц сост. метаболизирующих систем.с помощью общего клиренса можно рассчитать поддерж дозу, она= СL/Css (равновесн конц). О выведении ЛСиз организма можно судить по периоду полувыведения или периоду полуэ-лиминации, который определяют как время снижения концентрации препарата в крови на 50% от введенного количества препарата или выведения 50% биодоступного количества препарата. Термин "ПЕРИОД ПОЛУЭЛИМИНАЦИИ" более удачен, чем "ПЕРИОД ПОЛУВЫВЕДЕНИЯ", так как лекарства не только выводятся, но и биотрансформируются. Период полуэлиминации можно определить по графику "концентрация-время", измерив интервал времени, за который любая концентрация вещества на кривой уменьшилась наполовину. За один период полувыведения из организма выводится 50% ЛС, за два периода - 75%, за три периода - 90%, за четыре - 94%. Биологическая доступность, биоэквивалентность. Пик концентрации ЛС в крови. Время достижения максимальной концентрации. БИОДОСТУПНОСТЬотражает ту часть дозы, которая достигла системного кровотока, измеряется в процентах и зависит от: • состояния пациента (шок) • наличия портальной гипертензии • дозы препарата • характеристик лекарственного вещества • формы лекарственного вещества (раствор, суспензия, таблетка, таблетка в оболочке и т.д.) • взаимодействия с пищей Определение биодоступности осуществляется с помощью сопоставления A- C, определяемой при введении одной и той же дозы внутривенно и другим путем. При этом биодоступность при внутривенном введении принимается за 100%. Абсолют. Биодоступ-ть - это доля поглощенного препарата при внесосудистом введении по отношению к его количеству после в/в введения. Относительная биод-ть определяет относительную степень всасывания ЛС из испытуемого препарата и из препаратов сравнения. ( относительная биод-ть определяется для различных серий препаратов, для лекарственных средств при изменении технологии производства, для препаратов, выпущенных различными производителями, для различных ЛФ).
Концентрация A- Cвнутрь Время СИСТЕМНАЯ БИОДОСТУПНОСТЬ = 100(A- CВнутрь/A- CВ/В)% Биоэквивалентность-(относительная биодоступность) соотношение между количеством принятого и поступившего в кровоток лс. Терапевтическая эквивалентность- показатель эффективности дженерического препарата. Фармакологическая эквивалентность- показатель эффективности любого л.с. Время достижения максимальной концентрации ЛВ в крови.- отражает скорость его всасывания и скорость наступления терапевтического эффекта. Пример: Сmax стандартного препарата достигается через 1 ч, а тестируемого— через 4 ч. Такое различие во времени достижения максимальной концентрации препарата в крови может обусловить изменение клинических показаний к применению данного препарата. Биодоступность, фармакологическая, терапевтическая эквивалентность, биоэквивалентность. Исследование фармакокинетики у здоровых добровольцев. БИОДОСТУПНОСТЬотражает ту часть дозы, которая достигла системного кровотока, измеряется в процентах и зависит от: • состояния пациента (шок) • наличия портальной гипертензии • дозы препарата • характеристик лекарственного вещества • формы лекарственного вещества (раствор, суспензия, таблетка, таблетка в оболочке и т.д.) • взаимодействия с пищей Определение биодоступности осуществляется с помощью сопоставления A- C, определяемой при введении одной и той же дозы внутривенно и другим путем. При этом биодоступность при внутривенном введении принимается за 100%. Абсолют. Биодоступ-ть - это доля поглощенного препарата при внесосудистом введении по отношению к его количеству после в/в введения. Относительная биод-ть определяет относительную степень всасывания ЛС из испытуемого препарата и из препаратов сравнения. ( относительная биод-ть определяется для различных серий препаратов, для лекарственных средств при изменении технологии производства, для препаратов, выпущенных различными производителями, для различных ЛФ).
Концентрация A- Cвнутрь Время СИСТЕМНАЯ БИОДОСТУПНОСТЬ = 100(A- CВнутрь/A- CВ/В)% Биоэквивалентность-(относительная биодоступность) соотношение между количеством принятого и поступившего в кровоток лс. Терапевтическая эквивалентность- показатель эффективности дженерического препарата. Фармакологическая эквивалентность- показатель эффективности любого л.с. Время достижения максимальной концентрации ЛВ в крови.- отражает скорость его всасывания и скорость наступления терапевтического эффекта. Пример: Сmax стандартного препарата достигается через 1 ч, а тестируемого— через 4 ч. Такое различие во времени достижения максимальной концентрации препарата в крови может обусловить изменение клинических показаний к применению данного препарата. Исследование фармакокинетики у здоровых людей I фазу клинических исследований, как правило, проводят на 28-30 здоровых добровольцах. Цель этого этапа - получение сведений о переносимости, фармакокинетике и фармакодинамике нового ЛС, уточнение режима дозирования и получение данных по безопасности препарата. Изучение терапевтического действия препарата в этой фазе необязательно, так как у здоровых добровольцев ряд клинически важных свойств нового ЛС обычно не наблюдают. Исследования I фазы начинают с изучения безопасности и фарма-кокинетики однократной дозы, при выборе которой используют данные, полученные на биологических моделях. В дальнейшем изучают фармакокинетику препарата при многократном назначении, экскрецию и метаболизм нового ЛС (порядок кинетических процессов), его распределение в жидкостях, тканях организма, фармакодинамику. Обычно все эти исследования проводят для различных доз, лекарственных форм и путей введения. В ходе I фазы исследований можно также оценивать влияние на фармакокинетику и фармакодинамику нового препарата других ЛС, функционального состояния организма, приема пищи и т.д. Важной целью I фазы клинических испытаний считают выявление потенциальной токсичности и НЛР, но эти исследования непродолжительны и их проводят у ограниченного числа участников, следовательно, в ходе этой фазы удается выявить только наиболее частые и выраженные нежелательные явления, связанные с применением нового ЛС. В ряде случаев (онкологические препараты, препараты для терапии ВИЧ-инфекции) исследования I фазы можно проводить у больных. Это позволяет ускорить создание нового препарата и не подвергать добровольцев необоснованному риску, хотя такой подход можно рассматривать скорее как исключение. Исследования I фазы позволяют: - оценить переносимость и безопасность нового препарата; - в ряде случаев получить представление о его фармакокинетике (у здоровых людей, что естественно имеет ограниченное значение); - определить основные фармакокинетические константы (Cmax,C1); - сравнить фармакокинетику нового препарата при использовании различных лекарственных форм, путей и способов назначения. Всего фаз клинических испытаний 4: В фазе 2 лекарство впервые изучают у больных с профильным заболевание с целью определения его эффективности. Очень детально обследуется небольшое количество пациентов (10-200). В 3 фазе лекарство оценивают на значительно большей группе больных с целью дальнейшего определения его эффективности и безопасности. Если результаты 3 фазы положительны, то дается разрешение на клиническое использование. В 4 фазе проводится мониторинг безопасности лекарства в реальных условиях у большого числа больных. Медицина основанная на доказательствах. Уровни доказательности. Формулярная система: ее цель и компоненты. Медицина, основанная на доказательствах Evidence-basedmedicine –это добросовестное, точное и осмысленное использование лучших результатов клинических исследований для выбора лечения конкретного больного. Уровни доказательности(степень надежности) Уровень А доказательства получены на основе мета-анализа рандомизированных контролируемых исследований или на основе данных одного рандомизированного контролируемого исследования Уровень В доказательства получены на основе данных контролируемого нерандомизированного исследования или на основе данных исследования с высоким уровнем дизайна Уровень С доказательства получены на основе описательных исследований: исследования «случай-контроль», сравнительные исследования, корреляционные исследования, одномоментные исследования Уровень D доказательства получены на основе исследований отдельных случаев, серий случаев, консенсусов специалистов, заключений экспертных комиссий ФОРМУЛЯРНАЯ СИСТЕМА – это комплекс структур и управленческих мероприятий в здравоохранении, обеспечивающий применение рациональных, то есть организационно и экономически эффективных методов снабжения и использования лекарственных средств с целью обеспечения максимально высокого с учетом конкретных условий, качества медицинской помощи и оптимального использования имеющихся ресурсов. Цель: Достижение максимального терапевтического эффекта наиболее безопасным и экономичным путем. Рациональный отбор, использование лекарственных средств, экономически выгодные конкурентные закупки препаратов и их клиническая оценка. КОМПОНЕНТЫ СИСТЕМЫ: I. Стандарты (протоколы) лечения заболеваний и синдро-мов. II. Формулярные списки лекарственных средств на основе достоверной информации. III. Справочные пособия по формулярной системе. IV. Формулярно-терапевтические комитеты (ЛПУ, района, города, области). Фазы клинических исследований новых лекарственных препаратов. Принципы GCP при проведении клинических исследований. Для испытаний требуется: Информация о составе и источниках лекарства Информация о производителе Все данные изучения на животных Клинические планы и разработки протоколов Имена и сертификаты врачей Фазы клинических испытаний: В фазе 1 оценивают эффекты лекарства в зависимости от дозы на небольшом числе здоровых добровольцев. Задачей этой фазы является определить различия в реакции на лекарство животных и человека и установить границы безопасного диапазона доз. В фазе 2 лекарство впервые изучают у больных с профильным заболеванием с целью определения его эффективности. Очень детально обследуется небольшое количество пациентов (10-200). Часто используется слепой метод, включая в испытания наряду с тестируемым препаратом плацебо или официальное лекарство (позитивный контроль). В 3 фазе лекарство оценивают на значительно большей группе больных с целью дальнейшего определения его эффективности и безопасности. Если результаты 3 фазы положительны, то дается разрешение на клиническое использование. В 4 фазе проводится мониторинг безопасности лекарства в реальных условиях у большого числа больных. GCP – международный этический и научный стандарт качества планирования и проведения клинических исследований с участием человека в качестве субъекта, а также документального оформления и представления результатов таких исследований. 13 принципов: Проведение КИ в соответствии с этическими принципами GCP (согласно Хельсинской декларации) и нормативными требованиями Оценить соотношение ожидаемой пользы/риска до начала КИ Первостепенное значение в КИ имеют: права, безопасность и благополучие субъекта Достаточная доклиническая и клиническая информация об исследуемом продукте КИ должны отвечать научным требованиям и быть четко и подробно описаны в протокоде Утверждение/одобрение протокола Этическим комитетом Ответственность квалифицированного врача за оказываемую субъектам медицинскую помощь и принятие решений медицинского характера Квалификация всех лиц, вовлеченных в проведение КИ Добровольное информированное согласие каждого субъкта до его включения в КИ Полнота информации – записываемой, передаваемой и хранящейся Обеспечение конфиденциальности записей, идентифицирующих субъектов исследования Соответствие правилам Надлежащей Производственной практики в производстве, обращении и хранении исследуемых продуктов Внедрение процедурных систем, обеспечивающих качество проведения КИ Побочная реакция, нежелательное явление, нежелательная побочная реакция, непредвиденная нежелательная побочная реакция. НЕЖЕЛАТЕЛЬНЫЕ ЛЕКАРСТВЕННЫЕ РЕАКЦИИ (ПОБОЧНОЕ ДЕЙСТВИЕ ЛЕКАРСТВ) • Считается, что побочные реакции развиваются у 4-29% лиц, принимающих лекарства, • служат причиной 2-3% обращений к врачу, • и до 5% госпитализаций, • а в 3% случаев требуют проведения интенсивной терапии. • До 12% случаев побочного действия у госпитальных больных служат причиной увеличения срока госпитализации, • до 0,27% – причиной смерти (до 1,5% при внутривенном введении, преимущественно, у тяжелых больных). К развитию побочных эффектов предрасполагают: • возраст старше 60 лет или до одного месяца, • пол – чаще страдают женщины, • наличие побочных реакций в анамнезе, • заболевания печени, заболевания почек. Нежелательное явление (НЯ) - любые неблагоприятные с медицинской точки зрения проявления в клиническом состоянии пациента или субъекта клинического исследования, которые возникают во время лечения препаратом, но которые не обязательно имеют причинно-следственную связь с этим лечением. Нежелательная реакция/побочная реакция (НР) - все негативные реакции, связанные с применением ЛС в обычных дозах, использующихся для профилактики, диагностики или лечения заболеваний, а также для изменения физиологических функций. Серьезная нежелательная реакция (СНР) - Любое неблагоприятное с медицинской точки зрения событие в состоянии пациента или субъекта клинического исследования, связанное с применением ЛС и которое вне зависимости от дозы ЛС привело к нежелательному исходу, а именно: привело к смерти; представляет угрозу для жизни (в том числе случаи неэффективности ЛС, повлекшие угрозу для жизни пациента); требует госпитализации или ее продления; привело к стойкой или значительной нетрудоспособности или инвалидности; представляет собой врожденную аномалию или родовой дефект; Любое другое важное с медицинской точки зрения событие, которое непосредственно не привело к смерти, угрозе жизни или госпитализации пациента или субъекта клинического исследования, но может представлять существенный риск или потребовать вмешательства для предотвращения одного из нежелательных исходов, также должно рассматриваться как серьезное. Непредвиденная нежелательная реакция (ННР) - Нежелательная реакция, сущность которой не согласуются с имеющейся информацией о ЛС (например, с брошюрой исследователя для незарегистрированного исследуемого ЛС или с листком-вкладышем/сводной характеристикой ЛС, в случае применения зарегистрированного препарата). Серьезная непредвиденная нежелательная реакция (СННР) - реакция, одновременно отвечающая требованиям, предъявляемым к СНР и ННР. Классификация побочных эффектов по частоте, серьезные нежелательные побочные реакции. Типы побочных реакций. Нежелательные реакции ЛС (побочное действие) -это любая реакция на прием ЛС, не отвечающая цели его применения При выявлении опасных для жизни побочных эффектов, не указанных в аннотации на препарат, повлёкших временную потерю трудоспособности или госпитализацию пациента, а также любых побочных эффектов, связанных с приёмом нового ЛС (при его клинических испытаниях), провизор обязан оказать неотложную доврачебную помощь, заполнить «Карту-извещение регистрации побочных реакций» установленной формы и известить руководство аптечного учреждения и лечащего врача; в иных случаях достаточно рекомендовать обратиться к врачу. Побочные действия лекарств: Сопутствующие фармакологические эффекты: Функционально-метаболические или фармакодинамические Токсические (обратимые и необратимые) Мутагенные Онкогенные Тератогенные Эмбриотоксические Аллергические реакции: независимы от дозы; непредсказуемы. Лекарственная зависимость: Синдром отмены: обострение основного заболевания, развитие недостаточности «замещаемых систем»; собственно синдром отмены (тахифилаксия) Пристрастие: физическое, психическое, психологическое Побочные действия подразделяют на ряд категорий: · Определенные побочные эффекты – возникающие на фоне применения препарата, купирующиеся после его отмены и вновь возникающие при возобновлении приема. · Возможные побочные эффекты – возникающие на фоне применения препарата, купирующиеся после его отмены, но в связи с невозможностью повторного назначения не подтвержденные · Сомнительные побочные эффекты – возникающие на фоне применения препарата, но купирующиеся, несмотря на продолжение терапии. По течению различают: • а) острые, • б) хронические побочные эффекты. По тяжести клинических проявлений выделяют: • - фатальные или смертельные (агранулоцитоз при приеме хлорамфеникола [левомицетина], метамизола [анальгина, баралгина], сульфаниламидов); • - тяжелые, при которых очень высока опасность для жизни (анафилактический шок, желудочковая пароксизмальная тахикардия при лечении антиаритмическими средствами); • - средне-тяжелые, не несущие непосредственной угрозы жизни, но требующие не только отмены препарата, но и проведения специальной терапии; • - легкие, купирующиеся при отмене препарата или даже только при снижении дозы (если они не имеют аллергической основы). Соласно ВОЗ частота развития побочных эффектов классифицировано на:
Нежелательные побочные явления: токсические второстепенные, вторичные побочные реакции, токсичность, связанная с лекарственными взаимодействиями Токсические эффекты при применении ЛС развиваются при использовании ЛС в дозах, превышающих терапевтические (основная причина – передозировка). Токсические эффекты также возможны при использовании ЛС в обычных дозах у тех пациентов, которым следует назначать ЛС в меньших дозах, в т.ч. при почечной и/или печеночной недостаточности, когда возможна кумуляция ЛС в токсических концентрациях в организме. Наиболее часты токсические эффекты у препаратов с узким терапевтическим индексом, т.е. интервалом между минимальной концентрацией ЛВ в крови, вызывающей терапевтический эффект и концентрацией, вызывающей токсический эффект. К ним относятся: А/бактериальные препараты: Аминогликозиды, Хлорамфеникол, Ванкомицин . Психотропные препараты: Фенобарбитал, Карбамазепин ,Вальпроевая кислота. Препараты лития Антиаритмические препараты: Прокаинамид, Дизопирамид, Лидокаин Сердечные гликозиды: Дигоксин Бронхолитики: Теофиллин Цитостатики: Метотрексат, Циклоспорин 2.Второстепенные НПР – неизбежные НРП биологически активных веществ, входящих в состав препарата, составляющие спектр их фармакологического действия. (в-адреноблокаторы, стимуляторы, седативный эффект антигистаминных). 3.Вторичные НПР – напрямую не связанные с ЛС, а обусловлены последствиями его действия, т.е. являются косвенно возникающим неблагоприятным влиянием (дисбактериоз при использовании антибиотиков, инфекционные заболевания при применении глюкокортикоидов). 4.Токсичность, связанная с лекарственными взаимодействиями (ПД теофиллина при взаимодействии с эритромицином). Связаны с изменением всасывания, метаболизма, элиминации и фармакодинамики ЛВ. Нежелательные побочные реакции: непереносимость ЛС, идиосинкразия, аллергические реакции: клинические проявления, медикаментозное купирование анафилактического шока. Непереносимость – НПР ЛС, связанные с фармакологическими свойствами биологически активных веществ, входящих в состав препарата, и возникающих в субтерапевтических и терапевтических дозах. Может наблюдаться индивидуальная непереносимость любого препарата. Идиосинкразия – нехарактерные реакции ЛВ, которые не могут быть объяснены фармакологической активностью. Это генетически обусловленная патологическая реакция на определенный лекарственный препарат. В основе идиосинкразии лежат реакции, обусловленные наследственными дефектами ферментных систем. Встречаются реже, чем аллергические реакции.Частным случаем идиосинкразии является фотосенсибилизация – повышенная чувствительность кожи к УФО-лучам, возникающая при применении доксициклина, ломефлоксацина, спарфлоксацина, препаратов зверобоя. Реакции гиперчувствительности или аллергические реакции – реакции связанные с вовлечением иммунологических механизмов и протекающие с повреждением тканей организма. •Причиной аллергических реакций являются аллергены – антигены, вызывающие развитие аллергических реакций. Аллергены могут быть полноценными и неполноценными. Полноценные аллергены изначально обладают антигенными свойствами. Неполноценные аллергены или гаптены сами не обладают антигенными свойствами, но приобретают их после связывания с белками организма. При этом большинство ЛВ является гаптенами, а свойствами полноценных аллергенов обладают вакцины и сыворотки. наиболее часто вызывают развитие аллергических реакций. Возникают: 1. анафилактический шок. Симптомы развиваются практически моментально после введения ЛВ. Механизм развития связан с высвобождением большого количества гистамина, который вызывает снижение периферического сопротивления сосудов, приводящее к прогрессирующему снижению артериального давления. Признаки: Кожа-зуд ,гиперемия, крапивница, ангионевротический отек.Глаза-зуд ,избыточное отделение. Дыхательная система-ринит кашель, дисфония, отек гортани, бронхоспазм, густой слизистый секрет Сер.-сос. Система-сначала – тахикардия, затем – брадикардия,прогрессирующее снижение АД,аритмия,коллапс или шок,остановка сердцаЖКТ-ТошнотаДиареяРвотаВздутие животаСпазм купирование анафилактического шока ( методичка Ефремовой): Моментальное прекращение контакта с аллергеном: Наложение жгута выше места инъекции на 25 мин. (каждые 10 мин. Ослаблять жгут на 1-2 мин); К месту инъекции приложить лед или грелку с холодной водой на 15 мин; Обкалывание в 5-6 точках и инфильтрация места укуса или инъекции адреналином 0,1% - 0,5 мл с 5 мл физ. Раствора; Обеспечение проходимости дыхательных путей и адекватной вентиляции: При адекватном самостоятельном дыхании – оксигенотерапия; При отсутствии адекватного дыхания – интубация трахеи, ИВЛ; Придать положение с приподнятым ножным концом Обеспечение сосудистого доступа Проивошоковая терапия: в/в струйно андреналин в дозе 10 мкг/кг (0,01 мл/кг 0,1% раствора) При отсутствии выраженного эффекта возможно повторное введение адреналина через 5 мин Максимальное количество повторных введений не должно быть более 3! Обеспечение надежного венозного доступа (периферический катетер) Инфузия кристаллоидных и коллоидных растворов Противоаллергическая терапия: мембраностабилизатор – в/в не менее 5 мг/кг преднизолона болюсно При бронхоспазме – аминофиллин (эуфиллин) в/в струйно Другой вариант купирования анафилактического шока: •В/сердечное введение адреналина• В/венная инъекция глюкокорткоидов •Введение гистаминоблокаторов• Инъекция короткоживущих сердечных гликозидов• При развитии отека легких – введение аминофиллина, при необходимости – искусственная вентиляция легких Нежелательные побочные реакции: лекарственная зависимость, синдром отмены, тиолерантность, мутагенные, тератогенные, канцерогенные эффекты Под лекарственной зависимостью понимают психическое и (иногда) физическое состояние, характеризующееся поведенческими и другими реакциями, которые всегда включают настоятельную потребность в постоянном или периодическом приёме определённых ЛС для того, чтобы испытать его действие на психику или избежать неприятных симптомов, возникающих без приёма этого ЛС. Лекарственная зависимость может развиться к одному или нескольким ЛС. Характерно одновременное развитие толерантности. • Синдром психической зависимости — состояние организма, характеризующееся патогической потребностью в приёме какого-либо психотропного вещества с тем, чтобы избежать нарушений психики или дискомфорта, возникающих при прекращении применения. Этот синдром протекает без явлений абстиненции. • Синдром физической зависимости — состояние, характеризующееся развитием абстиненции при прекращении приёма ЛС или после введения его антагонистов. Характерен, в первую очередь, для ЛС, обладающих наркотическим эффектом. • Синдром отмены – сложный комплекс явлений, возникающих после резкого прекращения приема ЛС. Характерен для глюкокортикоидов, клонидина, в-адреноблокаторов, барбитуратов, бензодиазепины, непрямые антикоагулянты, Н2-гистаминоблокаторы. • Толерантность (привыкание) – ослабление действия ЛС при его повторном применении. Очень быстро развивающуюся толерантность называют тахифилаксией.Мутагенные эффекты. Тератогенные эффекты. Канцерогенные эффекты наиболее часто вызывают анаболические стероиды, контрацептивы, метотрексат, изотопы йода.ЛСмогут обладать ТЕРАТОГЕННОСТЬЮ, то есть таким повреждающим влиянием на дифференцировку тканей и клеток, которое приводит к рождению детей с разными аномалиями. КАНЦЕРОГЕННОСТЬ - это способность веществ вызывать развитие злокачественных опухолей. Эстрагены способствуют развитию рака молочной железы у женщин в детородном возрасте. Причины нежелательных лекарственных реакций. Факторы, учитываемые при проведении фармакотерапии для уменьшения риска развития нежелательного действия ЛС При проведении ФТ, к сожалению, нередко возникают нежелательные эффекты ЛС, но часть из них можно предупредить с по- мощью профилактики и коррекции. Нежелательные эффекты - любые реакции на ЛС, возникающие при использовании препаратов для лечения, диагностики или профилактики заболеваний и причиняющие вред организму. • Практически любое ЛС может вызвать нежелательные эффекты. • Нежелательные реакции могут быть специфическими или повторять клинические симптомы заболевания. • В 100% случаев пациенты должны быть осведомлены о возможных нежелательных реакциях на ЛС (особенно при длительной ФТ). В применении у детей о них должны знать родители. • Все побочные реакции на ЛС должны быть зарегистрированы медицинским персоналом и подвергнуты тщательному анализу. • Вероятность возникновения нежелательных эффектов особенно велика в группах риска: у детей раннего возраста и пожилых пациентов, больных с патологией органов биотрансформации, экскреции (печень, почки) и отягощённым анамнезом. • На вероятность возникновения нежелательных эффектов ЛС могут оказать влияние такие факторы, как физико-химическое состояние ЛС (липофильность), полипрагмазия, путь введения лекарственного препарата, профессия пациента (фармацевты, медицинские сёстры) и особенности организма (индивидуальная чувствительность, генетическая детерминированность, возраст, пол, наличие вредных привычек, фоновых заболеваний). По тяжести клинического течения нежелательные реакции можно разделить на: • фатальные, т.е. способные привести к смертельному исходу (например, анафилактический шок); • тяжёлые, требующие немедленной отмены ЛС и проведения коррекционных мероприятий; • средней тяжести, не требующие коррекционных мероприятий (необходима лишь отмена ЛС, например, при крапивнице); • лёгкие, не требующие отмены препарата (например, седативный эффект клонидина). В большинстве случаев нежелательные эффекты зависят от концентрации ЛС в крови. При этом их содержание может соответствовать терапевтическому или токсическому уровню. Некоторым нежелательным эффектам не свойственна такая зависимость. Задача медицинского персонала - предупредить возможность возникновения нежелательных эффектов: • своевременно распознать (важно отличать их от симптомов заболевания); • не допустить развития тяжёлых реакций и возникновения нового ятрогенного заболевания; • исключить одновременное назначение токсических веществ подобного действия; • при необходимости - отказаться от применения конкретного препарата. Классификация нежелательных эффектов ЛС • Нежелательные эффекты, возникающие при терапевтической концентрации препарата в плазме крови. • Нежелательные эффекты, возникающие при токсической концентрации препарата в плазме крови. • Нежелательные эффекты, возникновение которых не связано с концентрацией препарата в плазме крови. |