Рецензенты кандидат химических наук В. Г. Коробко доктор биологических наук В. А. Гвоздев Патрушев Л. И
 Скачать 5.83 Mb. Скачать 5.83 Mb.
|
Глава 11.ДНК-ДИАГНОСТИКА И ДНК-ТИПИРОВАНИЕ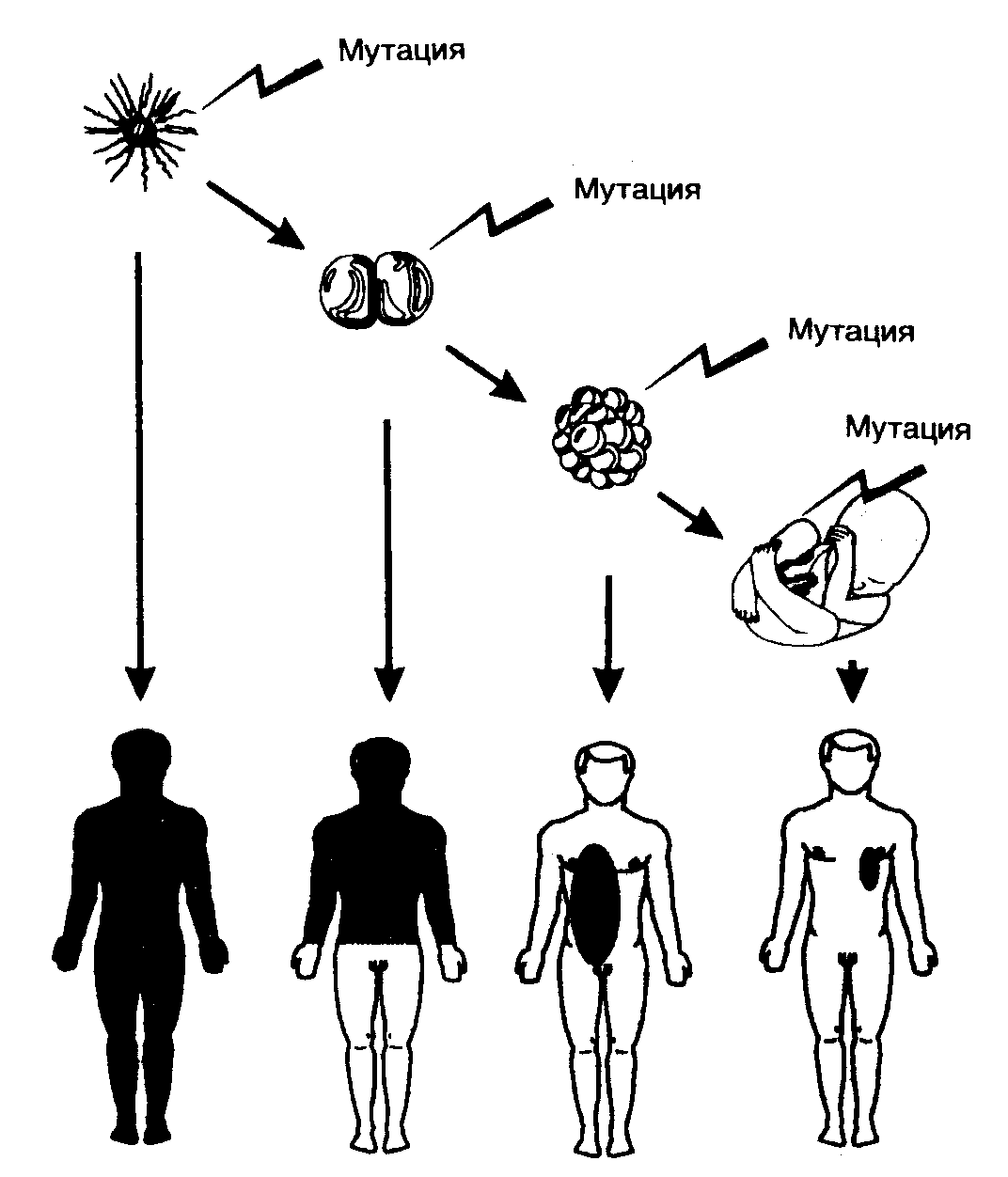 Рис. II.30. Генетические последствия мутаций, происходящих в геноме соматических клеток человека на разных стадиях эмбриогенеза Черным цветом закрашены места локализации клонов мутантных клеток разных размеров в организме человека Исследования показывают, что большинство заболеваний человека, а возможно, и все его болезни связаны с мутациями, приводящими к изменению уровней экспрессии конкретных генов. Мутации в определенных генах нарушают функционирование биохимических систем, что в конце концов приводит к развитию соответствующих патологических состояний организма (рис. II.30). В том случае, если мутации происходят в геноме клеток зародышевой линии человека, все соматические клетки организма-потомка, который развивается из мутантной зиготы, образовавшейся от слияния мутантных гамет в процессе оплодотворения, будут содержать указанную мутацию. Чем позже в онтогенезе человека возникает соматическая мутация, тем меньше размер клона мутантных клеток во взрослом организме. Если же мутация доминантна, т.е. патологический мутантный признак, определяемый мутантным геном, проявляется даже при наличии в соматических клетках копии нормального гена, полученного от другого родителя, то возникает наследственное заболевание. В случаях, когда мутация, определяющая мутантный фенотип, рецессивна (ее действие проявляется лишь в гомозиготном состоянии, при котором один и тот же мутантный ген получен от каждого из родителей), можно говорить о предрасположенности организма-гетерозиготы к соответствующему заболеванию и носительстве мутантного гена. Действительно, организм, у которого действие рецессивной мутации маскируется функционированием другого, полноценного аллеля, внешне (фенотипически) выглядит нормальным. Однако у такого организма гораздо больше шансов дать больное потомство в браке с носителем такого же мутантного гена, что является одной из причин запрета на близкородственные браки. С другой стороны, у носителей мутантных генов в гетерозиготном состоянии может произойти соматическая мутация в соответствующем аллельном гене соматических клеток, что также станет причиной развития приобретенного генетического заболевания. В качестве одного из примеров такого заболевания мы уже рассматривали ранее ретинобластому – онкологическое заболевание, поражающее сетчатку глаз, чаще всего, в детском возрасте. Это заболевание развивается в два этапа: вначале организм ребенка получает от одного из родителей мутантный ген RB1, являющийся рецессивным онкогеном (антионкогеном), а затем в онтогенезе в одной из соматических клеток в результате мутации происходит инактивация второй его копии, что вызывает малигнизацию клетки и развитие опухоли. Такой же механизм лежит в основе возникновения некоторых форм диабета, а также ряда онкологических и аутоиммунных заболеваний. Традиционная диагностика наследственных и инфекционных заболеваний строится на детальном изучении симптомов и проведении многочисленных биохимических анализов, включая культивирование патогенных микроорганизмов на сложных питательных средах. При этом выявление бессимптомного носительства вредных аллелей и микроорганизмов-возбудителей превращается в чрезвычайно трудоемкую задачу. В частности, традиционными цитогенетическими методами можно выявить в геноме человека лишь некоторые крупные хромосомные перестройки: протяженные делеции и транслокации генетического материала, потерю или приобретение целых хромосом. При этом мелкие делеции, транслокации и вставки, а также точковые мутации, которые являются наиболее часто встречающимися изменениями генетического материала, остаются не обнаруженными. То же имеет место и при диагностике бессимптомного носительства возбудителей инфекционных заболеваний бактериальной и вирусной природы, например вируса иммунодефицита человека, которые в латентной стадии инфекции могут присутствовать в организме человека лишь в небольшом числе копий. Разработанные недавно новые методы молекулярной биологии, и особенно метод ПЦР, значительно облегчили проведение диагностики наследственных и инфекционных заболеваний. При этом мутации выявляются в ДНК клинических образцов, а бессимптомное присутствие возбудителей обнаруживают по наличию геномных ДНК или РНК соответствующих вирусов или бактерий. В основе всех методов ДНК-диагностики лежат три фундаментальных принципа молекулярной биологии (рис. II.31). Это прежде всего существование комплементарных взаимодействий между двухцепочечными молекулами нуклеиновых кислот (первый принцип), которые после денатурации с последующей ренатурацией (второй принцип) позволяют им безошибочно находить друг друга и восстанавливать первоначальную вторичную структуру. Если же в процессе ренатурации нуклеиновых кислот добавить в пробы короткие олигонуклеотиды (зонды или праймеры), ковалентно соединенные с каким-либо меченым соединением, то они благодаря комплементарным взаимодействиям соединяются с тем участком нуклеиновой кислоты, который содержит последовательность нуклеотидов, строго соответствующую последовательности нуклеотидов зонда или праймера (третий принцип). Следовательно, наличие связавшейся с нуклеиновой кислотой метки с высокой точностью свидетельствует о присутствии в анализируемом образце искомых последовательностей нуклеотидов. 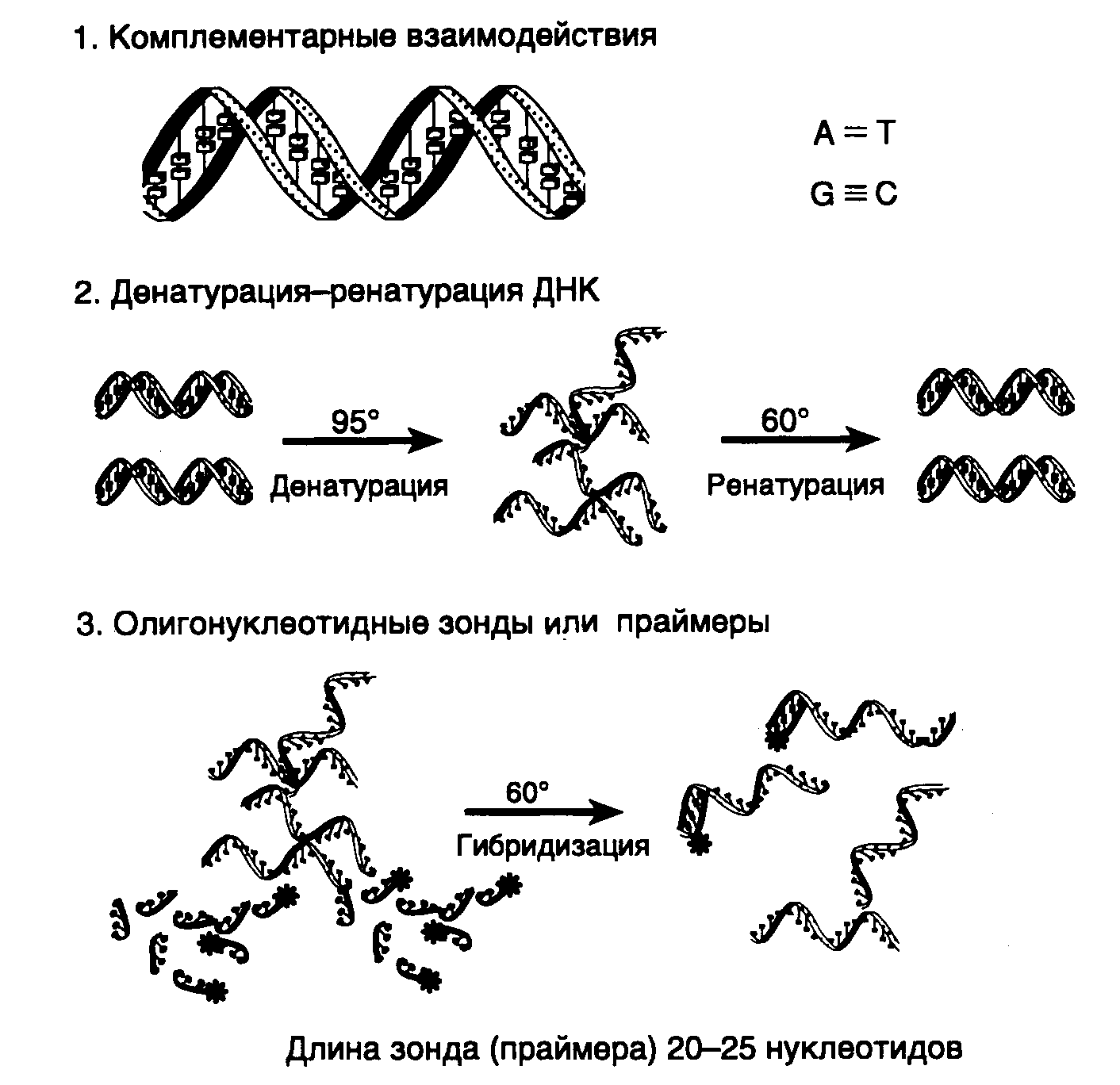 Рис. II.31. Три молекулярно-генетических принципа, лежащих в основе ДНК-диагностики Звездочками отмечено наличие радиоактивной, флуоресцентной или другой метки в олигонуклеотидных зондах или праймерах на одном из их концов Современные методы ДНК-диагностики находят широкое применение в медицине для обнаружения мутаций при наследственных (или приобретенных) заболеваниях и ДНК-типирования организмов (рис. II.32). ДНК-диагностика наследственных и приобретенных заболеваний может заключаться как в обнаружении известных, уже описанных мутаций, так и в поиске новых мутаций, приводящих к тому же патологическому состоянию организма. ДНК-типированием называют поиск генотипических особенностей у микро- или макроорганизма, которые позволяют его идентифицировать и(или) отнести к той или иной систематической группе. 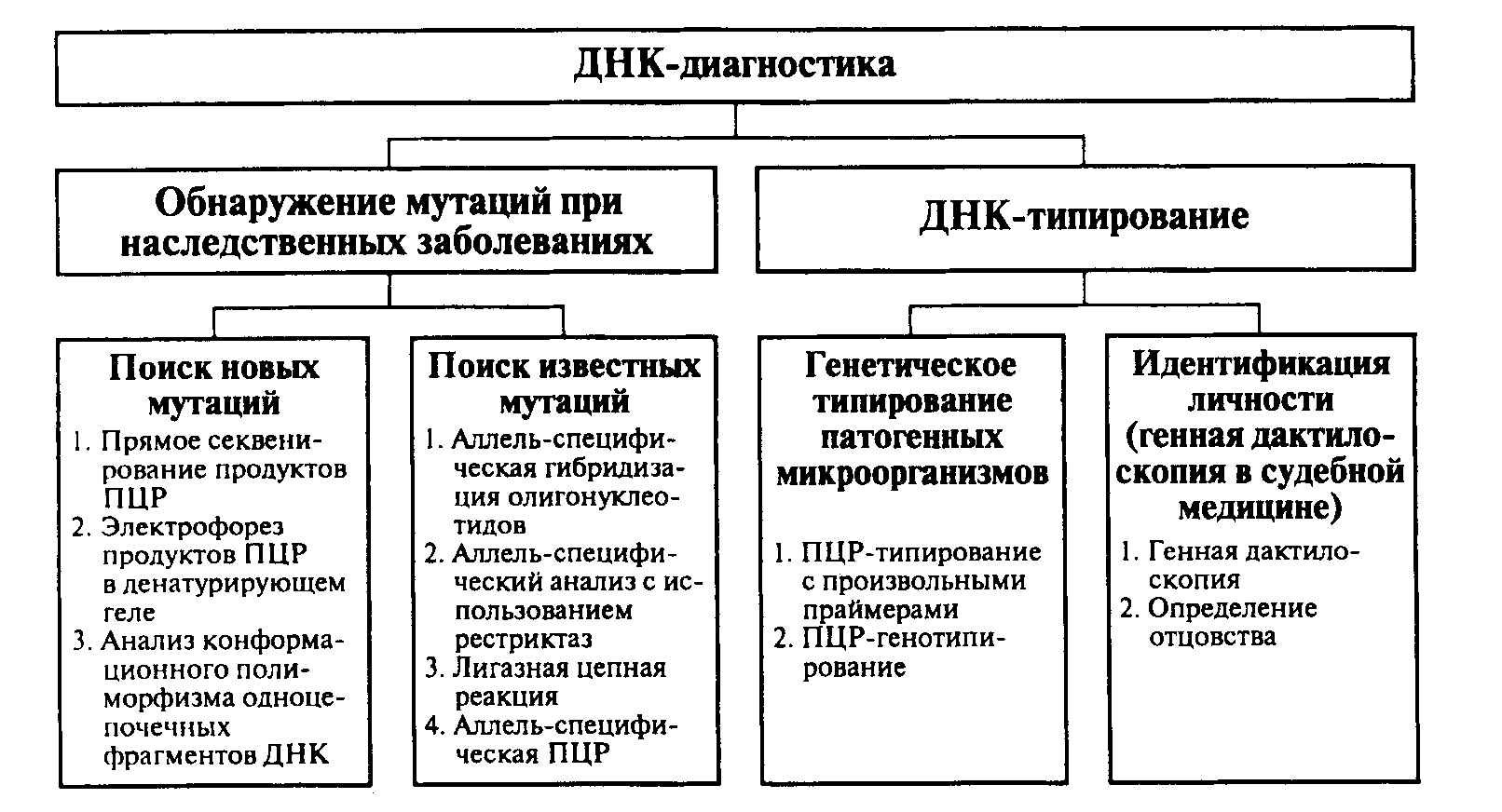 Рис. II.32. Применение методов ДНК-диагностики в медицине |
