способы синтеза антибиотиков. способы получения антибиотиков. Способы получения антибиотиков
 Скачать 0.8 Mb. Скачать 0.8 Mb.
|
Направленный биосинтез антибиотиков.Общие закономерности ферментационного процесса при биосинтезе антибиотиков.Биосинтез большинства вторичных метаболитов, в том числе антибиотиков, обычно осуществляется на определенной стадии развития микроорганизма, в условиях торможения основных процессов анаболизма—биосинтеза нуклеиновых кислот, белка, липидов, полисахаридов. Различают две принципиально различные стадии развития популяции продуцентов антибиотиков. Первая, носящая название трофофаза или фаза сбалансированного роста, характеризуется интенсивным синтезом соединений, требующихся для роста клеток, что сопровождается быстрым потреблением основных питательных компонентов среды. Эта фаза соответствует фазе логарифмического роста периодической культуры микроорганизмов. После исчерпания некоторых ингредиентов среды (в первую очередь, углерода, азота, молекулярного кислорода) и накопления продуктов метаболизма наступает вторая фаза (идиофаза, или фаза несбалансированного роста). Идиофаза отличается заметным торможением или прекращением роста микробной популяции, что соответствует переходу в стационарную фазу роста периодической культуры. Здесь начинают преобладать протеолитические процессы, происходит автолитический распад клеток. Именно в идиофазе многие микроорганизмы начинают синтезировать вторичные метаболиты, к числу которых относятся и антибиотики. В большинстве случаев максимум накопления антибиотика в культуральной жидкости наступает после максимума накопления биомассы. Это объясняется тем, что синтез ферментов, ответственных за образование антибиотиков, подавлен (репрессирован) во время трофофазы.[12] Описанные закономерности можно отобразить графически.(рис.1) 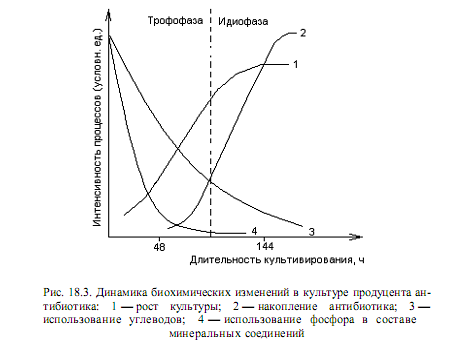 рис. 1. Схема, отражающая общие закономерности ферментационного процесса при биосинтезе антибиотиков: 1 – биомасса, 2 – антибиотик, 3 – углеводы, 4 – источники азота Для высокопродуктивной ферментации необходимо соблюдать определенные условия. Продуценты антибиотиков выращивают наразных средах как относительно простого состава, так и сложного. Последние получили название комплексных сред. В них могут входить соевая или хлопковая мука, кукурузный экстракт и другие природные многокомпонентные источники питательных веществ. Также в среды вносят индивидуальные органические соединения и минеральные соли. Для каждого штамма-продуцента состав оптимальной для биосинтеза антибиотика среды подбирается отдельно. Это относится даже к штаммам одного вида, продуцирующим один и тот же антибиотик. Существуют и некоторые общие закономерности, учитываемые при работе с большинством продуцентов. Быстрый катаболизм глюкозы резко снижает биосинтез антибиотиков. Показано, что глюкоза ослабляет биосинтез беталактамов, аминогликозидов и многих других антибиотиков, образуемых разными продуцентами. Неблагоприятное действие фосфора на биосинтез беталактамных антибиотиков объясняется на биохимическом уровне следующим механизмом: образование LLD-трипептида — ключевого соединения, с которого начинается синтез пенициллинов и цефалоспоринов, ингибируется глюкозо-6-фосфатом. Взаимодействие легкоокисляемого сахара и фосфата оказывает отрицательный эффект на биосинтез. Однако все вышеизложенное не означает, что фосфор может быть полностью исключен из среды. Биосинтез антибиотиков снижается при его избыточном количестве, поэтому для каждого штамма-продуцента подбирается оптимальное содержание фосфора в среде. Аммоний и другие легкоутилизируемые источники азота подобно легкоокисляемым углеводам усиливают рост продуцентов беталактамных, полиеновых антибиотиков (эритромицина, рифамицинов и других), но отрицательно влияют на их биосинтез. Соевая и хлопковая мука, БВК (белково-витаминный концентрат) медленно расщепляются в процессе ферментации, т. е. из них медленно высвобождаются аминокислоты и ионы аммония, поэтому их используют в качестве компонентов питательных сред, что позволяет получать высокий выход антибиотиков. Потребность в кислороде зависит от концентрации биомассы и ее метаболической активности. Оптимизация снабжения кислородом достигается увеличением скорости его переноса. После стадии ферментации культуральная жидкость содержит растворенный антибиотик, мицелий продуцента, продукты его лизиса, ряд компонентов неиспользованной питательной среды, в том числе высоко- и низкомолекулярные органические вещества и неорганические соли.[1] Таким образом, интенсивному биосинтезу антибиотиков способствует значительное уменьшение в среде источников углерода и азота, особенно легко усваиваемых. В этом случае происходит дерепрессия ферментов синтеза антибиотиков. Однако, выращивание продуцентов с самого начала ферментации на обедненных средах нецелесообразно, так как незначительное накопление биомассы в течение трофофазы ведет к незначительному накоплению антибиотика малым количеством клеток продуцента. Для каждого штамма – продуцента состав оптимальной среды для биосинтеза антибиотика подбирается отдельно. |
