способы синтеза антибиотиков. способы получения антибиотиков. Способы получения антибиотиков
 Скачать 0.8 Mb. Скачать 0.8 Mb.
|
Биохимические механизмы биосинтеза антибиотиков.Механизм биосинтеза беталактамных антибиотиков.Молекула пенициллина образуется из L-цистеина, L-валина и неполярных карбоновых кислот - предшественников бокового радикала молекулы пенициллина. Кроме указанных соединений обязательным компонентом биосинтеза пенициллина является L-а-аминоадипиновая кислота (L-a-AAK), которая образуется из кетоглутарата и ацетил- КоА при участии фермента гомоцитратсинтетазы по следующей схеме.(рис.3) 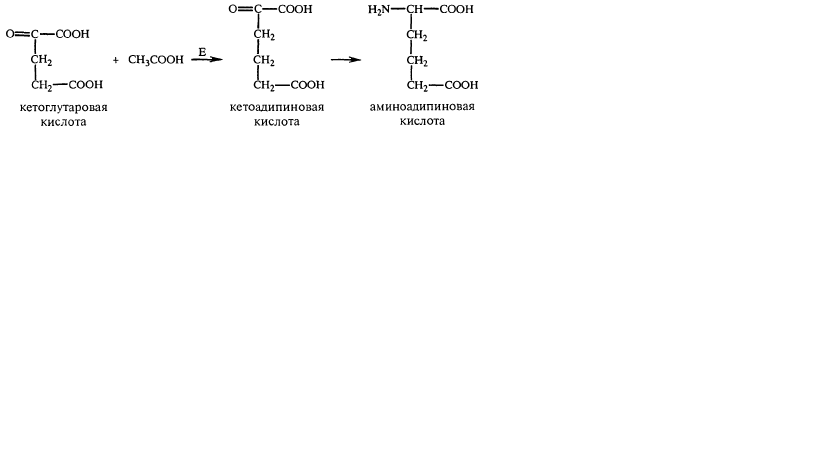 рис. 3. Образование аминоадипиновой кислоты Первым этапом биосинтеза молекулы -лактамного антибиотика следует считать образование трипептида: L-2-аминоадипил -L-цистеинил-D-валина (LLD). В начале процесса образуется дипептид (L-а-аминоадипил-L-цистеин), который затем, взаимодействуя с L-валином, образует трипептид. LLD-трипептид превращается в изопенициллин-N через моноциклический -лактам. (рис.4) 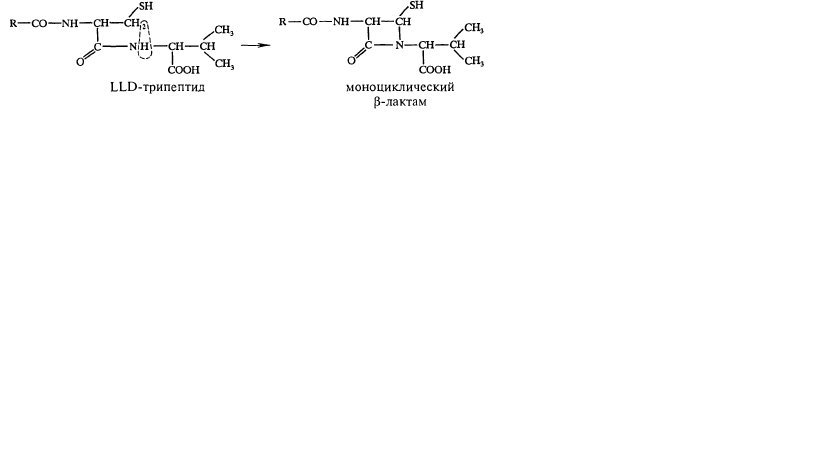 рис.4. Образование моноциклического -лактама Этот трипептид был обнаружен в мицелии продуцента пенициллина Р. chrysogenum. Его синтез осуществлен бесклеточным экстрактом Р. chrysogenum. Этот трипептид рассматривается в качестве основного промежуточного соединения в процессе биосинтеза -лактама молекулы антибиотика. -лактам образуется в результате замыкания кольца между С-3-цистеином и NН-группой валина. Этот процесс – первая стадия циклизации LLD-трипептида в первичный антибиотик - изопенициллин N. Первоначально возникновение основного ядра молекулы пенициллина - 6-аминопенициллановой кислоты (6-АПК) – было показано при культивировании гриба в среде, не содержащей предшественника, а затем 6-АПК выделили из культуральной жидкости продуцента пенициллина и определили ее строение. Позднее многие исследователи искали у Р. chrysogenum фермент, превращающий молекулу 6-АПК в пенициллин, т.е. осуществляющий ее ацилирование. В результате в 1968 г. появилось сообщение о том, что в мицелии гриба найден фермент пенициллинацилтрансфераза, способный переносить ацильную группу разных пенициллинов на 6-АПК. Образование фермента совпадает с периодом активного биосинтеза пенициллина, следовательно, фермент непосредственно участвует в этом процессе. Таким образом, можно утверждать, что изопенициллин-N и 6-АПК и есть непосредственные предшественники процесса образования пенициллина. Механизм биосинтеза аминогликозидных антибиотиков.Рассмотреть биосинтез аминогликозидных антибиотиков можно на примере стрептомицина. Стрептомицин состоит из двух частей: стрептотидина и стрептобиозамина. Биосинтез стрептомицина – сложнейший процесс, берущий начало от глюкозы. Процесс проходит через 13 ферментативных реакций, где задействованы: ферменты, коферменты, доноры и акцепторы функциональных групп, аминокислоты и т.д. При биосинтезе стрептидина глюкоза проходит через ряд превращений.(приложение 1) Этот сложнейший синтез касается только одной части стрептомицина. Для дальнейшего биосинтеза необходимы еще 2 фрагмента: N-глюкозамин и стрептоза.(рис.5, 6) 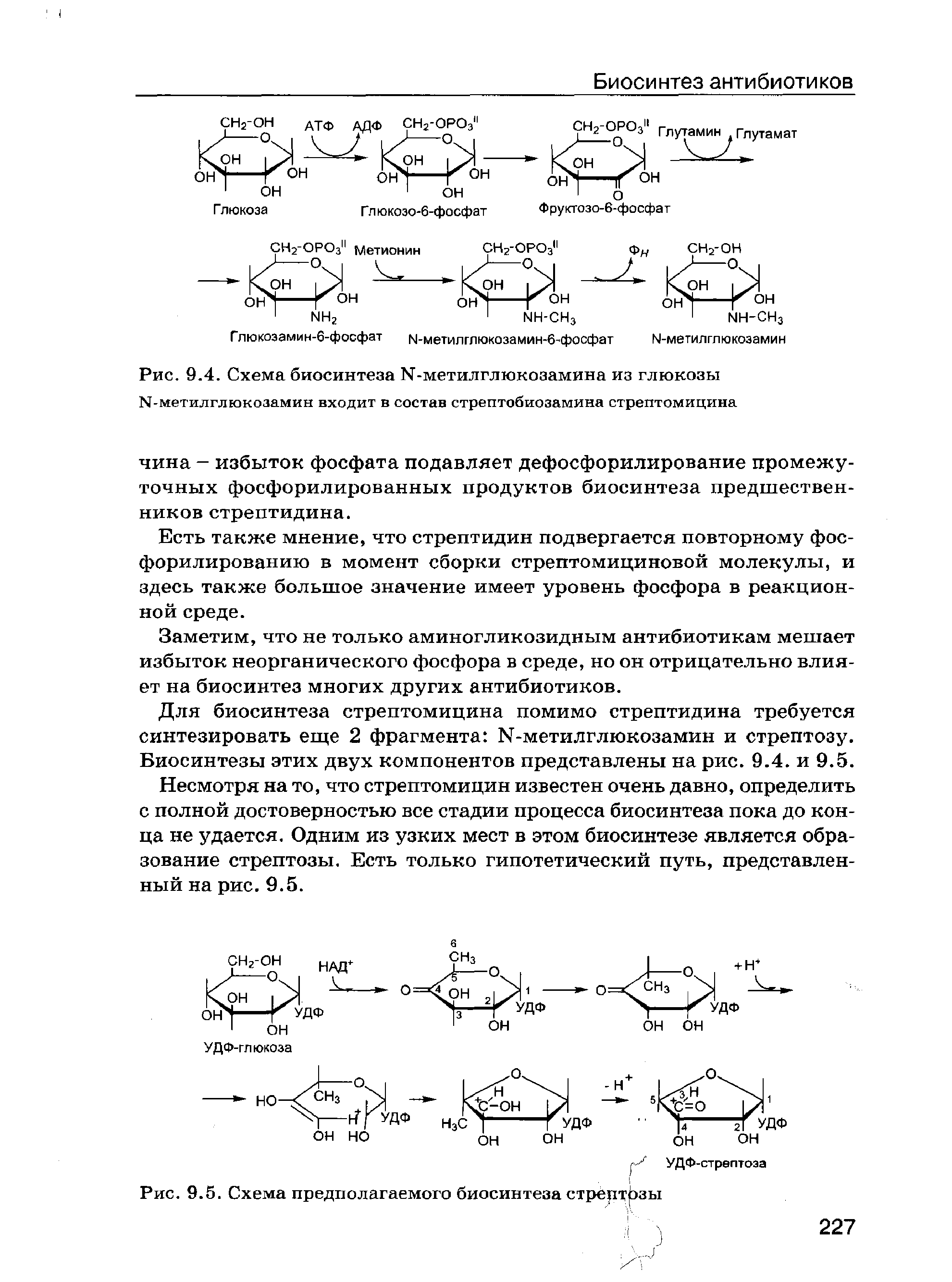 рис. 5. Схема синтеза N-метилглюкозамина 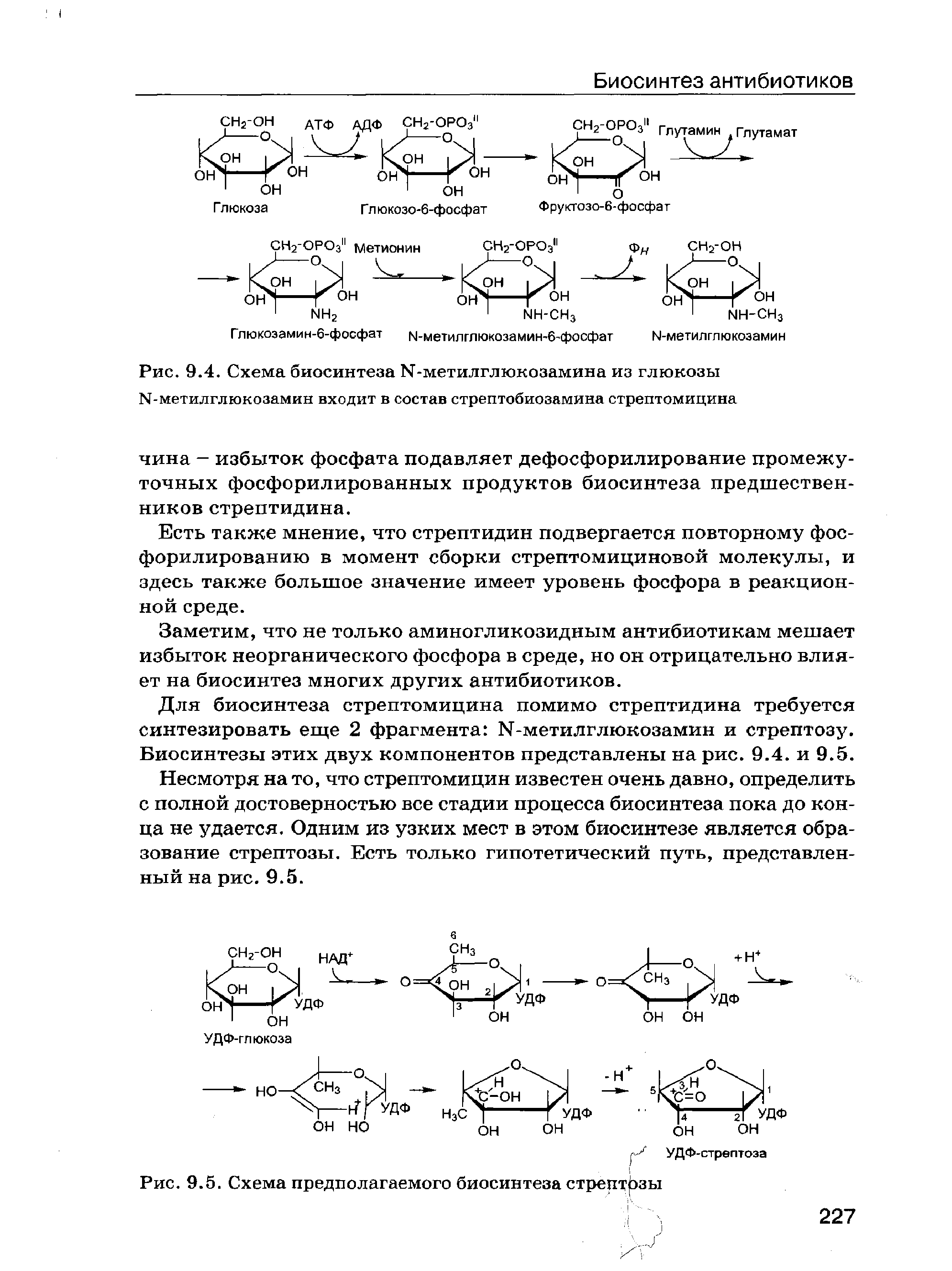 рис. 6. Схема синтеза стрептозы Сборка молекулы стрептомицина из трех полученных фрагментов – стрептидина, стрептозы и N-метилглюкозамина происходит за счет замыкания между ними гликозидных связей при участии не менее 20 ферментов.[8] Механизм биосинтеза тетрациклинов.Исходными структурными единицами являются восемь молекул малонил-КоА и одна молекула малониламин-КоА. Биосинтез происходит по принципу «голова к хвосту». Первым общим предшественником для всех тетрациклинов является метилпрететрамид, для его образования используется примерно 50 ферментных систем, а последующие 11 реакций приводят к образованию молекулы антибиотика. В этих реакциях участвует кофермент А. Исключительно важное значение имеет наличие НАДФН+, необходимыми являются три молекулы –продукт пентозофосфатного пути утилизации глюкозы. Следовательно, они образуются раньше, чем используются для биосинтеза антибиотика. Был постулирован тот факт, что чем ниже уровень реакций в ЦТК, тем более высоким является выход тетрациклина. Считают, что продуктивный штамм имеет дефект в энергетическом обмене, в результате чего усиливается утилизация уксусной кислоты для синтеза тетрациклина. [6] Схема биосинтеза молекулы тетрациклина представлена ниже.[9] (рис.7) 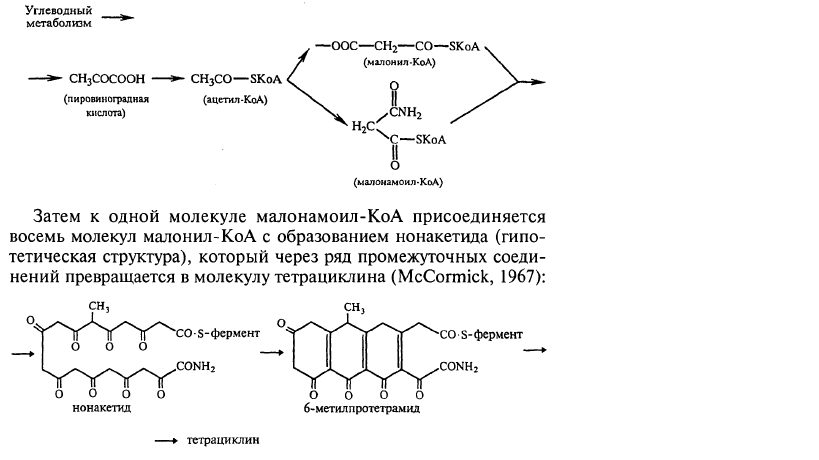  рис.7. Схема синтеза молекулы тетрациклина |
