способы синтеза антибиотиков. способы получения антибиотиков. Способы получения антибиотиков
 Скачать 0.8 Mb. Скачать 0.8 Mb.
|
Азтреонам, принцип получения и свойства.Химические модификации все чаще затрагивают структуру сконденсированного с беталактамом пяти- или шестичленного кольца. Если сера в пятичленном (пенициллины) или шестичленном (цефалоспорины) кольце замещена на кислород или углерод, то соединения называют «нетрадиционные» или «неклассические» беталактамы. К ним относится уже упоминавшийся, быстро проникающий через пориновые каналы имипенем. Также к «нетрадиционным» относят и такие беталактамы, в которых беталактамное кольцо не сконденсировано с другим кольцом (пяти- или шестичленным). Они получили название «монобактамы», а наибольшую известность приобрел ценный для медицинской практики препарат азтреонам:[1](рис.12) 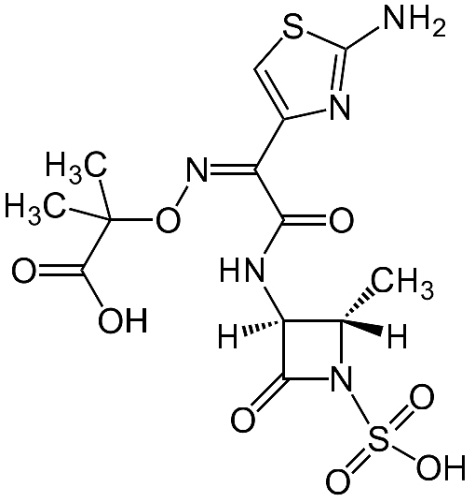 рис.12. Формула азтреонама Антимикробная активность этого препарата в основном проявляется в отношении аэробных грамотрицательных бактерий (по Williams, 1986). Азтреонам применяется в медицинской практике для лечения инфекций мочевыводящего тракта, желчного тракта, гонореи, остеомиелитов.[9] Таким образом, необходимость поисков новых антибиотиков обусловлена многими причинами. Так, ежегодно на нашей планете умирают от инфекционной патологии более 50 млн. человек. С инфекционными и паразитарными болезнями связаны 25 % смертности в мире, а с учетом роли инфекции в «неинфекционных» заболеваниях – почти 35 %. Кроме того, наблюдаются «возвращающиеся инфекции», т.е. инфекции, которые достались нам в наследство от предыдущих веков. Среди них туберкулез, малярия, лейшманиоз, инфекции, передающиеся половым путем (например, сифилис). В то же время, наблюдается появление новых инфекций. Наряду с этим выявлены и недостатки, связанные с высокой резистентностью микроорганизмов к антибиотикам и появлению штаммов не только антибиотикоустойчивых, но и антибиотикозависимых.[7] Мутасинтез, блокмутанты и мутасинтоны.Методы получения антибиотиков путем химического синтеза достаточно сложны и не могут конкурировать с их биосинтезом методом биотехнологии. Существует несколько способов получения как природных, так и полусинтетических антибиотиков: направленный биосинтез, метод генной инженерии и мутасинтез. Способ получения антибиотиков мутасинтезом состоит в использовании для их биосинтеза блокированных мутантов и, у которых отсутствует (блокировано) определенное звено в цепи реакций, и мутасинтонов (A, B, C) ведущих к синтезу антибиотика.[7] Мутасинтон – консервативный фрагмент молекулы антибиотика, модифицированный химически, вносимый в среду, где культивируется блок-мутант с целью образования мутасинтетического антибиотика.[1] Блокированные мутанты не способны образовывать нужный антибиотик, используя низкую субстратную специфичность ферментов вторичного метаболизма и вводя аналоги предшественника антибиотика, последние переводят в аналоги самого антибиотика в ходе процесса. Схема мутационного синтеза представлена ниже.[7](рис.13)           AB..DnEnМодифицированный антибиотик Синтез модифицированного антибиотика после введения аналога предшественника (D) AB CD Блокированное звено метаболизма Отсутствие синтеза антибиотика у «блокированного» мутанта ABФерментCDEАнтибиотик Предполагаемая последовательность реакций, ведущая к синтезу антибиотика рис.13. Схема мутационного синтеза Мутасинтетические антибиотики.Мутанты Nocardia mediterranei, у которых нарушена способность к ацилированию, образуют аналог предшественника рифамицина В -рифамицин SV, который служит исходным веществом для получения многих синтетических рифамицинов. Особенно успешны разработки в области биосинтеза полусинтетических пенициллинов и цефалоспоринов. Получение новых более эффективных аналогов пенициллина основано на изменении его ацильной группировки при сохранении в неизменном виде ядра пенициллина – 6-аминопенициллановой кислоты (6-АПК). В промышленности 6-АПК получают путем гидролиза природных пенициллинов с помощью специфического фермента пенициллинацилазы, образующейся с высоким выходом в процессе ферментации ряда штаммов микроорганизмов. Ацилазы различают по их субстратной специфичности. Некоторые из них способны катализировать и обратные реакции – процессы ацилирования аминогруппы 6-АПК с образованием модифицированного пенициллина. Таким путем было получено более 40000 полусинтетических пенициллинов. Существенным является то, что во многих случаях 6-АПК не выделяют из культуральной жидкости, например, при превращении бензилпенициллина в ампициллин.(рис.14) 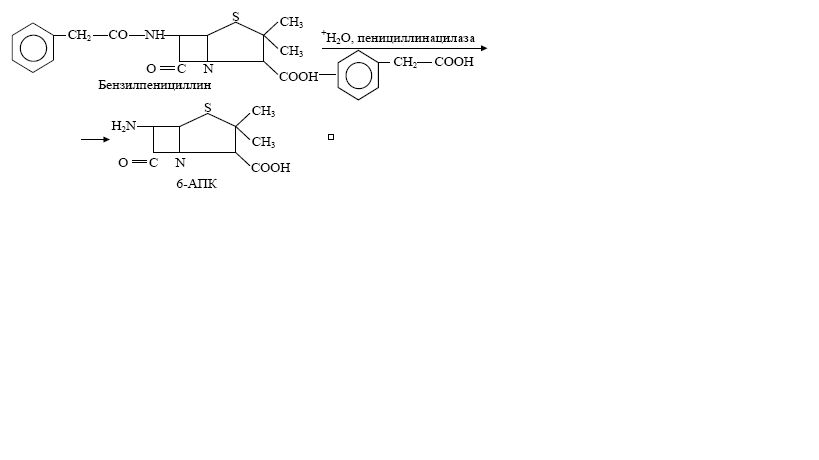 рис.14. Превращение бензилпенициллина в ампициллин Бензилпенициллин гидролизуют ацилазой мутанта Kluyvera citrophila при рН 7,8–8,0 и температуре 40–50 °С. Затем в ферментер вносят мутант Pseudomonas melanogenum и фенилглицин. Условия ферментации изменяют таким образом (рН 5,0–5,5), чтобы ацилаза второго мутантного организма осуществляла синтез ампициллина.[7](рис.15) 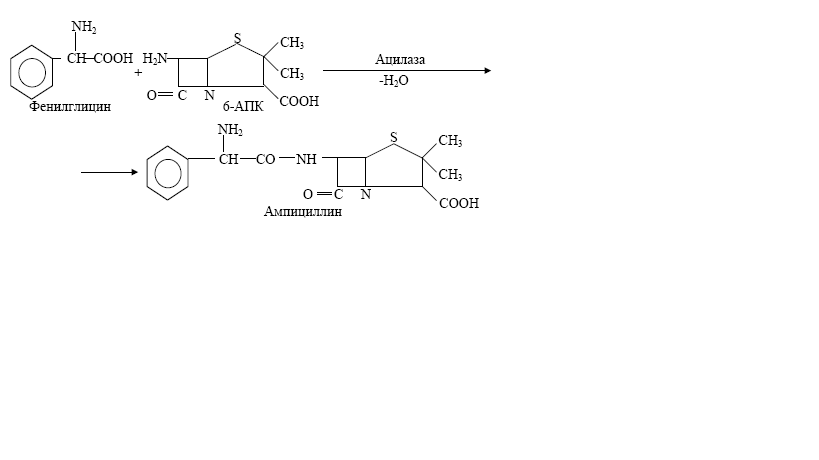 рис.15. Синтез ампициллина Таким образом, мутасинтез – это получение с помощью блок-мутантов и мутасинтонов мутасинтетических антибиотиков. |
