Справочный материал. Глава 24 – Кровь. Справочный материал по Физиологии. Глава 24 Кровь. Кровь относится к жидкостям внутренней среды организма
 Скачать 1.04 Mb. Скачать 1.04 Mb.
|
|
Рис. 24–2. Мазок крови [11]. 1 — эритроциты; 2 — сегментоядерный нейтрофил; 3 — палочкоядерный нейтрофил; 4 — эозинофил; 5 — базофил; 6 — лимфоцит; 7 — моноцит. Окраска по Романовскому–Гимзе. Гемопоэз Кроветворение — образование из стволовой кроветворной клетки клеток-предшественниц конкретных гемопоэзов, их пролиферация и дифференцировка, а также созревание клеточных элементов крови в условиях специфического микроокружения и под влиянием факторов гемопоэза. В пренатальном периоде гемопоэз происходит в нескольких развивающихся органах. Кроветворение после рождения, у детей, подростков и взрослого человека осуществляется в костном мозге плоских костей (череп, рёбра, грудина, позвонки, кости таза) и эпифизов трубчатых костей, а кроветворными органами для лимфоцитов являются селезёнка, тимус, лимфатические узлы, лимфоидные фолликулы в составе разных органов. Клетки кровяных островков желточного мешка до 12 нед внутриутробного развития образуют первые клетки крови — первичные эритробласты — крупные клетки, содержащие ядро и эмбриональные типы Hb. В течение второго месяца развития стволовые клетки крови заселяют печень, селезёнку и тимус. Образуются все виды клеток крови. Костный мозг у эмбриона закладывается к концу третьего месяца внутриутробного периода. К четвёртому месяцу в костном мозге появляются лимфоидные элементы и родоначальные клетки крови, а с пятого месяца возникает дифференцированное костномозговое кроветворение. Помимо этого, созревание лимфоцитов происходит и в других органах — печени, тимусе, селезёнке, лимфатических узлах. Последние в антенатальном периоде также являются органом эритроцитопоэза. К моменту рождения, после рождения и у взрослого кроветворение ограничивается костным мозгом и лимфоидной тканью. При недостаточности костного мозга восстанавливается экстрамедуллярный гемопоэз (кроветворение в печени, селезёнке и лимфатических узлах). Зрелые клетки периферической крови развиваются из предшественников, созревающих в красном костном мозге. Унитарная теория кроветворения (рис. 24–3) предусматривает, что родоначальница всех клеточных элементов крови — стволовая кроветворная клетка. Её потомки — полипотентные клетки-предшественницы лимфоцитопоэза (CFU-Ly) и миелопоэза (CFU-GEMM). В результате деления CFU-Ly и CFU-GEMM их потомки остаются полипотентными или превращаются в коммитированные (предопределённые судьбой) унипотентные клетки-предшественницы, также способные делиться, но дифференцирующиеся (развивающиеся) только в одном направлении. Пролиферацию унипотентных клеток–предшественниц стимулируют колониестимулирующие факторы и интерлейкины (особенно ИЛ3). 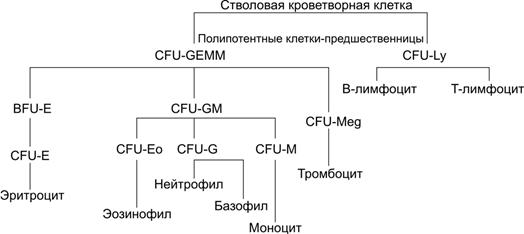 Рис. 24–3. Схема гемопоэза.; CFU GEMM — полипотентная клетка-предшественница миелопоэза; CFU Ly — полипотентная клетка-предшественница лимфоцитопоэза; CFU GM — полипотентная клетка-предшественница гранулоцитов и моноцитов; CFU G — полипотентная клетка-предшественница нейтрофилов и базофилов. Унипотентные предшественники: BFU E и CFU E — эритроцитов; CFU Eo — эозинофилов; CFU M — моноцитов; CFU Meg — мегакариоцитов. CFU — Colony Forming Unit — колониеобразующая единица (КОЕ), BFU — Burst Forming Unit — взрывообразующая единица. Эритропоэз (рис. 24–4). Начало эритроидного ряда — стволовая клетка эритропоэза, или взрывообразующая единица (BFU-E), из которой формируется унипотентный предшественник эритроцитов (CFU-E). Последний даёт начало проэритробласту. Дальнейшая дифференцировка приводит к увеличению содержания Hb и потере ядра. Из проэритробласта путём пролиферации и дифференцировки последовательно развиваются эритробласты: базофильный полихроматофильный оксифильный (нормобласт) и далее неделящиеся формы — ретикулоцит и эритроцит. От BFU-E до нормобласта — 12 клеточных поколений, а от CFU-E до позднего нормобласта — 6 или меньше клеточных делений. Длительность эритропоэза (от его стволовой клетки BFU-E до эритроцита) — 2 недели. Интенсивность эритропоэза контролирует эритропоэтин. Основной стимул для выработки эритропоэтина — уменьшение содержания кислорода в крови (рО2) — гипоксия (рис. 24–5). 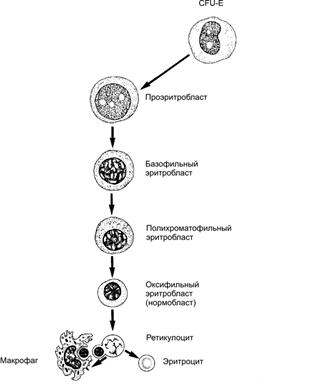 Рис. 24–4. Эритропоэз [11]. Из взрывообразующей единицы эритропоэза BFU-E дифференцируется унипотентный предшественник эритроцитов CFU-E. Последний даёт начало проэритробласту. Дальнейшая дифференцировка приводит к уменьшению размеров клеток и количества органелл, но к увеличению содержания Hb и потере ядра. При этом из проэритробласта последовательно дифференцируются базофильный, полихроматофильный, оксифильный (неделящийся нормобласт) эритробласт, ретикулоцит, эритроцит. Вытолкнутое из нормобласта ядро поглощает макрофаг. 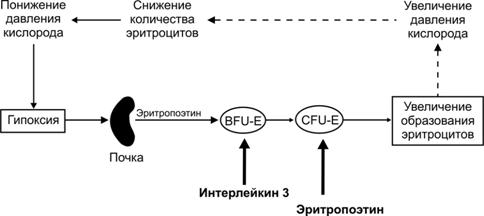 Рис. 24–5. Регуляция эритропоэза [11]. Пролиферацию взрывообразующей единицы эритропоэза (BFU-E) стимулирует ИЛ3. Унипотентный предшественник эритроцитов CFU-E чувствителен к эритропоэтину. Решающий стимул для образования эритроцитов — гипоксия, запускающая синтез эритропоэтина в почке, а у плода также в печени. Эритропоэтин выходит в кровь и поступает в костный мозг, где стимулирует размножение и дифференцировку унипотентного предшественника эритроцитов (CFU-E) и дифференцировку последующих клеток эритроидного ряда. В результате количество эритроцитов в крови увеличивается. Соответственно возрастает количество кислорода, поступающего в почку, что тормозит образование эритропоэтина. Гранулоцитопоэз (рис. 24–6). Гранулоциты образуются в костном мозге. Нейтрофилы и базофилы происходят из полипотентной клетки-предшественницы нейтрофилов и базофилов (CFU-G), а эозинофилы — из унипотентного предшественника эозинофилов (CFU-Eo). CFU-G и CFU-Eo — потомки полипотентной клетки-предшественницы гранулоцитов и моноцитов (CFU-GM). При развитии гранулоцитов можно выделить такие стадии: миелобласты промиелоциты миелоциты метамиелоциты палочкоядерные и сегментоядерные гранулоциты. Специфические гранулы появляются на стадии миелоцитов; с этого момента клетки называют в соответствии с типом образующихся из них зрелых гранулоцитов. Клеточные деления прекращаются на стадии метамиелоцита. Пролиферацию и дифференцировку клеток-предшественниц контролируют колониестимулирующие факторы (гранулоцитов и макрофагов — GM-CSF, гранулоцитов — G-CSF), ИЛ3 и ИЛ5 (предшественники эозинофилов). 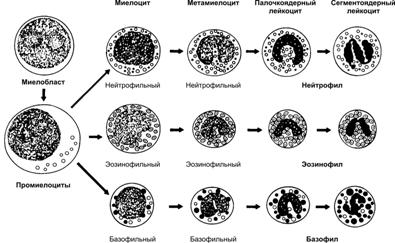 Рис. 24–6. Гранулоцитопоэз [11]. В ходе дифференцировки предшественников гранулоцитов выделяют: миелобласт, промиелоцит, миелоцит, метамиелоцит, палочкоядерный и сегментоядерный гранулоциты. Колониестимулирующий_фактор_гранулоцитов'>Колониестимулирующий_фактор_гранулоцитов_и_макрофагов'>Колониестимулирующий фактор гранулоцитов и макрофагов (GM-CSF). На образование и пролиферацию фагоцитов (гранулоцитов и моноцитов) влияет более десятка цитокинов. Наиболее значим GM-CSF, способствующий образованию моноцитов и гранулоцитов. GM-CSF продуцируют моноциты, Т-лимфоциты, фибробласты, клетки эндотелия. GM-CSF влияет на ранние стадии гемопоэза, стимулируя пролиферацию практически всех классов ранних клеток-предшественниц гранулоцитов и макрофагов. Колониестимулирующий фактор гранулоцитов (G-CSF) влияет на полипотентную клетку-предшественницу нейтрофилов и базофилов (CFU-G), стимулируя её дифференцировку в унипотентные клетки-предшественницы нейтрофилов и базофилов. G-CSF синтезируют макрофаги и фибробласты. Колониестимулирующий фактор макрофагов (M-CSF) стимулирует полипотентную клетку-предшественницу гранулоцитов и моноцитов (CFU-GM), а также на унипотентный предшественник моноцитов (CFU-M). M-CSF вырабатывают макрофаги и фибробласты. Интерлейкин-3 действует на стволовую кроветворную клетку и полипотентную клетку-предшественницу миелопоэза (CFU-GEMM), на большинство клеток-предшественниц миелоидного ряда, стимулируя формирование эритроцитов, гранулоцитов, моноцитов, тромбоцитов. Вырабатывается Т-лимфоцитами и клетками стромы костного мозга. ИЛ-3 поддерживает размножение практически всех классов ранних клеток-предшественниц. Моноцитопоэз. Моноциты и гранулоциты имеют общую клетку-предшественницу — колониеобразующую единицу гранулоцитов и моноцитов (CFU-GM), образующуюся из полипотентной клетки-предшественницы миелопоэза (CFU-GEMM). В развитии моноцитов выделяют две стадии — монобласт и промоноцит. Тромбоцитопоэз. Из мегакариобластов развиваются самые крупные (30–100 мкм) клетки костного мозга — мегакариоциты (рис. 24–7). При дифференцировке мегакариоцит увеличивается в размерах, его ядро становится дольчатым. Образуется развитая система демаркационных мембран, по которым происходит отделение («отшнуровка») тромбоцитов (рис. 24–8). Пролиферацию предшественников мегакариоцитов — мегакариобластов — стимулирует синтезируемый в печени тромбопоэтин. 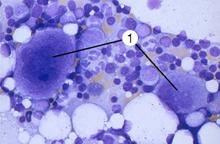 Рис. 24–7. Мазок костного мозга [11]. Видны клетки крови, преимущественно эритроциты, на разных стадиях дифференцировки. Хорошо заметен мегакариоцит (1) — очень крупная клетка с большим дольчатым ядром. Окраска по Романовскому–Гимзе. 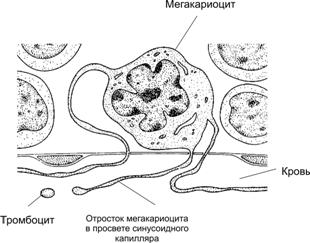 Рис. 24–8. Образование тромбоцитов [11]. Находящийся в костном мозге мегакариоцит образует протромбоцитарную псевдоподию. Последняя проникает сквозь стенку капилляра в его просвет. От псевдоподии отделяются тромбоциты и поступают в кровоток. Лимфопоэз. Из стволовой кроветворной клетки (CFU-blast) происходит полипотентная клетка-предшественница лимфопоэза (CFU-Ly), которая впоследствии даёт начало клеткам-предшественницам B-лимфопоэза, T-лимфопоэза и (частично) предшественницам NK-клеток. Ранние предшественники В-лимфоциты образуются в костном мозге, а Т-лимфоцитов — в тимусе. Дальнейшая дифференцировка включает в себя уровни про-B(T)-клеток, пре-B(T)-клеток, незрелых B(T)-клеток, зрелых («наивных») B(T)-клеток и (после контакта с Аг) — зрелых B(T)-клеток окончательных стадий дифференцировки. Продуцируемый клетками стромы костного мозга ИЛ7 способствует образованию Т- и В-лимфоцитов, воздействуя на их клетки-предшественницы. В отличие от других клеток крови, лимфоциты могут пролиферировать и вне костного мозга. Это происходит в тканях иммунной системы в ответ на стимуляцию. Пункция костного мозга. Для оценки гемопоэзов, особенно при заболеваниях крови, проводят пункцию костного мозга. Оснащение: игла Кассирского; шприц ёмкостью 10–20 мл; стерильные шарики и салфетки; спирт, 5% раствор йода, эфир; лейкопластырь; предметные стёкла; шлифованное стекло; пробирки с разводящей жидкостью для подсчёта абсолютного количества мегакариоцитов и миелокариоцитов. Обезболивание: премедикация с использованием промедола, седуксена, пипольфена и дроперидола; местное обезболивание раствором новокаина. Техника 1. Место пункции — грудина на уровне III–IV межреберья или рукоятка по средней линии. 2. Положение больного — на спине, под лопатки подкладывают валик. 3. После обработки кожи больного иглу Кассирского берут в правую руку и быстрым движением вводят в костномозговой канал. Иглу вводят строго по срединной линии вращающими движениями. При прокалывании наружной костной пластинки слышится хруст и ощущается чувство «провала»; при этом необходимо прекратить дальнейшее продвижение иглы вглубь. После этого из иглы вынимают мандрен, насаживают шприц и проводят аспирацию. Во избежание большой примеси крови к костному мозгу необходимо набирать как можно меньше материала (не более 0,5 мл). 4. Если аспират получить не удаётся, следует осторожно продвинуть иглу вглубь кости или, не вынимая иглу из кожи, сделать прокол соседнего участка кости, предварительно вставив мандрен. 5. При появлении в шприце костного мозга, аспирацию прекращают, шприц снимают с иглы, вставляют мандрен и в таком собранном виде иглу извлекают из кости. Место пункции смазывают йодом и накладывают стерильную повязку (салфетку прикрепляют лейкопластырем). 6. Из аспирированного костного мозга приготавливают мазок и проводят его исследование (см. рис. 24–7). Эритроциты Из красного костного мозга в кровь поступают преимущественно незрелые эритроциты — ретикулоциты. Они (в отличие от зрелых эритроцитов) содержат рибосомы, митохондрии и комплекс Гольджи. Окончательная дифференцировка в эритроциты происходит в течение 24–48 часов после выхода ретикулоцитов в кровоток. Количество поступающих в кровоток ретикулоцитов в норме равно количеству удаляемых эритроцитов. Ретикулоциты составляют около 1% всех циркулирующих красных клеток крови. Эритроциты (см. рис. 24–1,А, 24–2,1) — безъядерные клетки диаметром 7–8 мкм (нормоциты). Количество эритроцитов: у женщин — 3,9–4,91012/л, у мужчин — 4,0–5,21012/л. Более высокое содержание эритроцитов у мужчин обусловлено стимулирующим эритропоэз влиянием андрогенов. Продолжительность жизни (время циркуляции в крови) — 100–120 дней. Определение количества эритроцитов В сухую чистую пробирку наливают 4 мл 3% раствора натрия хлорида. Капиллярной пипеткой набирают из свежей капли 0,02 мл крови, осторожно выдувают её в пробирку и пипетку промывают в верхнем слое жидкости. Хорошо перемешивают. Концом круглой стеклянной палочки отбирают каплю разведённой крови и наносят на край камеры Горяева (с притёртыми до ньютоновских колец покровным стеклом). Через 1 мин приступают к подсчёту эритроцитов. Увеличение микроскопа должно быть малым, диафрагма прикрытой. Подсчёт ведут в 5 больших квадратах, расположенных по диагонали, каждый из которых разделён на 16 маленьких. При подсчёте необходимо использовать следующее правило: подсчитывают все клетки, лежащие целиком или большей своей частью внутри маленького квадрата, клетки, пересекаемые разграничительными линиями (контурами квадратов) пополам, сосчитывают лишь по левому и верхнему контурам квадрата. Полученное значение умножают на 50, при этом получают количество эритроцитов в 1 мкл периферической крови. Форма и размеры. Эритроцит в крови имеет форму двояковогнутого диска диаметром 7–8 мкм. Считают, что именно такая конфигурация создаёт наибольшую площадь поверхности по отношению к объёму, что обеспечивает максимальный газообмен между плазмой крови и эритроцитом. При любой другой форме эритроцитов говорят о пойкилоцитозе. Разброс размеров эритроцитов — анизоцитоз, клетки диаметром >9 мкм — макроциты, <6 мкм — микроциты. При ряде заболеваний крови изменяются размеры и форма эритроцитов, а также снижается их осмотическая резистентность, что приводит к разрушению (гемолизу) эритроцитов. Гемолиз — разрушение эритроцитов вследствие как внутренних дефектов клетки (например, при наследственном сфероцитозе), так и под влиянием разных факторов микроокружения. При этом содержимое клетки выходит в плазму; - и димеры Hb связываются гаптоглобином и транспортируются в печень для разрушения. Гемолиз приводит к снижению общего количества циркулирующих эритроцитов и развивается гемолитическая анемия. Анизоцитоз — появление эритроцитов аномальных размеров. Причины — дефекты некоторых ферментов в эритроцитах (например, аденозиндезаминазы и 4-гидроксифенилпируватгидроксилазы). Макроцитоз в сочетании с анемией и появлением мегалобластов наблюдают при дефиците фолатов и витамина B12, применении некоторых ЛС и при наследственных заболеваниях (например, оротовая ацидурия, синдром Леша-Найена). Макроцитоз без появления мегалобластов — признак заболевания печени, наблюдают, например, при злоупотреблении алкоголем, гипотиреоидизме. Мегалобласт. Термин «мегалобласт» (крупные эритроидные клетки) применяют для обозначения первой генерации эритроидных клеток (т.е. термин относят как к нормальным, так и к патологическим эритроидным клеткам). Нормобластический эритропоэз: пронормобласт (проэритробласт) базофильные и полихроматофильные нормобласты (эритробласты) ортохромные (оксифильные) нормобласты (эритробласты) после выталкивания ядра молодые эритроциты (нормоциты) именуют ретикулоцитами (зернистость окрашивается бриллиантовым крезиловым синим) эритроциты. Мегалобластный эритропоэз: промегалобласт базофильный мегалобласт полихроматофильный мегалобласт ортохроматический (оксифильный) мегалобласт. Лекарственные средства. К появлению макроцитов и развитию мегалобластной анемии могут привести препараты, применяемые при болезнях злокачественного роста (метотрексат), бактериальных (триметоприм) и паразитарных (пириметамин) инфекциях. Микроцитоз. Эритроциты диаметром <6 мкм наблюдают при гемоглобинопатиях и талассемии. Пойкилоцитоз (табл. 24–4). Сфероцитоз (эллиптоцитоз, овалоцитоз) — присутствие в крови эритроцитов сферической или эллиптической (овальной) формы — сфероцитов. Чаще всего это макроциты. Одна из причин — дефектный спектрин с нарушенной способностью связываться с белком полосы 4.1. Стоматоцитоз. В эритроците (стоматоците) центрально расположено просветление в виде стомы, щели (наследственный сфероцитоз, Rh ноль синдром). Акантоцитоз. Большинство эритроцитов имеет множественные шиповидные выросты. Акантоцитоз возникает, например, при экспрессии дефектного трансмембранного гликопротеина полосы 3. Пиропойкилоцитоз. При повышении температуры тела в периферической крови могут появиться эритроциты аномальной формы (при этом найдена, в частности, точечная мутация гена спектрина). Типы патологических эритроцитов (табл. 24–4). Патологические включения. Базофильные включения в эритроцитах, тельца Жолли и кольца Кэбота находят в эритроцитах при анемиях (табл. 24–4). |
