Тема Соединения со смешанными функциями Гидроксиальдегиды и гидроксикетоны. Гидрокси и оксокислоты Цель занятия
 Скачать 1.67 Mb. Скачать 1.67 Mb.
|
Конкретные задачи1. Студент должен знать: строение гетероциклических соединений – пиррола, фурана, тиофена, имидазола, пиразола, пиридина, пиримидина и пурина; электронное строение пиррольного и пиридинового атома азота; ароматичность и критерии ароматичности; реакции электрофильного замещения в гетероциклических ароматических системах; проявление кислотности и основности гетероциклических соединений. 2. Студент должен уметь: писать формулы пяти- и шестичленных гетероциклических соединений с одним или двумя гетероатомами, доказывать их ароматичность; писать уравнения реакций, показывающих их основные, кислотные и ароматические свойства; писать формулы пиримидиновых и пуриновых оснований в лактимной и лактамной формах; составлять структуры нуклеозидов, нуклеотидов, фрагментов первичной структуры нуклеиновых кислот. Мотивация. Гетероциклические соединения широко распространены в природе и играют важную биологическую роль. Они входят в состав нуклеиновых кислот (пурин, пиримидин), пигментов растений и животных (пиррол), гормонов (индол), витаминов (пиррол, тиофен, пиридин), аминокислот (индол, имидазол, пирролидин), алкалоидов (пиридин, пиперидин); лекарственных препаратов (имидазол, хинолин, индол, пиразолон, пиридин), красителей (-оксииндол). Вопросы для самоподготовки1. Напишите структурные формулы 2.5-диметилфурана, 2-аминопиридина, 3-оксииндола, 2,6-диоксипиримидина; 2,6,8-триоксипурина. 2. Получите из пиридина никотиновую кислоту. Напишите уравнение реакции ее с NH3. 3. Почему мочевая кислота проявляет кислотные свойства? 4. Напишите формулы пиримидиновых и пуриновых оснований, входящих в состав нуклеиновых кислот. Этапы занятий и контроль усвоения знаний
Содержание этапов занятия1-й этап. Преподаватель проверяет наличие выполненного домашнего задания в рабочих тетрадях и оценивает его по пятибалльной системе. 2-й этап.Студент письменно отвечает на билет программированного контроля. Ответ оценивается по принятой балльной системе (0, 5, 10 баллов). 3-й этап. На 1 занятии по теме «Гетероциклические соединения» студенты учатся писать формулы пяти- и шестичленных гетероциклов с одним гетероатомом. Разбирают электронное строение «пиррольного» и «пиридинового» атомов азота, рассматривают свойства, характерные для этих соединений: ароматичность, кислотно-основные, нуклеофильные. На 2 занятии рассматриваются пяти- и шестичленные гетероциклические соединения с двумя гетероатомами: имидазол, пиразол, пиримидин, окси- и аминопрозводные пиримидина – урацил, тимин, цитозин в лактимной и лактамной формах; конденсированные гетероциклические соединения: индол, пурин, окси- и аминопроизводные пурина – аденин, гуанин, мочевая кислота в лактимной и лактамной форме; разбирается строение нуклеозидов, нуклеотидов, фрагментов полинуклеотидной цепи. ТеорияПятичленные гетероциклические соединения с одним гетероатомом 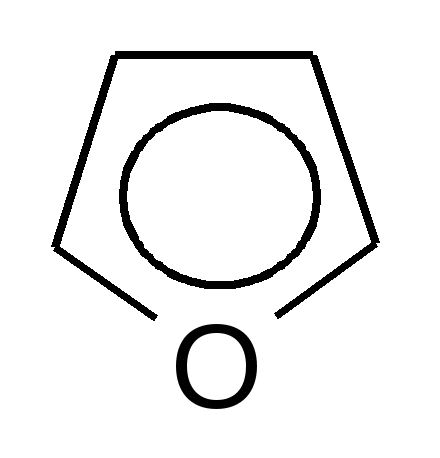 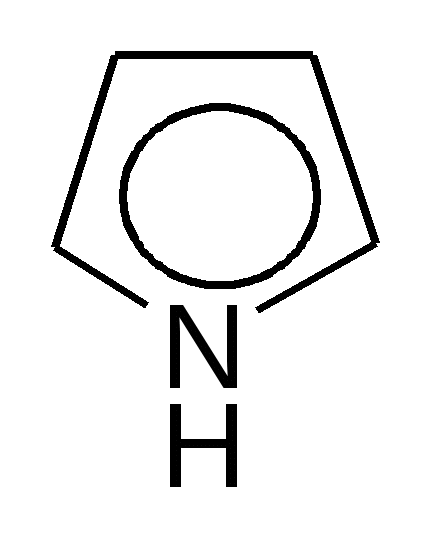 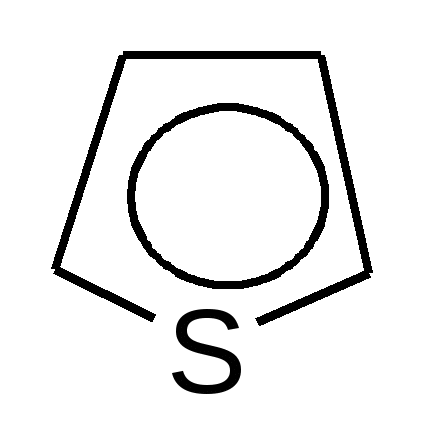 фуран пиррол тиофен Все эти соединения являются ароматическими, так как отвечают критериям ароматичности:
- скелет;
натуральное число. 4р Электрона поставляют атомы углерода и 2р- электрона – гетероатомы N, O или S. Образуется - электронный секстет;
Общей чертой ароматических гетероциклов и производных бензола является высокая термодинамическая устойчивость. Отличие от бензола.
Поэтому легче идут реакции с раскрытием кольца. Например, реакции восстановления. Электронное строение «пиррольного» атома азота 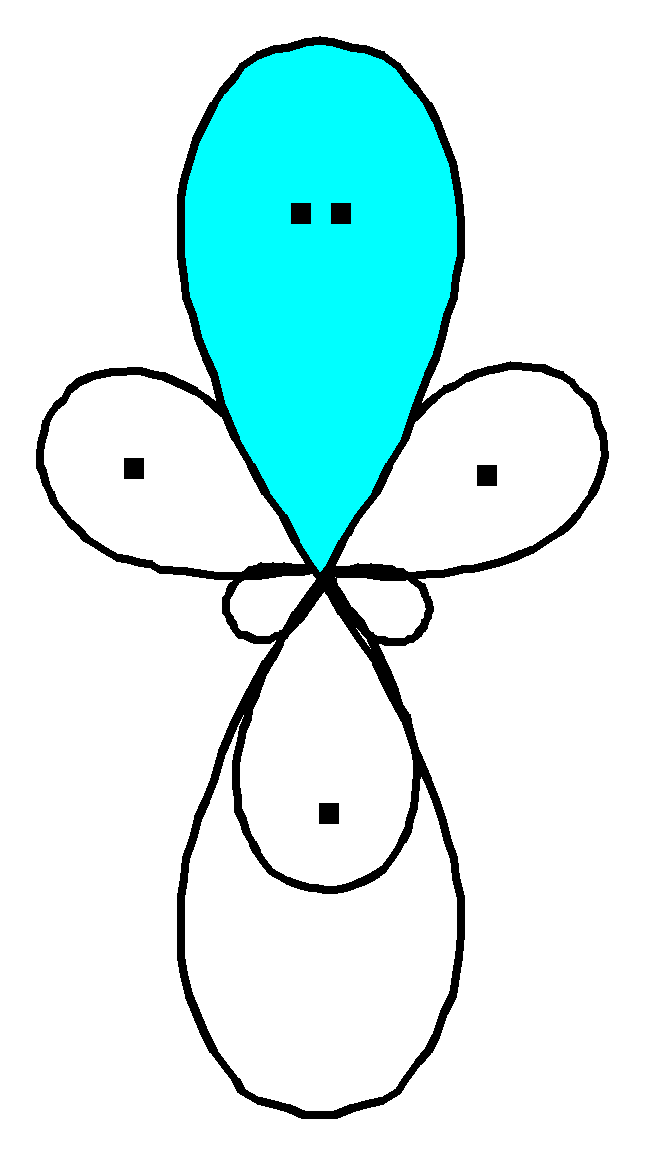  Химические свойства пятичленных гетероциклических соединений на примере пиррола.
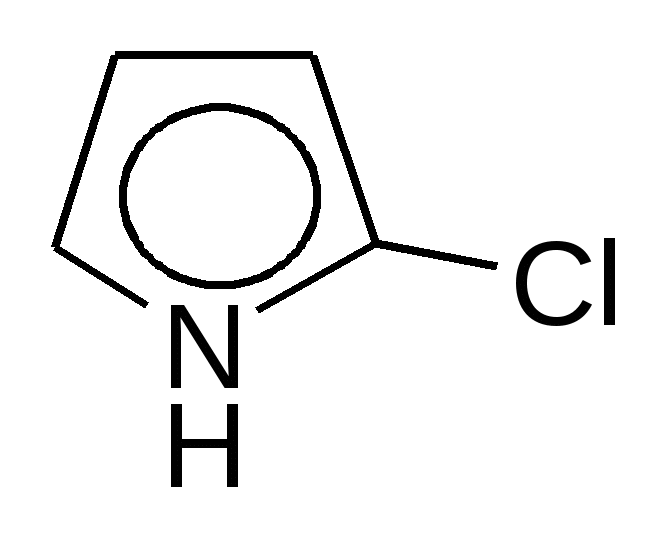 SO2Cl2   + SO2 + HCl + SO2 + HCl-хлорпиррол   SO3 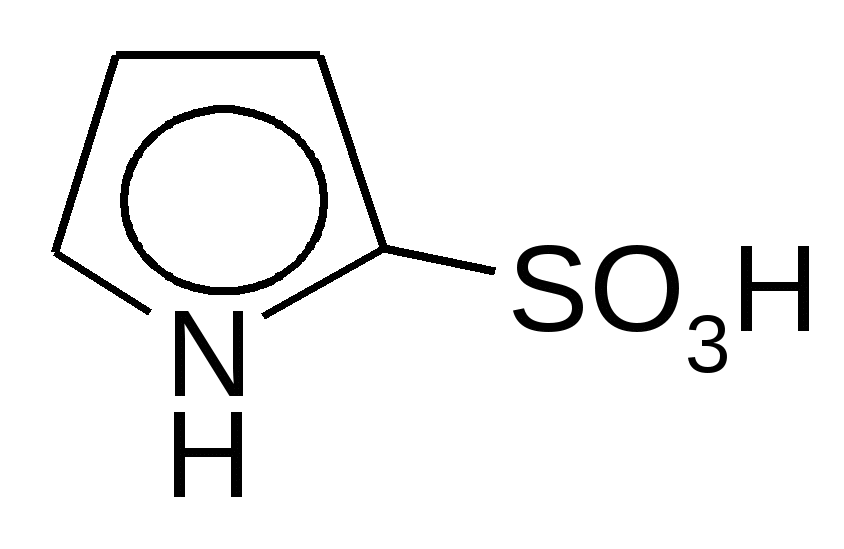 в пиридине в пиридине - сульфопиррол 2. Основные свойства почти отсутствуют, так как электронная пара втянута в сопряжение: Коснпиррола=10-14; Косн анилина =10-10. При насильственном протонировании сильными минеральными кислотами ароматическая система нарушается, пиррол превращается в неустойчивый дивиниламин, который быстро полимеризуется с образованием смолы:  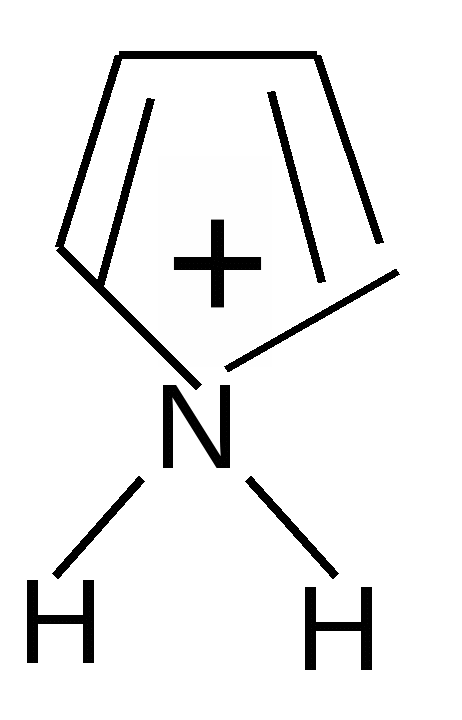 Н+ полимеризация Н+ полимеризация  смола смоланеустойчивый дивинилимин Это свойство осмоляться под действием кислот называется «ацидофобностью», и его надо учитывать при выборе реагентов в реакциях электрофильного замещения (см. п.1) 3. Кислотные свойства – тоже слабые. Взаимодействие со щелочными металлами идет с образованием неустойчивых солей.  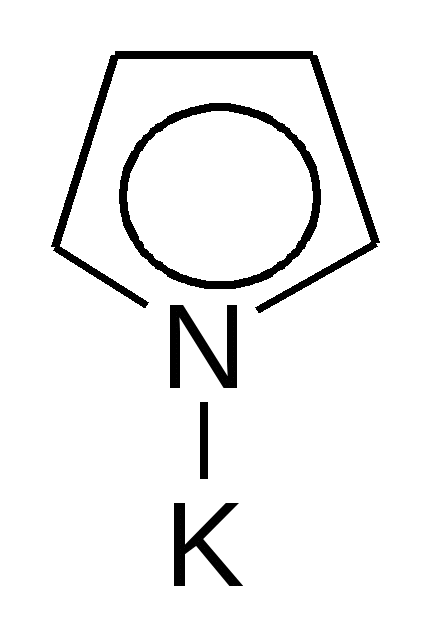 К/t К/t  + Н2 + Н2Н2О неустойчивая соль пирролят калия 4. Восстановление (HI, t=30°). Протекает легче из-за меньшей энергии сопряжения по сравнению с бензолом. 2[H] 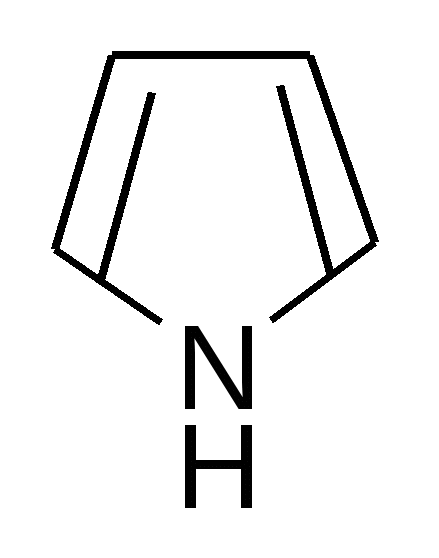 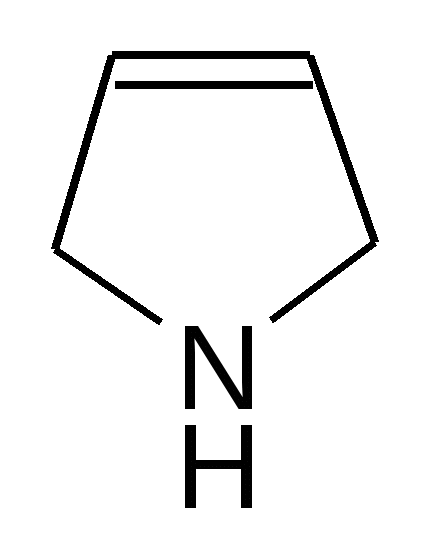 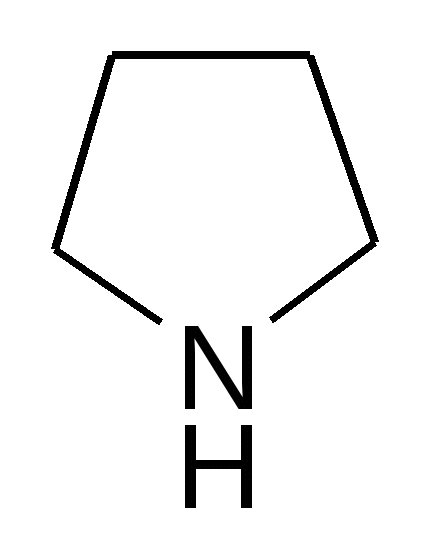 2[H] 2[H]   пиррол пирролин пирролидин По мере восстановления основность повышается. Восстановленное пиррольное кольцо входит в состав алкалоидов, аминокислот (пролин, оксипролин). Его производное – N-винилпирролидон применяется в медицине в качестве заменителя плазмы крови и клеящего, связующего материала. 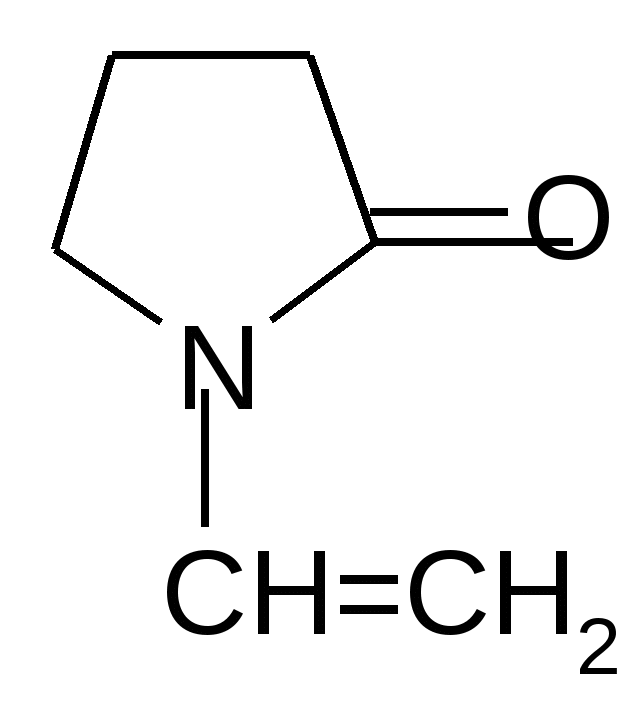 В природных соединениях ароматический пиррольный цикл часто встречается в различных многоядерных системах, из которых особенно важно ароматическое порфириновое ядро, входящее в состав гемоглобина и хлорофилла. Порфирин имеет единое - электронное облако, содержащее 26 - электронов; 22 электрона одиннадцати сопряженных двойных связей и 2 неподеленные пары электронов атома азота. Этот цикл отличается также высокой термодинамической устойчивостью. |
