Теория и технология производства стали 1. Учебник для вузов. М. Мир, ООО Издательство act
 Скачать 7.23 Mb. Скачать 7.23 Mb.
|
|
Рис. 9.7. Схемы расклинивающего (отталкивающего) действия одноименно заряженных ионов, расположенных на поверхности газовых пузырьков аа{и bb\ (I), и эффекта Меренгони в поверхностных слоях abи а'Ь', охватывающих газовые пузыри (заштрихованная часть — жидкость) (II) В. Я. Явойский выделил следующие факторы, определяющие склонность шлака к вспениванию: 1. Поверхностная вязкость шлака, т. е. механическая прочность поверхностной пленки, определяемая, в свою очередь, концентрацией поверхностно-активных крупных анионов (кремнекислородных или кремнефосфористых комплексов). 2. Гетерогенность шлаков, присутствие в них хорошо смачиваемых шлаком (лиофильных) твердых частиц. 3. Содержание поверхностно-активных компонентов, вызывающих расклинивающий эффект и поверхностную диффузию в направлении только что образовавшихся участков пленки пузыря (эффект Меренгони). 4. Температура шлака (низкая температура определяет повышенные механическую прочность пленки, поверхностную вязкость шлака и замедленный характер растворения взвешенных в шлаке твердых частиц). 5. Интенсивность и характер газового потока, пронизывающего слой шлака (увеличение интенсивности газовыделения, а главное — степени дисперсности газовых пузырей, образующих поток, пронизывающий шлаковый расплав, приводит к росту вспениваемости шлака). 6. Химический состав шлака. В основных шлаках склонность к пенооб-разованию повышается при повышении концентрации SiO2 и Р2О5 и понижении истинной основности (т. е. основности, рассчитанной по концентрации растворенного оксида кальция). Присадка плавикового шпата в подвижных шлаках несколько повышает склонность шлаков к вспениванию в связи с повышением в шлаке концентрации поверхностно-активного иона F-. Повышение концентрации оксидов железа увеличивает склонность шлаков к вспениванию в результате стимулирующего действия на развитие подшлакового процесса окисления углерода, сопровождающегося образованием множества мелких пузырей, медленно всплывающих в шлаке. 7. Давление газовой среды над слоем шлака (повышение давления в плавильном пространстве печи, наличие настильной упругой струи факела, осаживающей пену, приводят к уменьшению ценообразования). Наибольшей склонностью к вспениванию обладают шлаки с основностью 1,5-1,6 (рис. 9.8). Повышение в шлаке содержания оксидов железа и марганца способствует снижению склонности шлаков к вспениванию. Все мероприятия по ускорению шлакообразования для получения по расплавлении более благоприятной и более высокой основности способствуют уменьшению вспениваемости шлаков. К ним относятся различные приемы интенсивного перемешивания ванны, методы ускоренного нагрева, способы замены обычных шлакообразующих (известняка, железной руды) комплексными, заранее подготовленными флюсами (продукты, например, совместного обжига известняка, железной и марганцевой руд и др.), использования шлакообразующих в порошкообразном виде и т. д. Технология ведения плавки стали в современных высокомощных дуговых электропечах включает операцию искусственного вспенивания шлака. Для этого на шлак или под шлак вводят (чаще вдувают) порошок кокса или каменного угля, инициируя протекание реакции окисления углерода непосредственно в шлаке. Образующиеся мелкие пузырьки СО обеспечивают интенсивное вспенивание шлака; соответственно создаются благоприятные условия для экранирования дуг, уменьшения облучения стен и свода печи и улучшения усвоения тепла ванной. 9.8. СВОЙСТВА ШЛАКОВ Свойства шлаков определяются их составом и температурой. На практике при проведении расчетов вместимости металлургических агрегатов, при конструировании плавающих на границе шлака и металла устройств для отсечки шлака и в других случаях необходимо знание плотности шлака. Основные компоненты шлака при комнатной температуре имеют следующую плотность, г/см3: 1) «легкие» компоненты — Si02 (тридимит) 2,26, СаО 3,4, MgO 3,65; 2) «тяжелые» компоненты — МпО 4,5, Fe2O3 5,24, FeO 5,7. Плотность шлака практически определяется содержанием в нем «тяжелых» оксидов (рис. 9.9). Плотность реальных шлаков во время плавки непосредственно в сталеплавильном агрегате изменяется в зависимости от степени вспенивания шлака. Вязкость жидких сталеплавильных шлаков колеблется в широких пределах, причем характер изменения вязкости от температуры зависит от со става шлака. Из рис. 9.10 видно, что, в то время как вязкость кислых шлаков по мере изменения температуры изменяется плавно («длинные» шлаки), основные шлаки имеют короткий температурный интервал перехода из жидкого в твердое состояние («короткие» шлаки); вязкость таких шлаков обычно резко возрастает при снижении температуры ниже 1500 ºС. 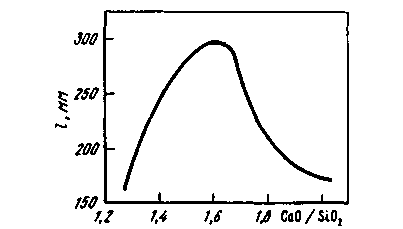 Рис. 9.8. Толщина слоя шлака l в 160-т мартеновских печах в момент расплавления ванны 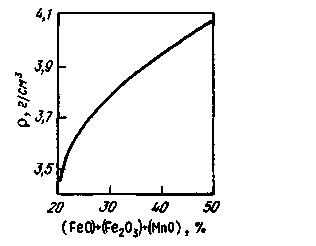 Рис. 9.9. Зависимость плотности основных шлаков от содержания оксидов железа и марганца 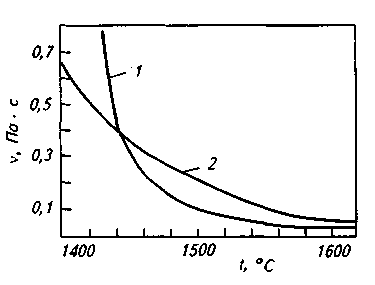 Вязкость основных шлаков в значительной степени зависит от содержания таких тугоплавких составляющих, как Сг2О3 (t пл= 2280 °С). и MgO (tпл = 2800 °С). При продувке кислородом расплава, содержащего более 2 % Сг, содержание Сг2О3 в шлаке может превысить 20 %. Температура плавления такого шлака возрастает настолько, что шлак становится комкообраз-ным. При интенсивном разрушении футеровки агрегата в шлаке начинает увеличиваться содержание MgO, вязкость такого шлака растет вплоть до превращения шлака в вязкую, полутвердую массу. Теплоемкость шлаков в зависимости от состава и температуры изменяется в довольно узких пределах: 0,8— 1,2кДж/(кг*К). Жидкие шлаки обладают электрической проводимостью, что является показателем их ионного строения. Электрическая проводимость основных шлаков выше, чем кислых. При повышении температуры электрическая проводимость увеличивается. При температурах сталеплавильных процессов электрическая проводимость шлаков в зависимости от их состава колеблется в пределах от 0,2 до 1,0 Ом-1 • см -1. Данные об электрической проводимости шлаков необходимы при организации процессов электроплавки, электроподогрева шлака в ковше при внепечной обработке металла, при электрошлаковом переплаве и т. п. Электрическая проводимость обычно выше у шлаков, обладающих повышенной теплопроводностью и пониженной вязкостью. Теплопроводность шлаков изменяется в зависимости от состава в широких пределах; при повышении температуры теплопроводность возрастает. Реальные шлаки представляют собой многокомпонентные системы, поэтому сложно определить их температуру плавления, зная температуры плавления составляющих этих шлаков. Обычно используют данные тройных диаграмм состояния шлаковых систем, позволяющие приближенно судить о температурах плавления реальных шлаков более сложного состава. Из диаграммы состояния СаО-А12О3 (рис. 9.11) следует, что при введении в основной шлак А12О3 (в боксите много А12О3) 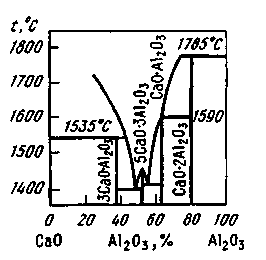 Рис. 9.11. Диаграмма состояния СаО-А12О3 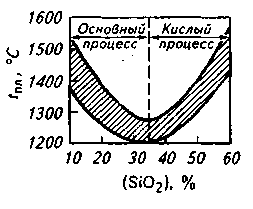 Рис. 9.12. Зависимость температуры плавления шлаков /щ, от содержания в них SiO2 температура плавления шлака снизится (или при неизменной температуре возрастет ререгрев шлака над температурой плавления) и соответственно понизится вязкость шлака и повысится его жид-коподвижность. На температуру плавления шлаков в значительно степени влияет изменение содержания в них кремнезема (рис. 9.12). Содержание SiO2 в шлаке определяет его основную характеристику: основный шлак или кислый. 10. СТРОЕНИЕ ЖИДКОЙ СТАЛИ 10.1. ОБЩИЕ СВЕДЕНИЯ Жидкое состояние вещества считается промежуточным между твердым и газообразным. И если идеальный газ характеризуется полным разупорядоче-нием строения, а идеальное твердое тело (кристалл) — полным упорядочением в расположении частиц и неизменностью этого расположения в пространстве и времени, то для жидкости такой идеальной модели пока нет. Известный английский физик Дж. Бернал предложил классифицировать состояния материи следующим образом: кристаллы обладают регулярной и связанной структурой, жидкости — нерегулярной и связанной структурой, газы — нерегулярной и несвязанной структурой. Структура жидкости отличается от структуры кристалла и газа. Кроме того, каждая жидкость имеет ряд структур, которые могут свободно переходить одна в другую. Расплавленные металлы обладают комплексом свойств, с одной стороны, сходных со свойствами неметаллических жидкостей, а с другой — со свойствами твердых металлов. Характерными отличительными признаками металлических жидкостей (расплавов) от всех остальных жидкостей являются: высокие электрические и гальваномагнитные свойства (электрическая проводимость, т. э. д. с., эффект Холла, обусловленные наличием коллективизированных валентных электронов), высокая плотность в размещении частиц (ионов); при этом удельный объем металлической жидкости в точке плавления не превышает удельный объем кристалла более чем на 2— 6 %, т. е. при плавлении кристалла расстояния между составляющими его частицами изменяются незначительно. Железо является Зd-переходным металлом. Конфигурация внешних электронных оболочек в твердом железе 3p63d64s2. Радиус атома железа 0,128нм. Кристаллическое железо в зависимости от температуры и давления может находиться в нескольких модификациях ( При рассмотрении железа и его сплавов следует учитывать свойственные сталеплавильным процессам небольшие перегревы металла относительно температуры плавления. Если температура плавления стали в зависимости от ее состава обычно колеблется в пределах от 1450 до 1535 °С, то температура жидкого стального расплава в сталеплавильном агрегате составляет 1500—1650 °С. Например, температура плавления стали -1500 °С, а температура жидкого расплава в пени -1600 ºС, т. е. степень перегрева < 10 %. При таких малых перегревах жидкость (в данном случае жидкая сталь) по некоторым свойствам оказывается ближе к твердому телу, чем к газу. Это обстоятельство (неполная разупорядоченность при переходе стали в расплавленное состояние) необходимо учитывать при рассмотрении проблем, связанных с технологией плавки и качеством металла. Используемые понятия и термины. В специальной литературе, освещающей проблемы строения жидких металлов, используют термины: статистическая теория жидкости, парный потенциал взаимодействия, функция радиального распределения атомов. Статистическая теория обосновывает взаимосвязь действующих на частицы сил и структуры. Частицы в жидких металлах — это катионы, окруженные электронным газом. Энергия взаимодействия двух частиц, находящихся одна от другой на расстоянии r, характеризуется величиной, называемой эффективным парным потенциалом взаимодействия и обозначаемой обычно Поскольку истинный вид парного потенциала взаимодействия определить достаточно сложно, в расчетах используют специальные модели. На рис. 10.1, а показан общий вид парного потенциала взаимодействия частиц (ионов) в жидких металлах, а на графике б приведен пример использования модели парного потенциала взаимодействия. Согласно этой модели, названной моделью жидкости твердых сфер: 1) частицы не могут быть сближены на расстояние, меньшее, чем а; 2) на некотором расстоянии r, равном эффективному диаметру частиц а (r=а), действуют большие силы отталкивания и В статистической теории жидкости используется также функция радиального распределения. Физический смысл этого понятия может быть объяснен следующим образом. Для одноатомной жидкости, не подвергаемой внешним воздействиям и обладающей одинаковыми во всех направлениях свойствами (изотропной), все положения любой ее частицы равновероятны. В такой жидкости распределение частиц относительно любой произвольно выбранной частицы сферически симметрично, а величина g, характеризующая интенсивность взаимодействия частиц, определяется только расстоянием rмежду частицами. Функцию g(r) называют радиальной функцией атомного распределения (или просто функцией радиального распределения) и определяют экспериментально методами рентгене-, электроне- и нейтронографии. Величина g(r) характеризует изменение вероятности обнаружения какой-либо частицы в сферическом слое на расстоянии г от частицы, выбранной за начало координат (в области вблизи начала координат вероятность нахождения другой частицы равна нулю). На определенном расстоянии от начала координат (обычно равном нескольким диаметрам частицы) все взаимные расположения частиц равновероятны, т. е. имеет место дальний порядок. Колебания значений функции g(r) вблизи начала координат свидетельствуют о наличии ближнего порядка. Если известны- потенциал межчастичного взаимодействия Модели строения жидкого металла. В настоящее время существует большое число модельных теорий строения жидкости. 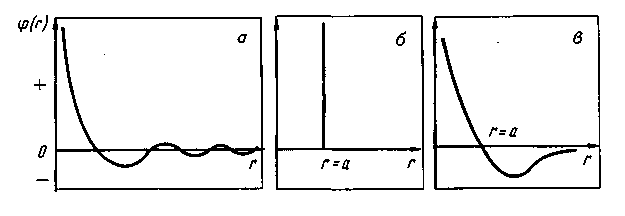 Рис. 10.1. Схематический вид эффективных парных потенциалов взаимодействия В 1924 г. советский ученый Я. И. Френкель один из первых, кто обратил внимание на то, что жидкие металлы при температурах, близких к температуре плавления, по многим характеристикам незначительно отличаются от кристаллических тел. При этом свободный объем жидкости, равный избытку объема по сравнению с объемом соответствующего твердого тела при абсолютном нуле, представлен отдельными микрополостями, вакантными узлами или «дырками». Модель получила название дырочная. В соответствии с этой моделью из-за наличия дырок степень порядка в расположении атомов в жидкости меньше, чем у кристалла. Наличием дырок объясняются большие текучесть, сжимаемость, термическое расширение и коэффициенты диффузии у жидкости. Упорядоченное расположение атомов имеется только вблизи каждой частицы (ближний порядок). В рамках дырочной теории тепловое движение в жидкости имеет такой же характер, как и в твердых телах, т. е. сводится в основном к гармоническим колебаниям частиц около некоторого среднего положения. Через какое-то (сколь угодно малое) время частица может занять новое положение, перескочив на расстояние, близкое к межатомному. В 1927 г. Стюарт и Морроу разработали модель строения жидкости, основанную на представлении о том, что при плавлении межмолекулярное взаимодействие в определенной степени сохраняется (по крайней мере, вплоть до достижения определенной критической степени перегрева). При этом допускается, что упорядоченное размещение частиц в жидкости не ограничивается непосредственно соседними частицами, а простирается на большие объемы, комплексы или группы (так называемый дальний порядок взаимного расположения частиц). Эти группы вначале были названы сиботаксисами'. Сиботаксисы не имеют резко очерченных границ; преимущественная ориентация молекул или атомов в сердцевине непрерывно сменяется беспорядочным расположением частиц в разделяющем сиботак1 Ковчег (греч.).сисы объеме; сиботаксисы непрерывно зарождаются и разрушаются. 1 Ковчег (греч.). В последние годы в технической литературе вместо термина «сиботак-сис» часто стали применять «кластер»2 (используют также термины «микрогруппировка», «группировка», «рой», «комплекс» и др.). Принято считать, что кластер (или сиботаксис, рой и т. п.) не может быть квалифицирован как представитель другой фазы; он не имеет физической границы раздела, при переходе через которую параметры состояния и свойства изменялись бы скачкообразно, и в то же время он характеризует структуру самой жидкости. Теория жидкого состояния до сих пор находится в стадии разработки, так как не ясны вопросы, связанные с определением продолжительности жизни кластеров, частотой их зарождения и распада, с определением соотношения объемов, занимаемых кластерами и разупорядоченной зоной, с определением степени перегрева, температуры, при которой наступает полное разупорядочение расплава. По некоторым данным, полное разупорядочение наступает при очень высоких перегревах (800-900 °С) над линией ликвидуса. Имеются и другие модели жидкостей. Следует отметить вклад в исследование- жидкого состояния стали ряда российских ученых: В. И. Данилова, Я. И. Френкеля, Н. А. Вато-лина, В. И. Явойского, П. В. Гельда, С. И. Попеля, Б. А. Баума, А. М. Самарина, А. А. Вертмана, П. П. Арсентьева, В. А. Григоряна, Г. Н. Еланского и др. |
