Инфекции. ИНФЕКЦИИ. В. В. Макаров, А. К. Петров, Д. А. Васильев основы учения
 Скачать 1.76 Mb. Скачать 1.76 Mb.
|
|
Ворота инфекции - первое, исходное патогенетическое звено локализации и развития инфекционного процесса, имеющее важнейшее эпизоотологическое значение. В анатомо-физиологическом смысле это ткани, органы и их системы, через которые происходит проникновение возбудителей в организм, во многом специфичные и не одинаковые. Они обеспечены механизмами биологической защиты, которые возбудителю приходится преодолевать, и именно успешное преодоление последних определяет дальнейшую судьбу инфекционного процесса. В общих случаях важнейшими и эффективными факторами, препятствующими проникновению, являются механическое напряжение неповрежденного слоя клеток на внешних и внутренних поверхностях организма, его регенерация изнутри наружу и секреция жидкостей, постоянно смывающих с этого слоя загрязняющие агенты. Кожа как механический барьер в неповрежденном виде обычно непроницаема для микробов, а отторжение высыхающих чешуек кератина освобождает ее поверхностный слой от контаминации. Кислотность пота и наличие жирных кислот в секрете сальных желез неблагоприятно действуют на бактерии. Сильным антибактериальным эффектом в отношении чужеродных бактерий обладает постоянная микрофлора нормальной кожи (главным образом, Staphylococcus sp). Вместе с тем через кожу при ее повреждениях или физиологической неполноценности происходит контактное заражение возбудителями многих инфекций с поверхностной локализацией (вирусы везикулярной болезни и оспы свиней, фузобактерии некробактериоза, возбудители раневых клостридиозов, актинобациллеза, дерматомикозов), а также осуществляется инокуляция возбудителей трансмиссивных, векторных системных кровяных и нейроинфекций инъекционным путем в результате укусов специфическим или механическим переносчиком (арбовирусные, протозойные инфекции и боррелиозы, болезнь Ауески и бешенство, инфекционная анемия лошадей, нодулярный дерматит и миксоматоз). Конъюнктива защищена механическим промыванием слезами и содержащимся в них лизоцимом. Сходный протективный эффект достигается в молочной железе за счет отделения молока и секретируемых с ним антител классов IgG и IgA (англ. Ig - универсальное обозначение молекулы иммуноглобулина). Для защиты мочеполового тракта столь же эффективно промывание мочой и образование микрофлорой влагалища (Lactobacillussp.) молочной кислоты - сильного ингибитора большинства чужеродных микробов. Успешное проникновение, приживление возбудителей и развитие локальных инфекций в этих системах возможно также, главным образом, при их анатомо-физиологической неполноценности (кератиты, конъюнктивиты, маститы стафилококковой и иной эндогенно-инфекционной природы), хотя существуют болезни со специфической передачей и первичным тропизмом возбудителей (риккетсиозный кератоконъюнктивит, пустулезный вульвовагинит, бруцеллез, эпидидимит баранов, случная болезнь). Важно отметить, что кожа, слизистые и другие поверхностные ткани, кроме ворот инфекции, являются местом локализации многих явлений инфекционно-аллергического характера. Органы пищеварения на исходном этапе защищаются слюноотделением и механическим промыванием ротовой полости, а продуцирующийся со слюной лизоцим является сильнейшим фактором антибактериальной защиты. Таким же эффектом обладают противоположно направленная способность желудка и кишечника изгонять нежелательные продукты с помощью рвоты или диареи, соляная кислота, гидролитические факторы желудка и тонкого отдела кишечника. Далее по ходу пищеварительного тракта защитные функции также выполняют иммунологические эффекторы секреторной защиты (прежде всего копроантитела класса IgA), продуцируемые плазматическими клетками слизистых оболочек кишечника, и колицины - вещества, вырабатываемые представителями нормальной кишечной микрофлоры, с сильным антибиотикоподобным действием на патогенные бактерии. Важным протективным элементом является быстрое обновление эпителиального покрова желудка и кишечника. Пищеварительный тракт животных служит воротами проникновения для возбудителей многих важнейших как локальных, так и генерализованных инфекций; в частности, у свиней, в виду особенностей их поведения, содержания и кормления, большинство инфекций передается именно алиментарным путем. Через органы пищеварения проникают патогенные микроорганизмы, как правило, устойчивые к неблагоприятным факторам внешней среды (с учетом фекально-оральной или кормовой передачи инфекции), не инактивирующиеся в кислой среде и в присутствии гидролитических ферментов, имеющие короткий цикл размножения. Алиментарный путь с типичной фекально-оральной передачей характерен для возбудителей острых кишечных и токси- коинфекций (энтеро-, корона-, ротавирусы, E. coli, сальмонеллы, иерсинии, энтеропатогенные клостридии). Алиментарное заражение происходит также при ряде генерализованных инфекций, возбудители которых в естественных условиях распространяются и передаются по типу кормовых или почвенных инфекций, проникая в циркулирующие системы из различных отделов желудочно-кишечного тракта (классическая чума свиней, колисептицемия, болезнь Тешена, листериоз, сибирская язва, лептоспирозы, рожа). Органы дыхания в числе прочих ворот инфекции являются наиболее уязвимыми, к чему предрасполагают их анатомо-физиологические особенности. С патогенетической точки зрения они принципиально делятся на два крупных отдела: • проводящие , или дыхательные пути , выстланные слизистой оболочкой, содержащие в стенках секретирующие слизь клетки, гладкие мышцы и отчасти хрящ, обладающие специальными системами для выведения частиц и местной системой образования антител класса IgA; • альвеолы , или дыхательная часть , участвующие в воздухообмене, где воздух контактирует с кровью и куда поступает весь сердечный выброс. Дыхательные пути вынужденно открыты для внешних воздействий, а легкие имеют огромную суммарную площадь, представляя собой самую большую поверхность организма, контактирующую с окружающей средой и выполняющую диффузионные функции [например, у человека общая площадь внутренней поверхности альвеол меняется между выдохом и вдохом от 40 до 120 м2 (для сравнения, площадь кожного покрова равна 1.5-2.3 м2)]. Проникновению возбудителей в организм способствуют значительные дыхательные объемы, особенно у крупных животных (например, у лошади массой 500 кг - 180 литров в минуту), задержка аэрозолированных капель и частиц пыли за счет присутствия волос в носовых ходах и слизи на всем протяжении респираторного тракта, разнообразие эпителиального покрова на разных участках и его восприимчивость ко многим вирусам и бактериям, наличие благоприятных условий для их приживления, колонизации и размножения (температура, pH, слизь), исключительно тонкий по условиям газообмена капиллярно-альвеолярный барьер между кровью и воздухом. В респираторном тракте выработаны различные механизмы защиты как проводящей, так и дыхательной ее части. Прежде всего крупно-дисперсные, взвешенные в воздухе загрязняющие агенты задерживаются в носу. Далее по ходу воздухоносных путей на слизистой оседают более мелкие частицы. Эти осевшие в носовой полости или более низких проводящих путях нежелательные субстанции удаляются навстречу друг другу в область глотки вдыханием или восходящим потоком слизи и откашливанием, где они проглатываются. Слизь, секретируемая бронхиальными слизистыми железами и бокаловидными клетками, поднимается вверх по бронхам к трахее за счет ритмичного «кнутообразного» движения многочисленных тонких ресничек (клеточных отростков реснитчатого эпителия бронхов) с частотой до 20 ударов в секунду. Избыточное накопление слизи стимулирует кашель. В секретах дыхательного тракта обычно присутствуют антитела класса IgA и лизоцим. Такое очищение нижней части воздухоносных путей называется слиземерцательным механизмом, или мукоцилиарным клиренсом. Работа ресничек бронхиального эпителия исключительно эффективна, хотя некоторые вдыхаемые токсины и агрессивные субстанции (аммиак, табачный дым) могут существенно угнетать и даже парализовать их активность (рисунок 2). Сканирующая электронная микроскопия 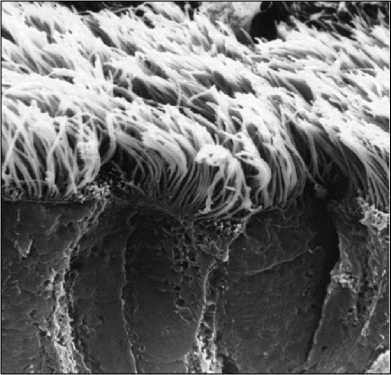 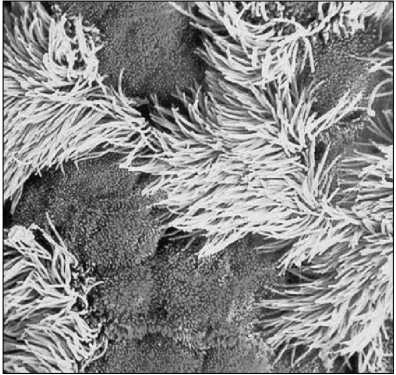 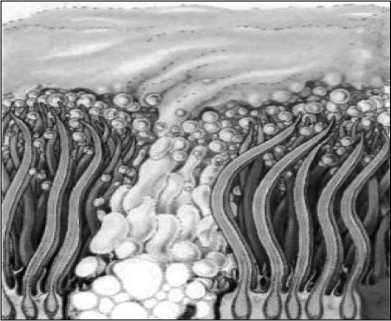     Ворсинки и покрывающий их слой слизи (схема) Бактерии среди ворсинок Рисунок 2. Бронхиальный мерцательный эпителий [Internet]. В альвеолах - дыхательном отделе системы слиземерцательный механизм отсутствует и в норме воздухообменная часть респираторного тракта должна быть стерильна. Достигшие этого уровня микроорганизмы и другие частицы поглощаются легочными макрофагами. Они в большинстве своем изгоняются вверх в мокроту, в область глотки и проглатываются либо удаляются через лимфатические и кровеносные сосуды. В последнем случае облегчается проникновение патогенных агентов в циркулирующие системы с последующим развитием генерализованной инфекции. Респираторный тракт животных служит воротами инфекции при многих важнейших болезнях, особенно у КРС и птицы при концентрации поголовья в хозяйствах промышленного типа. Одним из условий приживления и размножения здесь патогенных микроорганизмов служит наличие у них рецепторного сродства или иного аффинитета к гликопротеинам, или мукополисахаридам слизи [что нашло отражение в наименовании ортомиксо-, парамиксовирусов, микобактерий (от лат. myxo - слизь)]. Аэрогенным путем передаются возбудители локальных респираторных инфекций (рино-, рео-, адено-, корона-, герпесвирусы), генерализованных инфекций с преимущественной локализацией первичного и вторичного процессов в различных отделах респираторного тракта (вирусы парагриппа, инфекционного ринотрахеита, ньюкаслской болезни, инфекционного ларинготрахеита, оспы кур), генерализованных инфекций с проникновением возбудителей в циркулирующие системы «напрямую» через легочные макрофаги глубоких отделов (вирусы оспы овец, чумы КРС, чумы плотоядных, пастереллы, микобактерии). Аэрогенной трансмиссии способствуют особенности инфекционных процессов и патогенеза при различных инфекциях животных, обусловливающие экскрецию патогенных микроорганизмов в воздух и пребывание их в состоянии аэрозолей. Больные животные с поражениями респираторных органов и ротовой полости как источники инфекции при дыхании, кашле, особенно чихании, со слюной выделяют громадное количество возбудителя, который длительное время может сохранятся во взвешенном состоянии и распространяться на значительные расстояния [например, в крупном птичнике при сильном поражении птицы ньюкаслской болезнью выделяется и разносится ветром 10 млрд инфекционных частиц вируса в час (Dawson, 1973)]. Капельные или пылевые частицы аэрозоля, попадая в органы дыхания, в зависимости от их размера задерживаются в разных отделах. Капельки более 5 мкм задерживаются в проводящей части, в то время как частицы менее 1 мкм проникают глубоко и оседают в дыхательной области. Коэффициент задержки аэрозоля очень высок и составляет, например, для частиц размером 3-5 мкм 80 %, для частиц 0.5 мкм - 50 % (Огарков В.И. и др., 1975). Носоглотка и миндалины в качестве ворот инфекции имеют особое значение в силу своего промежуточного положения. Взаимно противоположное направление клиренса верхних и нижних дыхательных путей в сторону этой анатомической области обусловливает наибольшую подверженность инфицированию ее тканей, которые высокочувствительны к патогенным микроорганизмам самой различной природы (вирусам ящура, классической и африканской чумы свиней, стафилококкам, стрептококкам). Миндалины - большие скопления лимфоидной ткани в виде кольца вокруг отверстий пищеварительного и дыхательного трактов - выполняют физиологические функции своеобразного индикатора внешнего антигенного окружения организма. При оро-на- зальном заражении здесь происходит не только первичное приживление, но и персистирование возбудителей в период скрытой инфекции и носительства. Плацента в самом общем представлении служит естественным анатомическим барьером для защиты плода от проникновения нежелательных агентов различной природы, даже структур молекулярного уровня организации, в частности, материнских антител. Однако трансплацентарное заражение (трансовариальное у птиц, а также через зародышевые клетки у млекопитающих) как механизм вертикальной передачи инфекции - важное эпизоотологическое явление, характерное для целого ряда возбудителей в качестве основного способа трансмиссии (парвовирус свиней, вирусы лейкозов и лейкемий) или достаточно эффективного факультативного пути передачи патогена (пестивиру- сы классической чумы свиней, диареи и «пограничной» болезни, орбивирусы блутанга и болезни Акабане, листерии). Частные механизмы и процессы вертикальной передачи и становления врожденной (конгенитальной) инфекции в большинстве случаев не выяснены, однако персистентно инфицированные трофобласты плаценты, макрофаги и механизм «троянского коня» (см. ниже) вместе с повреждениями плацентарного барьера различной этиологии могут быть одними из ведущих факторов ее реализации. Циркулирующие системы организма - второе патогенетическое звено в локализации и развития инфекционного процесса. Под циркулирующими системами подразумеваются ткани и органы, в силу своего физиологического назначения диффузно распределенные по всему организму и способные к внутриорганизменному распространению разнообразных субстанций и агентов, в том числе патогенных (возбудителей, токсинов, медиаторов). Поэтому к ним относятся не только кровеносная и лимфатическая, но и периферическая нервная системы [участие последней характерно для передачи нейровирус- ных инфекций, в частности, вирусов бешенства и герпесвирусов (например, болезни Ауески)]. Распространение возбудителей по организму из локальных очагов инфекции, или их диссеминация - важнейший механизм генерализации инфекционного процесса и развития системных инфекций. Основной формой внутриорганизменной циркуляции возбудителей, а также факторов патогенности и иных растворимых продуктов инфекционного процесса, является бактериемия и вирусемия (микробиемия), токсемия, ан- тигенемия. В соответствии со способом проникновения в кровь бактерий и вирусов природа бактериемии и вирусемии может быть двоякой. Непосредственное попадание их в организм иньекционным способом обусловливает процесс прямого порядка и диссеминацию возбудителя, поступившего извне (при трансмиссивных инфекциях), в то время как проникновение в кровь после изначального местного приживления в воротах инфекции опосредовано размножением возбудителя внутри, в условиях инфицированного организма (как при локальных, так и генерализованных инфекциях с различной передачей). В период пребывания в кровяном русле бактерии и вирусы связываются с форменными элементами крови или остаются в плазме. Связь с клетками крови способствует их выносу из кровяного русла при диапедезе в небольших сосудах и развитию экстраваскулярных очагов инфекции. Циркуляция патогенных микроорганизмов по отношению к органу-мишени имеет характер центростремительного, первичного распространения, а к уже активному очагу инфекции - центробежного, вторичного. При острых инфекциях первичное появление возбудителя в крови, независимо от его внешнего или внутреннего происхождения, как правило, отличается низким уровнем, весьма скоротечно, происходит в инкубационном периоде и хронологически совпадает с первым пиком острой лихорадочной реакции. Возбудители острых инфекций обычно имеют короткие циклы размножения, быстро обеспечивают диссеминацию и достижение соответствующих органов-мишеней. При генерализованных и системных инфекционных процессах, хронической или персистентной инфекции вторичное поступление возбудителя в кровь, периодическое или постоянное, и центробежное распространение происходят вследствие его интенсивного размножения в очагах инфекции и выхода оттуда, что совпадает уже с развитием манифестной формы и повторными пиками лихорадочной реакции. Вторичная бактериемия и вирусемия в периоды обострения хронических процессов обусловливает также возможность экскреции возбудителя и период заразительности. Именно вторичные бактериемия или вирусемия лежат в основе патогенетических явлений ремитирующего течения ряда хронических инфекций (туберкулез, бруцеллез, инфекционная анемия лошадей). Орган-мишень - третье важнейшее звено патогенеза. Это определение означает органы в самом широком смысле, в зависимости от уровня их участия в инфекционном процессе (включая клетки и ткани), к которым у патогенного микроорганизма существует тропизм. Как для облигатных, так и прочих патогенов, инвазирующих организм и распространяющихся по его циркулирующим системам, существует вполне определенная закономерность относительно их дальнейшего существования - свободного в тех же циркулирующих системах и межклеточных пространствах либо внутриклеточного. Для внеклеточных возбудителей вызываемые ими патологические процессы, как правило, не являются топически (и клинически) закономерными; они характеризуются сепсисом, гранулемами, абсцессами, что определятся особенностями взаимодействия патогенов с организмом хозяина и реакциями на их проникновение и размножение, в основном, воспалительного, т.е. общего порядка. Такие явления обычны для генерализованных (системных) инфекций, вызываемых патогенными сапрофитами или факультативными паразитами, оппортунистических, почвенных инфекций, некоторых микозов и протозоозов. Вместе с тем для большинства инфекционных болезней характерна локализация инфекционного процесса, основанная на тропизме возбудителя к клеткам, тканям органов или систем организма, определяющем их мишеневое назначение при той или иной инфекции, строго определенная, обусловливающая клинически типичное их проявление. Именно этим отличаются инфекции, относящиеся к категории локальных (кишечные, респираторные, кожные и т.п.), и некоторые раневые . Предпочтение возбудителем тех или иных клеток и тканей - сложное явление патобиологического порядка, отражающее прежде всего эволюционно сложившиеся адаптации конкретного микроорганизма к своему оригинальному типу циркуляции и кругооборота в соответствии с универсальным биосистемным принципом биологического узнавания. В качестве исходного этапа в основе этого лежит его тропизм, или избирательная локализация в тех условиях, которые в оптимальной степени отвечают потребностям возбудителя (аффинитет поверхностных структур и клеточные рецепторы для адсорбции, приживления и колонизации, питательные субстанции и иные требуемые для его жизни факторы). Природа специфического узнавания возбуДитель мишень на клеточном уровне хорошо изучена при многих инфекциях, особенно кишечных и респираторных, для энтеро- и пневмопатогенных бактерий и вирусов. Бактерии, вирусы, токсины проявляют способности химического паразитизма (по Румянцеву С. Н., 1983) и реагируют с клеточными рецепторами, осуществляющими в норме функции рецепторов для гормонов и иных обычных сигнальных или пластических субстанций (например, никотин-ацетилхолиновые синаптические рецепторы миоцитов и нервных клеток для вируса бешенства, см. ниже). Для патогенеза большинства инфекционных болезней характерно, что патогенные микроорганизмы разных систематических групп, с различной физиологией (от простейших до вирусов) реализуют свой биологический потенциал именно на клеточном уровне. Внутриклеточная среда в условиях организма является основным местом развития инфекционных процессов, вызываемых живыми патогенами (Петровская В. Г., 1967), а внутриклеточный паразитизм - основной формой их существования. Это относится не только к облигатным внутриклеточным паразитам (вирусам, хламидиям, риккетсиям, некоторым простейшим), но и многим патогенным бактериям (таблица 5). Патогенные микроорганизмы в процессе преодоления протективных механизмов ворот инфекции, проникновения внутрь организма, диссеминации или по достижении органа-мишени в тканевом пространстве встречаются прежде всего с «профессиональными» фагоцитами - свободно перемещающимися по организму крупными отростчатыми специализированными полиморфно- или мононуклеарными клетками, очень сходными со свободно живущими простейшими в своем активном поведении и функциях. Именно с основным отличительным свойством фагоцитов - способностью активно поглощать микроорганизмы и иные чужеродные частицы, связан внутриклеточный паразитизм с их участием как явление обратного порядка. В патогенетическом смысле важно, что именно макрофаги служат клетками-мишенями во многих случаях внутриклеточной инфекции, хотя эту роль могут выполнять и другие клеточные элементы (разные типы клеток для вирусов, энтероциты для шигелл и сальмонелл, лимфоциты для тейлерий, эритроциты для плазмодиев). На этом патобиологическом уровне инфекции феномен внутриклеточного паразитизма включает и «непаразитические» патогенные микроорганизмы - возбудителей сапронозов и оппортунистических инфекций (листерии, легионеллы, дрожжи). Внутриклеточные патогены в целом хорошо адаптированы к переживанию и размножению в клетках. Хотя внутриклеточная среда представляет собой для паразита экстремальные условия (Дж. Моулдер, 1965), здесь создаются исключительные выгоды для его существования: • обеспечены метаболические, энергетические и генетические потребности; • возбудители защищены от действия иммунных механизмов и иных факторов (фагоцитоза, антител, бактериофагов, антибиотиков); • размножение идет по упрощенному циклу (например, у вирусов, диморфных грибов). Это же относится и к персистенции патогенных микроорганизмов в макрофагах; в частности, в нестимулированных макрофагах размножаются и персистируют микобактерии туберкулеза, бруцеллы, листерии, различные вирусы (см. таблицу 5). Чувствительность макрофагов генетически детерминирована и, как правило, определяет восприимчивость к инфекционным болезням. Например, вирус африканской чумы свиней размножается только в свиных макрофагах, но не в макрофагах человека, кролика, мыши и других видов животных (Enjuanes, 1977). В целом для возбудителей такого рода характерна корреляция между степенью резистентности к ним макрофагов и восприимчивостью животных. Ими выработаны специальные механизмы, позволяющие избегать антимикробного действия факторов завершенного фагоцитоза (таблица 6). При этом внутримакрофагальная локализация, сохранение и размножение возбудителей способствуют их беспрепятственной повсеместной диссемина- ции вместе со свободно мигрирующими по организму макрофагами, что имеет исключительное значение в развитии экстенсивной патологии, характерной для многих генерализованных инфекций; этот патогенетический феномен получил название механизма «троянского коня» (по Mims, 1978). Именно с его помощью происходит заражение так называемых забарьерных органов - плода, мозга, суставов при листериозе, маеди-висне, бруцеллезе (см. ниже). |
