Инфекции. ИНФЕКЦИИ. В. В. Макаров, А. К. Петров, Д. А. Васильев основы учения
 Скачать 1.76 Mb. Скачать 1.76 Mb.
|
|
Рисунок 5. Ящур и противоящурная вакцинация в Западной Европе в середине 20 в. - канонический пример эффективности тотальной систематической вакцинации в контроле эпизоотических инфекций. це»), особенно у молодых животных]. В 1965 г. в стране возник и получил повсеместное распространение ящур типа А22 (первоначально А «Иранский»). Новая инфекция в течение двух лет практически беспрепятственно иррадиировала из точки заноса и первичного возникновения, распространилась по территории всей страны, включая Сибирь, нанеся беспрецедентный ущерб экономике. Во многом вследствие этого началось отечественное промышленное производство противоящурных вакцин по прогрессивной технологии и успешная реализация европейской стратегии систематической вакцинации по всей стране (с отставанием на 10-15 лет) с тем же результатом. Эпизоотии ящура были взяты под контроль, продолжалась регистрация лишь эпизодических вспышек остаточного ящура типов О и А22 по южной периферии, в регионах Средней Азии и Закавказья. Однако в Западной Европе 25-летнее управление инфекцией этим путем так и не позволило полностью искоренить ящур. Поэтому в середине 1980 гг. была согласована и принята новая противоящурная концепция - «эрадика- ция против вакцинации», позволившая достичь желаемого благополучия. Суть новой противоящурной стратегии заключается в отмене повсеместной вакцинации и соблюдении жестких, гарантированных мер санитарной профилактики и предупреждения заноса инфекции, создании путем фронтальной вакцинации иммунного барьера в особо угрожаемых зонах (в основном, на Балканах, граничащих с эндемичной по ящуру Турцией), в случаях возникновения эмерджентных вспышек - их радикальное искоренение (стемпинг-аут) и, при необходимости, кольцевая вакцинация животных близлежащей зоны. В СССР и России длительное успешное управление инфекцией с помощью систематической вакцинации и результаты основательного долгосрочного научного мониторинга эпизоотической ситуации также сделали возможной постановку вопроса о принципиальной смене противоящурных мероприятий. В 1996-1999 гг. реализован переход к новой противоящурной стратегии, сходной с таковой в Западной Европе (А.А. Гусев, В.М. Захаров). Положенный в ее основу зональный принцип позволил выделить на территории РФ регионы с очень высокой и высокой степенью риска возникновения ящура (Северный Кавказ, юг Поволжья, пограничные с Китаем районы Сибири и Дальнего Востока). В этих зонах, составляющих 6% территории страны, содержалось около 18% крупного и 20% мелкого рогатого скота от общероссийского поголовья. Именно до размеров этой зоны сокращена применяемая до этого в течение многих лет повсеместная систематическая вакцинация в масштабах всей страны, что по своей сути представляет фронтальную вакцинацию с целью создания иммунного барьера в угрожаемых зонах. Это беспрецедентное в истории отечественной ветеринарии мероприятие привело к значительному повышению экономической эффективности противоящурных мероприятий (контроль ящура в России теперь обходится в 500 тысяч $ в год). В случаях возникновения эмерджентных вспышек экзогенного ящура проводится ликвидация первичных очагов (стемпинг-аут) и кольцевая вакцинация вокруг них (рисунок 6). 60 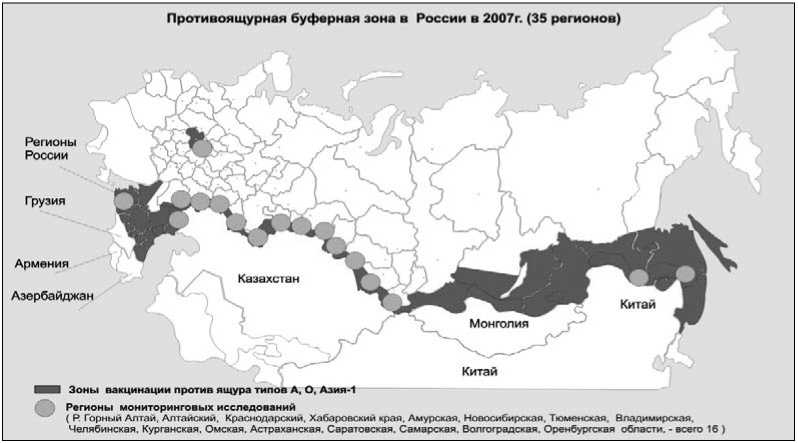 Рисунок 6. Реализация новой стратегии борьбы с ящуром в РФ. Контрольные вопросы. Приведите правильное определение ящура как нозологической формы. Приведите характеристику вируса ящура. В чем его основные эпизоотологические особенности? Опишите краткую историю и основные особенности эпизоотологии ящура. Чем характеризовался стратегический прогресс борьбы с ящуром в Западной Европе и впоследствии в СССР и РФ во второй половине 20 века? Какова текущая эпизоотическая обстановка по ящуру в мире? Опишите кратко современный нозоареал инфекции. Какие животные восприимчивы к ящуру? В чем эпизоотологическое и клиническое различие восприимчивых животных разных видов? Как происходит заражение животных и территориальное распространение ящура? Что служит преимущественным источником инфекции при ящуре? Опишите патогенез и симптоматологию ящура. Какие клинико-эпизоотологические признаки ящура имеют диагностическое значение? Почему важна дифференциальная диагностика ящура? Какие методы применяются для идентификации вируса ящура и какие серологические тесты для определения антител? Какова роль международной торговли и других межгосударственных связей в территориальном распространении ящура? Каковы современная тактика и стратегия контроля ящура в РФ? «Чуме все возрасты покорны». Шутка эпизоотологов. АФРИКАНСКАЯ ЧУМА СВИНЕЙ Африканская чума свиней (АЧС, African Swine Fever, ASF) - контагиозная генерализованная инфекция свиней, характеризующаяся выраженной вариабельностью вирулентности различных изолятов вируса и высокой его устойчивостью к физическим и химическим факторам инактивации. При остром течении болезнь патогенетически и клинически проявляется как геморрагическая лихорадка. В условиях длительной энзоотии возможны подострое и хроническое течение. Смертность в первичных случаях, при возникновении на неэнзоотичных территориях, обычно достигает 100 % безотносительно к возрасту поражаемых животных. АЧС, относящаяся на данном этапе к категории наиболее важных трансграничных инфекций с катастрофическим потенциалом, - одна из самых серьезных проблем эпизоотологии в виду способности к возникновению и эпизоотическому распространению в самых неожиданных регионах мира, чрезвычайно большого прямого и особенно непрямого ущерба (высокой летальности восприимчивых животных, расходов на различные ограничительные меры и искоренение, соответственно), невозможности специфической профилактики. Возбудитель. Вирус рода Asfirvirus - единственный член семейства Asfarviridae. Это представитель группы крупных ядерно-цитоплазматических дезоксирибовирусов, принадлежность к которой объясняет его своеобразие по целому ряду важных естественно-исторических, таксономических, патогенетических и иммунологических свойств. Существует до десяти иммунологических типов и более 20 генотипов. Вирус АЧС устойчив в экстремальном диапазоне pH от < 1.9 до > 13.4, резистентен к протеолитическим ферментам и нуклеазам, не инактивируется при созревании мяса, трупном окоченении и аутолизе трупа. Длительно сохраняется при низких температурах (6 лет при 5о в темноте), в крови, фекалиях и тканях (при комнатной температуре в сыворотке до полутора лет, в фекалиях более 10 дней). В полевых условиях вирус устойчив к гниению, сохраняется в различных выделениях больных свиней - крови, истечениях, сгустках и т.п. В свином навозе вирус остается инфекционным от 60 до 100 дней. Органические материалы и биологические жидкости организма значительно повышают резистентность вируса (например, при pH 13.4 без сыворотки вирус сохраняется 21 час, а в присутствии сыворотки - 7 дней). Вирус инактивируется при 56°C за 70 мин., при 60°C - 20 мин., растворами едкого натра (0.8%, 30 мин.), гипохлорита (2.3% активного хлора, 30 мин.), формалина (0.3%, 30 мин.), ортофенилфенола (3%, 30 мин.) и иодсодержащими препаратами. Может размножаться, сохраняться, накапливаться в одушевленных векторах - аргасовых клещах рода Ornithodoros и распространяться ими. Эпизоотологические данные. Болезнь известна с начала 20 в., с первых попыток интродукции свиней культурных пород в колониальные страны юго-восточной Африки (R.Mont- gomery, 1921). На первом этапе естественной истории, до выноса в Португалию (1957) и Испанию (1960), АЧС имела стереотип типичной природно-очаговой экзотической болезни с естественной циркуляцией вируса в популяциях диких африканских свиней, внутрисемейной трансмиссивной передачей клещами O. moubata, течением в виде персистентной толерантной инфекции. При возникновении первых случаев антропургического цикла на домашних (неаборигенных) свиньях инфекция приобретала острое течение с высокой летальностью. На последующих этапах естественной истории АЧС эволюционировала в сторону самостоятельного антропургического цикла с передачей «от свиньи к свинье» и укоренением в южно-европейских странах, двукратным эмерджентным заносом и распространением в странах Центральной и Южной Америки (1971 и 1978-1983). Важнейшей эпизоотологической особенностью («коварством») АЧС явилось чрезвычайно быстрое изменение форм течения инфекции среди домашних свиней от острого с летальным исходом до хронического и бессимптомного носительства и непредсказуемого распространения. Распространение АЧС во второй половине 1970 гг. имело глобальный характер со всеми признаками пандемии. Эпизоотическая ситуация в традиционном нозоареале субсахарной Африки оставалась на уровне гиперэнзоотии. Неблагополучными, помимо энзоотичной зоны Перинейского полуострова с возрастающей напряженностью, оказались Куба (1971, 1980 гг.), СССР (1977), Италия, (1978), Мальта (1978-1979), Гаити, Бразилия (1978-1984), Франция (1984), Бельгия (1985), Голландия (1986). В результате предпринятых беспрецедентных мер усилиями международных организаций и фондов Евросоюза и стран Центральной Америки вспышки, эпизоотии, энзоотии АЧС в этих регионах были ликвидированы путем применения жесткой радикальной тактики (поголовный систематический мониторинг, стемпинг аут вплоть до депопуляции в масштабах государств). Особенно показателен успех быстрого искоренения АЧС в 1977 г. в трех областях СССР, а также, после полувекового неблагополучия, в Испании и Португалии в период 1985-1995 гг., с высокой противоэпизоотической и экономической эффективностью. В начале 21 в. АЧС оставалась эндемичной для субэкваториальной части африканского контингента, вне Африки неблагополучной оставалась только Италия (о. Сардиния). АЧС в 2007 г. появилась в Грузии, распространилась по всей республике и в виде эпизоотических вспышек - в сопредельных странах и регионах [Армения, Азербайджан, Абхазия, Нагорный Карабах, РФ (Чечня, Северная Осетия), север Ирана], что подтвердило исключительное значение болезни на современном этапе. До 2012-2014 гг. на территории европейской части РФ в результате прогрессирующего эпизоотического распространения сформировалась масштабная энзоотия с заносом инфекции в сопредельные страны Восточной Европы (Белоруссия, Польша, Прибалтика, Украина, Молдавия) (рисунок 7). Восприимчивы к АЧС только представители семейства Suidae. Домашние свиньи всех пород и возрастов и европейские кабаны при естественной инфекции и искусственном заражении чрезвычайно чувствительны. Контаги- озность и летальность в первичных эпизоотических очагах достигает 100%. В энзоотичных зонах эти показатели в ходе быстрой эволюции болезни существенно снижаются вплоть до преобладания бессимптомного носительства (персистентной инфекции). Африканские дикие свиньи (бородавочники, кустарниковые) в природных очагах традиционного нозоареала в подавляющем большинстве инфицированы инаппарантно. Источниками инфекции в передаче АЧС служат свиньи-носители в энзо- отичных зонах, особенно африканские дикие свиньи, а также кровь, ткани, секреты, экскреты больных и павших животных. Внутри организма больных свиней общая инфекционность туши превышает 1013 (!) инфицирующих единиц (ИЕ) вируса. 96 % ее аккумулируется в костном мозге, который составляет до 10% массы туши. Один грамм крови, мышечной ткани, лимфоузлов, костного мозга (что идет в отходы прежде всего) содержит от 108 до 109.5 ИЕ вируса (т.е. при самом общем пересчете одна капля крови содержит сотни тысяч инфицирующих доз). Все это обусловливает «приоритетную» роль в распространении АЧС мяса инфицированных свиней, консервируемого и неизбежно попадающего затем в пищевые отходы. Передача инфекции в пределах пораженной группировки свиней происходит путем прямого контакта больных со здоровыми или через разнообразные контаминированные объекты, вовлекаемые в процессы свиноводства (инфицированные помещения, кормушки, поилки, инвентарь, одежда и т.п.). В межхозяйственные контакты и непрямую передачу вовлекаются разнообразные перевозки и транспорт, персонал, посетители. Абсолютно преобладающим фактором возникновения новых случаев АЧС, заноса и распространения инфекции безотносительно к расстояниям, включая межгосударственные и межконтинентальные масштабы, являются необезвреженные пищевые отходы, содержащие инфицированные продукты свиного происхождения (основной источник доступного кормления свиней в личных подсобных хозяйствах). Этому способствуют традиционные во всем мире способы консервирования и потребления свинины, предполагающие посол, копчение, вяление и иные способы сохранения качества продуктов без стерилизующей термической об- 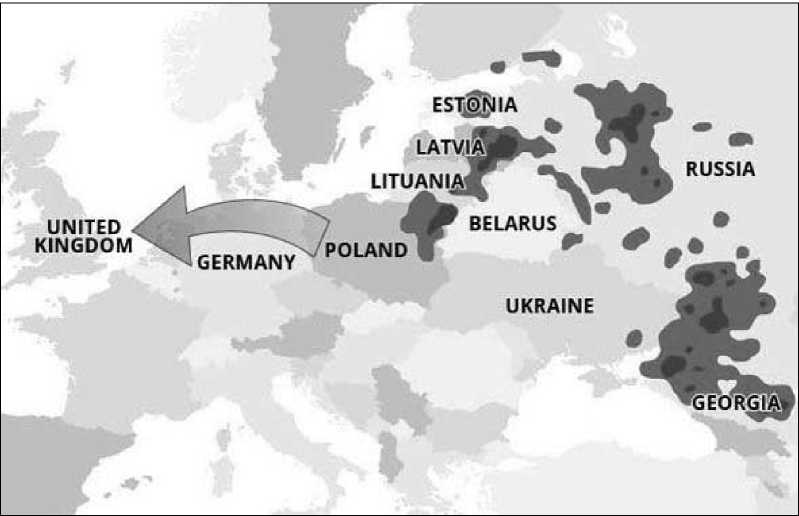 Рисунок 7. АЧС на территории стран Восточной Европы в 2012-2014 гг. и прогнозируемый вектор дальнейшего распространения [фото express.co.uk/news]. работки; при этом, одновременно с сохранением их потребительских качеств, происходит консервирование инфекционного вируса. Вирус АЧС, как единственный ДНК-содержащий арбовирус, способен к трансмиссии биологическими векторами - только аргасовыми (мягкими, беспанцырными) клещами рода Ornithodoros с прохождением полного инфекционного двуххозяинного цикла и формированием трехчленной паразитарной системы. Аргасовые клещи-орнитодорины распро странены всесветно, в пределах ареала связаны с пустынными и полупустынными ландшафтами, в меньшей степени - степными. Поэтому подобная трансмиссивность АЧС эпизоотологически важна и реальна лишь в регионах с жарким климатом, кле- щи-орнитодорины в Палеарктической зоне обитают южнее 47° северной широты (в РФ до Ростовской и юга Волгоградской областей). Патогенез. АЧС - типичная кормовая инфекция. Инфекционный цикл включает алиментарное заражение, которое при ороназальной экспозиции вируса достигается при очень небольших его дозах (10-100 ИЕ). В области миндалин вирус, в силу своих крупных размеров, поглощается мононуклеарными фагоцитами, которые являются в организме свиньи единственными спонтанно чувствительными клетками-мишенями, проникает в локальные лимфоузлы. Далее следует персистентная вирусемия по типу сепсиса с развитием экстенсивной патологии: ранняя лейкопения и тромбоцитопения (через 48-72 часа), коагулопатия, низкая свертываемость крови и, как следствие, тяжелый геморрагический синдром с кровоизлияниями в паренхиматозных органах, эпителиальной ткани, стенках сосудов. Особая роль в патогенезе принадлежит застойной спленомегалии (увеличенная в объеме в 2-4 раза, густого темного цвета, с раздавливающейся пульпой), что служит патогномоничным признаком острой АЧС. Селезенка, как орган-депо крови, в этих условиях способна необратимо вывести из обращения до 30% и более кровяного объема; такая кровопотеря уже несовместима с жизнью животного и является одной из наиболее вероятных причин смерти. Вирус выделяется с секретами, экскретами, кровью за 2 дня до клинического проявления и в течение 30 и более дней (в зависимости от вирулентности и формы течения болезни). Таким образом вирусоносители длительно поддерживают циркуляцию инфекции в группировках домашних и диких свиней. Симптомы. При острой форме течения АЧС (высоковирулентный вирус) инкубационный период составляет 5-15 дней (в среднем 4-7). Клинические признаки - лихорадка (40.5-420 C), покраснение кожи (у белых свиней - концы ушей, хвост, задние конечности, вентральная поверхность грудной клетки и живота), отказ от корма, вялость, цианоз и некоординированные движения за 24-48 час до смерти, повышение частоты пульса и дыхания, рвота, диарея (иногда кровавая), выделения из глаз, смерть через 6-13 дней (возможно более 20 дней), возможные аборты у супоросных свиней, летальный исход до 100% (у домашних свиней) (рисунок 8/1, 2, 3). Выздоровевшие животные остаются пожизненными носителями. При подострой форме (умеренно вирулентный вирус) - меньшая интенсивность симптомов, продолжительность болезни до 30 дней, аборты у супоросных свиней, смерть через 15-45 дней, более низкая смертность (30-70%, большая вариабельность). При хронической форме - различные экстенсивные признаки: потеря веса, нерегулярные подъемы температуры, респираторные симптомы, некрозы кожи, хронические кожные язвы, артриты, опухание суставов, продолжительность течения 2-15 мес., низкая смертность. Патоморфологические изменения. При острой форме течения - выраженные кровоизлияния в гепато-гастраль- ных и почечных лимфоузлах, точечные кровоизлияния (петехии) в корковом слое почек, в мозговом веществе и почечных лоханках, застойная спленомегалия (рисунок 8/4, 5, 6), отечность и цианоз бесшерстных участков, кровоподтеки на коже окороков и живота, избыток плевральной, перикардиальной и/или перитонеальной жидкости, петехии в слизистой оболочке глотки, мочевого пузыря и висцеральной поверхности органов, отеки мезентериальных 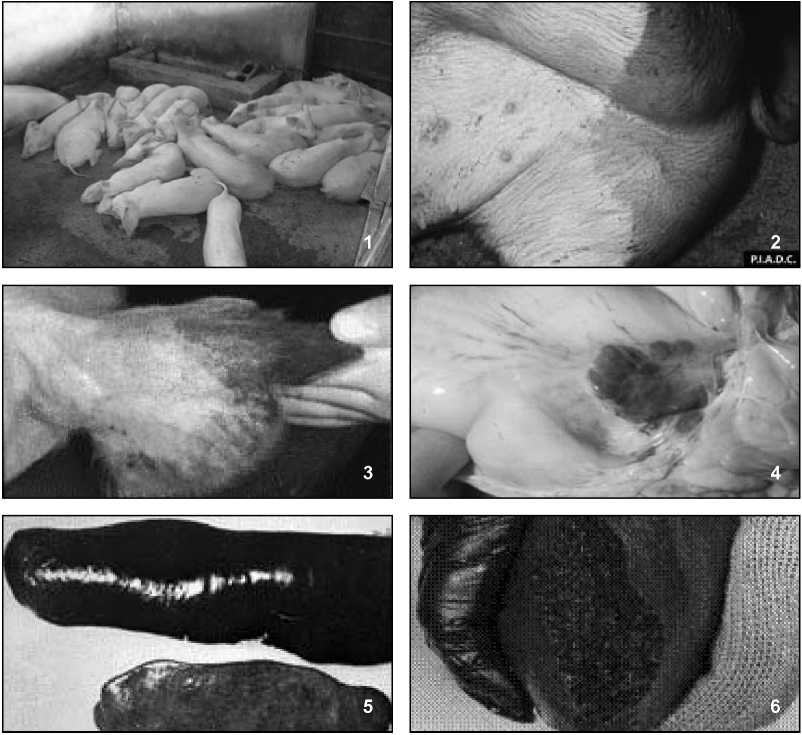 Рисунок 8. Некоторые типичные признаки острой АЧС: 1 - горячие, больные, красные свиньи, 2, 3 - геморрагии наружных покровов, 4 - геморрагичные гепато-гастральные лимфоузлы, 5 - селезенки при АЧС (вверху) и КЧС (внизу), 6 - спленомегалия (фото PIADC). структур толстого кишечника, примыкающей части и стенок желчного пузыря. В зависимости от изолята вируса не все поражения могут быть выражены в равной степени. В числе прочих основными являются три признака: сильное увеличение и окрашивание от темно-красного до черного цвета рыхлой, крошащейся селезенки, увеличение гепато-гастральных лимфоузлов, увеличение и геморрагии почечных лимфоузлов. При хронической форме - перикардит, спадение легких, возможны фокальный казеозный некроз и минерализация легких, увеличение лимфатических узлов. Диагностика. АЧС клинически и патоморфологически сходна с инфекциями свиней, сопровождающимися развитием геморрагического синдрома. Поэтому первостепенной является дифференциальная диагностика прежде всего от классической чумы свиней - клиническим и постмортальным исследованием АЧС и КЧС неразличимы. АЧС необходимо дифференцировать также от репродуктивного и респираторного синдрома свиней, рожи, пастереллеза, сальмонеллеза, всех септицемических состояний. Решающее значение имеет получение образцов патологического материала и лабораторный анализ. Лабораторная диагностика предполагает отбор в качестве специмен- тов для выделения вируса проб крови, взятых на ранней лихорадочной стадии болезни, в растворе гепарина (10 МЕ/мл) или ЭДТА (0.5%), небольших фрагментов (2-5 г) селезенки, почек и лимфоузлов, хранящихся при 40С. Для серологических исследований - сывороток крови выздоровевших животных, полученных на 8-21 дни после заражения. Выделение и идентификацию вируса проводят инокуляцией первичной культуры свиных моноцитов/макрофагов или клеток костного мозга (большинство изолятов вируса вызывает гемадсорбцию), заражением свиней невак- цинированных и вакцинированных против КЧС (специфическая биопроба), определением антигена методом прямой иммунофлюоресценции, вирусного генома - с помощью ПЦР. В качестве серологических тестов используют выявление группоспецифических (общих) антигенов с помощью иммунофер- ментного анализа и реакции непрямой иммунофлюоресценции, методы им- муноблотинга и иммуноэлектрофореза, серотипизацию изолятов - в реакции задержки гемадсорбции. «Золотой стандарт» в диагностике АЧС - реакция гемадсорбции, метод прямой иммунофлюоресценции и ПЦР. В РФ разработаны и эффективно применяются на практике средства и методы лабораторной диагностики, регламентируемой ГОСТ'ом 28573-90 «Свиньи. Методы лабораторной диагностики африканской чумы». |
