Инфекции. ИНФЕКЦИИ. В. В. Макаров, А. К. Петров, Д. А. Васильев основы учения
 Скачать 1.76 Mb. Скачать 1.76 Mb.
|
|
Контрольные вопросы. В чем заключается особая значимость бешенства/гидрофобии как инфекционной болезни? Какие животные восприимчивы к бешенству? Каков механизм заражения бешенством? Опишите два экотипа бешенства. Чем характеризуется бешенство природно-очагового экотипа? Какие типы эпизоотических цепей реализуются при бешенстве? Каково проявление эпизоотического процесса при бешенстве? Какие животные являются источниками инфекции при бешенстве разных экотипов? Каким путем происходит распространение вируса бешенства в инфицированном организме? Есть ли при бешенстве вирусемия? Почему при бешенстве не происходит иммунного ответа? Каковы возможности предупреждения бешенства у человека, укушенного больной собакой или лисой? Опишите основные симптомы бешенства классического и природно-очагового экотипов. По каким внешним признакам можно предполагать бешенство лисицы? Что такое тельца Негри? Назовите документы, регламентирующие диагностику и меры борьбы с бешенством. Опишите общий алгоритм искоренения бешенства на неблагополучной территории. Вакцины каких типов применяются для профилактики бешенства животных разных видов? Применяют ли живые антирабические вакцины для иммунизации собак? Опишите, что такое оральная вакцинация лисиц. Какова история и эффективность ее применения? Какие животные служат источником заражения бешенством/гидрофобией человека? Для биотических компонентов природного очага болезни характерно то, что основная триаДа очага - возбуДитель, переносчик и животные - являются сочленами биоценоза... Е. Н. Павловский БЛУТАНГ Блутанг (Bluetongue, синий язык, катаральная лихорадка овец) - трансмиссивная природно-очаговая экзотическая вирусная инфекция домашних и диких жвачных животных многих видов, одна из наиболее опасных инфекций ветеринарного значения. Характеризуется весьма злокачественным течением у овец с воспалительно-некротическими поражениями лицевой части, катаральным воспалением желудочно-кишечного тракта и коронитами, нередко сопровождается смертностью (рисунок 15). Особая актуальность блутанга обусловлена одной из форм ее эмерджентности - беспрецедентным распространением из традиционных африканских нозоареалов на так называемые неэндемичные территории с реальной угрозой для животноводства РФ. Возбудитель. Вирус блутанга - представитель рода орбивирусов семейства Reoviridae. Серогруппа блутанга включает не менее 24 серотипов, которые глобально распространены как самостоятельные варианты возбудителя с различной вирулентностью и эпизоотическим потенциалом. Вирус малоустойчив к физическим и химически воздействиям: разрушается при замораживании и в зоне рН <6.0 и >8.0, инактивируется в-пропиолактоном, иодофорами и фенолом, при 50 °C за 3 часа, при 60 °C за 15 мин, стабилен в присутствии белков (сохраняется несколько лет в крови при 20 °C). Эпизоотологические данные. Традиционный глобальный нозоареал блутанга до начала 21 в. располагался широкой периэкваториальной полосой в зоне, ограниченной с севера и юга 40° и 35° соответствующей широты. Вирус присутствует везде, где есть мокрецы рода Culicoides - его биологические переносчики (Африка, Америка, Австралия, многие страны Южной Азии и Океании). Однако инфекция в клинически выраженной форме стационарно наблюдалась только в отдельных странах (США, некоторые африканские страны). На рубеже 20-21 вв., в связи с существенным повышением континентальной температуры на территории   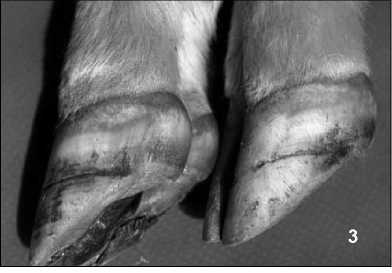   2 Рисунок 15. Основные признаки блутанга - массовая смертность овец (1), синий язык (2) и коронит (3). Западной Европы, ареал блутанга значительно расширился вплоть до 60° северной широты (юг Скандинавии). К блутангу восприимчивы с наиболее выраженными манифестными проявлениями овцы (см. рисунок 15) - клинические индикаторы эпизоотического процесса без формирования вирусоносительства. Заболеваемость овец в эпизоотиях достигает 100%, это наиболее значимый аспект эпизоотологии блу- танга. Смертность на эндемичных территориях обычно низкая (до 10 %), но в отдельных эпизоотиях достигает 50%. Существуют выраженные различия восприимчивости овец в зависимости от породы. Крупный рогатый скот (в основном), а также козы, одногорбые верблюды, многие дикие экзотические жвачные являются персистентно инфицированными носителями и резервуарными хозяевами естественной инфекции (обычно в инаппарантной форме). Блутанг не контагиозен, трансмиссия осуществляется специфическими биологическими переносчиками-векторами (мокрецами рода Culicoides). После кровососания на виремичном хозяине в их организме вирус размножается и только по прошествии внешнего инкубационного периода продолжительностью от 5 до 20 дней (в зависимости от температуры внешней среды) происходит дальнейшая передача инфекции по эпизоотической цепи. При этом важным является механизм сохранения инфекции в межэпизоотическом периоде, в частности, универсального для трансмиссивных инфекций процесса перезимовывания, который заключается в персистенции вируса в зараженных резервуарных хозяевах. При блутанге возможно и характерно внутриутробное заражение плодов. Другие канонические пути и способы передачи инфекции в естественных условиях неосуществимы. Источники вируса - инфицированные переносчики, кровь, сперма. Природная очаговость. Блутанг - типичная природно-очаговая инфекция. Для внутригодовой динамики заболеваемости характерна выраженная сезонность, обусловленная фенологическими пиками активности переносчиков, обычно совпадающими с периодами дождей в тропических регионах или весенне-летне-осенними месяцами в странах умеренного климата. Паразитарная эпизоотологическая система блутанга представляет классический стереотип трехчленной замкнутой, сложной эписистемы (рисунок 16). Резервуарными хозяевами и источниками инфекции в эпизоотических цепях трансмиссивного (неконтактного) типа служат персистентно инфицированные домашние и дикие жвачные, в числе которых ведущее эпизоотологическое значение принадлежит КРС. Овцы в виду краткосрочного, острого и клинически выраженного переболевания источниками трансмиссивной инфекции не являются. Мокрецы рода Culicoides - одна из наиболее многочисленных групп насекомых-переносчиков инфекций. Из 1400 известных их видов 20 вовлечены в экологию блутанга. Признанными переносчиками блутанга являются мокрецы местных, тропических видов, обитающие в Африке и средиземноморских  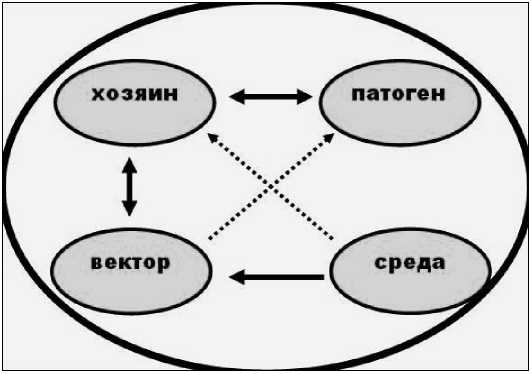 Рисунок 16. Универсальная структура паразитарных эписистем арбовирусных инфекций и связи соактантов. странах Европы, в Северной и Южной Америке, в Австралии. Важно, что укоренение, передачу блутанга на новых, неэндемичных территориях (в частности, в Северо-Западной Европе) и природно-очаговые циклы инфекции оказались способны поддерживать мокрецы автохтонных палеарктических видов, ранее не встречавшиеся с вирусом блутанга. Занос на неэндемичные территории возможен при импорте и иных формах перемещения из неблагополучных стран персистентно инфицированных животных-вирусоносителей, прежде всего в рамках международной торговли КРС, экзотическими, зоопарковыми и т.п. животными. Существенным фактором заноса может также служить пассивный перенос инфицированных переносчиков в составе аэропланктона, распространяющегося потоками ветров на многие сотни километров от природных очагов. Патогенез. Как и при прочих трансмиссивных (кровяных) болезнях воротами инфекции является кровеносная система в любой точке поверхности восприимчивого животного («из крови в кровь»). После инъекционного заражения теплокровного хозяина вирус через кратковременную первичную вирусемию распространяется по организму в регионарные лимфоузлы и размножается там. Затем, в течение вторичной вирусемии, вирус поражает уже патогенетические мишени - фагоцитирующие клетки эндотелия сосудов, макрофаги и дендритные клетки различных органов, размножается в моноцитах и лимфобластах крови, адсорбируется на эритроцитах и тромбоцитах, проникает в них за счет инвагинаций мембран. Формируется персистентная клеточно-ассоциированная вирусемия в присутствии вируснейтрализующих антител. Внеклеточная вирусемия краткосрочна, тогда как ассоциированная с клетками вирусемия продолжительна и характерна для патогенеза блутанга. Вирус не выделяется из больного организма в окружающую среду, больной не является непосредственным источником инфекции, в его присутствии прямого контактного заражения не происходит. Внутрисосудистая персистенция вируса блутанга таким образом исключает иные способы его эстафетной передачи по эпизоотической цепи (заражение) и территориального распространения, кроме облигатной трансмиссии через одушевленного кровососущего вектора-переносчика. Поражение эндотелиальных клеток мелких сосудов вызывает васкулярные тромбозы и ишемические некрозы тканей. Эти патологические процессы на клеточном уровне в свою очередь провоцируют образование защечных язв внутри ротовой полости, воспаление коронарных связок, мышечные некрозы, экстравазаты, сопровождающиеся лицевыми и пульмонарными отеками, плевральными и перикардиальными выпотами. При конгенитальной (внутриутробной) инфекции наблюдаются случаи мальформации плодов или аборты. В зависимости от периода беременности клинические проявления различны: в первой трети преобладает эмбриональная смертность, во второй трети - врожденные аномалии, такие как гидранэн- цефалия или ретинальная дисплазия за счет разрушения предшественников мозговых клеток, в последней трети плод вырабатывает иммунологическую резистентность и не подвержен инфекции. Иммунитет. Постинфекционный иммунитет не имеет практического значения, т.к. все больные и находившиеся в эпизоотическом очаге животные (прежде всего овцы) из-за тяжелых последствий переболевания и опасности носительства обычно подлежат ликвидации. Персистенция вируса в организме животных-резервуаров протекает по типу толерантной инфекции под иммунным контролем с наличием определяемых сывороточных антител и сохранением вируса на предельно низком, трудно выявляемом уровне в лимфоцитах. Именно серопозитивность является единственным критерием идентификации инфицированных животных при эпизоотологическом мониторинге, контроле благополучия животных при транспортировке, международных закупках и т.п. Искусственный приобретенный иммунитет - основа специфической защиты овец и КРС в контроле блутанга. Используются убитые или живые вакцины из модифицированного вируса, хотя модифицированные вакцинные варианты вируса могут вызвать инфекцию в полевых условиях. Симптомы. Инкубационный период острого течения блютанга у жвачных всех видов составляет 6-8 дней (от 4 до 20). Клиническое проявление болезни наиболее злокачественно, с фатальным исходом отмечается главным образом у овец отдельных пород и оленей некоторых видов. Инфекция у КРС протекает в основном субклинически из-за межвидовых различий в чувствительности к вирусу и реакции эндотелиальных клеток. При острой форме течения у овец развиваются общие признаки катаральной лихорадки, в частности, гипертермия до 420 C, депрессия, застойная гиперемия и отек лицевой части, век и ушей, воспаление, изъязвление, эрозии и некроз слизистой рта, опухание, иногда цианотичность языка, хромота из-за коронита или пододерматита и миозита, аборты, другие тератогенные эффекты и последствия конгенитальной инфекции (смерть эмбрионов, мацерация, другие дефекты внутриутробного развития), осложнения в виде пневмонии, истощение, смерть в результате одной из перечисленных причин на 8-10 день или длительное выздоровление с облысением, бесплодием, задержкой роста. Патологоанатомические изменения. Отмечаются гиперемия, отек, геморрагии и изъязвления слизистой респираторного и пищеварительного трактов (рот, пищевод, ротовая полость, кишечник, трахея), гиперемия копытной пластинки и венчика, гипертрофия лимфатических узлов и спленомегалия, тяжелая мышечная дистрофия, двусторонняя бронхолобулярная пневмония (развивается как осложнение). Диагноз. Блутанг у овец и КРС как основных поражаемых объектов сходен по эпизоотологическим и клиническим признакам с группой заразных и незаразных заболеваний, таких как контагиозная эктима и оспа овец, ящур, инфекционный ринотрахеит, парагрипп-3, злокачественная катаральная горячка, эпизоотическая геморрагическая болезнь оленей, чума мелких жвачных, ценуроз, фотосенсибилизация, растительные отравления, пневмонии различной этиологии, полиартриты, копытная гниль, абсцессы конечностей. Поэтому в дифференциальной диагностике определяющая роль принадлежит лабораторным исследованиям. Специментами для вирусологических исследований служат пробы гепаринизированной крови от живых животных, от свежих трупов - селезенки, печени, красного костного мозга, крови из сердца, лимфоузлов, от абортированных плодов и конгенитально инфицированных новорожденных животных - пред- молозивной сыворотки вместе с образцами от свежих трупов. Все пробы хранят при 4 °С, не замораживая (!). Для серологических исследований получают парные пробы сывороток. Выделение и идентификация вируса проводится классическими методами вирусной изоляции (заражение овец, внутрисосудистая инокуляция 10-12 дневных куриных эмбрионов, реакция нейтрализации в культуре клеток) и с помощью ПЦР Важнейший этап лабораторной диагностики - определение серотиповой принадлежности изолятов вируса в реакции перекрестной нейтрализации. Для серологического тестирования используют ИФА, РДП, РН и РСК. Лечение блутанга не применяется, больные животные подлежат уничтожению. Профилактика и меры борьбы. Общая профилактика в благополучных зонах включает карантин, серологический надзор, полевые эколого-энтомологические исследования. Одним из решающих мероприятий является строгий «выходной» и «входной» серологический контроль при импортно-экспортных операциях с КРС, а также экзотическими дикими жвачными. По рекомендациям Кодекса здоровья наземных животных МЭБ ограничительный период при блутанге должен составлять 60 дней. Специфическая профилактика блутанга разных серотипов в настоящее время предполагает использование преимущественно убитых культуральных вакцин с адъювантами, производимых по унифицированной технологии. Такие вакцины применяют в формате систематической тотальной вакцинации КРС (как резервуарных хозяев) и овец (как наиболее восприимчивых) во многих регионах мира, что позволяет успешно контролировать заболеваемость. Как показывает опыт мероприятий последних лет, тактика тотальной вакцинации имеет не только профилактическую, но и противоэпизоотическую эффективность, позволяет в короткие сроки ликвидировать эпизоотическую заболеваемость на неблагополучных территориях. Как в благополучных, так и неблагополучных зонах важнейшим элементом профилактики и борьбы с блутангом является контроль переносчиков-векторов. Блутанг в Западной Европе. В последние годы 20 в. нозоареал блутанга существенно расширился за счет стран южной Европы, находящихся в достаточной географической близости к энзоотичным территориям африканского севера. Здесь происходят крупные эпизоотии и вспышки болезни, причиной которых могут служить периодические заносы инфекции с зараженными переносчиками, распространяющимися через средиземноморское пространство потоками ветров или иными способами. Пять серотипов вируса были изолированы в двенадцати странах региона, где эпизоотии блутанга сопровождались гибелью миллионов овец (см. рисунок 15/1). Летом 2006 г. блутанг, вызванный вирусом 8 серотипа центрально-африканского происхождения, неожиданно возник и распространился в несвойственном регионе - северо-западной Европе. Особо тяжелое, злокачественное течение болезни отмечено у овец, коз (летальность около 30 и 60%, соответственно), а также у КРС - основного паразитосистемного хозяина; по сравнению с предшествующей эпизоотической ситуацией на юге Европы в последнем случае клинический профиль практически не отличался от такового у овец. Эмерджентная обстановка потребовала реализации комплекса чрезвычайных мер в Германии, Франции, Голландии и других странах, которые включали ветеринарный надзор (зонинг, трасинг и др.), контроль вектора (химическая и физическая защита от насекомых) и вакцинацию. Фирмой Merial была экстренно изготовлена в необходимых объемах инактивированная вакцина против блутанга 8 серотипа, по аналогии с выпускаемыми ранее препаратами из вирусов африканских серотипов. При ее тотальном использовании (главным образом КРС и овцам) в общем комплексе мер получен наиболее эффективный результат. Вакцинация защищала не менее 80% популяции и предупреждала развитие вирусемии у животных (что особенно важно при инфекции трансмиссивного типа с заражением кровососущими переносчиками). Кампания поголовной иммунизации, реализованная дважды, в 2008 и 2009 гг., за счет средств Еврокомиссии, переведенная затем на добровольную основу, позволила сократить число вспышек инфекции до несущественных значений (0,25 %). В 2013 г. блутанг 8 серотипа на северо-западе Европы уже не регистрировали. Эти успешные результаты являются эталоном межгосударственного кооперативного решения крупномасштабных эмерджентных проблем в эпизоотологии, особенно с учетом векторной природы блутанга. БЛУТАНГОПОДОБНЫЕ БОЛЕЗНИ Это оригинальная группа трансмиссивных природно-очаговых экзотических арбовирусных инфекций, сходных с блутангом таксономической близостью возбудителей, по клиническим признакам, стереотипности паразитарных эписистем (см. рисунок 16), трансмиссии мокрецами рода Culicoides, эмерджентной зависимости от изменений факторов экологического (природно-климатического) порядка и других эпизоотологически рациональных характеристик. Важный объединяющий признак - очевидная общность патогенеза с наблюдаемой закономерной последовательностью этапов (стадий) развития патологических процессов и явлений в направлении «заражение интактных самок домашних жвачных в ранней стадии беременности первичная острая инфекция, от бессимптомной до лихорадочной, с различными экстенсивными симптомами трансплацентарная инфекция плодов отложенный терато генный эффект, проявляющийся мальформацией через 3-6 месяцев». Эпизоотическая геморрагическая болезнь оленей (ЭГБО). Заболевание известно в США и Канаде с 1890 г. с такими синдромальными названиями, как «черная нога», «черный язык», микотический стоматит, геморрагическая септицемия, и др. Нозологическая самостоятельность ЭГБО была оформлена в 1955 г. Это острая, нередко фатальная инфекция животных семейства Cervidae (оленевые) и других диких жвачных многих видов, прежде всего высоколетальная (до 90%) для белохвостых оленей (Odocoileusvirginianus), и, реже, блутангоподобная болезнь КРС. В последнем случае клинические признаки разной степени выраженности - лихорадка, анорексия, дисфагия, изъязвление и некротические поражения слизистой рта, гиперемия и отеки конъюнктивы, язвы на морде, гиперемия сосков и вымени, экстенсивные геморрагии, дегидратация, хромота свидетельствуют о патогенетическом сходстве с блю- тангом (см. выше). Орбивирус-возбудитель ЭГБО таксономически и иммунологически близок к вирусу блутанга. В числе его восьми или более серотипов серотип 2 представляет вирус-возбудитель отдельной нозологической формы - болезни Иба- раки. Передается мокрецами рода Culicoides, активность которых в течение года - от круглогодичной в тропических странах до периода август-октябрь на севере США и в Канаде - определяет внутригодовую динамику и сезонно сть инцидентности. Как и вирус блутанга, вирус ЭГБО вне обязательной связи с заболеваемостью в мире выделяется повсеместно, где существуют ареалы мокрецов, включая Северную Америку, Африку, Азию, Австралию, Японию. Систематические эпизоотии с высокой инцидентностью возникают среди оленей разных видов только в Западном полушарии - на севере США и юге Канады. В начале 21 в. возникли эмерджентные эпизоотические вспышки ЭГБО среди КРС в четырех странах Старого Света - по всему южному периметру Средиземноморского региона (Марокко, Алжир, Израиль, Турция) с весьма серьезными клиническими проявлениями и последствиями. В связи с этим в 2008 году болезнь включена в Список МЭБ как опасная инфекция, подлежащая нотификации. Болезнь Ибараки. Эта блутангоподобная трансмиссивная инфекция КРС, протекающая с клиническими признаками, сходными с таковыми у этих животных при блутанге и ЭГБО (некоторые авторы считают болезнь синонимом ЭГБО у КРС). Вирус (серотип 2 из серогруппы орбивируса ЭГБО) с 1959 г. вызывает экстенсивные вспышки и эпизоотии в Японии и распространяется в тропическом регионе Дальнего Востока, в частности, в Корее и на Тайване. Серопозитивные животные обнаруживаются в Австралии и Индонезии. |
