Общая микробиология. Виды микроскопии назначение и принципы применения
 Скачать 1.57 Mb. Скачать 1.57 Mb.
|
ТаблицаСхема проведения реакции агглютинации
В каждую пробирку с разведенной сывороткой вносят по 1-2 капли антигена (1-2 млрд. микроорганизмов в 1 мл), энергично встряхивают и помещают на 2 часа в термостат при температуре 37ºС, после чего предварительно учитывают результаты реакции, начиная с контролей (сыворотки и антигена). Отсутствие агглютинации в контрольных пробирках и наличие взвешенных хлопьев в опытных пробирках свидетельствуют о положительной реакции. Пробирки оставляют при комнатной температуре на 18-20 ч, после чего окончательно учитывают результаты. Интенсивность реакции выражается плюсами. При полной агглютинации (++++) жидкость совершенно прозрачная, а на дне пробирки осадок из хлопьев склеивающихся микроорганизмов. Чем меньше микроорганизмов агглютинировалось, тем мутнее жидкость и тем меньше хлопьевидный осадок на дне (+++, ++, +). При отрицательной реакции (–) осадка нет, взвесь остается равномерно мутной и по виду неотличима от содержимого пробирки с контролем антигена. Применение РА для серологической диагностики инфекционных заболеваний – брюшного тифа и паратифов (реакция Видаля), сыпного тифа (реакция Вейгля), бруцеллеза (реакции Райта и Хаддлсона), туляремии и других заболеваний – основано на определении антител (агглютининов) в сыворотке больных. Для проведения реакции берут у взрослого 3-5 мл крови из локтевой вены или пальца, мочки уха, а у маленьких детей 1 мл из пятки. Отделяют сыворотку крови и разводят изотоническим раствором натрия хлорида от 1:50 или 1:100 до 1:800 или 1:1600. Более низкие концентрации антител обычно не используют потому, что в крови могут находится нормальные антитела, которые способны в небольших разведениях вызывать реакцию агглютинации. В качестве антигена в этой реакции используют диагностикумы – взвеси заведомо известных убитых и в отдельных случаях живых микроорганизмов. Диагностикумы из убитых организмов весьма устойчивы, не теряют своих свойств в течение нескольких лет и не представляют опасности заражения. Техника проведения и учёт результатов РА с сывороткой больного не отличаются от таковых при развернутой реакции агглютинации для определения вида микроорганизмов. Реакция непрямой агглютинации (гемагглютинации) (РНГА) При пассивной агглютинации растворимые антигены (белки, полисахариды и их комплексы микробного происхождения) соединяют с нерастворимым носителем, выполняющим исключительно индикаторную функцию. Носителем могут быть эритроциты, частицы латекса, поликриламида, бентонита и др. Связывание антигена с носителем происходит в результате адсорбции или химического соединения. Микробные полисахариды, например, можно адсорбировать на нативных эритроцитах без какой-либо их предварительной обработки. Различные белки (в том числе микробные ферменты) возможно присоединять к эритроцитам, только обработав их различными химическими веществами, обладающими дубильным действием: танином, хромахлоридом, формальдегидом или бисдиазотированным бензидином. Такая обработка предотвращает разрушение красных кровяных клеток, которое может произойти при непосредственном контакте антигена с эритроцитами. Когда антиген, связанный с носителем, соответствует антителу, наблюдается агглютинация частиц носителя. Чувствительность непрямой реакции агглютинации 0,02… 0,04 мкг азота белка антител/мл. Методика. Кровь, взятую из яремной вены взрослого барана, помещают в стеклянную банку с бусами, дефибринируют встряхиванием в течение 10-15 мин и фильтруют через ватно-марлевый фильтр. После центрифугирования в течение 10 мин при 2000 об/мин эритроциты отмывают 3-4 раза в изотоническом растворе натрия хлорида, осадок ресуспендируют в нем и добавляют 5-кратный объём 4% формалина (рН 7,0), в котором оставляют эритроциты на 3-4 дня при температуре 4ºС. Затем эритроциты вновь осаждают и повторяют процедуру со свежим раствором формалина, после чего их отмывают 20-кратным объёмом изотонического раствора натрия хлорида и доводят до 20% концентрации. Фиксированные эритроциты хранят при температуре 4ºС. Пригодность эритроцитов контролируют следующим образом: 1) после замораживания и оттаивания 5% взвеси эритроцитов в дистиллированной воде гемолиза не наблюдается; 2) при смешивании 0,1 мл 0,2% взвеси эритроцитов с изотоническим раствором натрия хлорида спонтанной агглютинации не наблюдается. Для сенсибилизации эритроцитов к 8 объёмам дистиллированной воды добавляют 1 объём антигена, 1 объём 50% взвеси формалинизированных эритроцитов и 1 объём 0,1-0,2% раствора хрома хлорида или танина в разведении 1:20000-1:2000000. Смесь оставляют на 10-15 мин при комнатной температуре, затем добавляют равный объём изотонического раствора натрия хлорида и центрифугируют 20 мин при 2000об/мин. Осадок сенсибилизированных эритроцитов отмывают 2-3 раза 20-кратным объёмом изотонического раствора натрия хлорида, затем ресуспендируют до 5% концентрации в стабилизирующем растворе, состоящем из равным объёмов 30% раствора сахарозы и донорской сыворотки человека. В качестве контроля используют формалинизированные эритроциты, сенсибилизированные другим антигеном, или формалинизированные несенсибилизированные эритроциты. РНГА удобно ставить на микропанелях аппарата Такачи, используя для разведения материала микротитратор. Исследуемые сыворотки прогревают 30 мин при температуре 56ºС для удаления неспецифических гемагглютининов, готовят 2-кратные разведения на стабилизирующем растворе и по 1 капле каждого разведения вносят в две лунки U-образного микротитратора Такачи. В первый ряд добавляют по одной капле 1% суспензии сенсибилизированных антигеном эритроцитов, во второй ряд – такое же количество контрольных эритроцитов. Пластины тщательно встряхивают и помещают на 30-40мин в термостат при температуре 37ºС. Результаты реакции учитывают по наличию гемагглютинации. Положительна она в том случае, если титр гемагглютинации с опытными эритроцитами по меньшей мере в 4 раза превышает титр гемагглютинации с контрольными эритроцитами. Обязателен контроль сенсибилизированных эритроцитов на отсутствие спонтанной агглютинации. Реакция торможения непрямой гемагглютинации (РТНГА) Реакцию проводят для обнаружения антигенов возбудителей в исследуемом материале, добавляя в нему иммунную сыворотку. При наличии гомологичного антигена происходит связывание антител, поэтому после добавления сенсибилизированных антигеном эритроцитов их агглютинации не происходит, что оценивается как положительный результат. Для большей чувствительности реакции специфическую иммунную сыворотку добавляют к исследуемому материалу в минимальном количестве (2 гемагглютинирующие единицы). Титр иммунной сыворотки определяют предварительно с помощью РНГА. За одну гемагглютинирующую единицу принимают предельное разведение сыворотки, которое вызывает склеивание эритроцитов. Методика. В лунки полистироловых пластин или агглютинационные пробирки вносят по 0,025 мл 1% раствора нормальной сыворотки кролика и делают серийные 2-кратные разведения исследуемого материала. Затем во все лунки добавляют по 0,025 мл имунной сыворотки, пластинку встряхивают и оставляют на 30 мин при температуре 37ºС или на 1 ч при комнатной температуре. Далее во все лунки добавляют по 0,025 мл антигенного диагностикума, встряхивают и оставляют на 2 ч, после чего учитывают результаты. При проведении этой реакции к контролю для РНГА добавляют контроль специфичности иммунной сыворотки, состоящий из специфического антигена, иммунной сыворотки (2, 1, 0,5 гемагглютинирующей единицы) и взвеси сенсибилизированных эритроцитов. РТНГА применяют также для обнаружения специфических антител (полных и блокирующих), для чего к исследуемой сыворотке добавляют дозированное количество антигена. Если в ней содержатся антитела, то происходит связывание их антигеном, поэтому после добавления эритроцитов, сенсибилизированных антителами (2-й этап РТНГА), склеивания эритроцитов не происходит. Благодаря использованию минимального количества антигена (2 нейтрализующие дозы) реакция высокочувствительна. Количество нейтрализующих доз в антигенном препарате определяют с помощью РНГА, при этом делают серийные 2-кратные разведения антигена в 1 % растворе нормальной сыворотки кролика и в лунки вносят антительный эритроцитарный диагностикум. Нейтрализующей дозой антигена считают его максимальное разведение, дающее полное склеивание сенсибилизированных эритроцитов. Перед проведением реакции испытуемые сыворотки разводят 1:5-1:10 и инактивируют при температуре 56°С в течение 30 мин. Для адсорбции гемагглютининов к сывороткам добавляют 50 % взвесь формалинизированных или свежих отмытых эритроцитов барана из расчета 0,1 мл взвеси на 1 мл разведенной сыворотки. Смесь встряхивают и инкубируют 30 мин при температуре 37ºС или 1 ч при комнатной температуре, после чего эритроциты осаждают центрифугированием. Можно для осаждения эритроцитов оставить сыворотки в холодильнике до следующего дня. При проведении опыта исследуемый материал разводят в 1 % растворе нормальной сыворотки кролика в объеме 0,025 мл в лунках панели микротитратора. Затем в каждую лунку добавляют по 2 нейтрализующих дозы антигена в объеме 0,025 мл. Пластины встряхивают и оставляют на 30 мин при температуре 37 °С или на 1 ч при комнатной температуре. Затем во все лунки вносят по 0,025 мл антительного эритроцитарного диагностикума. Пластины встряхивают и инкубируют 1,5-2 ч при комнатной температуре, после чего учитывают результаты реакции. Учет можно производить также и на следующий день. Титром исследуемой сыворотки считают максимальное разведение ее, в котором не происходит склеивания эритроцитов. Опыт сопровождают следующими видами контроля: 1) стабильности сенсибилизированных эритроцитов (эритроциты +1 % раствор нормальной сыворотки кролика); 2) полноты истощения гемагглютининов в каждой испытуемой сыворотке (испытуемая сыворотка в наименьшем разведении + формалинизированные эритроциты); 3) правильности определения минимальной нейтрализующей дозы антигена (2, 1 и 0,5 нейтрализующей дозы антигена + антительный эритроцитарный диагностикум). Реакция обратной непрямой гемагглютинации (ронга) применяется для индикации бактериальных и вирусных антигенов в исследуемых материалах, а также для экспресс-диагностики ряда инфекций. В отличие от РНГА при данной реакции эритроциты сенсибилизируют не антигеном, а антителами, агглютинация которых происходит при добавлении антигена. Эритроциты предварительно фиксируют формалином, или глютаральдегидом, а затем связывают их с гамма-глобулином, который выделяют из иммунных сывороток и очищают от других сывороточных белков. Связывание гамма-глобулина с поверхностью эритроцитов происходит с помощью хлорида хрома. Для этого к 8 объемам дистиллированной воды добавляют 1 объем иммуноглобулинов, выделенных из иммунной сыворотки, 1 объем 50 % взвеси формалинизированных эритроцитов и 1 объем 0,1-0,2 % раствора хлорида хрома. Смесь оставляют на 10-15 мин при комнатной температуре, затем обрабатывают эритроциты как при реакции пассивной гемагглютинации. Специфичность антительного диагностикума проверяют в реакции торможения пассивной гемагглютииации гомологичным антигеном. Реакция должна тормозиться гомологичным антигеном не менее чем в 16 раз и не тормозиться гетерологичным. Используется контроль на отсутствие спонтанной гемагглютинации. С помощью этой реакции проводят индикацию возбудителей в материале, взятом из органов погибших людей и животных, например, из мозга, селезенки, печени легких. Готовят 10 % суспензию указанных органов на изотоническом растворе натрия хлорида, центрифугируют их в течение 30-60 мин при 10000 об/мин и используют надосадочную жидкость в качестве антигена. Методика. Готовят 2-кратные разведения исследуемого материала (антигена) на стабилизирующем растворе. Вносят по 1 капле каждого разведения антигена в 3 соседние лунки микропанели (реакция занимает 3 параллельных ряда лунок). В каждую лунку первого ряда добавляют по 1 капле стабилизирующего раствора, в лунки второго ряда – по 1 капле гомологичной иммунной сыворотки в разведении 1: 10, третьего ряда – по 1 капле гетерологичной иммунной сыворотки. Второй и третий ряды служат контролями специфичности реакции. Смесь оставляют на 20 мин при комнатной температуре. Во все лунки добавляют по 1 капле 1 % суспензии сенсибилизированных эритроцитов (эритроцитарный антительный диагностикум) и тщательно встряхивают пластины. Результаты реакции учитывают через 30-40 мин. При наличии специфического антигена гемагглютинация отмечается в первом и третьем ряду (с гетерологичной сывороткой) и отсутствует во втором ряду, где антиген предварительно нейтрализован гомологичной сывороткой. Реакцию сопровождают контролями сенсибилизированных эритроцитов на спонтанную агглютинацию. Реакция торможения обратной непрямой гемагглютинации (РТОНГА) позволяет определить наличие антител в сыворотках людей и животных. Методика. Сыворотки разводят в 10 раз изотоническим раствором натрия хлорида, прогревают 20 мин при температуре 65 °С для разрушения неспецифических ингибиторов, а затем готовят 2-кратные разведения сывороток на стабилизирующем растворе и рабочую дозу антигена, содержащую 4 агглютинирующие единицы. Вносят по 1 капле каждого разведения сыворотки в лунки микропанели и добавляют в них по 1 капле антигена, разведение которого соответствует рабочей дозе. После контакта компонентов смеси в течение 20 мин при комнатной температуре во все лунки вносят по 1 капле эритроцитарного антительного диагностикума и тщательно встряхивают. Через 1,5-2 ч инкубации при комнатной температуре по гемагглютинации учитывают результаты реакции. Титром сыворотки является ее наибольшее разведение, которое полностью тормозит реакцию гемагглютинации с четырьмя агглютинирующими единицами антигена. Реакцию сопровождают контролями сенсибилизированных эритроцитов на спонтанную агглютинацию в присутствии: а) стабилизирующего раствора; б) нормального антигена (из материала, не содержащего вирус); в) исследуемой сыворотки. Преимущество реакции заключается в ее универсальности и возможности использования для выявления различных антигенов. Оценка результатов гемагглютинации. Результаты РНГА, РОНГА и РТОНГА учитывают по степени агглютинации эритроцитов: (++++) – полная агглютинация; (+++) – менее полная агглютинация; (++) – частичная агглютинация; (+) – следы агглютинации; (–) – отсутствие агглютинации. Реакция считается положительной, если агглютинация полная (++++) или почти полная (+++), диагностикум не дает спонтанной агглютинации в присутствии каждого компонента реакции и контроль специфичности антигена или антитела положительный. Методы, основанные на использовании меченых реагентов В настоящее время разработано много методов, предусматривающих применение меченых антител и антигенов. Чаще с этой целью используют радиоактивную или ферментную метку. Радиоиммунологические методы В радиоиммунологическом анализе специфичность реакции антиген-антитело сочетается с высокой чквствительностью, обеспечиваемой применением радиоактивной метки. В качестве метки чаще применяют радионуклиды йода (131J или 125J). Возможность проводить конкурентный анализ, а также анализ в жидкой или твердой фазе приводит к созданию большого числа различных методик. Для определения антигенов используют классический радиоиммунологический анализ (РИА). В основу РИА положен принцип конкурентного взаимодействия определяемого немеченого антигена и известного количества меченого антигена с активными центрами антител. При этом происходит вытеснение меченого антигена из его комплекса с антителом вследствие последующего добавления больших концентраций немеченого антигена или гаптена той же специфичности. Реакция (при высоком разведении ингредиентов) подчиняется закону действующих масс: вытеснение меченого антигена пропорционально введенному количеству немеченого антигена или гаптена. Конкуренцию между определяемым и меченым антигенами можно оценить количественно с помощью радиометрии, предварительно определив образовавшиеся иммунные комплексы от несвязавшегося меченого антигена. Концентрацию определяемого антигена рассчитывают, исходя из сравнения соотношений свободного и связанного меченых реагентов с соответствующим стандартом. Применяют также так называемые твердофазные методы. В качестве твердофазного носителя используют поверхности планшетов с лунками, бус, пленками из полистирола или других полимерных синтетических материалов. Адсорбированные (иммобилизированные) антигены и антитела длительное время сохраняют способность вступать в серологические реакции. Существуют различные модификации проведения твердофазного РИА: конкурентный метод, обратный метод, непрямой метод. РИА используют для определения антигенов вирусов гепатита, СПИДа, в лабораторной диагностике легионеллеза, дифтерии и других инфекций. Этот метод весьма эффективен при диагностике аллергии. Аллерген, иммобилизованный на сорбенте, инкубируют с сывороткой больного, после чего добавляют радиоактивно меченые анти-JgE-антитела. Метод иммунного окрашивания после переноса на нитроцеллюлозные мембраны (иммуноблоттинг) Этот метод применяется для количественного определения белков и гликопротеинов, которые после электрофоретического разделения в полиакриламидном геле переносят на микропористую нитроцеллюлозную мембрану. Неспецифически связанные с мембраной антигены обрабатывают специфическими антителами, связывание которых проявляют антиглобулиновыми антителами, конъюгированными с радиоактивной или ферментной меткой. Схема последовательных этапов иммуноблоттинга
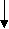
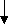
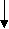
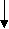
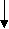
Методика.
Иммуноферментные методы В основу метода положена конъюгация антитела или гаптена с ферментом, которая не приводит к утрате антителом или гаптеном специфичности, а ферментом - каталитической активности. Однако в составе комплекса антиген-антитело конъюгаты гаптен-фермент или антитело-фермент теряют свою каталитическую активность. Соединение молекул антитела с ферментом осуществляется с помощью преимущественно глутаральдегида – бифункционального реагента, взаимодействующего с Е-аминогруппами белковых молекул. В качестве фермента успешно применяют в зависимости от модификации метода либо пероксидазу, β-галактозидазу, щелочную и кислую фосфотазы (реже ацетилхолин, глюкоамилазу, глюкозооксидазу), либо лизоцим, глюкозо-6-фосфат-дегидрогеназу и малатдегидрогеназу. Используемый для маркирования антител фермент не должен присутствовать в исследуемых, содержащих антиген клетках, так как эндогенная ферментативная активность недопустима. Известно много вариантов постановки ИФА. Различают гомогенный и гетерогенный вариант иммуноферментного анализа. В основе гомогенного ИФА, применяемого для определения низкомолекулярных субстанций (гаптены), лежит ингибирование активности фермента при соединении его с гаптеном (активность фермента восстанавливается в результате реакции АГ-АТ) либо, наоборот, потеря активности маркерного фермента в результате реакции АГ-АТ. Поэтому удаление свободного АГ из смеси, содержащей АГ в связанном виде, в составе иммунных комплексов невозможно. В противоположность этому при гетерогенном ИФА АГ или АТ фиксируется на твердой фазе (как правило, пластик), а непрореагировавшие компоненты реакции удаляются многократным отмыванием. В ИФА различают методы конкурентного и неконкурентного анализа. Конкурентный метод твердофазного ИФА может быть проведен при необходимости количественного определения антигена, который может быть получен в чистом виде. Первым этапом в этом случае будет присоединение антитела к носителю за счет химической реакции или физико-химических взаимодействий. Избыток антитела удаляют отмыванием и, внося строго определенное количество меченого антигена и различие количества намеченного антигена, строят калибровочную кривую. По окончании реакции иммунные комплексы АГ-АТ оказываются присоединенными к твердой фазе за счет антитела и избыток антигена удаляют отмывкой, добавляют субстрат для фермента, останавливают реакцию по истечении определенного времени и проводят колориметрическое определение продуктов ферментативной реакции. В другом варианте конкурентного ИФА с твердой фазой первично связывается антиген. После отмывки добавляют меченые энзимом антитела и стандартный или исследуемый антиген. Связывание меченых антител конкурентно тормозится растворенным антигеном. Количество продуктов ферментативной реакции обратно пропорционально концентрации растворенного антигена. К числу неконкурентных методов относится метод двойных антител, или как его иногда называют, "сэндвич-метод". Фиксированные на твердой фазе антитела инкубируют со стандартным или анализируемым антигеном. После отмывания добавляют избыток меченых антител (специфичных к этому же антигену), навязавшиеся антитела отмывают. Продукт ферментативной реакции образуется в количествах, пропорциональных количеству связанного антигена. Довольно часто используют немеченые вторые антитела; о реакции в данном случае судят по связыванию энзим-меченых антител, специфичных по отношению к IgG (вторые антитела). В любом случае первые и вторые антитела должны принадлежать животным разных видов. Для иммуноферментного определения антител часто используется непрямой, неконкурентный ИФА. Антиген фиксируют на твердой фазе, после отмывания проводят инкубацию с раствором антител. Если произошло специфическое связывание антител, их можно количественно определить при помощи меченой ферментом антиглобулиновой сыворотки, ферментативной реакции. Кроме описанных известны следующие модификации твердофазного ИФА. Вместо совместной инкубации меченых и немеченых антигенов со связанными антителами можно непосредственно инкубировать только стандартный или анализируемый антиген, а затем после отмывания проводить инкубацию с избытком энзим-меченого антигена, который взаимодействует с "незанятыми" антителами. Кроме того, стандартный или анализируемый антиген можно инкубировать с избытком энзим-меченых антител и по окончании иммунной реакции добавлять эту смесь к антигену, фиксированному на твердой фазе. Определяют количество свободных энзим-меченых антител, связанных антигеном на твердой фазе. В обоих случаях концентрация продукта ферментативной реакции пропорциональна концентрации анализируемого антигена. Результаты учитывают фотометрически. В настоящее время выпускается большое количество разнообразных иммуноферментных диагностических наборов как для определения антител в сыворотке или других биологических жидкостях, так и для определения антигенов. В качестве последних могут выступать возбудители различных заболеваний (вирусы коксаки В, гепатита А и В, СПИДа, простого герпеса, краснухи; бруцеллы, холерный вибрион, сальмонеллы, трепонемы, кишечная палочка), а также различные белки, определение содержания которых в крови или секретах представляет диагностический интерес (аутоантитела, факторы неспецифической защиты, гормоны, цитокины, белки острой фазы и др.). Методика. Для проведения ИФА необходимы следующие буферные растворы.
Ортофенилендиамин готовят ex tempore следующим образом: 10 мг ортофенилендиамина, 6,1 мл 0,1 М лимонной кислоты, 6,4 мл 0,2 М Na2HPO4 12H2O (для полного растворения подогреть на водяной бане), 12,5 мл дистиллированной воды, 0,35 мл 3% Н2О2 . Растворяют 80 мг 5-аминосалициловой кислоты в 100 мл дистиллированной воды, доводят рН раствора до 6,0 ex tempore с помощью 1 М NaOH. Перед использованием на каждые 9 мл раствора добавляют 1 мл 0,05% Н2О2 . Для проведения ИФА необходимы полистироловые планшеты, имеющие лунки с плоским дном и автоматические пипетки. Для количественного учета используют спектрофотометр – регистратор экстинции при длине волны 492 нм. Методика реакции. Первый этап ИФА – сорбция соответствующего разведения антител или антигена (в концентрации 10-20 мкг/мл) на карбонатно-бикарбонатном буфере в объеме 0,2 мл на твердую фазу в течение 1-2 ч при температуре 37С и 10-12 ч при температуре 4С. Затем отмывают лунки (для удаления несорбированного на носителе антитела или антигена) водопроводной водой, отмывочным буфером с 0,05% твин-20 в течение 5 минут (2 раза) при комнатной температуре. После этого вносят в каждую лунку по 0,2 мл 1% раствора бычьего сывороточного альбумина на КББ и инкубируют в течение 1 ч при температуре 37С для закрытия участков поверхности лунок, оставшихся свободными после сорбции первого компонента реакции на твердый носитель. Лунку отмывают от несвязанного бычьего сывороточного альбумина и вносят исследуемый материал (антиген или антитела) по 0,2 мл в разведениях на фосфатно-солевом растворе (рН 7,2) с 0,05% твин-20. Каждое разведение материала вводят в две лунки и помещают в термостат на 1-3 ч при температуре 37С. Отмывают непрореагировавшие в иммунной реакции антигены или антитела и вносят по 0,2 мл конъюгированных антител против исследуемого антигена или антител в рабочем рахзведении на фосфатно-солевом растворе с 0,05% твин-20. Затем их инкубируют в течение 2 ч при температуре 37С. Несвязанный конъюгат отмывают с помощью буфера 3 раза по 10 минут. В лунку вносят 0,1 мл раствора субстрата (хромогена) и выдерживают 30 минут в темноте при комнатной температуре. В процессе инкубации в присутствии пероксидазы ортофенилендиамин окрашивается в желтый цвет, а аминосалициловая кислота – в коричневый. Для остановки реакции расщепления субстрата в лунку добавляют по 0,1 мл 1М NH2SO4 (или 1M NaOH). Контроль реакции – исследуемые антиген или антитела заменяют гомологичным компонентом реакции. Контроль конъюгата – 0,2 мл 1% бычьего сывороточного альбумина на КББ + 0,2 мл конъюгированных антител в рабочем разведении. Результаты реакции учитывают визуально или инструментально. При визуальном учете выявляют то наибольшее разведение исследуемого материала, в котором окраска интенсивнее, чем в контроле (бычьим сывороточным альбумином). При учете результатов реакции с помощью спектрофотометра положительным считается то наибольшее разведение исследуемого материала, где уровень экстинции превышает не менее чем в 2 раза уровень экстинции соответствующего разведения гетерологичного компонента реакции. Иммунофлуоресцентные методы В основу флуоресцентного метода положено такое взаимодействие антигена с антителом, при котором один из компонентов реакции обладает способностью к вторичной флуоресценции благодаря предварительному ковалентному соединению с флуоресцентным красителем. Образовавшиеся таким образом иммунные комплексы становятся хорошо видимыми, ярко светящимися структурами на темном фоне под флуоресцентным микроскопом. В качестве флуоресцентных красителей используют флуоресценизотиоцианат, родамин, В-изотиоционат, мессамин-родамин В200-сульфохлорид и др., имеющие реакционноспособные группы (сульфохлорид, изотиоцианат и др.). Эти группы соединяют со свободными аминогруппами молекул антител, которые не теряют при обработке флуорохромами специфического сродства к соответствующему антигену. Известны различные варианты постановки иммунофлуоресцентного анализа. Прямая РИФ – предполагает применение иммунофлуоресцирующих сывороток против каждого изучаемого антигена. Непрямая РИФ – основана на использовании двух различных антисывороток. Вначале применяют немеченные антитела против изучаемого антигена, а на втором этапе реакции образовавшийся комплекс антиген-антитело обрабатывают меченной антисывороткой, содержащей антитела против гамма-глобулинов того вида животных, на которых были получены антисыворотки, использованные на первом этапе реакции (антивидовая сыворотка). Антикомплементарная РИФ – предполагает применение меченых антител против комплемента. Используется в тех случаях, когда комплекс антиген-антитело способен фиксировать комплемент. Добавление к такой системе антикомплементарной меченой сыворотки позволяет выявлять антиген по специфическому свечению в люминисцентном микроскопе. Достоинством непрямой и антикомплементарной РИФ является использование лишь одной светящейся сыворотки (антивидовой или, соответственно, антикомплементарной) при изучении различных антигенов, что значительно упрощает реакцию. РИФ может быть использована для изучения различных микробных антигенов в препаратах из материала больных, срезов тканей, инфицированных культур клеток и др., а также для определения количества антител в иммунной сыворотке. Важнейшей областью применения непрямого иммунофлуоресцентного анализа является обнаружение аутоантител в сыворотках пациентов с аутоиммунными заболеваниями. Методика. Исследуемый материал помещают на стекло и фиксируют в ацетоне 10 мин при комнатной температуре, после чего высушивают в течение 20 мин при температуре 37ºС. Дальнейшая обработка препаратов зависит от применяемого варианта РИФ. При прямой РИФ препарат окрашивают специфической меченой антисывороткой во влажной камере 30 мин при температуре 25ºС, после чего промывают буферным солевым раствором (рН 7,2) 10 мин при температуре 25ºС. При непрямой РИФ препарат вначале обрабатывают немеченой специфической антисывороткой во влажной камере 30 мин при температуре 25ºС, после чего промывают буферным солевым раствором (рН 7,2) 10 мин при температуре 25ºС. Далее препарат окрашивают антивидовой меченой сывороткой во влажной камере 30 мин при температуре 25ºС и промывают буферным солевым раствором (рН 7,2). При антикомплементарной РИФ препарат вначале обрабатывают немеченой специфической антисывороткой и комплементом морской свинки (1:10) во влажной камере в течение 30 мин при температуре 25ºС, после чего промывают и окрашивают антикомплементарной (против глобулинов морской свинки) меченой сывороткой во влажной камере 30 мин при температуре 25ºС и промывают буферным солевым раствором (рН 7,2). Приготовленные препараты высушивают с помощью фильтровальной бумаги и изучают в люминесцентном микроскопе – сначала при помощи сухого объектива (40), а затем, поместив на препарат каплю нефлуоресцирующего масла, с помощью иммерсионного объектива (90). При этом обращают внимание не только на наличие зеленого или зелено-желтого свечения, но и его интенсивность, характер распределения свечения в изучаемой клетке. Для исключения ложноположительных результатов реакцию сопровождают рядом контролей, среди которых особое значение имеет контроль с гетерологичным антигеном. Для исключения аутофлуоресценции и неспецифического связывания меченых антител с поверхностью клеток при изучении инфицированных культур клеток обязательно используют контроль с нормальной, неинфицированной культурой. Для подавления аутофлуоресценции препаратов можно использовать бычий альбумин, меченый сульфародамином. Применение двойной флуоресцентной метки Для одновременного анализа различных антигенов в одной и той же ткани, например, в клетках одного типа, применяют антисыворотки, меченые различными флуорохромами (ФИТЦ, ТРИТЦ). Иммуноферритиновый (иммунно-электронно-микроскопический) метод выявления антигенов основан на применении антител, меченых ферритином. Ферритин представляет собой железосодержащий белок с молекулярной массой 750 кДа, где содержание железа может доходить до 23%. Ферритин хорошо выявляется в электронном микроскопе и поэтому используется как маркер при иммуно-электронной микроскопии. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
