Вопросы к зачётуэкзамену по патологической физиологии
 Скачать 1.35 Mb. Скачать 1.35 Mb.
|
13.2.1. Гипобиотические процессыАтрофия - процесс уменьшения объема органа или ткани вследствие их недостаточного питания или нарушения обмена веществ. По механизму развития различают несколько видов атрофии. Атрофия от бездействия. Например, если перерезать сухожилие скелетной мышцы и лишить ее одной из точек прикрепления, произойдет уменьшение объема мышцы вследствие невозможности ее полноценных сокращений. Показана возможность развития атрофии скелетной мускулатуры у животных от неподвижности (гипокинезий) при их искусственной иммобилизации. Атрофия от денервации органа. Известно, что нервы оказывают на органы и ткани троякое влияние: а) регулируют кровоснабжение органов через вазомоторные нервы; б) оказывают трофическое влияние на ткани, активируют обмен веществ и в) вызывают возбуждение деятельности (сокращение, секреция и др.). Перерезка нерва лишает ткань нормального кровоснабжения и трофического влияния нервной системы. Вследствие этого в денервированном органе или ткани угнетается обмен веществ, уменьшается объем органа. Атрофия вследствие длительного сдавления органа или ткани, которое нарушает их нормальное питание и обмен веществ (рис. 13-5). Например, опухоль, оказывая давление на кость, может вызвать ее истончение и последующее разрушение. При закупорке мочеточника моча скапливается в нем и в почечной лоханке, вызывает атрофию ткани почки от давления на нее со стороны лоханки (гидронефроз). Дистрофия клеток. Разнообразные патологические процессы сопровождаются существенными нарушениями обмена веществ в
клетках, которые называются дистрофией (дегенерацией, перерождением). В зависимости от характера изменения обмена веществ в клетках различают белковые, жиролипоидные и углеводные дистрофии. 13.2.2. Гипербиотические процессыГипертрофия Различают несколько видов гипертрофии. Рабочая гипертрофия - к ней относятся гипертрофия скелетных мышц и сердца у спортсменов, гипертрофия молочных желез во время лактации, гипертрофия гладких мышц матки во время беременности. Рабочая гипертрофия часто сочетается с гиперплазией клеток - усилением их размножения (например, в матке при беременности). Заместительная (компенсаторная), или викарная, гипертрофия увеличение объема оставшегося органа после удаления одного из парных органов (почки, легкие, надпочечники и др.). Процесс гипертрофии сопровождается также усиленным размножением клеток поврежденного органа (гиперплазией). Регенерационная гипертрофия - увеличение оставшейся части органа после удаления некоторой его части (например, печени, поджелудочной железы, селезенки). Корреляционная гипертрофия - увеличение органа после удаления одного из функционально связанных между собой органов (например, увеличение гипофиза после удаления щитовидной железы). Нарушения функции органов при гипертрофии. Удаление парного органа вызывает характерные изменения функции в оставшемся органе при компенсаторной гипертрофии. Вначале (1-я фаза) наблюдается недостаточность функции по сравнению с функцией обоих парных органов. В дальнейшем (2-я фаза) функция гипертрофированного органа постепенно повышается, однако объем ее никогда не достигает объема деятельности двух парных органов. Обычно деятельность гипертрофированного органа составляет 60-70% объема работы двух парных органов до операции. Масса гипертрофированного органа также колеблется в пределах 60-80% массы обоих органов здорового организма.
Компенсаторная гипертрофия почки, надпочечника, легкого и других органов сопровождается увеличением скорости размножения и числа клеток в этих органах (гиперплазия). Процесс перехода гипертрофии клеток в гиперплазию выражает общебиологический закон, согласно которому делению каждой клетки предшествует увеличение ее в объеме. Активацию процесса размножения клеток можно наблюдать, считая число митозов в клетках гипертрофированного органа. Так, при компенсаторной гипертрофии почки у крыс уже через 2 суток после удаления другой почки число митозов в канальцах возрастает в 3 раза. После удаления одного легкого у крысы через 7 дней число митозов в оставшемся легком возрастает также в 3 раза. Срок достижения максимальной гипертрофии парного органа после удаления другого, как показано в эксперименте, колеблется от 20 до 180 дней в зависимости от вида органа и вида животного. Однако при компенсаторной гипертрофии парного органа полной компенсации не происходит, и организм животного или человека продолжает существовать в условиях большей или меньшей недостаточности функции оставшегося органа. Процесс компенсаторной гипертрофии в легком после удаления другого легкого начинается с явления растяжения альвеол, напоминающего эмфизему, к которому вскоре присоединяются гипертрофия альвеол, утолщение межальвеолярных перегородок, эластического каркаса и развитие капиллярной сети. Отмечается также размножение структурных компонентов межальвеолярных перегородок. Жизненная емкость и остаточный воздух в оставшемся легком после удаления другого оказываются несколько большими, чем в одном легком до операции, но значительно меньшими, чем в обоих легких. На развитие процесса гипертрофии существенное влияние оказывают характер питания животного и деятельность регулирующих систем. Установлено, что увеличение в пище белка вызывает значительное усиление процесса компенсаторной гипертрофии почек.
Гипертрофия почки может возникнуть и без удаления парного органа. Так, повреждение одной из почек (пиелонефрит, гидронефроз) сопровождается компенсаторной гипертрофией здоровой почки. Вероятным механизмом этого процесса являются нервногормональные влияния. Недостаток соматотропного гормона передней доли гипофиза после гипофизэктомии сопровождается задержкой компенсаторной гипертрофии почки. К аналогичному эффекту приводит и тиреоидэктомия. Установлено, что гормоны надпочечных желез (кортизол и кортикостерон) в какой-то степени подавляют гипертрофию, но полностью не предотвращают ее развитие. Регенерация Регенерация (возрождение) - процесс восстановления разрушенных или утраченных тканей, органов и отдельных частей живых существ. Регенерация широко распространена в природе, бывает как у растений, так и у животных. Она имеет большое значение и у здоровых, и больных людей. Различают физиологическую и патологическую регенерации. Физиологической регенерацией называется процесс постоянного восстановления клеток многоклеточного организма. Особенно интенсивно эти процессы протекают для клеток крови и эпидермальных структур (эпидермис, волосы, ногти). Патологической регенерацией называются процессы возрождения органов и тканей после их повреждения. Регенерировать могут клетки всех 4 видов тканей. Регенерация соединительной ткани. Особенно сильно выражена способность регенерации у рыхлой соединительной ткани. Вы- раженной регенераторной способностью обладает также костная ткань. Регенераторные процессы протекают в периосте, эндосте и костном мозгу. Размножающиеся малодифференцированные камбиальные клетки костной ткани - остеобласты - являются основными элементами, восстанавливающими поврежденную костную ткань. Этот процесс сопровождается резорбцией поврежденной костной ткани и рассасыванием избыточно образованной новой ткани остеокластами. Процесс регенерации костной ткани имеет большое значение при заживлении переломов костей. Хорошо регенерируют сухожилия, фасции, значительно слабее выражены регенераторные процессы в хрящевой ткани. Источником регенерации являются не сами хрящевые клетки, а перихондрии, содержащие малодифференцированные элементы - хондробласты. Жировая ткань обладает весьма слабой регенераторной способностью.
Регенерация эпителиальной ткани. Эпителиальные ткани (многослойный плоский эпителий кожи, роговая оболочка глаза) характеризуются весьма выраженной регенераторной способностью. Регенерация эпидермиса имеет очень большое значение в процессах заживления ран. Эпителий слизистых оболочек также обладает значительной генераторной способностью. Хорошо известно быстрое заживление ран в полости рта, губ, полости носа и др. Многослойный эпителий эпидермиса кожи возрождается из глубокого зародышевого слоя, однослойный цилиндрический эпителий - из элементов крипт. В случае наличия раздражающих факторов, препятствующих регенерации эпителия, слизистой оболочки (например, в желудке, мочевом пузыре), регенерация становится резко патологической, возникают атипичные разрастания эпителия, способные к злокачественному перерождению. Железистый эпителий регенерирует по-разному. Хорошо регенерирует печеночная ткань. В.В. Подвысоцкий удалял у собак 3/4 печени, и оставшаяся ткань восстанавливала целостность органа до первоначального объема. При этом имела место не столько гиперплазия - размножение клеток, сколько гипертрофия - увеличение их объема. Регенераторные процессы возможны также в эпителиальных тканях почки, слюнных желез, поджелудочной железы. Регенерация мышечной ткани. Мышечная ткань регенерирует значительно слабее соединительной ткани и эпителия. Регенерация мышечных волокон скелетной мускулатуры совершается путем амитотического деления клеток, граничащих с поврежденным участком. На концах поврежденной мышцы при этом возникают особые колбовидные выпячивания, называемые мышечными почками. Появляясь с двух концов поврежденной мышцы, эти почки сливаются, а в поврежденных мышечных волокнах восстанавливается поперечная исчерченность. Регенерация гладкой мускулатуры выражена относительно слабо, она может происходить за счет митотического деления гладкомышечных клеток.
Регенерация нервной ткани. Нервные клетки (периферической и вегетативной нервной системы, моторные и чувствительные нейроны спинного мозга, симпатических узлов и др.) регенерируют весьма слабо, хотя возможность их регенерации в настоящее время не отрицается. Аксоны нервных клеток обладают сильной регенераторной способностью. Регенерация аксонов нервных клеток головного мозга (кора, подкорковые узлы) происходит весьма слабо или отсутствует. Если перерезать периферический нерв, возникают дегенерация аксона к периферии от места перерезки и регенерация его конца, связанного с клеткой перерезанного нерва. После перерезки мякотного нерва аксоны и мембраны в периферическом отрезке подвергаются аутолизу, и продукты их резорбируются. Остаются клетки Шванна, образующие как бы трубочки, в которые и врастают регенерирующие волокна центрального конца перерезанного нерва. На концах растущих аксонов формируются колбочки и разветвления. Регенерирующие аксоны перерезанного нерва «ползут» по шванновским трубочкам периферического конца этого нерва со скоростью 1-3 мм в сутки. Таким образом, возможна регенерация аксонов до 1 м и более. Роль клеток Шванна, по-видимому, очень существенна, так как в мозгу, где их опорная и трофическая функции заменены клетками глии, регенерация нервных волокон не происходит. Если центральные и периферические концы перерезанного нерва отодвинуты далеко друг от друга, регенерирующие концы аксонов не достигают шванновских клеток периферического конца перерезанного нерва, и полная регенерация не наступает. Одним из важных процессов при регенерации аксонов нервных клеток в этом случае является образование на их концах колбовидных утолщений, пуговок. Если количество этих утолщений велико (после травмы толстого смешанного нерва), то на конце перерезанного нерва образуется опухолевидное разрастание - неврома. Окружающие ткани раздражают эти необычные окончания чувствительных нервов и вызывают резкие болевые ощущения, называемые каузалгиями.
В эксперименте предпринимались многочисленные попытки сшивать центральные концы двигательных нервов с периферическими концами чувствительных нервов, а также различные чувствительные нервы друг с другом. Эти опыты вызывали образование различных необычных рефлексов или неврогенных «химер». Если двигательный нерв, например подъязычный, сшить с периферическим концом чувствительного нерва, например язычного, то двигательные аксоны не образуют в языке чувствительных окончаний. Под эпителием возникают лишь сплетения, лишенные функционального значения. Если сшить чувствительную ветвь блуждающего нерва, например центральный конец возвратного нерва, с периферическим концом чувствительного кожного нерва, то блуждающий нерв регенерирует и образует чувствительные окончания в коже. Раздражение кожи в этих случаях может вызвать кашель наподобие того, который возникает при раздражении слизистой оболочки гортани - нормальной рефлексогенной зоны возвратного нерва. Обмен веществ регенерирующей ткани. Установлено, что уже через 2 ч после повреждения в гистиоцитах рыхлой соединительной ткани, а затем в лейкоцитах и фибробластах активируются окислительно-восстановительные ферменты (сукцинатдегидрогеназа, глутатион) и гидролазы (фосфатаза, пептидаза, липаза и др.). В дальнейшем отмечается активация 5-нуклеотидазы, АТФазы и других ферментов. Активация этих ферментов вызывает увеличение процесса расщепления белка, освобождает липиды (лецитин, жирные кислоты), которые понижают поверхностное натяжение в регенерирующих клетках. Регенерирующая ткань характеризуется активацией анаэробного гликолиза. Распад лейкоцитов и освобождение из них стимулирующих рост продуктов (нуклеопротеиды и др.) вызывают усиленное митотическое деление регенерирующих клеток. Усиление гликолиза в растущих регенерирующих клетках сопровождается накоплением молочной и пировиноградной кислот и приводит к тканевому ацидозу. Активация протеолитических ферментов приводит также к освобождению из поврежденных регенерирующих клеток гистамина. Гистамин вызывает расширение сосудов, окружающих регенерирующую ткань или врастающих в нее. Расширение сосудов улучшает поступление новых количеств лейкоцитов, доставляющих новые порции стимуляторов роста в регенерирующую ткань. В клетках этой ткани увеличиваются осмотическое давление и гидратация (содержание воды) (рис. 13-6).
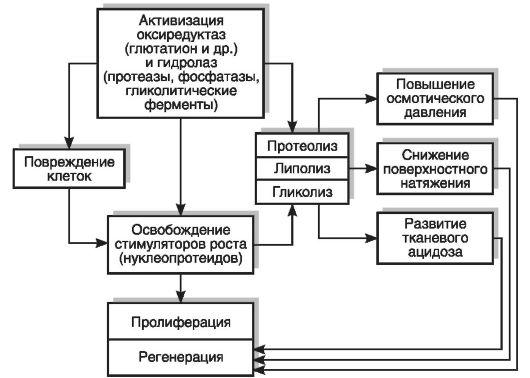 Рис. 13-6. Обмен веществ в регенерирующей ткани Рис. 13-6. Обмен веществ в регенерирующей тканиМеханизмы регенерации. Регенерировать могут как взрослые дифференцированные клетки, так и менее дифференцированные (камбиальные) клетки различных тканей (например, герминативный слой эпителиальных клеток кожи, гистиоциты рыхлой соединительной ткани), возможны превращения клеток в менее дифференцированные формы (метаплазия, анаплазия). Метаплазия у млекопитающих, однако, наблюдается в пределах только одного вида тканей, например из рыхлой соединительной ткани может образоваться хрящевая и костная ткани, из эпителия выводных протоков печени или слюнных желез - соответствующие секреторные клетки и т.д. Процесс регенерации обусловливается рядом факторов: 1. Первым и важнейшим стимулом для регенерации является повреждение. Именно продукты поврежденной ткани (протеазы, полипептиды и низкомолекулярные белки) выполняют роль стимуляторов размножения клеток. Ранее они назывались «раневые гормоны». 2. Важным фактором заживления и регенерации являются лейкоциты и продукты их распада. Эти продукты имеют собирательное название - «трефоны» (от греч. trephos - питаю). 3. На основании опытов с тканевыми культурами было установлено стимулирующее влияние одной растущей клетки данной ткани на другую. Предполагали, что это влияние определяется особыми веществами - «десмонами» (от греч. desmos - ткань). Десмоны могут выделяться в рингеровский раствор при промывании им кусочка регенерирующей ткани. Десмоны специфичны и не влияют на рост тканей другого вида (например, десмоны соединительной ткани не влияют на мышечную). 4. Большое влияние на регенерацию оказывает состояние питания организма и его регулирующих систем. При голодании регенерация хотя и происходит, но значительно слабее. Хорошо известно, что заживление ран у лиц с алиментарной дистрофией резко замедлено. Особое значение имеют полноценное белковое питание и витамины, в частности витамины С и А. У больных цингой заживление ран и переломов резко задерживается. Это показано и в эксперименте над животными с авитаминозом С. Резко стимулирующее влияние на регенерацию оказывает витамин А как при внутреннем, так и при местном (на рану) применении, например в виде рыбьего жира.
5. С увеличением возраста регенерирующая способность всех тканей понижается. При этом особое значение имеет состояние реактивности целого организма. Например, пересадка относительно «старой» по возрасту конечности молодому головастику вызывает ее хорошее приживление и регенерацию. Пересадка «молодой» конечности более старшему по возрасту головастику вызывает менее выраженную регенерацию, что говорит о влиянии целого организма на регенераторный процесс. 6. Большое значение в регуляции регенерации имеют железы внутренней секреции. Так, тиреоидэктомия снижает регенерирующую способность тканей, а введение гормонов щитовидной железы стимулирует заживление ран. Удаление поджелудочной железы приводит к замедлению заживления ран, а кастрация затрудняет заживление переломов. Гипофизэктомия вызывает значительное замедление регенерации конечностей у аксолотля. Минералокортикоиды (альдостерон) стимулируют, а глюкокортикоиды (кортизол) угнетают регенерацию. Роль зобной железы в процессах регенерации пока выяснена недостаточно. 7. Большое значение в качестве стимулятора регенерации имеет нервная система. В личиночных стадиях амфибий перерезка спинного мозга или периферических нервов не оказывает существенного влияния на регенерацию хвоста и конечностей. Однако у выс- ших млекопитающих и человека показано существенное влияние различных отделов нервной системы на регенерацию. Экспериментальные повреждения коры головного мозга у собак, кроликов и крыс задерживали процессы заживления ран. Особенно сильное влияние на регенерацию и репаративные процессы оказывают повреждения вентромедиальных ядер гипоталамуса. Разрушение этих ядер вызывает угнетение процессов заживления ран и приживления трансплантатов. Экспериментальная перерезка или травмы (военные, бытовые) смешанных периферических нервов вызывают резкие нервно-дистрофические явления. Одним из ярких выражений этого влияния является образование незаживающих трофических язв. Они возникают часто на месте случайной царапины, а иногда и без видимого повреждения. Нарушение обмена веществ в тканях, в частности в коже, приводит к ослаблению процессов регенерации эпидермиса. На поверхности кожи образуется дефект - язва, она обычно окружена вялыми грануляциями, заживает очень долго, иногда несколько лет. После временного заживления она легко возобновляется. Замедление процессов регенерации в данном случае вызывается нарушением трофического влияния нервной системы и сосудодвигательными расстройствами в денервированной ткани.
Заживление ран Заживление ран является типичным примером патологической регенерации тканей, наступающей после их повреждения. Заживление повреждений внутренних органов происходит за счет размножения элементов соединительной ткани с последующим превращением ее в рубец. Заживление кожи осуществляется также за счет соединительной ткани и сопровождается регенерацией эпителия. Легкие повреждения эпидермиса кожи восстанавливаются полностью за счет регенерации эпидермиса. Различают заживления первичным и вторичным натяжением. Заживление первичным натяжением - края раны склеиваются фибрином, вышедшим в рану с кровью и лимфой. Начинается процесс свертывания крови в ране и выпадение фибрина. В случае больших количеств выпавшего фибрина последний образует корку - струп, под которым совершается заживление. После заживления струп отпадает. Особенностью химического состава струпа является большое (13-14%) содержание в нем гидроксипролина. Сущность начала заживления как первичным, так и вторичным натяжением заключается в том, что под краями раны скапливаются лейкоциты, которые выделяют вещества, стимулирующие размножение прежде всего соединительнотканных клеток - гистиоцитов. Последние превращаются в фибробласты, образующие коллагеновые и эластические волокна. Постепенно дефект в ткани заполняется этими клетками. Одновременно к пленке фибрина начинают двигаться размножающиеся клетки эпидермиса. Стимулом для размножения этих клеток является факт соприкосновения их с необычной средой - выпавшим в рану фибрином. Размножаясь, клетки эпителия заполняют и затягивают дефект, вызванный ранением. Возникает полное заживление. Заживление вторичным натяжением происходит обычно при инфицировании раны (нагноении) или при ее относительно больших размерах, когда рана не может первично быть склеенной выпавшим фибрином. В этих случаях, кроме процессов, характерных для первичного натяжения, рана постепенно заполняется новой, молодой соединительной тканью, очень богатой кровеносными сосудами. Она приобретает ярко-красный цвет и имеет вид зернышек, связанных друг с другом, отсюда и название «грануляционная» (от лат. granulum - зернышко). Грануляционная ткань образуется за счет размножения гистиоцитов и фибробластов, со стороны здоровой ткани в нее врастают кровеносные сосуды. Грануляционная ткань весьма богата водой, ее коллоиды находятся в состоянии гидратации. Грануляционная ткань - это защитный барьер против инфекции. При попытке инфицирования кролика палочкой сибирской язвы через грануляционную ткань все микробы поглощались клетками соединительной ткани, и заражение не наступало. При заражении той же дозой палочки сибирской язвы под кожу здоровый кролик погибал через несколько часов. После заполнения грануляционной тканью раны в ней начинают происходить изменения. Кровеносные сосуды затягиваются, клетки постепенно разрушаются и рассасываются. Остаются только волокна субстанции соединительной ткани, образующие рубец. Эпителизация раны после заживления вторичным натяжением не происходит, и рубец (например, на коже) остается видимым многие годы. +7. Различные стадии процесса заживления раны: а - в момент нанесения раны (она заполняется кровью, выпавшие нити фибрина соединяют края раны); б - через день (в рану поступают нейтрофилы, начинается фагоцитоз); в - через 2 дня (края эпидермиса смыкаются, в рану проникают моноциты, фибробласты); г - через 7 дней (струп отторгается, в ране остается немного моноцитов, нейтрофилов, образуется грануляционная ткань) (по Россу) Опухоли. Характеристика понятия. Биологические особенности доброкачественных и злокачественных опухолей. Опухолевый рост - типовая форма нарушения тканевого роста, возникающая под действием канцерогена. Характерезуется атипизмом роста, обмена веществ, структуры и функции. Опухолевый рост проявляется патологическим разрастанием ткани с атипичными свойствами. Согласно цитологической и гистологической структуре опухолевых клеток и тканей выделяют доброкачественные и злокачественные опухоли. Доброкачественные опухоли. Клетки их морфологически похожи на нормальные и формируют характерные для данной ткани,высокодифференцированные структуры. Такие опухоли растут медленно и, как правило, не метастазируют. Злокачественные опухоли. Клетки их морфологически отличаются от нормальных и образуют низкодифференцированные тканевые структуры. Эти опухоли растут быстро, инвазируют в соседние ткани, формируют метастазы. Выделяют следующие разновидности злокачественных опухолей: ♦ Карциномы - злокачественные опухоли, происходящие из эпителия. ♦ Саркомы - злокачественные опухоли, возникающие из тканей мезенхимального происхождения (соединительных, костной, хрящевой). Этиология Инициальным звеном опухолевого роста является образование опухолевых клеток под воздействием канцерогенов. Опухолевая трансформация - процесс превращения нормальных клеток в опухолевые вследствие трансформации нормальной генетической программы в программу формирования опухолевого атипизма. ПРИЧИНЫ Факторы химической, физической и биологической природы, способные вызвать опухолевую трансформацию, называют канцерогенами. • Химические канцерогены. Более 75% случаев злокачественных опухолей человека вызвано воздействием химических факторов внешней среды. К возникновению опухолей приводят преимущественно продукты сгорания табака, некоторые компоненты пищи и промышленные соединения. Известно более 1500 химических соединений, обладающих канцерогенным эффектом. Из них не менее 20 опре- делённо являются причиной опухолей у человека. Например, к ним отнесены 2-нафтиламин, бензидин, 2-аминотиофенил, вызывающие рак мочевого пузыря у работников анилинокрасочной и резиновой промышленности; бис-(хлорметил)-эфир, приводящий к возникновению рака бронхов и лёгких. • Физические канцерогены: ионизирующее излучение (α-, β- и γ-излучение), рентгеновские и ультрафиолетовые лучи, поток нейтронов. Так, врачи-рентгенологи заболевают лейкозами в 8-9 раз чаще, чем врачи других специальностей. • Онкогенные вирусы. ♦ ДНК-вирусы, вызывающие опухолевую трансформацию, называют онковирусами. Гены ДНК-онковирусов способны непосредственно внедряться в геном клетки-мишени. Участок ДНК-вируса (собственноонкоген), интегрированный с клеточным геномом, может осуществить опухолевую трансформацию клетки. Не исключают также, что один из генов онковируса может играть роль промотора клеточного протоонкогена. К ДНК-содержащим онковирусам относят некоторые аденовирусы, паповавирусы и герпесвирусы (так, вирус Эпстайна-Барр вызывает развитие лимфом, а вирус гепатита B способен инициировать рак печени). ♦ РНК-содержащие вирусы, относящиеся к ретровирусам. Интеграция РНК-генов ретровирусов в клеточный геном происходит не непосредственно, а после образования их ДНК-копий. УСЛОВИЯ, СПОСОБСТВУЮЩИЕ ВОЗНИКНОВЕНИЮ ОПУХОЛЕЙ (ФАКТОРЫ РИСКА) Наследственные факторы. Существует не менее 300 так называемых семейных форм злокачественных опухолевых заболеваний. В ряде
случаев генетическая природа предрасположенности к возникновению опухолей определена. К числу наиболее значимых относятся следующие: • Аномалии генов, контролирующих процесс репарации ДНК. Это определяет повышенную чувствительность к канцерогенным воздействиям. • Аномалии генов-супрессоров опухолевого роста. Выявлены при новообразованиях толстой кишки и поджелудочной железы (делеция 18q21.1), множественном канцероматозе (потеря гетерозиготности в 10q23). • Аномалии генов синтеза молекул межклеточного взаимодействия, например, E-кадгерина (расположенного в 16q22.1). Уменьшение экспрессии E-кадгерина - один из молекулярных механизмов, способствующих инвазии и метастазированию опухоли. • Другие генные и хромосомные дефекты: мутации гена рецептора андрогенов (расположенного в хромосоме X) вызывают рак молочной железы у мужчин; различные хромосомные дефекты зарегистрированы при лейкозах; аномалии хромосом 8 и 9 выявляются при наследственных формах меланом кожи. Низкая активность механизмов противоопухолевой защиты организма (см. ниже). Патогенез Клетка под воздействием канцерогена претерпевает ряд последовательных изменений, которые приводят к опухолевому росту. Механизм развития опухолевого роста называют канцерогенезом. ОБЩИЕ ЭТАПЫ КАНЦЕРОГЕНЕЗА Вне зависимости от конкретной причины опухолевой трансформации клетки, гистологической структуры и локализации новообразования, в процессе канцерогенеза можно выделить несколько общих этапов • На первом этапе происходит взаимодействие канцерогенов химической, физической или биологической природы с протоонкогенами и антионкогенами (онкосупрессорами) генома нормальной клетки. • На втором этапе канцерогенеза (в результате воздействия канцерогена на геном) подавляется активность антионкогенов и происходит трансформация протоонкогенов в онкогены. Последующая экспрессия онкогена - необходимое и достаточное условие для опухолевой трансформации.
• На третьем этапе канцерогенеза, в связи с экспрессией онкогенов, синтезируются и реализуют свои эффекты (непосредственно или с участием клеточных факторов роста и рецепторов к ним) онкобелки. С этого момента генотипически изменённая клетка приобретает опухолевый фенотип. +• Четвёртый этап канцерогенеза характеризуется пролиферацией и увеличением числа опухолевых клеток, что ведёт к формированию новообразования (опухолевого узла). Этиология опухолей. Современные теории возникновения злокачественных опухолей. |
