|
|
Лекции по органической химии 1 курс. Введение органическая химия
Способы получения алкенов
В природе этиленовые углеводороды (олефины; алкены) встречаются довольно редко. Иногда низшие олефины в небольших количествах растворены в нефти и входят в состав попутного нефтяного газа. Лишь в некоторых месторождениях нефть содержит значительные количества высших олефинов (например, канадская нефть). Довольно много этиленовых углеводородов получается при крекинге и пиролизе углеводородов нефти и содержатся в крекинг-бензинах. Важным источником этилена, пропилена и бутиленов служат получающиеся при этом газы (газы крекинга); в таблице приведены данные о содержании в них непредельных углеводородов в зависимости от вида переработки нефтепродуктов.
Некоторые данные о содержании непредельных углеводородов в газах образующихся при крекинге и пиролизе высших фракций нефти
Вид переработки |
Содержание, %
|
этилена
|
пропилена
|
бутилена
|
изобутилена
|
бутана
|
Жидкофазный крекинг
|
2,1
|
12,4
|
10,3
|
-
|
10,6
|
Парофазный крекинг
|
19,8
|
22,4
|
10,0
|
6,9
|
2,0
|
Каталитичесий крекинг
|
1,2
|
6,8
|
3,3
|
0,5
|
47,9
|
пиролиз
|
20,4
|
17,8
|
4,0
|
6,0
|
1,0
|
При крекинге цепи молекул углеводорода разрываются в различных местах и между образующимися в виде "осколков" радикалами с более короткими цепями перераспределяется водород. Таким образом, получается смесь более коротких непредельных углеводородов. Например:
 СН2=СН2 + СН3—СН2—СН3 СН2=СН2 + СН3—СН2—СН3
СН3—СН2—СН2—СН2—СН3 СН2—СН=СН2 + СН3—СН3
пентан СН3—СН2—СН=СН2 + СН4
(этилен и пропан; пропилен и этан; бутилен и метан.)
Дегидрирование алканов
В присутствии катализаторов при высокой температуре происходит отщепление водорода (реакция дегидрирования) от молекул насыщенных углеводородов с образованием двойных связей. Так, при пропускании бутана над катализатором, содержащим окислы тяжелых металлов (например, Cr2O3), при температурах 400-600 оС образуется смесь бутенов:
 СН3—СН2—СН2—СН3 СН2=СН—СН2—СН3 + Н2 СН3—СН2—СН2—СН3 СН2=СН—СН2—СН3 + Н2
бутан СН3—СН=СН—СН3 + Н2 (бутилены)
Этот метод дает особую возможность использовать в качестве сырья для химической промышленности попутный нефтяной газ. Последний, как уже знаем, содержит метан, этан, пропан и бутан. Путем дегидрирования их переводят в непредельные углеводороды, являющиеся исходными веществами для многих синтезов.
Отдельные представители алкенов
Этен (этилен). Как уже было указано, этилен может быть получен из этилового спирта действием концентрированной H2SO4. В промышленности используют этилен газов крекинга, а так же этилен, получаемый дегидрированием этана, входящего в состав попутного нефтяного газа. Этилен – бесцветный горючий газ, почти без запаха; в воде при 0 оС растворяется до ¼ объема этилена. (Теплота сгорания 11200 ккал/кг, температура самовоспламенения 540 оС; область воспламенения 3-32 % объемных; в воздухе горит слабокоптящим пламенем.) (Минимально взрывоопасное содержание кислорода при разбавлении этилено-воздушных смесей углекислым газом 12,1 % объемн.; азотом 10 % объемн.; максимальная нормальная скорость горения 0,74 м/сек; Температура горения = 2112 оС. Устойчив, приблизительно, до температуры 350 оС. Выше этой температуры начинает разлагаться на метан и ацетилен. При более высоких температурах этилен разлагается на ацетилен и водород. Для предотвращения взрыва при аварийном истечении этилена и тушения факела в закрытых объемах необходима минимальная концентрация СО2 – 42 % объемн.; азота – 52 % объемн.)
Этилен находит применение как исходное вещество для синтеза этанола, различных галогенпроизводных, окиси этилена, иприта, для получения полиэтилена других синтетических высокополимеров. Имеет значительное применение для ускорения созревания овощей и фруктов. Для этой цели при 18-20 оС достаточно добавить к воздуху 0,005-0,01 объемного процента этилена.
Пропен (пропилен) входит в состав газов крекинга. Может быть получен дегидированием пропана, входящего в состав попутного нефтяного газа. Служит сырьем для получения глицерина и изопропилового спирта; из последнего затем получают ацетон. Полимеризацией пропилена получают полипропилен:
nCH2=CH ...CH2—CH—CH2—CH—CH2—CH—...
CH3 CH3 CH3 CH3
пропилен полипропилен
В качестве катализатора используют смесь триэтилалюминия Al(C2H5)3 с четыреххлористым титаном TiCl4 (катализатор Циглера-Натта).
(Полипропилен по ряду свойств превосходит полиэтилен. Имеет более высокую температуру плавления (164-170 оС), чем полиэтилен. Молекулярный вес 60000-200000. Стоек к действию кислот и масел даже при повышенной температуре. Полипропиленовая пленка прозрачнее полиэтиленовой. Вследствие большей устойчивости ее к действию теплоты пищевые продукты, упакованные в полипропленовую пленку, могут быть подвергнуты стерилизации. По имеющимся данным, волокно из полипропилена по прочности превосходит все другие синтетические волокна.)
Пропилен бесцветны горючий газ. (Теплота сгорания 10900 ккал/кг; растворимость в воде незначительна. Температура самовоспламенения 410 оС; область воспламенения 2,2-10,3 % объемн; максимальная нормальная скорость горения 0,683 м/сек. Минимальное взрывоопасное содержание кислорода при разбавлении пропиленово-водушных смесей углекислым газом – 14,6 % объемн.; азотом – 11,9 % объемн. Для предупреждения взрыва при аварийном истечении пропилена и тушения факела в закрытых объемах минимальная концентрация СО2 – 305 объемн.; азота – 43 % объемн.)
Бутилены (1-бутен и 2-бутен), (изобутилен) – бесцветные горючие газы. Вместе с бутаном их выделяют из паров крекинга (бутан- бутиленовая фракция). Путем дегидрирования эту смесь превращают в 1,3-бутадиен- исходное сырье для получения одного из видов синтетического каучука. (Теплота сгорания 10800 ккал/кг; Температура самовоспламенения 384 оС, область воспламенения 1,69-9,4% объемн.)
При полимеризации изопропилена с катализаторами (фтористый бор-BF3 или хлористый алюминий AlF3) ценный высокополимер – полиизобутилен:
СН3 СН3 СН3 СН3 СН3 СН3
...+СН2=С + СН2=С + С=СН3 +... ...—СН2—С—СН2—С—С—СН2—...
СН3 СН3 СН3 СН3 СН3 СН3
молекулы изобутилена полиизобутилен
Лекция: Ненасыщенные углеводороды (алкадиены, алкины).
Диеновые углеводороды (алкадиены)
Диеновыми углеводородами или алкадиенами, называются ненасыщенные углеводороды с открытой цепью углеродных атомов, в молекулах которых имеются две двойные связи. Состав этих углеводородов может быть выражен формулой СnH2n-2.
Номенклатура и классификация
Индивидуальные углеводороды с двумя двойными связями называют, пользуясь принципами международной заместительной номенклатуры для алкенов, с той лишь разницей, что в наименовании перед окончанием – ен, обозначающим двойную связь, ставят греческое числительное –ди, так образуется родовое для этих углеводородов окончание – диен (отсюда и название диеновые). Перед названием основы (т.е. главной цепи, включающей обе двойные связи) ставят цифры, обозначающие номера углеродных атомов, за которыми следуют двойные связи. Отдельные представители имеют также и тривиальные названия.
Диеновые углеводороды, в которых две двойные связи находятся рядом и не разделены простыми связями, называют углеводородами с кумулированными двойными связями. Например:
1 2 3
СН2=С=СН2 1,2-пропадиен (аллен)
При нагревании в присутствии щелочи диеновые углеводороды с кумулированными двойными связями (аллены) могут перегруппировываться в алкины, например:
t, ОН-
СН3—СН=С=СН—СН3 СН3—СН2—СС—СН3
2,3-пентадиен 2-пентин
Диеновые углеводороды, в молекулах которых две двойные связи разделены двумя или более простыми связями, называются углеводородами с изолированными двойными связями. Например:
1 2 3 4 5 1 2 3 4 5 6
СН2=СН—СН2—СН=СН2 СН2=СН—СН2—СН2—СН=СН2 1,4-пентадиен 1,5-гексадиен (диаллил) (аллил СН2=СН—СН2— )
Ненасыщенные углеводороды ряда ацетилена (алкины) Углеводородами ряда ацетилена или ацетиленовыми углеводородами называют ненасыщенные углеводороды, в молекулах которых имеется тройная связь, т.е. группировка —СС—. Гомология, изомерия и номенклатура Состав каждого члена гомологического ряда ацетиленовых углеводородов может быть выражен общей эмпирической формулой СnH2n-2. Простейшим членом этого ряда является углеводород ацетилен состава С2Н2, строение которого выражают структурная и упрощенная структурная формулы: Н—СС—Н и СНСН Гомологи ацетилена можно рассматривать как его производные, образовавшиеся в результате замещения одного или обоих атомов водорода в молекуле ацетилена на углеводородные радикалы. Изомерия. Возможны два типа ацетиленовых соединений R—C C—Н и R—CC—R'. (Линейная геометрия тройной связи делает невозможной цис- и транс-изомерию алкинов.) В соединениях первого типа при углероде с тройной связью имеется водород, в соединения второго типа при атомах углерода с тройной связью водорода нет. Изомерия ацетиленовых углеводородов, так же как и этиленовых, обусловлена изомерией углеродного скелета и изомерией положения кратной связи. Интересно отметить, что общая формула состава ацетиленовых углеводородов СnH2n-2 аналогична общей формуле состава диеновых углеводородов. Иначе говоря, непредельные углеводороды с двумя двойными связями изомерны непредельным углеводородам с одной тройной связью. Например, 1,3-бутадиен СН2=СН—СН=СН2 изомерен двум ацетиленовым углеводородам: СН3—СН2—ССН (1) и СН3—СС—СН3 (2). Все эти углеводороды имеют состав С4Н6. Номенклатура Международная заместительная номенклатура. Ацетиленовые углеводороды называют по заместительной номенклатуре так же, как предельные, с той лишь разницей, что наличие тройной связи обозначают путем замены в заместительном названии предельного углеводорода окончания –ан на –ин. Поэтому углеводороды с тройной связью по международной номенклатуре объединяют общим названием – алкины. Перед основой названия ставят цифру, соответствующую номеру углеродного атома главной цепи молекулы, за которым следует тройная связь. Принцип выбора главной цепи и нумерации атомов такой же, как в случае этиленовых углеводородов. Таким образом, ацетиленовые углеводороды, формулы которых написаны выше, называют так: (1)- 1-бутин и (2) – 2-бутин. Углеводород строения СН3 5 4 3 2 1 СН3—СН – СС—СН3 (3) может быть назван: 4-метил-2-пентин. Рациональная номенклатура. По рациональной номенклатуре углеводороды с тройной связью рассматривают как производные ацетилена, в названии указывают наименования радикалов, связанных с группировкой —СС—, а в конце названия ставят слово ацетилен. Поэтому приведенные выше углеводороды называют следующим образом: (1) – этилацетилен; (2) – диметилацетилен; (3) – метилизопропилацетилен. Свойства ацетиленовых углеводородов (алкинов) Физические свойства. Зависимости изменения физических свойств в гомологических рядах ацетиленовых углеводородов по мере возрастания числа атомов углерода в их молекулах аналогичны тем зависимостям, которые наблюдаются в рядах предельных и этиленовых углеводородов. Простейшие гомологи нормального строения до С5Н8 – газы, от С5Н8 до С16Н30 – жидкости, высшие ацетиленовые углеводороды – твердые тела. Все эти соединения бесцветны. Химические свойства. Ацетиленовым углеводородам, так же как этиленовым, свойственны реакции присоединения по месту кратной связи, в данном случае тройной. Тройная связь, так же как и двойная, по характеру отличается от простой связи. Она осуществляется тремя парами обобщенных электронов. Из них, как и в случае двойной связи, одна пара осуществляет простую связь (-связь), а две другие электронные пары находятся в особом состоянии (-связи); осуществляемые ими связи проявляют повышенную склонность к поляризации. Этим обуславливаются реакции присоединения по месту тройной связи. Последние идут ступенчато: вначале тройная связь разрывается в двойную, и образуются производные этиленовых углеводородов. Затем разрывается и двойная связь, превращаясь в простую с образованием производных предельных углеводородов. При энергичном химическом воздействии возможен распад молекул с разрывом углеродной цепи по месту тройной связи. Отдельные представители Ацетилен. Представляет собой бесцветный горючий и взрывоопасный газ; Ткип. –83,6 оС. Теплота сгорания 48116 Кдж/моль; 1 объем С2Н2 растворяется в 1 объеме воды при 20 оС. Температура самовоспламенения 335 оС; нижний предел воспламенения 2,5 % объемных, верхний предел воспламенения в воздухе зависит от энергии источника зажигания. Ацетилен разлагается с большим выделением тепла и, при определенных условиях, со взрывом. Для предупреждения взрыва при аварийном истечении ацетилена и тушения факела в закрытых объемах минимальная концентрация СО2 57 % объемных, азота – 70 % объемных. В чистом виде почти не имеет запаха; неприятный запах технического ацетилена обусловлен наличием в нем примесей. На воздухе ацетиле горит сильно коптящим пламенем. В технике громадное количество ацетилена получают действием воды на карбид (ацетиленид) кальция СаС2 по реакции (Велер, 1862г.):  С CН С CН  III Ca + 2HOH III + Ca(OH)2 III Ca + 2HOH III + Ca(OH)2 C CН карбид кальция В свою очередь карбид кальция получают в электрических печах из негашеной извести и угля: СаО + 3 С СаС2 + СО Очень важным современным методом получения ацетилена является термоокислительный крекинг метана, входящего в состав природных газов (при температуре свыше 1500 оС). Теплота выделяется при сгорании метана в присутствии недостаточного количества кислорода: 1500 оС 6СН4 + 4О2 СНСН + 8Н2 + 3СО + СО2 + Н2О Ацетилен является ценным исходным веществом для многих промышленных синтезов. Из него по реакции Кучерова получают уксусный альдегид, который затем переводят либо в уксусную кислоту, либо в этиловый спирт. Ацетилен служит исходным материалом для получения особого вида синтетического каучука (полихлоропренового), пластмасс, из него получают различные растворители; он может быть исходным веществом для синтеза ароматических углеводородов и т.п. Все эти крайне разнообразные и ценные продукты, главным образом, получаются через ацетилен из весьма доступного сырья – извести и угля или из метана природного газа. Ацетилен широко применяли для освещения; с этой целью использовали специальные горелки, в которых происходило хорошее смешение ацетилена с воздухом и получалось яркое пламя. Если в пламя горящего ацетилена вдувать кислород, то достигается высокая температура, при которой плавятся металлы. На этом основано применение ацетилена для автогенной сварки. Ацетилен очень опасен в обращении. С воздухом или с кислородом образует гремучую смесь (1 объем ацетилена и 2,5 объема кислорода); сильно взрывчаты ацетилениды серебра и меди. Для работы ацетилен, получив его тем или иным способом, либо сазу же пускают в реакцию, либо предварительно набирают в стальные баллоны, в которых его растворяют в ацетоне под давлением 12-15 атмосфер.
Лекция: Ароматические углеводороды (арены)
Ароматическими соединениями обычно называют карбоциклические соединения, в молекулах которых имеется особая циклическая группировка из шести углеродных атомов – бензольное ядро. Простейшим веществом, содержащим такую группировку, является углеводород бензол; все остальные ароматические соединения этого типа рассматривают как производные бензола.
Благодаря наличию в ароматических соединениях бензольного ядра они по некоторым свойствам значительно отличаются от предельных и непредельных алициклических соединений, а также и от соединений с открытой цепью. Отличительные свойства ароматических веществ, обусловленные наличием в них бензольного ядра, обычно называют ароматическими свойствами, а бензольное ядро – соответственно ароматическим ядром.
Следует отметить, что само название “ароматические соединения” теперь уже не имеет своего первоначального прямого значения. Так были названы первые изученные производные бензола, потому что они обладали ароматом или же были выделены из природных ароматических веществ. В настоящее же время к ароматическим соединениям относят многие вещества, обладающие и неприятными запахами или совсем не пахнущие, если в его молекуле содержится плоское кольцо с (4n + 2) обобщенными электронами, где n может принимать значения 0, 1, 2, 3 и т.д., - правило Хюккеля.
Ароматические углеводороды ряда бензола.
Первый представитель ароматических углеводородов – бензол – имеет состав C6H6 . Это вещество было открыто М.Фарадеем в 1825 г. в жидкости, образующейся при сжатии или охлаждении т.н. светильного газа, который получается при сухой перегонке каменного угля. Впоследствии бензол обнаружили (А.Гофман, 1845г.) в другом продукте сухой перегонки каменного угля – в каменноугольной смоле. Он оказался весьма ценным веществом и нашел широкое применение. Затем было установлено, что очень многие органические соединения являются производными бензола.
Строение бензола.
Долгое время оставался неясным вопрос о химической природе и о строении бензола. Казалось бы, что он представляет собой сильно непредельное соединение. Ведь его состав C6H6 по соотношению атомов углерода и водорода отвечает формуле CnH2n-6, тогда как соответствующий по числу углеродных атомов предельный углеводород гексан имеет состав C6H14 и отвечает формуле CnH2n+2. Однако бензол не дает характерных для непредельных соединений реакций; он, например, не обеспечивает бромной воды и раствора KMnO4, т.е. в обычных условиях не склонен к реакциям присоединения, не окисляется. Напротив, бензол в присутствии катализаторов вступает в характерные для предельных углеводородов реакции замещения, например, с галогенами:
C6H6 + Cl2 C6H5Cl + HCl
Выяснилось все же, что в определенных условиях бензол может вступать и в реакции присоединения. Там, в присутствии катализаторов он гидрируется, присоединяя 6 атомов водорода:
C6H6 + 3H2 C6H12
Под действием света бензол медленно присоединяет 6 атомов галогена:
C6H6 + 3Cl2 C6H6Cl6
Исследование бензола с применением новейших методов указывает на то, что в его молекуле между углеродными атомами нет ни обычных простых, ни обычных двойных связей.. В бензоле углеродные атомы соединены при помощи особых, равноценных между собой связей, которые были названы ароматическими связями. По природе своей они отличаются от двойных и простых связей; наличие их и обуславливает характерные свойства бензола. С точки зрения современных электронных представлений природу ароматических связей объясняют следующим образом.
Как уже было указано ранее, простая связь между атомами углерода осуществляется одной парой, а двойная – двумя парами обобщенных электронов. Одна из электронных пар двойной связи находится в таком же состоянии, как пара электронов, осуществляющая простую связь (-связь). Вторая же электронная пара осуществляет связь особого характера (π-связь). В соответствии с формулой Кекуле в бензоле должны быть три π-связи. На самом же деле в бензоле нет обычных пар π-электронов фиксированных между двумя определенными С-атомами, как это изображает схема I. В шестичленном цикле бензола все простые связи С-С и С-Н (-связи) лежат в одной плоскости. Облака π-электронов всех С-атомов, имеющие форму объемных восьмерок, направлены перпендикулярно плоскости бензольного кольца. Каждое из таких облаков перекрывается облаками двух соседних углеродных атомов. Это показано на следующем рисунке:
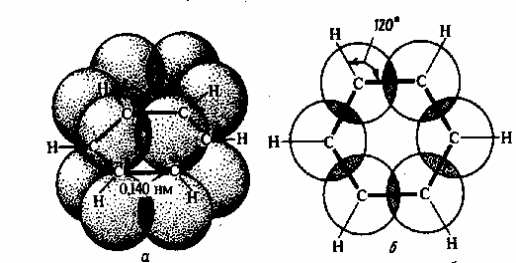
Рис. 9. Взаимное перекрывание 2р-орбиталей в молекуле бензола:
а – вид сбоку, б – вид сверху.
Плотность облаков π-электронов в бензоле равномерно распределена между всеми С-С-связями. Следовательно, π-электроны обобщены всеми углеродными атомами кольца, образуя единое кольцевое облако шести электронов (ароматический электронный секстет). Таким образом объясняется равноценность (выравненность) ароматических связей, придающих бензольному ядру характерные (ароматические) свойства. Равномерное распределение облака π-электронов и выравненность связей в бензоле иногда изображают формулой (4). И в настоящее время бензол продолжают изображать формулой Кекуле (1). Но всегда надо помнить, что она неверно отражает характер связей в бензоле.
Очень часто для простоты формулу бензола по Кекуле представляют шестиугольником с двойными связями без символов углерода и водорода (2). Иногда можно встретить изображение бензола и просто шестиугольником (3); но такой способ не рекомендуется, так принято изображать кольцо циклогексана; следовательно, в каждом его углу подразумевается группа СН2, а не СН. В последние годы, когда хотят подчеркнуть выравненность связей в бензоле, его изображают шестиугольником с кружочком внутри (4).
   НС (1) (2) (3) (4) НС (1) (2) (3) (4)
     НС СН НС СН
 
   НС СН НС СН
НС
Гомологи бензола.
Гомологи бензола представляют собой его производные, образованные в результате замещения атомов водорода бензольного ядра предельными углеводородными заместителями; состав их, так же как и бензола, выражает формулой Сn Н2n-6.
Гомологи бензола, так же как и другие соединения, в которых наряду с бензольным ядром имеются ацикличические группировки (группировки жирного ряда), иногда называют жирноароматическими соединениями.
Число ароматических соединений, содержащих ядра бензола, очень велико, и они находят большое и разнообразное применение. Основой их являются ароматические углеводороды, среди которых различают: а) ароматические углеводороды ряда бензола, содержащие одно бензольное ядро (одноядерные), и б) многоядерные ароматические углеводороды, содержащие два и более бензольных ядер. Среди них различают: а) ароматические углеводороды с конденсированнымибензольными ядрами; в них два или несколько ядер имеют общие углеродные атомы; б) ароматические углеводороды с неконденсированными бензольными ядрами, в которых каждое ядро изолировано, т.е. не имеет общих с другими ядрами углеродных атомов.
Все остальные одноядерные и многоядерные ароматические соединения являются замещенными производными соответствующих ароматических углеводородов.
    8 1 8 9 1 8 1 8 9 1

7          9 2 7 2 дифенил 9 2 7 2 дифенил
6 3 6 3 С12Н10
5 10 4 5 10 4
нафталин антрацен —СН2—
C10H8 C14H10
дифенилметан
      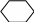  —СН— —CH2—CH2— —СН— —CH2—CH2—
I
CH3 1,1-дифенилэтан 1,3-дифенилэтан (дибензил)
  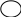 
—CH=CH—
с    имм-дифенилэтилен имм-дифенилэтилен
   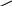
  —CC— CH —CC— CH

д ифенилацетилен ифенилацетилен
трифенилметан
Номенклатура и изомерия.
В названиях гомологов бензола указывают наименования заместителей, соединенных с бензольным ядром, и, если требуется, их число. Простейшим в этом ряду является метилбензол С6Н5 –СН3; за ним следует этилбензол С6Н5-СН2-СН3. Т.к. в бензоле все водородные атомы равноценны, эти соединения, являющиеся его однозамещенными производными, не имеют изомеров, строение их можно представить формулами:
CH3 СН2—СН3
 
 
метилбензол этилбензол
(толуол)
В ряду ароматических углеводородов часто применяют тривиальные названия, например, метилбензол иначе называют толуолом.
По международной номенклатуре (правила ИЮПАК) все ароматические углеводороды объединяют названием – арены. Соответственно, их одновалентные остатки, образованные отнятием водорода от углеродных атомов ядра (одновалентные ароматические радикалы), называют арилами и обозначают - Ar. Остаток бензола – С6Н5 называется фенилом, строение его можно обозначить символом
   
   — (радикал фенил) — (радикал фенил)
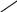 ; ;
или
Ациклические (жирные) остатки, соединенные с бензольным ядром, называют боковыми цепями.
Этилбензолу изомерны двухзамещенные гомологи бензола, содержащие в соединении с ароматическим ядром два метильных остатка (заместителя) С6Н5(СН3)2. Они называются диметилбензолами или ксилолами.
Если в бензоле имеется не один, а несколько заместителей, то для обозначения их положения углеродные атомы ядра нумеруют. Взаимное расположение двух заместителей (Х) в ядре бензола обозначают специальными символами: 1,2-(или, что то же, 1,6-) положение, т.е. когда заместители находятся рядом (при соседних углеродах), называют орто – (или сокращенно О-) положением; 1,3-(или, что то же, 1,5-) положение, т.е. когда заместители расположены через один углерод друг от друга, называют мета-(или м-) положением; наконец, 1,4-положение, когда заместители расположены друг от друга через два углерода, называют пара (или п-) положением:
Х Х Х
   1 1 1 1 1 1
6    2 Х 6 2 6 2 2 Х 6 2 6 2
5 3 5 3 5 3 3 5 3 5 3
 4 4 Х 4 4 4 Х 4
Х
орто- мета- пара-
Очевидно, что для гомологов бензола возможны заместители двух типов: образованные отнятием водорода от углеродного атомов бензольного ядра (собственно арилы), либо от атомов углерода боковой цепи. Так, из толуола СН3—С6Н5 за счет бензольного ядра образуетсяся остаток толил СН3—С6Н4—, а за счет боковой метильной группы – бензил С6Н5—СН2—. При этом в бензольном ядре водород может быть отнят от углерода в орто-, мета- и пара- положении к метильной группе; таким образом, толилов может быть три:
СН3 СН3 СН3
     1 1 1 1 1 1
6    2 6 2 6 2 —СН2— 2 6 2 6 2 —СН2—
5 3 5 3 5 3 3 5 3 5 3
 4 4 4 4 4 4
о-толил м-толил п-толил бензил
Двухвалентные остатки ароматических углеводородов объединяют названием арилены. Для бензола возможны три двухвалентных радикала С6Н4—, называемых фениленами:
   1 1 1 1 1 1
6    2 6 2 6 2 2 6 2 6 2
5 3 5 3 5 3 3 5 3 5 3
 4 4 4 4 4 4
о-фенилен м-фенилен п-фенилен
Физические свойства.
Бензол и его простейшие гомологи – бесцветные жидкости с характерными запахами, не смешивающиеся с водой. Некоторые высшие гомологи – твердые вещества. Температуры кипения и плавления ароматических углеводородов зависят от величины и изомерии боковых целей, а также от взаимного положения их в бензольном ядре.
Химические свойства
Как уже было указано, бензол, несмотря на то, что по составу он является ненасыщенным соединением, проявляет склонность преимущественно к реакциям замещения, и бензольное ядро очень устойчиво. В этом заключаются свойства бензола, которые называют ароматическими свойствами. Последние характерны и для других ароматических соединений; однако различные заместители в бензольном ядре влияют на его устойчивость и реакционную способность; в свою очередь бензольное ядро оказывает влияние на реакционную способность соединенных с ним заместителей. Рассмотрим следующие группы реакций ароматических углеводородов: а) реакции замещения, б) реакции присоединения и в) действие окислителей.
|
|
|
 Скачать 1.47 Mb.
Скачать 1.47 Mb. СН2=СН2 + СН3—СН2—СН3
СН2=СН2 + СН3—СН2—СН3 СН3—СН2—СН2—СН3 СН2=СН—СН2—СН3 + Н2
СН3—СН2—СН2—СН3 СН2=СН—СН2—СН3 + Н2 
 С CН
С CН III Ca + 2HOH III + Ca(OH)2
III Ca + 2HOH III + Ca(OH)2 




 НС СН
НС СН

 8 1 8 9 1
8 1 8 9 1









 — (радикал фенил)
— (радикал фенил)
 3 5 3 5 3
3 5 3 5 3  4 4 Х 4
4 4 Х 4 4 4 4
4 4 4