онкобил. 1. Эпидемиология рака
 Скачать 1.79 Mb. Скачать 1.79 Mb.
|
|
Компьютерная томография (КТ), или рентгеновская компьютерная томография (РКТ) - рентгеновский метод исследования, основанный на компьютерной обработке данных о степени поглощения рентгеновского излучения в разных точках изучаемого пространства. КТ как бы отражает поверхностное строение атомов вещества (рентгеновскую или электронную плотность), так как поглощение рентгеновского излучения в значительной степени связано с переходом электронов с орбиты на орбиту: чем ярче выглядит ткань на КТ, тем она плотнее.
Основные части компьютерного томографа - гентри, стол, компьютер, консоль оператора (рис. 6.7). Гентри - основная считывающая информацию часть, в его отверстие (апертуру) помещается пациент. Внутри гентри имеется постоянно вращающееся кольцо большого диаметра, на котором закреплены рентгеновская трубка и одна или несколько (до 64) линеек рентгеночувствительных датчиков, которых может быть 256 и больше. Сигналы от датчиков поступают в основной компьютер, обрабатывающий информацию и создающий изображение. Стол, на котором располагается пациент, ступенчато или непрерывно втягивается в отверстие гентри. Ступенчатая подача  Рис. 6.7. Аппараты для рентгеновской компьютерной томографии Рис. 6.7. Аппараты для рентгеновской компьютерной томографиинеобходима при пошаговом исследовании, когда задают толщину выделяемого среза и шаг томографа, а изображения выдаются с соответствующими паузами. Непрерывная подача стола происходит при спиральном (безостановочном) сканировании (вращении кольца при включенной рентгеновской трубке), когда основной компьютер стремительно обрабатывает информацию и выдает изображения в реальном режиме времени. Операторская консоль - основной пульт управления аппаратом, рабочее место рентгенолаборанта и врачарентгенолога. Современные компьютерные томографы являются одновременно спиральными (с непрерывной системой вращения), субсекундными (получение 1 среза менее чем за 1 с) и мультискановыми (оснащены несколькими линейками датчиков). Распределение плотности черно-белого изображения на мониторе связано с поглотительными способностями различных тканей по шкале Хаунсфилда (от 0 единиц, соответствующих чистой воде, и до 1000 единиц, присущих воздуху; шкала продолжена в обе стороны, подобно шкале Цельсия на обычном термометре). Артефакты при КТ могут возникнуть на границе сред с большой разницей их плотности (металлические конструкции и естественные костные кольца - затылочное, верхняя апертура грудной клетки, позвоночный канал, малый таз и др.).
Получаемые изображения близки по анатомической сути пироговским топографическим срезам человеческого тела. В отличие от базовой рентгенодиагностики КТ позволяет визуализировать мягкие ткани и не требует искусственного контрастирования, для того чтобы увидеть внутренние органы. Но для обнаружения патологических изменений в органах и тканях, а также для корректной дифференциальной диагностики выявленных образований контрастирование является неотъемлемым техническим приемом. Самым распространенным способом стандартного контрастирования при КТ является пероральный прием 3% водного раствора водорастворимого контрастного вещества для выделения изображений желудка и петель кишечника. Если не использовать этот прием при исследованиях органов брюшной полости и малого таза, то за опухоль можно принять обычное кишечное содержимое. Целесообразность внутривенного контрастирования определяется клинической задачей или выясняется в процессе исследования. Как правило, внутривенное введение контрастного препарата необходимо для уточнения органопринадлежности, характера и распространенности патологического процесса. При этом особенности накопления и вымывания контрастного вещества опухолевыми массами в большинстве случаев позволяют с уверенностью говорить о злокачественном или доброкачественном характере образования, не прибегая к пункционной биопсии и другим инвазивным методам морфологической верификации. Несомненно, основное предназначение КТ - диагностика онкологических заболеваний. Стремительно развивающиеся возможности спиральной КТ обусловили создание ряда приложений. КТ-кардиоангиография представляет собой 3-мерную визуализиацию сердца и кровеносного русла. Виртуальная КТ-эндоскопия позволяет изучать как бы изнутри трахеобронхиальное дерево, околоносовые пазухи, сосуды и толстую кишку. Не заменяя обычную эндоскопию, такая имитация продвижения по полым органам полезна в случаях, когда выполнить стандартную эндоскопию не представляется возможным. В отдельных случаях методика последующего переформатирования (Multiplanar reconstruction - MPR) изображения опухоли и прилежащих структур в интересующих специалиста плоскостях полезна при решении вопросов о тактике и объеме хирургического вмешательства.
Возможности КТ традиционно описываются по областям исследования - сверху вниз по телу человека. Головной мозг, орбиты, кости основания и свода черепа. Для обнаружения первичных и метастатических опухолей головного мозга КТ обладает широкими возможностями. Для правильной оценки анатомических структур и выявления возможных аномалий необходимо хорошее пространственное разрешение, поэтому толщина срезов не должна превышать 5 мм. Критической зоной является стволовая часть головного мозга, замкнутая в костное кольцо и неизменно перекрываемая артефактами. Опухоли головного мозга характеризуются патологической зоной измененной плотности определенной формы, с признаками объемного воздействия на окружающие структуры, со сдавлением прилежащих полостей и активным накоплением контрастного вещества при внутривенном контрастировании. Некоторым первичным опухолям, таким, как краниофарингиома, присуща кистозная структура. Следует отметить, что 2/3 краниофарингиом наблюдаются в первые 2 десятилетия жизни, имеют срединное расположение в хиазмально-селлярной области и составляются от 3 до 9 % всех первичных опухолей ЦНС. Тем не менее в большинстве случаев степень злокачественности выявленного новообразования удается оценить только при гистологическом исследовании после операции. Перифокальный отек, несомненно, является важным помощником в выявлении множественного метастатического поражения головного мозга, однако метастазы диаметром 0,5 см, как правило, вообще не имеют перифокального отека и могут выявляться только при внутривенном контрастировании. В области глазниц могут встречаться невриномы зрительного нерва, опухоли ретробульбарного пространства. К сожалению, достоверными признаками злокачественности являются только разрушение костных стенок орбиты и распространение опухоли на окружающие анатомические структуры. Небольшое новообразование не может быть идентифицировано по степени злокачественности.
В костях основания и свода черепа можно обнаружить метастазы остеолитического, остеобластического или смешанного строения, имеющие те же признаки, что и в традиционной рентгенодиагностике. Лицевой череп, придаточные пазухи носа, полость носа, носоглотка. В настоящее время КТ является ведущим методом в рентгенодиагностике новообразований носоглотки, гортани и челюстно-лицевой области. Во всех случаях исследование выполняется в двух проекциях (аксиальной и фронтальной), с толщиной томографического среза 2-3 мм, в нативном режиме и с внутривенным контрастированием в объеме 50-100 мл, при этом послойное исследование предпочтительнее спирального, так как обеспечивает более четкую визуализацию мелких костных структур. Данный метод позволяет получить ответ на вопрос, распространяется ли опухоль на лицевой скелет и основание черепа. Однако во всех этих областях нельзя с достаточной точностью отличить полип или аденоид от злокачественной опухоли даже при внутривенном контрастировании (особенно в носоглотке) до появления признаков инвазии окружающих тканей. Шея, щитовидная железа. Хорошо визуализируются опухоли и кисты шеи, пораженные лимфатические узлы. Щитовидная железа часто перекрывается артефактами от костей верхнего плечевого пояса и редко демонстрирует свою тонкую структуру. Однако опухолевые узлы, особенно при достаточно больших размерах, видны без искажений. Легко можно проследить взаимоотношения опухоли с окружающими тканями и анатомическими зонами, в том числе с верхним средостением. В большинстве случаев требуется внутривенное контрастное усиление. Гортаноглотка, гортань. Наиболее ценные сведения можно получить о степени экзоорганного распространения опухоли. Для уточнения границ новообразования и определения состояния крупных сосудов шеи целесообразно использовать внутривенное контрастирование. Тем не менее КТ не является методом первичной диагностики новообразований этой области, для этого достаточно фиброларингоскопии с биопсией.
Органы грудной клетки (средостение, легкие, плевра). Рентгеносемиотика заболеваний этих органов полностью совпадает с базовой рентгенодиагностикой при большей информативности КТ (те же признаки улавливаются более детально). Более точные сведения можно получить о прорастании новообразования из легкого в плевру или средостение, из плевры - в мягкие ткани и костный каркас грудной стенки, в грудные позвонки, из средостения - в обратном направлении. Кисты и опухоли данных органов визуализируются четко. При КТ видны даже неизмененные медиастинальные лимфатические узлы. Пораженные лимфатические узлы могут быть охарактеризованы по форме, размерам, плотности, склонности к конгломерации и агрессии по отношению к окружающим тканям. При этом затруднена дифференциальная диагностика гиперпластической и метастатической лимфаденопатии, отдельных видов лимфопролиферативных заболеваний и невозможна диагностика микрометастазов в лимфатических узлах. Для оценки состояния лимфатических узлов корней легких и связи опухоли с сосудами целесообразно использовать болюсное контрастное усиление по стандартным методикам. При установленном диагнозе рака пищевода КТ применяется для оценки степени распространения экзоорганного компонента опухоли в средостение. Для диагностики опухолей диафрагмы требуются дополнительные приемы (искусственный пневмоперитонеум). Кисты и опухоли перикарда доступны для КТ-диагностики; новообразования миокарда могут диагностироваться этим методом при применении КТ-ангиографии (приоритет остается за УЗИ и МРТ). Органы брюшной и забрюшинной локализации. Условно данная область исследования продолжается от куполов диафрагмы до гребней подвздошных костей (толщина среза 7-10 мм). Многообразие проявлений опухолевых и опухолевидных поражений печени обусловливает сложность их дифференциальной диагностики. Решающее значение в уточненной диагностике новообразований печени принадлежит 4-фаз- ному исследованию с болюсным внутривенным контрастированием.
Первичные и метастатические опухоли печени (рис. 6.8) имеют вид округло-овальных узловых образований пониженной плотности, как правило, хорошо накапливающих контрастное вещество. Причем диффузное гетерогенное контрастирование всего объема опухоли в артериальную фазу характерно для гепатоцеллюлярного рака, в то время как при фокальной нодулярной гиперплазии контрастное вещество накапливается гомогенно. Характерный для метастазов симптом «ободка» в большинстве случаев также наиболее отчетливо определяется в ранние фазы внутривенного контрастирования. Отдифференцировать гемангиомы от прочих новообразований печени можно по наличию «глыбчатого» усиления по периферии очага, медленно нарастающего и переходящего в почти полное контрастирование всего очага к отсроченной фазе. Липомы имеют отрицательные значения плотности; других предположений при этом нет. Менее очевидна диагностика рака поджелудочной железы, так как этот вид опухоли имеет изоденсивную плотность и при внутривен- 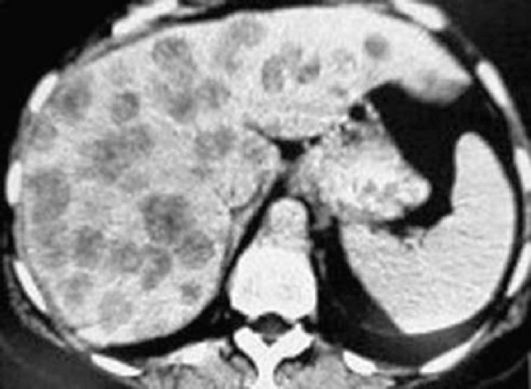 Рис. 6.8. Метастазы рака желудка в печень. Компьютерная томограмма Рис. 6.8. Метастазы рака желудка в печень. Компьютерная томограмманом контрастировании меняет свои свойства одинаково с непораженной паренхимой органа. При раке головки поджелудочной железы обнаруживаются признаки механической желтухи в виде расширения внутри- и внепеченочных желчных протоков, застойного желчного пузыря, блока холедоха на уровне опухоли. Дополнительными симптомами опухоли в любой части железы являются ее объемное увеличение, отсутствие дифференциации с окружающими тканями, признаки прорастания в соседние органы. Селезенка может быть патологически изменена при системных лимфопролиферативных заболеваниях, новообразованиях печени и некоторых других процессах, что проявляется в виде спленомегалии. Очаговые изменения округлой формы характерны для метастатического поражения. Первичные опухоли селезенки не имеют правильной округлой формы, значения плотности - гиподенсивные, структура - однородная.
Надпочечники в норме треугольной формы. Увеличение их размеров и округление формы при «мягкотканой» плотности >15 единиц по шкале Хаунсфилда указывают на опухолевую природу изменений - от аденомы до злокачественного поражения, без полной уверенности в дифференциальном диагнозе. Диагноз устанавливают после сопоставления данных УЗИ, КТ (структурные и денситометрические характеристики) и клинико-лабораторных показателей. Опухоли паренхимы и полостной системы почек диагностируют с высокой достоверностью, особенно при оптимальном применении внутривенного «усиления». Обычно они оцениваются как объемное образование неправильной округлой формы с гиподенсивными значениями плотности, с признаками инвазивного роста. При контрастном усилении плотность опухоли быстро увеличивается из-за хорошей васкуляризации. Для оценки состояния мочеточников, как правило, необходимо их антеградное и ретроградное контрастирование. Малый таз. В диагностике новообразований малого таза КТ способна дать информацию о распространенности злокачественного процесса в случае уже установленного диагноза, но при первичной и дифференциальной диагностике возможности ее ограничены, особенно при раке шейки, вульвы, тела матки, яичников, простаты, прямой кишки в стадиях Т1-2 и в некоторых случаях - в стадии Т3. Хорошие результаты удается получить при оценке метастатического поражения тазовых лимфатических узлов. Приоритет в дифференциальной диагностике новообразований этих органов принадлежит базовому и специализированному УЗИ и МРТ. Костно-суставная система. КТ является эффективным методом оценки состояния крупных плоских и длинных трубчатых костей, превосходящим по возможностям базовую рентгенодиагностику. Оценка состояния суставов в целях онкологической диагностики с помощью КТ также эффективна, а для других целей, как правило, используется МРТ. Исследование мелких и тонких костей сопряжено с техническими трудностями и менее результативно.
При диагностике первичных костных опухолей КТ позволяет получить изображения не только эндооссального (внутрикостного) компонента и периоста, но и экзооссального (внекостного) мягкотканого компонента опухоли. В некоторых случаях обнаружение внешнего компонента имеет решающее значение при дифференциальной диагностике опухолевой, диспластической и воспалительной патологии. Проще, чем при базовой рентгенодиагностике, оценка остеолитических (результат деятельности клеток-остеокластов) и остеобластических (последствия работы остеобластов) изменений, особенно в случае их сочетания. В диагностике опухолей мягких тканей немаловажным преимуществом КТ является возможность определения их взаимоотношений с костями и суставами. В обоих случаях приобретается ценная информация о границах распространения опухоли и ее контакте с другими анатомическими структурами. При диагностике метастазов действуют те же принципы, что и при исследованиях первичных опухолей. Магнитно-резонансная томография (МРТ) относится к неионизирующему (т.е. практически безвредному) методу лучевой диагностики, основанному на использовании физического явления, называемого ядерно-магнитным резонансом (ЯМР). Физическая основа метода - регистрация радиоволн, излучаемых намагниченными атомами водорода после воздействия на них внешнего радиоволнового сигнала, и компьютерная обработка данных. Контрастность тканей на МРТ отражает особенности ядерных структур вещества. Одна и та же ткань может на одной МРТ получиться темной, на другой - светлой, что зависит от выбора формы облучающего сигнала или импульсной последовательности. Напряженность («мощность») магнитного поля, создаваемого тем или иным аппаратом, определяет его основные технико-диагностические возможности: чем выше напряженность, тем шире возмож-
ности. Наиболее распространены МР-томографы с напряженностью 0,23-0,5-1,0-1,5 Тл. В высокоспециализированных научных центрах встречаются установки с мощностью 1,5-3,0 Тл. Основными компонентами любого МР-томографа (рис. 6.9) являются: магнит (постоянный, электрический резистивный или сверхпроводящий - создает постоянное магнитное поле, в которое помещают пациента); градиентные катушки (создают слабое переменное градиентное магнитное поле в центральной части постоянного поля - для выбора области исследования); радиочастотные катушки (передающие и приемные); компьютер (управление работой градиентных и радиочастотных катушек, регистрация сигналов, обработка данных, реконструкция томограмм). Диагностические преимущества МРТ (по сравнению с другими методами получения изображения) основаны на возможности построения анатомических изображений с учетом нескольких физических параметров, в частности, протонной плотности, времени релаксации Т1 и Т2, что в сочетании с применением большого количества разнообразных импульсных последовательностей (протоколов исследования) почти всегда позволяет выявить различия в отображении нормальных и патологически измененных тканей, особенно если применяются методики внутривенного введения специальных, парамагнитных контрастных препаратов, изменяющих физические параметры исследуемых органов и тканей (время  Рис. 6.9. Аппарат для магнитно-резонансной томографии Рис. 6.9. Аппарат для магнитно-резонансной томографиирелаксации и магнитную восприимчивость). Все остальные базовые диагностические методы обеспечивают построение анатомических изображений на основе лишь одного физического параметра: при УЗИ - это эхогенность тканей, при рентгенографии и РКТ - коэффициент поглощения рентгеновских лучей, при радионуклидных исследованиях - интенсивность (энергия) гаммаизлучающих или позитронизлучающих радионуклидов.
Отдельный вид исследований - МР-спектроскопия; она используется только в крупных научно-исследовательских учреждениях с целью оценки концентрации различных веществ в органах и тканях. С помощью МРТ в медицинских целях можно получить изображения органов и тканей, содержащих какое-либо количество воды (возбуждение атомов водорода). Образования, не содержащие воду или углерод, на МРТ не отображаются. Это следует иметь в виду при изучении изменений, которые сопровождаются образованием кальцинатов. Технические препятствия могут возникнуть при исследовании больных с кардиостимуляторами и металлическими протезами (в том числе зубными). В мощном магнитном поле возможно нагревание металлических предметов до критических температур. В настоящее время созданы специальные сплавы, не имеющие такого недостатка; качество металлических конструкций подтверждается специальным сертификатом. Во время процедур могут возникать и другие артефакты: физиологические (связанные с поведением пациента или движением внутренних органов), системные (искажения по методам построения изображений) и аппаратные (связанные с измерительной аппаратурой). Технически МРТ не связана с жесткой необходимостью выполнять исследование только в одной плоскости. Возможности метода позволяют выстраивать диагностическую картину в любой произвольно определяемой плоскости, что значительно повышает наглядность отображения патологических процессов в сложных анатомических областях и облегчает их топическую диагностику (например, в гепатопанкреатодуоденальной области). Выработанный с годами алгоритм исследования предусматривает построение поперечных (аксиальных) срезов, как при КТ, с дополнительными изображениями во фронтальной, сагиттальной и косых плоскостях. В последние годы подобные возможности появились и у КТ - специальные программы обработки изображений
в режиме мультипланарной (многоплоскостной) и 3-мерной реконструкции. Однако дифференциация тканей (контрастное отображение каждого тканевого слоя) гораздо лучше видна при МРТ. По ряду показателей (точность, чувствительность и специфичность) МРТ превышает информативности КТ в одних областях на 1-2 %, в других - на 40 % и более. Известны успехи применения МРТ в диагностике заболеваний ЦНС, сердечно-сосудистой и костно-суставной систем, органов малого таза. Почти равные возможности демонстрируют КТ и МРТ в оценке состояния паренхиматозных органов брюшной полости и забрюшинного пространства, больших плоских костей, лимфатических узлов таза, шеи, грудной полости. В исследованиях этих областей данные методы являются конкурентными. В то же время в изучении стволовой части головного и всего спинного мозга, сердца и сосудистых структур (в том числе головного мозга), конечностей (особенно суставов), органов малого таза преимущество принадлежит МРТ. Вполне объяснимо стремление ЛПУ иметь в своем арсенале оба аппарата. Наиболее часто в онкологической практике МРТ необходима для дифференциальной диагностики первичных и вторичных опухолей ЦНС (ствол и спинной мозг), сердца и перикарда, позвоночника. 16. Цитологической исследование в диагностике злокачественных опухолей Гистологическая и цитологическая диагностика. Прижизненное морфологическое (гистологическое и цитологическое) исследование является одним из наиболее достоверных методов диагностики; его роль в современных лечебно-профилактических учреждениях резко возрастает, особенно в онкологии. Заключение патоморфолога (гистолога, цитолога) помогает клиницисту в правильном распознавании заболевания и тем самым служит руководством к дальнейшим лечебным воздействиям, определяет характер и объем операции, сигнализирует о рецидивах, метастазах, эффективности предыдущего лечения, индивидуальных свойствах опухоли. Неоценима роль патоморфолога в выявлении предопухолевых процессов и ранних стадий злокачественных опухолей. Гистологическая диагностика новообразований основывается на изучении клеток и тканевых структур, наблюдаемых в опухоли и патологически измененной ткани. Основными гистологическими критериями злокачественности новообразования служат атипия клеток, инфильтративный и деструктивный рост. Цитологическая диагностика основывается на изучении морфологических признаков отдельных клеток и комплексов с учетом взаиморасположения в них клеток. Основными критериями злокачественности опухолевой клетки являются атипия и полиморфизм. При обоих методах диагностики в качестве сравнительных эталонов служат ткани и клетки в различные периоды их развития (например, эмбриональном) и при различных физиологических и патологических состояниях (гормональные сдвиги, регенерация, воспаление и др.). Широкому использованию цитологического исследования в онкологической практике способствовали следующие положительные качества метода: 1 - возможность распознавания рака в самой начальной (преклинической) стадии; 2 - доступность и безопасность получения материала из любой ткани и органа; 3 - возможность повторного исследования и динамического наблюдения за очагом поражения, подвергающимся или не подвергающимся лечебным воздействиям; 4 - обеспечение срочности выдачи заключений; 5 - простота приготовления препаратов, несложность оснащения лаборатории и низкая стоимость исследований. Метод цитологического исследования оказался одним из тех, в которых остро нуждается профилактическая онкология, в частности в обеспечении массовости онкологического обследования населения, ибо метод обладает высокой информативностью, дешевизной исследований и возможностью массового охвата населения. Использование цитологического метода при профилактических гинекологических осмотрах в и зарубежных странах повысило выявляемость рака шейки матки в 4 - 6, а предраковых изменений - в 15 - 20 раз. Морфологическому исследованию подвергается биоптический, операционный, секционный материал, а также секреты и экскреты человеческого организма. Биопсия может быть открытой - эксцизионной (иссечение патологически измененного участка полностью, в пределах здоровых тканей) и инцизионной (частичное иссечение опухоли или очага поражения) или закрытой - пункционной. Закрытая биопсия является ценным и незаменимым методом обследования, обеспечивающим получение материала для гистологического и особенно цитологического анализа практически из любой части организма. Одновременное исследование материала биопсии гистологическим и цитологическим методами является наиболее результативным и целесообразным, ибо методы дополняют один другой. Немедленное микроскопическое исследование в течение 15 - 20 мин иссеченной во время операции ткани носит название срочной биопсии и служит для установления точного диагноза и решения вопроса о характере и объеме оперативного вмешательства. Срочная микроскопическая диагностика требует высокой квалификации патоморфолога. В последнее время с этой же целью используют методы цитологического анализа, обеспечивающие ту же достоверность, но в еще более короткий срок - 3 - 5 мин. Объектами цитологического исследования могут быть материалы биопсий аспирационной, пункционной, отпечатки с оперативно удаленных тканей, а также различные выделения человеческого организма (мокрота, влагалищный секрет и др.). По способу получения материала на исследование клиническая цитология подразделяется на: пункционную - изучение пунктатов; эксфолиативную - исследование секретов и экскретов, экскохлеационную - изучение соскобов с очагов поражения; аспирационную - исследование аспиратов из закрытых полостей (плевральная, брюшная и другие полости) и полых органов (пищеварительных, мочевыводящих и др.). Для обеспечения полноценного морфологического исследования материал должен быть получен в достаточном количестве, непосредственно из очага поражения, причем из жизнеспособной (не некротизированной) ткани, а для гистологического препарата - на границе с окружающей здоровой тканью. В сопроводительном направлении помимо основных сведений о больном, клиническом диагнозе сообщается о локализации и глубине расположения очага поражения (опухоли), предпринимавшихся (и каких именно) лечебных воздействиях, гормональном состоянии организма, методе получения материала (пункция, соскоб, биопсия, радикальная операция и др.). Абсолютно недопустимо разделение иссеченной ткани или пунктата на несколько частей и отправление их в различные лаборатории. Чем более ранняя стадия злокачественного новообразования имеет место, тем большие требования предъявляются к забору, обработке и последующему микроскопическому исследованию материала. Результаты гистологической и цитологической диагностики опухолей в значительной степени зависят от метода забора и качества получаемого на исследование материала. По препаратам правильно выполненной биопсии и оперативно удаленных тканей гистологический метод обеспечивает 96 - 100% достоверных заключений. Правильные цитологические заключения для опухолей разных органов и тканей составляют 50 - 95%. Это связано с рядом обстоятельств, среди которых важная роль принадлежит способу взятия, обработки, окраски материала и опыту врача. Ошибки морфологических заключений делятся на гипердиагностические и гиподиагностические. Избыточная диагностика приводит к неоправданным и небезопасным вмешательствам. Гиподиагностика при раке опасна упущением своевременного срока лечения и перехода опухоли в запущенное состояние. Причины ошибочных морфологических заключений могут быть связаны с рядом обстоятельств: 1) неполноценность полученного на исследование материала; 2) неполное использование имеющихся морфологических методов исследования; 3) пределы метода; 4) своеобразие опухоли, когда имеется несоответствие между морфологическими признаками и биологической потенцией опухолевых клеток; 5) неполнота и нечеткость клинических данных; 6) степень подготовки специалистов. Существующие гистологические классификации новообразований различных органов и тканей еще несовершенны. Комитетом ВОЗ разработаны и рекомендованы к использованию 16 международных гистологических классификаций опухолей. Цитологическая классификация опухолей еще не разработана. Предложенная международная цитологическая классификация по опухолям матки (1973) представляет собой фактически гистологическую классификацию, и в ней сохранено разделение рака на инвазивную и неинвазивную формы, чего до настоящего времени практически по цитограммам осуществить невозможно. При разработке цитологических классификаций, помимо основных критериев злокачественности, следует учитывать те изменения, которые претерпевают клетки, отделившиеся самопроизвольно (отделяемое влагалища, мокрота) или насильственно (при пункции, соскобе), тенденция к округлению, сдвиги в тинкториальных и биохимических свойствах и др. При оформлении морфологического заключения следует пользоваться международной гистологической классификацией, в нем требуется отразить не только нозологическую форму, но и гистологический вариант опухоли, отметить степень анаплазии, распространение процесса, реакцию окружающих тканей, в частности присутствие лимфоидно-гистиоцитарного инфильтрата в очаге и по соседству с опухолью. По цитологическим препаратам не на все поставленные вопросы можно ответить. Судить об инфильтративном росте - важном признаке злокачественного процесса - цитологу можно лишь по косвенным признакам. В гистологическом и цитологическом заключении должны быть описательная часть и диагноз, что позволит клиницисту избрать правильную тактику ведения больного. Морфолог может воздержаться от окончательного диагноза лишь в случаях неполноценного или недостаточного количества материала, доставленного на исследование. При определении степени злокачественности опухоли учитывают ряд критериев: 1 - степень сходства опухолевых клеток с их материнскими аналогами - чем более злокачественна опухоль, тем в меньшей мере они похожи на материнские; 2 - сохранение опухолевыми клетками свойства формировать структуры нормальных прототипов; 3 - утеря или извращение функции (выделение секрета, образование кератогиалина); 4 - степень митотической активности - признак условный, он различен для опухолей разных тканей, органов и даже форм опухолей одной и той же ткани. Дальнейший прогресс гистологической диагностики опухолей связан с обогащением ее данными гистохимических, энзимологических, иммунологических, цитогенетических, электронно-микроскопических исследований. Возможности цитологического метода также далеко еще не раскрыты. Его совершенствование будет продолжаться за счет выявления цитоморфологических признаков не изученных или мало изученных опухолей, а также дополнения данными цито- и энзимохимического, цитогенетического, иммунологического анализа, фазово-контрастной, суправитальной, люминесцентной, ультрафиолетовой, инфракрасной микроскопии уже изученных опухолей и благодаря совершенствованию клинических способов забора полноценного материала. 17. Методы морфологической диагностики рака |
