1. Гипоталамус
 Скачать 1.9 Mb. Скачать 1.9 Mb.
|
|
25% -поражение крупных бронхов. 50%-Средних. 75%-мелких. БИЛЕТ 8 1. Ассимиляция, диссимиляция. Понятие об основном обмене. Метаболизм – все происходящие в организме преобразования веществ и энергии. Анаболизм (ассимиляция) – совокупность процессов биосинтеза органических веществ (компонентов клетки и других структур органов и тканей). Обеспечивает рост и развитие, обновление биологических структур, накопление энергии. Химическая модификация и перестройка поступающих с пищей молекул в другие более сложные. (например, включение аминокислот в синтезируемые белки). Катаболизм (диссимиляция) – совокупность процессов расщепления сложных молекул до более простых веществ с использованием части из них в качестве субстрата для биосинтеза и расщепления другой части до конечных продуктов с образованием энергии. Конечные продукты: вода, СO2, CO, мочевина и др. Процессы анаболизма и катаболизма находятся в организме в состоянии равновесия. Больше анаболизма ---->рост, накопление массы Больше катаболизма----> частичное разрушение тканевых структур Состояние равновесия зависит от возраста: в детстве преобладает анаболизм, во взрослом возрасте наблюдается равновесие, в старческом возрасте преобладает катаболизм., зависит от состояния здоровья, от выполняемой физической или психоэмоциональной нагрузки. Почти половина всей энергии, получаемой в результате катаболизма, теряется в виде тепла в процессе образования АТФ. Следовательно, величина теплопродукции является точным выражением величины обмена в организме человека. Основной обмен – это минимальные для бодрствующего организма затраты энергии, определяемые в строго контролируемых стандартах. Условия:
Основной обмен зависит от пола, возраста, роста и массы тела.. У мужчин в сутки примерно 1700 ккал, у женщин на 1 кг массы тела на 10 % меньше, чем у мужчин, у детей больше, чем у взрослыз. 2 методики определения основного обмена:
Для косвенного определения интенсивности обмена могут быть использованы некоторые физиологические параметры, связанные с потреблением кислорода: ЧДД и вентиляционный объем, ЧСС и минутный объем кровотока (МОК). Рабочий обмен – это совокупность основного обмена, энергозатрат, связанных с выполнением работы и специфически динамического действия пищи. Степень энергетических затрат при различной физической активности определяется коэффициентом суточного расхода энергии. (лёгкая работа – 3400-3600 ккал, тяжёлая мышечная работа – 4000-5000ккал) Обмен веществ начинается с поступления питательных веществ в ЖКТ и воздуха в лгке:
2. Рефлекс Основным механизмом деятельности ЦНС является рефлекс. Рефлекс - это ответная реакция организма на действия раздражителя, осуществляемая с участием ЦНС и направленная на достижение полезного результата. Рефлекс в переводе с латинского языка означает "отражение"-. Впервые термин "отражение" или "рефлектирование" был применен Р. Декартом (1595-1650) для характеристики реакций организма в ответ на раздражение органов чувств. Он первым высказал мысль о том, что все проявления эффекторной активности организма вызываются вполне реальными физическими факторами. После Р. Декарта представление о рефлексе было развито чешским исследователем Г. Прохазкой, который развил учение об отражательных действиях. В это время уже было отмечено, что у спинальных животных движения наступают в ответ на раздражение определенных участков кожи, а разрушение спинного мозга ведет к их исчезновению. Дальнейшее развитие рефлекторной теории связано с именем И. М. Сеченова. В книге "Рефлексы головного мозга" он утверждал, что все акты бессознательной и сознательной жизни по природе происхождения являются рефлексами. Это была гениальная попытка ввести физиологический анализ в психические процессы. Но в то время не существовало методов объективной оценки деятельности мозга, которые могли бы подтвердить это предложение И. М. Сеченова. Такой объективный метод был разработан И. П. Павловым - метод условных рефлексов, с помощью которого он доказал, что высшая нервная деятельность организма, так же как и низшая, является рефлекторной. И.П. Павлов экспериментально обосновал взгляд на рефлекс, как основной акт любой нервной деятельности. Он же разделил все рефлексы, по механизму образования, на безусловные и условные. Структурной основой рефлекса, его материальным субстратом (морфологической основой) является рефлекторная дуга - совокупность морфологических структур, которая обеспечивает осуществление рефлекса (путь, по которому проходит возбуждение при осуществлении рефлекса). В основе современное представления о рефлекторной деятельности лежит понятие полезного приспособительного результата, ради которого совершается любой рефлекс. Информация о достижении полезного приспособительного результата поступает в ЦНС по звену обратной связи в виде обратной афферентации, которая является обязательным компонентом рефлекторной деятельности. Принцип обратной афферентации введен в рефлекторную теорию П. К. Анохиным. Таким образом, по современным представлениям структурной основой рефлекса является не рефлекторная дуга, а рефлекторное кольцо, состоящее из следующих компонентов (звеньев): * рецептор; * афферентный нервный путь; * нервный центр; * эфферентный нервный путь; * рабочий орган (эффектор); * обратная афферентация Анализ структурной основы рефлекса проводится путем последовательного выключения отдельных звеньев рефлекторного кольца (рецептора, афферентного и эфферентного пути, нервного центра). При выключении любого звена рефлекторного кольца рефлекс исчезает. Следовательно, для осуществления рефлекса необходима целостность всех звеньев его морфологической основы. Клетки ЦНС имеют многочисленные связи Друг с другом, поэтому нервная система человека может быть представлена как система нейронных цепей (нейронных сетей), передающих возбуждение и формирующих торможение. В этой нервной сети возбуждение может распространяться от одного нейрона на многие другие нейроны. Процесс распространения возбуждения от одного нейрона на многие другие нейроны получил название иррадиации возбуждения или дивергентного принципа распространения возбуждения. Различают два вида иррадиации возбуждения: * направленная или системная иррадиация когда возбуждение распространяется по определенной системе нейронов и формирует координированную приспособительную деятельность организма; * бессистемная или диффузная (ненаправленная) иррадиация, хаотичное распространение возбуждения, при котором координированная деятельность невозможна (рис. 9). В ЦНС к одному нейрону могут сходиться возбуждения от различных источников. Эта способность возбуждений сходиться к одним и тем же промежуточным и конечным нейронам получила название конвергенции возбуждений . 3. Реобаза. Хронаксия. Существует определенное соотношение между временем действия раздражителя и его амплитудой. Эта зависимость получил название кривой «сила-длительность» или по имени автора Гоорвега-Вейса-Лапика. 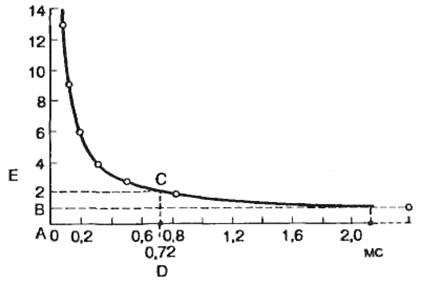 На этой кривой видно, что уменьшение значения тока ниже определенной критической величины не приводит к возбуждению ткани независимо от продолжительности времени, в течение которого действует этот раздражитель, а минимальная величина тока, вызывающая возбуждение , получила название порога раздражения, или реобазы. Величина реобазы определяется разностью между критическим потенциалом и мембранным потенциалом покоя. С другой стороны, раздражитель должен действовать не меньше определенного времени. Уменьшение времени действия раздражителя ниже критического значения приводит к тому, что раздражитель любой интенсивности не оказывает эффекта. Для характеристики возбудимости ткани по времени ввели понятие порога времени – минимальное (полезное) время, в течение которого должен действовать раздражитель пороговой силы с тем, чтобы вызвать возбуждение (отрезок AC) Порог времени определяется емкостью и резистивной характеристикой клеточной мембраны. Те.. постоянной времени T = R*C В связи с тем, что величина реобазы может изменяться, особенно в естественных условиях, и это может привести к значительной погрешности в определении порога времени, Лапик ввел понятие хронаксии для характеристики временных свойств клеточных мембран. Хронаксия – время, в течение которого должен действовать раздражитель удвоенной реобазы. Чтобы вызвать возбуждение. Использование этого критерия позволяет точно измерить временные характеристики возбудимых структур, поскольку измерение происходит на крутом изгибе гиперболы (AD на рис) 4. Дыхание в покое при нагрузке и гипервентиляции. Необходимо для работы - Секундомер. Испытуемый делает максимальный вдох и задерживает дыхание. По секундомеру отмечают время наступления непроизвольного вдоха. Затем делается максимальный выдох и задерживается дыхание. Определяют время наступления непроизвольного вдоха. Опыт повторяют после выполнения физической нагрузки (10-15 приседаний). Испытуемый делает гипервентиляцию легких, делает глубокий вдох и задерживает дыхание. По секундомеру отмечается время наступления непроизвольного выдоха. Сравнивают полученные результаты.
Билет № 9. 1. Строение и функции мембраны, ионные каналы и их функции, ионные градиенты. Согласно современным представлениям, биологические мембраны образуют наружную оболочку всех животных клеток и формируют многочисленные внутриклеточные органеллы. Наиболее характерным структурным признаком является то, что мембраны всегда образуют замкнутые пространства, и такая микроструктурная организация мембран позволяет им выполнять важнейшие функции. Строение и функции клеточных мембран.
Современными методами электронной микроскопии была определена толщина клеточных мембран (6—12 нм). Химический анализ показал, что мембраны в основном состоят из липидов и белков, количество которых неодинаково у разных типов клеток. Сложность изучения молекулярных механизмов функционирования клеточных мембран обусловлена тем, что при выделении и очистке клеточных мембран нарушается их нормальное функционирование. В настоящее время можно говорить о нескольких видах моделей клеточной мембраны, среди которых наибольшее распространение получила жидкостно-мозаичная модель. Согласно этой модели, мембрана представлена бислоем фосфолипидных молекул, ориентированных таким образом, что гидрофобные концы молекул находятся внутри бислоя, а гидрофильные направлены в водную фазу. Такая структура идеально подходит для образования раздела двух фаз: вне- и внутриклеточной. В фосфолипидном бислое интегрированы глобулярные белки, полярные участки которых образуют гидрофильную поверхность в водной фазе. Эти интегрированные белки выполняют различные функции, в том числе рецепторную, ферментативную, образуют ионные каналы, являются мембранными насосами и переносчиками ионов и молекул. Некоторые белковые молекулы свободно диффундируют в плоскости липидного слоя; в обычном состоянии части белковых молекул, выходящие по разные стороны клеточной мембраны, не изменяют своего положения. Электрические характеристики мембран: Емкостные свойства в основном определяются фосфолипидным бислоем, который непроницаем для гидратированных ионов и в то же время достаточно тонок (около 5 нм), чтобы обеспечивать эффективное разделение и накопление зарядов и электростатическое взаимодействие катионов и анионов. Кроме того, емкостные свойства клеточных мембран являются одной из причин, определяющих временные характеристики электрических процессов, протекающихщих на клеточных мембранах. Проводимость (g) — величина, обратная электрическому сопротивлению и равная отношению величины общего трансмембранного тока для данного иона к величине, обусловившей его трансмембранной разности потенциалов. Через фосфолипидный бислой могут диффундировать различные вещества, причем степень проницаемости (Р), т. е. способность клеточной мембраны пропускать эти вещества, зависит от разности концентраций диффундирующего вещества по обе стороны мембраны, его растворимости в липидах и свойств клеточной мембраны. Проводимость мембраны является мерой ее ионной проницаемости. Увеличение проводимости свидетельствует об увеличении количества ионов, проходящих через мембрану. Строение и функции ионных каналов. Ионы Na+, K+, Са2+, Сl- проникают внутрь клетки и выходят наружу через специальные, заполненные жидкостью каналы. Размер каналов довольно мал. Все ионные каналы подразделяются на следующие группы:
4. По механизмам открывания:
В настоящее время установлено, что ионные каналы имеют следующее строение: 1.Селективный фильтр, расположенный в устье канала. Он обеспечивает прохождение через канал строго определенных ионов. 2.Активационные ворота, которые открываются при определенном уровне мембранного потенциала или действии соответствующего ФАВ. Активационные ворота потенциалзависимых каналов имеется сенсор, который открывает их на определенном уровне МП. 3.Инактивационные ворота, обеспечивающие закрывание канала и прекращение проведения ионов по каналу на определенном уровне МП.(Рис). Неспецифические ионные каналы не имеют ворот. Селективные ионные каналы могут находиться в трех состояниях, которые определяются положением активационных (м) и инактивационных (h) ворот: 1.Закрытом, когда активационные закрыты, а инактивационные открыты. 2.Активированном, и те и другие ворота открыты. 3.Инактивированном, активационные ворота открыты, а инактивационные закрыты Функции ионных каналов:
Функцию ионных каналов изучают различными способами. Наиболее распространенным является метод фиксации напряжения, или «voltage-clamp». Сущность метода заключается в том, что с помощью специальных электронных систем в процессе опыта изменяют и фиксируют на определенном уровне мембранный потенциал. При этом измеряют величину ионного тока, протекающего через мембрану. Если разность потенциалов постоянна, то в соответствии с законом Ома величина тока пропорциональна проводимости ионных каналов. В ответ на ступенчатую деполяризацию открываются те или иные каналы, соответствующие ионы входят в клетку по электрохимическому градиенту, т. е. возникает ионный ток, который деполяризует клетку. Это изменение регистрируется с помощью управляющего усилителя и через мембрану пропускается электрический ток, равный по величине, но противоположный по направлению мембранному ионному току. При этом трансмембранная разность потенциалов не изменяется. Изучение функции отдельных каналов возможно методом локальной фиксации потенциала «path-clamp». Стеклянный микроэлектрод (микропипетка) заполняют солевым раствором, прижимают к поверхности мембраны и создают небольшое разрежение. При этом часть мембраны подсасывается к микроэлектроду. Если в зоне присасывания оказывается ионный канал, то регистрируют активность одиночного канала. Система раздражения и регистрации активности канала мало отличается от системы фиксации напряжения. Ток через одиночный ионный канал имеет прямоугольную форму и одинаков по амплитуде для каналов различных типов. Длительность пребывания канала в открытом состоянии имеет вероятностный характер, но зависит от величины мембранного потенциала. Суммарный ионный ток определяется вероятностью нахождения в открытом состоянии в каждый конкретный период времени определенного числа каналов. Наружная часть канала сравнительно доступна для изучения, исследование внутренней части представляет значительные трудности. П. Г. Костюком был разработан метод внутриклеточного диализа, который позволяет изучать функцию входных и выходных структур ионных каналов без применения микроэлектродов. Оказалось, что часть ионного канала, открытая во внеклеточное пространство, по своим функциональным свойствам отличается от части канала, обращенной во внутриклеточную среду. Именно ионные каналы обеспечивают два важных свойства мембраны: селективность и проводимость. Селективность, или избирательность, канала обеспечивается его особой белковой структурой. Большинство каналов являются электроуправляемыми, т. е. их способность проводить ионы зависит от величины мембранного потенциала. Канал неоднороден по своим функциональным характеристикам, особенно это касается белковых структур, находящихся у входа в канал и у его выхода (так называемые воротные механизмы). Рассмотрим принцип работы ионных каналов на примере натриевого канала. Полагают, что в состоянии покоя натриевый канал закрыт. При деполяризации клеточной мембраны до определенного уровня происходит открытие m-активационных ворот (активация) и усиление поступления ионов Na+ внутрь клетки. Через несколько миллисекунд после открытия m-ворот происходит закрытие h-ворот, расположенных у выхода натриевых каналов (инактивация). Инактивация развивается в клеточной мембране очень быстро и степень инактивации зависит от величины и времени действия деполяризующего стимула. При генерации одиночного потенциала действия в толстом нервном волокне изменение концентрации ионов Na+ во внутренней среде составляет всего 1/100000 от внутреннего содержания ионов Na гигантского аксона кальмара. Кроме натриевых, в клеточных мембранах установлены другие виды каналов, избирательно проницаемых для отдельных ионов: К+, Са2+, причем существуют разновидности каналов для этих ионов. Ходжкин и Хаксли сформулировали принцип «независимости» каналов, согласно которому потоки натрия и калия через мембрану независимы друг от друга. Свойство проводимости различных каналов неодинаково. В частности, для калиевых каналов процесс инактивации, как для натриевых каналов, не существует. Имеются особые калиевые каналы, активирующиеся при повышении внутриклеточной концентрации кальция и деполяризации клеточной мембраны. Активация калий-кальцийзависимых каналов ускоряет реполяризацию, тем самым восстанавливая исходное значение потенциала покоя. Особый интерес представляют кальциевые каналы. Входящий кальциевый ток, как правило, недостаточно велик, чтобы нормально деполяризовать клеточную мембрану. Чаще всего поступающий в клетку кальций выступает в роли «мессенджера», или вторичного посредника. Активация кальциевых каналов обеспечивается деполяризацией клеточной мембраны, например входящим натриевым током. Процесс инактивации кальциевых каналов достаточно сложен. С одной стороны, повышение внутриклеточной концентрации свободного кальция приводит к инактивации кальциевых каналов. С другой стороны, белки цитоплазмы клеток связывают кальций, что позволяет поддерживать длительное время стабильную величину кальциевого тока, хотя и на низком уровне; при этом натриевый ток полностью подавляется. Кальциевые каналы играют существенную роль в клетках сердца. Электрогенез кардиомиоцитов рассматривается в главе 7. Электрофизиологические характеристики клеточных мембран исследуют с помощью специальных методов. | ||||||||||||
